孕妇B族链球菌感染对母婴结局的影响分析
2018-05-11杨振莉姜贻乾来汉江
杨振莉 姜贻乾 来汉江
B 族链球菌(Group B streptococcus,GBS)寄居于阴道和直肠,在围生期感染中是第一位的致病菌,可以导致围生儿死亡,同时也是孕产妇生殖道感染的重要致病菌,可以导致泌尿系统感染、羊膜绒毛膜炎、产褥感染、孕产妇败血症和早产[1]。美国疾病预防控制中心(CDC)在 1996、2002、2010年 3次制定并修订了《围产期B族链球菌感染筛查及防治指南》,但国内至今尚未出相关的指南,本研究旨在分析孕妇GBS感染的高危因素及预防性使用抗生素对母婴结局的影响。
1 对象和方法
1.1 对象 选取2016年3月至2017年10月孕35周后在本院产检并分娩的孕妇2 449例(择期剖宫产因产程未启动不纳入研究范围),对所有孕妇在孕35~37周进行GBS筛查。其中2017年1至10月孕35周后GBS筛查阳性的107例孕妇设为试验组,在临产或破膜后预防性使用抗生素;同期有1 027例孕妇GBS筛查阴性。另将2016年3至12月GBS筛查阳性,临产或破膜后未使用抗生素的125例孕妇设为对照组。两组年龄、孕周、产次等比较差异均无统计学意义(均P>0.05),见表1。

表1 两组孕妇临床资料对比
1.2 方法 所有标本取材前不进行外阴消毒,不使用阴道窥阴器,将一根无菌阴道棉拭子于阴道下1/3旋转1周取阴道分泌物,后将同根棉拭子于肛门周围旋转1周。采用细菌培养方式,将送检标本接种于一次性选择性羊血琼脂培养基,35℃环境下含5%二氧化碳培养箱培养18~24h,挑取β溶血、革兰染色阳性、触酶试验阴性、CAMP试验阳性的可疑菌落进行进一步鉴定,鉴定仪器VITEK-compact全自动微生物分析仪及配套鉴定卡(法国生物梅里埃公司),菌株分离、菌株鉴定按常规操作流程。
1.3 临床处理 试验组在临产或破膜后按美国CDC修订的《围产期B族链球菌感染筛查及防治指南》(2002年版)直接给予抗生素预防性治疗,首选青霉素,其次为头孢唑啉,如两者均过敏,则选克林霉素;对照组临产或破膜后不直接使用抗生素。
1.4 观察指标 (1)设带菌高危因素为肥胖(孕早期BMI≥24kg/m2)、高龄妊娠(年龄>35 岁)、经产妇、妊娠期糖耐量异常者、多次人工流产者(人工流产次数≥2次)、合并阴道炎者[2]。比较2017年1至10月不同因素孕妇间的GBS阳性率,分析可能的高危因素;(2)比较两组孕妇的妊娠结局和新生儿情况,观察预防性使用抗生素的临床意义。
1.5 统计学处理 采用Prism 5.0统计软件。计数资料组间比较采用χ2检验,采用logistic回归分析孕妇GBS感染的高危因素。P<0.05为差异有统计学意义。
2 结果
2.1 孕妇GBS感染高危因素分析 孕早期BMI≥24kg/m2、经产妇、妊娠期糖耐量异常、合并阴道炎者的GBS阳性率均高于孕早期BMI<24kg/m2、初产妇、妊娠期糖耐量正常和无阴道炎者,差异均有统计学意义(均P<0.05);不同年龄组和流产次数者GBS阳性率比较差异均无统计学意义(均P>0.05),见表2。将孕早期BMI、产次、妊娠期糖耐量与合并阴道炎纳入多因素logistic回归分析发现,孕早期BMI≥24kg/m2、经产妇、妊娠期糖耐量异常、合并阴道炎为影响GBS感染的高危因素(均P<0.05),见表 3。
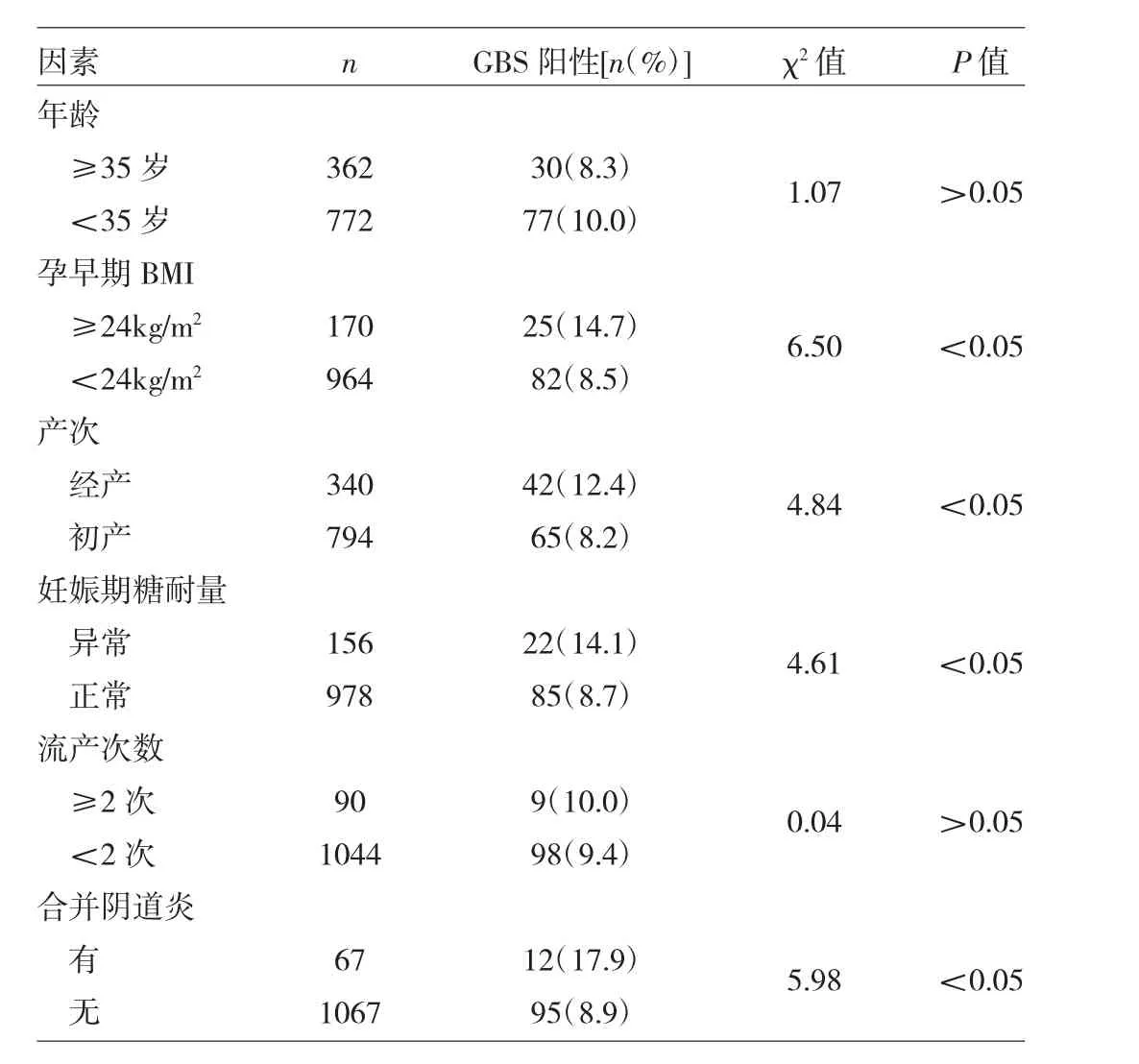
表2 2017年1至10月孕妇GBS感染高危因素分析

表3 多因素logistic回归分析影响孕妇GBS感染高危因素
2.2 两组孕妇妊娠结局和新生儿情况分析 试验组孕妇临产或破膜后使用青霉素85例,使用头孢唑啉12例,使用克林霉素10例。预防性使用抗生素后,试验组产后出血、产褥感染、胎儿窘迫、新生儿上呼吸道感染发生率较对照组明显降低,差异均有统计学意义(均P<0.05);两组胎膜早破、早产、低出生体重儿、新生儿肺炎、新生儿败血症发生率比较差异均无统计学意义(均P >0.05),见表 4~5。

表4 两组孕妇妊娠结局分析[例(%)]

表5 两组新生儿情况分析[例(%)]
3 讨论
研究表明,妊娠妇女GBS感染率为10.1%~32.4%[3-5],不同地区、不同种族的妊娠晚期妇女GBS感染率各不相同,为6.5%~36.0%[6-9],本研究妊娠晚期孕妇GBS感染率为9.5%(232/2449)。孕妇GBS感染对妊娠结局及新生儿感染均造成不良影响,甚至导致新生儿死亡。国内一直未出台GBS筛查及防治指南,可能与国内缺乏相应的大数据、检测技术的完美度、卫生经济学等方面的考虑有关。从卫生经济学的角度来讲,如能找到与感染相关度高的风险因素,及时对这些高风险孕妇进行筛查,进行针对性干预,既能减少感染概率,改善母婴预后,又能减少卫生资源的大量消耗,故本研究对妊娠期感染GBS可能的高风险因素进行了分析,发现妊娠期GBS感染与肥胖、产次、妊娠期糖耐量异常、阴道炎有关,提示以上3种情况可能会增加GBS感染,关于危险因素导致的GBS感染的具体机制尚未明确[10],分析可能与阴道上皮细胞内的糖原含量超过正常水平,使阴道酸度增加以及阴道炎等导致阴道内环境改变,GBS更容易寄居有关。
2002年美国CDC针对妊娠期GBS感染提出了抗生素预防治疗方案,为了评价新方针使用后的效果,美国CDC将2003至2005年围生期孕妇及新生儿GBS感染的发病率与2000至2001年作了比较,发现2003至2005年间白种婴儿早发型疾病比2000至2001年间低33%,但是黑种婴儿早发型疾病则上升了70%[11],提示GBS感染存在种族差异。本研究试验组预防性使用抗生素治疗后,两组胎膜早破、早产、低出生体重儿、新生儿肺炎、新生儿败血症发生率比较差异均无统计学意义,提示预防性治疗可以改善孕妇不良结局,但对胎儿的严重不良预后方面作用不明显。这可能与抗生素使用时间较迟,对胎膜早破、早产的动因未能及时干预与清除有关,相应的,低出生体重儿发生率也增加,新生儿严重感染也无法有效预防。提示预防新生儿GBS感染还是要从预防孕妇感染等更早的干预手段入手才更有效。
据国外文献报道,近年随着抗生素在临床的大量使用,GBS对青霉素的耐药率逐渐升高,并且对红霉素和克林霉素的耐药率从<5%升高至20%~30%[12-13]。在目前大力提倡合理使用抗生素的大环境下,对GBS阳性孕妇进行抗生素预防值得进一步探讨,可从对相关高风险因素进行针对性干预来减少GBS感染的发病率,另外通过母体免疫预防新生儿GBS感染应当是未来有效控制GBS感染的一种新思路与新方法。当前GBS相关疫苗从早期的荚膜多糖疫苗到荚膜多糖结合疫苗再到蛋白疫苗,已经取得了非常大的进步,随着GBS相关疫苗研究的不断深入,特别是保护性抗体水平临界值的确立及抗体浓度对应疫苗剂量的建立,GBS疫苗对于预防新生儿GBS感染将发挥重要作用[14]。
[1]时春艳,曲首辉,杨磊,等.妊娠晚期孕妇B族链球菌带菌状况的检测及带菌对妊娠结局的影响[J].中华妇产科杂志,2010,45(1):12-16.doi:10.3760/cma.j.issn.0529-567x.2010.01.005.
[2]Bloom SL,Cox SM,Bawdon RE,et al.Ampicillin for neonatalgroup Bstre ptococcal prophylaxis How rapidly can bacterieidal concentrations beachieved?[J].Am J Obstet Gynecol,1996,175(4 Pt 1):974-976.
[3]张景林,袁林,杨永弘.600名妊娠妇女及新生儿GBS感染情况的研究[J].中华流行病学杂志,1995,16:36-39.
[4]马延敏,吴连方,黄醒华.孕妇B族链球菌带菌与母婴预后的关系[J].中华妇产科杂志,2000,35:32-35
[5]梁梅英,王山米.产前B族链球菌感染对母儿的影响[J].中华围产医学杂志,1999,2(1):285-286.doi:10.3760/cma.j.issn.1007-9408.1999.01.005.
[6]Sweet RL,Gibbs RS.Infectious diseases of the female genital tract[M].15th Edition.Wolters Kluwer:Lippincott Williams&Wilkins,2009:1-9.
[7]Verani JR,McGee L,Schrag SJ.Prevention of perinatal group B streptococcal disease.Revised guidelines from CDC[J].MMWR Recomm Rep,2002,59(RR-10):1-36.
[8]Van Dyke MK,Phares CR,Lynfield R,et al.Evaluation of universal antenatal screening for group B streptococcus[J].N Engl J Med,2009,360(25):2626-2636.doi:10.1056/NEJMoa0806820.
[9]Barcaite E,Bartusevicius A,Tameliene R,et al.Prevalence of matemal group B streptococcal colonization in European countries[J].Acta Obstet Gynecol Scand,2008,87:260-271.
[10]Eschenbach D.Reviewer's commentary on Reduction of the use of antimicrobial drugs following the rapid detection at delivery of Streptococcus agalactiae in vagina by real-time PCR assay[J].BJOG,2013,120(9):1108-1109.
[11]Centers for Disease Controland Prevention(CDC).Perinatalgroup B streptococcal disease affter universal screening recommendations--United States,2003-2005.United states[J].MMWR,2007,56(28):701-705.
[12]Verani JR,Schrag SJ.Group B Streptococcal disease in infants:progress im prevention and continued challenges[J].Clin Perinatol,2010,37(2):375-392.doi:10.1016/j.clp.2010.02.002.
[13]Verani JR,McGee I,Schrag SJ,et al.Prevention of perinatal group B Streptococcal disease-revised guidelines from CDC,2010[J].MMWR Recomm Rep,2010,59(RR-10):1-36.
[14]高坎坎,钟华敏,梁绮华,等.B族链球菌相关疫苗的研究进展[J].中华妇幼临床医学杂志(电子版),2017,13(1):116-119.doi:10.3877/cma.j.issn.1673-5250.2017.01.022.
