口服硝苯地平与静脉注射拉贝洛尔治疗妊娠期高血压急症有效性及安全性比较的系统评价Δ
2018-03-14柳汝明
李 琳,黄 桦,柳汝明,李 骞,张 峻
(昆明医科大学第一附属医院临床药学科,云南 昆明 650032)
妊娠期高血压为妊娠期常见并发症,发病率为5%~10%[1],且是导致妊娠期、围产期妇女和围产儿死亡的主要原因之一[2-3]。据世界卫生组织统计,每年约有50 000名妇女死于妊娠期高血压[4]。当血压持续升高至收缩压(systolic blood pressure,SPB)≥160 mm Hg(1 mm Hg=0.133 kPa)和(或)舒张压(diastolic blood pressure,DPB)≥110 mm Hg,且持续时间>15 min,被定义为妊娠期高血压急症[5]。此时,为防止妊娠期、围产期妇女心脑血管意外和胎盘早剥等严重母胎并发症的发生,需及时进行降压治疗[6]。静脉注射拉贝洛尔一直被用作妊娠期高血压急症急性发作时的一线治疗药物[7]。但近年来不断有证据证实口服速效型硝苯地平治疗妊娠期高血压急症的疗效和安全性[8-9],其亦可作为妊娠期高血压急症的一线治疗方案,特别是在静脉用药无效时。且与静脉注射拉贝洛尔相比,口服硝苯地平更经济、更易得,尤其是在国内普遍缺乏拉贝洛尔的地区和医院。目前,已有多个临床随机对照试验(randomized controlled trial,RCT)对口服硝苯地平与静脉注射拉贝洛尔分别治疗妊娠期高血压急症的有效性及安全性进行了比较[10-16]。本研究采用循证医学的方法,对口服硝苯地平与静脉注射拉贝洛尔分别治疗妊娠期高血压急症的有效性及安全性进行系统评价,以期为临床提供可靠的参考依据。
1 资料与方法
1.1 纳入与排除标准
1.1.1 研究类型:RCT,无论是否采用分配隐藏或盲法,文种限中英文。
1.1.2 研究对象:患者妊娠期间有高血压急症,SPB≥160 mm Hg,DPB≥110 mm Hg;妊娠周期≥22周;目标血压为SPB≤150 mm Hg,DPB≤100 mm Hg。
1.1.3 干预措施:观察组患者口服硝苯地平;对照组患者静脉注射拉贝洛尔。
1.1.4 结局指标:主要结局指标为降至目标血压所用硝苯地平与拉贝洛尔的时间、达到目标血压所用治疗剂量与初始剂量的比值;次要结局指标为围产期妇女不良反应发生率、5分钟Apgar评分<7分新生儿数及重症监护住院新生儿数。
1.1.5 排除标准:(1)房室传导阻滞者;(2)支气管哮喘者;(3)充血性心力衰竭者;(4)仅有摘要,未下载到全文的文献;(5)重复发表的文献;(6)无法提取数据进行文献荟萃(Meta)分析的文献。
1.2 检索策略
计算机检索PubMed、Cochrane Library、EM-base、Science Direct Journal、中国知网、维普数据库、中国生物医学文献数据库及万方数据库等8个数据库,收集口服硝苯地平与静脉注射拉贝洛尔分别治疗妊娠期高血压的相关文献。检索时限为建库至2017年3月。中文检索词包括“硝苯地平”“拉贝洛尔”“妊娠”“高血压”和“随机对照试验”等;英文检索词包括“Nifedipine”“Labetalol”“Pregnancy”和“Hypertension”等。
1.3 文献的筛选、资料的提取与质量评价
1.3.1 文献筛选:(1)由2名研究者阅读检索到的文献标题和摘要进行初筛,初步剔除明显不合格的文献。(2)下载全文对文献资料进行逐一阅读和分析,确定文献是否合格;如有争议,通过讨论达到意见一致或与第3名研究者协商解决。(3)在阅读文献的过程中,根据入选文献中的参考文献补充符合纳入标准的文献。
1.3.2 资料提取及方法学质量评价:由2名研究者独立进行资料提取及文献质量评价。采用Cochrane协作网的偏倚风险评价工具对纳入文献进行偏倚风险评价,评价内容包括:(1)随机分配方法;(2)是否采用分配隐藏;(3)是否采用盲法;(4)结果数据是否完整,有无退出/失访,是否说明失访原因及进行意向性分析;(5)有无选择性报告研究结果;(6)其他偏倚来源。每篇纳入文献根据上述6条标准作出“是”(低度偏倚)、“否”(高度偏倚)和“不清楚”(缺乏相关信息或偏倚情况不确定)的判断。
1.4 统计学方法
采用RevMan 5.3软件对纳入文献进行Meta分析。连续型变量采用MD为效应指标,二分类变量采用OR为效应指标,各指标均给出其点估计和95%CI。采用χ2检验对纳入研究进行异质性检验,并结合I2定量评判异质性的大小。若异质性检验结果为I2≤50%,P≥0.1,可认为多个同类研究没有异质性,采用固定效应模型进行Meta分析;反之,如异质性检验为I2>50%,P<0.1,则研究结果存在差异,有统计学意义,需要进一步分析异质性的来源,明显的临床异质性采用亚组分析或敏感性分析等方法进行处理,或只行描述性分析,在排除明显临床异质性的影响后,采用随机效应模型进行Meta分析。
2 结果
2.1 文献检索结果及纳入文献的基本特征
根据检索策略,初步检索到相关文献1 100篇,经逐层筛选,最终纳入符合标准的文献7篇[10-16],均为英文文献,共480例患者。纳入文献的基本特征见表1。
2.2 纳入文献的方法学质量评价
纳入文献的方法学质量评价见表2。
2.3 Meta分析结果
2.3.1 达到目标血压所用时间:5篇文献[10-11,14-16]报告了达到目标血压所用时间,共280例患者。异质性检验,I2=76%(P<0.1),提示各研究间存在异质性,对异质性可能产生的原因进行分析后,将系统评价根据纳入研究的药物剂量进行亚组分析,仍存在异质性,最终采用随机效应模型进行Meta分析。结果显示,观察组患者达到目标血压所用的时间明显短于对照组(MD=-12.12,95%CI=-20.25~-3.99,P=0.003),差异有统计学意义,见图1。
2.3.2 达到目标血压所用治疗剂量与初始剂量的比值:7篇文献[11-16]均报告了达到目标血压所用治疗剂量与初始剂量的比值,共480例患者。异质性检验,I2=92%(P<0.1),提示各研究间存在异质性,将系统评价根据纳入研究的药物剂量比值进行亚组分析,仍存在异质性,最终采用随机效应模型进行Meta分析。结果显示,两组患者达到目标血压所用治疗剂量与初始剂量比值的差异无统计学意义(MD=-0.51,95%CI=-1.08~0.05,P=0.07),见图2。

表1 纳入文献的基本特征Tab 1 Basic characteristics of included studies

表2 纳入文献的方法学质量评价Tab 2 Methodology of quality evaluation on included studies

图1 两组患者达到目标血压所用时间比较的Meta分析森林图Fig 1 Forest plot of Meta-analysis on the comparison of required times to achieve target blood pressure between two groups
2.3.3 围产期妇女不良反应发生率:4篇文献[10-12,16]报告了围产期妇女不良反应发生率,共260例患者,不良反应包括头痛、头晕、恶心及心动过速等。异质性检验,I2=78%(P<0.1),提示各研究间存在异质性,将系统评价根据纳入研究的药物剂量比值进行亚组分析,仍存在异质性,最终采用随机效应模型进行Meta分析。结果显示,两组围产期妇女不良反应发生率的差异无统计学意义(OR=0.98,95%CI=0.27~3.50,P=0.97),见图3。
2.3.4 5 min Apgar评分<7分新生儿数:3篇文献[10,13-14]报告了5 min Apgar评分<7分新生儿数,共189例患者。异质性检验,I2=0%(P=0.99),提示各研究间具有同质性,采用固定效应模型进行Meta分析。结果显示,两组5 min Apgar评分<7分新生儿数的差异无统计学意义(OR=0.42,95%CI=0.14~1.25,P=0.12),见图4。
2.3.5 重症监护住院新生儿数:5篇文献[11-14,16]报告了重症监护住院新生儿数,共356例新生儿进入重症监护室。异质性检验,I2=0%(P=0.57),提示各研究间具有同质性,采用固定效应模型进行Meta分析。结果显示,两组重症监护住院新生儿数的差异无统计学意义(OR=0.74,95%CI=0.43~1.29,P=0.29),见图5。
3 讨论
妊娠期高血压是目前国内外妇产科的常见疾病,重度患者可出现昏迷、心肾功能衰竭等严重症状,高血压急症持续>15 min则可能导致中枢神经系统损伤,可对妊娠期、围产期妇女及围产儿的健康造成较大的影响。而对妊娠期高血压急症患者进行及时、规范化的处理可以降低患者子痫前期和子痫的发生风险,改善不良结局。因此,对于妊娠期高血压急症患者,需尽快给予对症降压处理。降压治疗不仅需要降低血压,防止并发症的发生,还要充分考虑患者与胎儿的安全[17]。
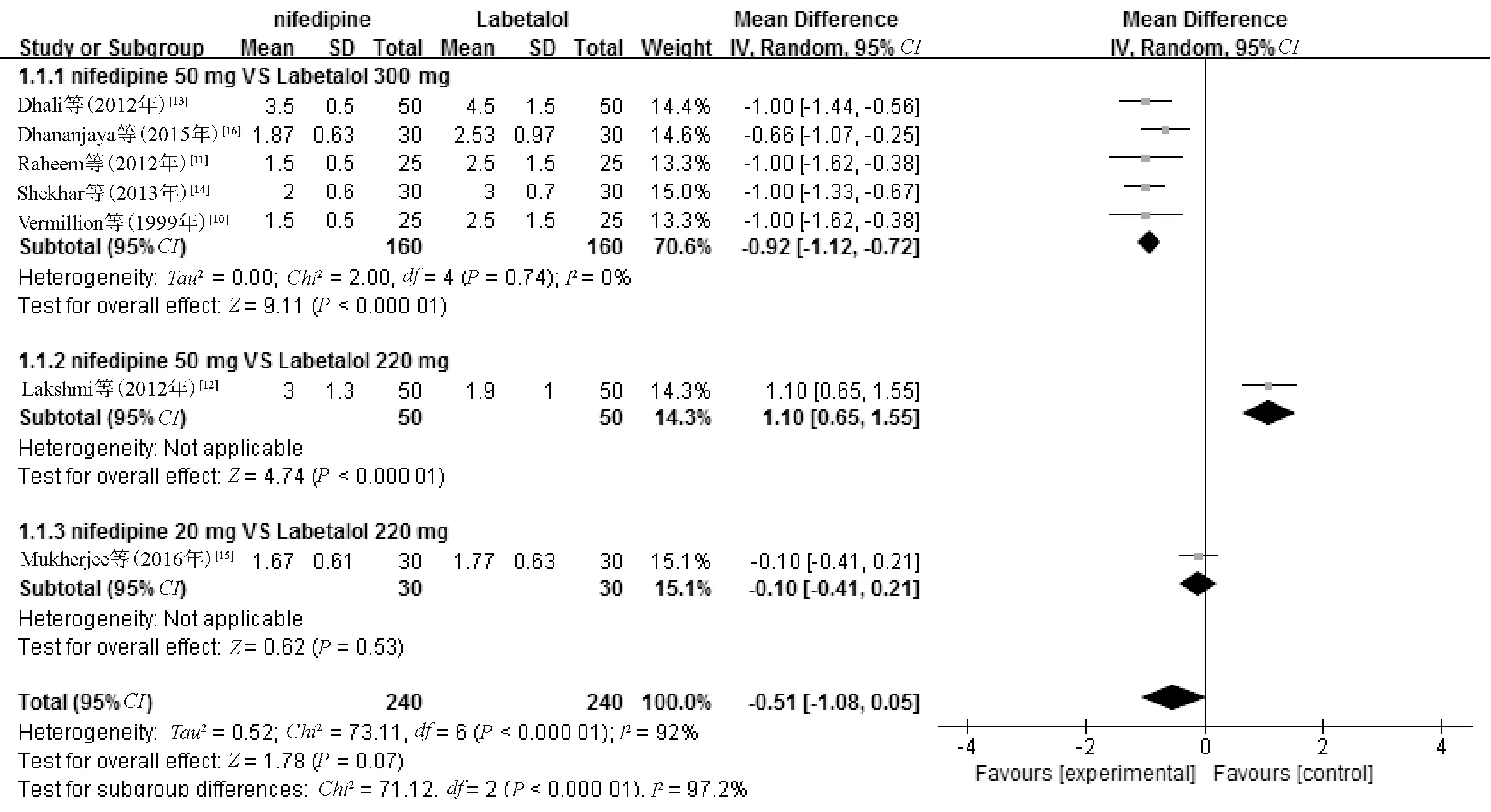
图2 两组患者达到目标血压所用治疗剂量与初始剂量的比值比较的Meta分析森林图Fig 2 Forest plot of Meta-analysis on the comparison of ratio of target blood pressure required therapeutic dose to initial dose between two groups
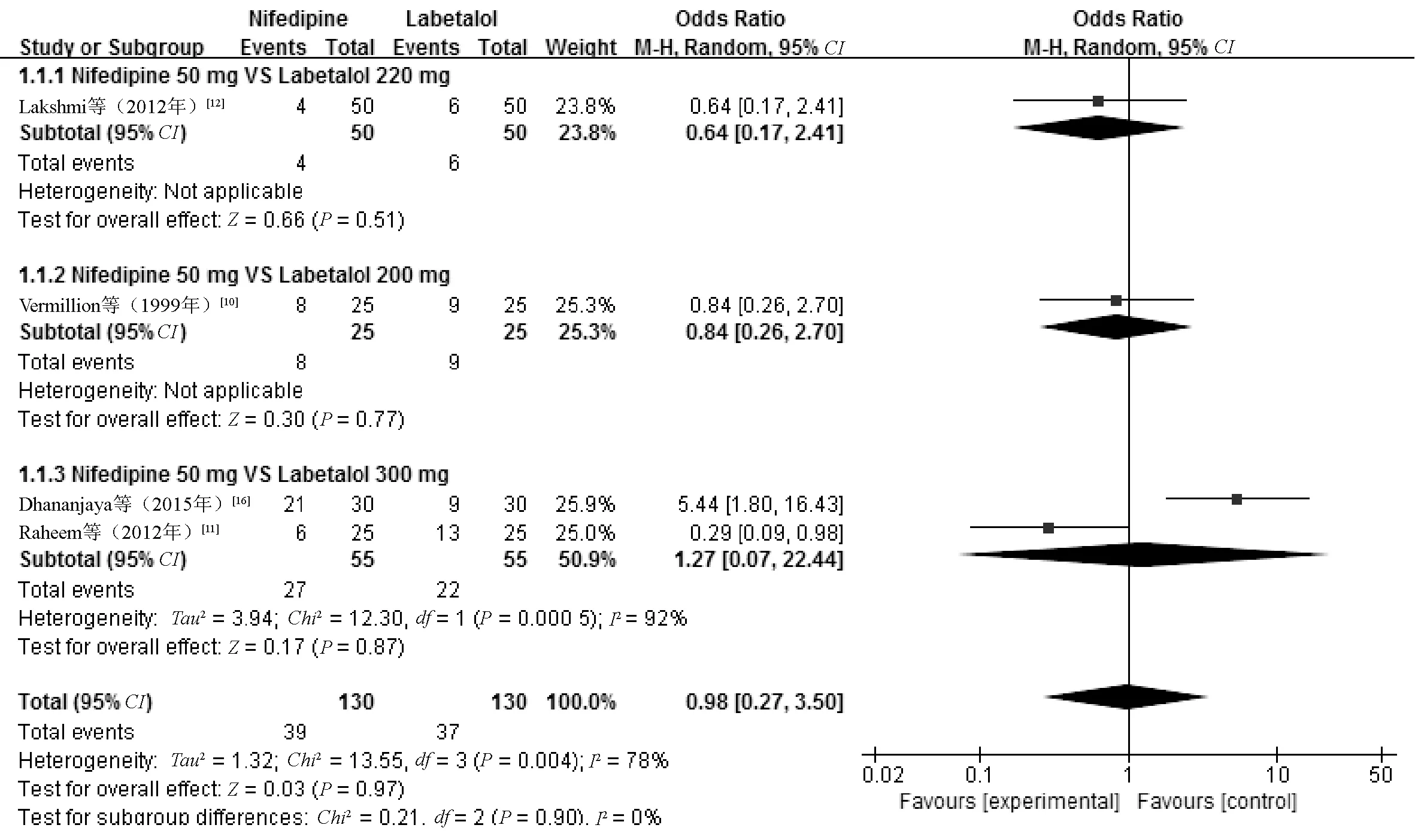
图3 两组围产期妇女不良反应发生率比较的Meta分析森林图Fig 3 Forest plot of Meta-analysis on the comparison of incidences of adverse drug reactions in perinatal women between two groups

图4 两组5 min Apgar评分<7分新生儿数比较的Meta分析森林图Fig 4 Forest plot of Meta-analysis on the comparison of numbers of newborns scored <7 in 5 min Apgar score between two groups
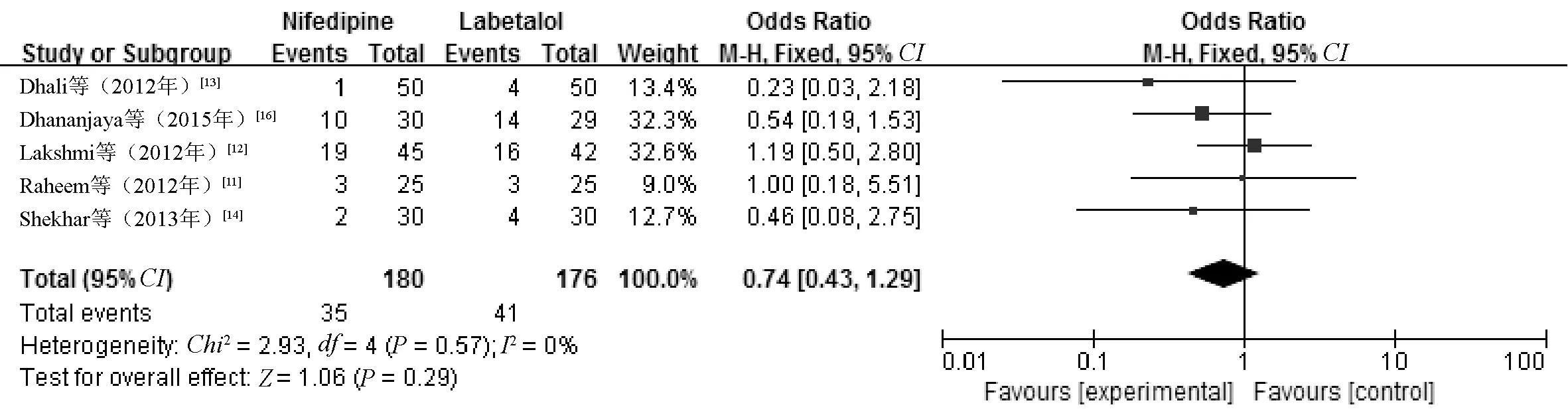
图5 两组重症监护住院新生儿数比较的Meta分析森林图Fig 5 Forest plot of Meta-analysis on comparison of numbers of hospitalized newborns in ICU between two groups
拉贝洛尔是α和β受体阻断剂,其降压作用显著且安全性高,无反跳现象,被广泛用于高血压病的治疗。拉贝洛尔能有效降低妊娠期高血压患者的血压而不会减少胎盘的血流量,也不会对患者的心输出量造成明显影响[18]。该药在治疗妊娠期高血压急症时通常静脉给药,初始剂量20 mg,最大累计药量为220或300 mg;妊娠期妇女常见的不良反应为头痛、恶心、呕吐及面色潮红等,新生儿则表现为心动过速、低血压和低体质量[19]。硝苯地平为二氢吡啶类钙通道阻滞剂,通过抑制Ca2+内流,发挥松弛平滑肌、扩张冠状动脉血管的作用,有利于改善脐动脉血流及子宫胎盘缺血、缺氧状态。该药在治疗妊娠期高血压急症时通常口服给药,初始剂量5~10 mg,最大累计药量不超过60 mg;妊娠期妇女常见的不良反应为头痛、眩晕、心悸、面色潮红及水肿等。
本研究对纳入的7个RCT共480例患者进行了Meta分析,结果显示,口服硝苯地平与静脉注射拉贝洛尔都能有效治疗妊娠期高血压急症,但口服硝苯地平组患者达到目标血压所用的时间更少;两组患者达到目标血压所用剂量与初始剂量比值的差异无统计学意义。治疗过程中,两组围产期妇女出现的不良反应包括头痛、头晕、恶心及心动过速等,两组围产期妇女不良反应发生率的差异无统计学意义。对胎儿的安全性主要通过5 min Apgar评分<7分新生儿数及重症监护住院新生儿数进行评价,两组的差异均无统计学意义。
本研究存在一定的局限性:首先,纳入文献均为已发表文献,未对灰色文献进行检索;且纳入文献的数量少,纳入研究的样本量小,所得的结果可能存在偏倚。其次,纳入研究所用的药物剂量存在差别,可能是导致异质性的原因之一;虽然根据不同的剂量对各研究进行了亚组分析,但仍存在异质性,最终采用随机效应模型进行Meta分析。此外,纳入的文献中有部分数据不完整,部分文献是否采用分配隐藏和盲法也不清楚。因此,还需要更多设计严格的大样本随机对照研究为临床提供更可靠的证据。
综上所述,当前研究数据显示,口服硝苯地平与静脉注射拉贝洛尔都能安全、有效地用于妊娠期高血压急症的治疗,且口服硝苯地平血压达标所用时间更少,为临床妊娠期高血压急症的治疗提供了参考。
[1]Rosas-Peralta M,Borrayo-Sánchez G,Madrid-Miller A,et al.Hyper-tension during pregnancy:the challenge continues[J].Rev Med Inst Mex Seguro Soc,2016,54(Suppl l):s90-s111.
[2]Roberts JM,Pearson G,Cutler J.Summary of the NHLBI Working Group on Research on Hypertension During Pregnancy[J].Hype-rtension,2003,41(3):437-445.
[3]Hypertension in pregnancy: diagnosis and management.Clinical guidelines[CG107][EB/OL].[2014-06-20].https://www.nice.org.uk/guidance/cg107.
[4]Khan KS,Wojdyla D,Say L,et al.WHO analysis of causes of maternal death:a systematic review[J].Lancet,2006,367(9516):1066-1074.
[5]Committee on Obstetric Practice.Committee Opinion no.514: emer-gent therapy for acute-onset, severe hypertension with preeclampsia or eclampsia[J].Obstet Gynecol,2011,118(6):1465-1468.
[6]Berg CJ,Chang J,Callaghan WM,et al.Pregnancy-related mortality in the United States,1991-1997[J].Obstet Gynecol,2003,101(2):289-296.
[7]Committee on Obstetric Practice.Committee Opinion No.623: Eme-rgent therapy for acute-onset, severe hypertension during pregnancy and the postpartum period[J].Obstet Gynecol,2015,125(2):521-525.
[8]Firoz T,Magee LA,Macdonell K,et al.Oral antihypertensive therapy for severe hypertension in pregnancy and postpartum:a systematic review[J].BJOG,2014,121(10):1210-1218.
[9]Arulkumaran N,Lightstone L.Severe pre-eclampsia and hypertensive crises[J].Best Pract Res Clin Obstet Gynaecol,2013,27(6):877-884.
[10] Vermillion ST,Scardo JA,Newman RB,et al.A randomized,double-blind trial of oral nifedipine and intravenous labetalol in hypertensive emergencies of pregnancy[J].Am J Obstet Gynecol,1999,181(4):858-861.
[11] Raheem IA,Saaid R,Omar SZ,et al.Oral nifedipine versus intravenous labetalol for acute blood pressure control in hypertensive emergencies of pregnancy:a randomised trial[J].BJOG,2012,119(1):78-85.
[12] Lakshmi BS,Dasari P.Oral nifedipine versus intravenous labetalol in hypertensive urgencies and emergencies of pregnancy:a randomized clinical trial[J].Obstetric Medicine,2012,5(4):171-175.
[13] Dhali B,Bhattacharya S,Ganguly RP,et al.A randomized trial of intravenous labetalol & oral nifedipine in severe pregnancy induced hypertension[J].Int J Reprod Contracept Obstet Gynecol,2012,1(1):42-46.
[14] Shekhar S,Sharma C,Thakur S,et al.Oral nifedipine or intravenous labetalol for hypertensive emergency in pregnancy:a randomized controlled trial[J].Obstet Gynecol,2013,122(5):1057-1063.
[15] Mukherjee S,Khan S,Jain U,et al.A comparative evaluation of intravenous labetalol versus oral nifedipine for control of severe pregnancy-inducedhypertension with low-dose regimen[J].Int J Med Sci Public Health,2016,5(6):1183-1186.
[16] Dhananjaya BS,Jamuna R.Oral nifedipine versus intravenous labetalol in hypertensive emergencies of pregnancy: A randomised trial[J].Res J Pharm Biol Chem Sci,2015,6(2):1673-1681.
[17] 曾美玲.硝苯地平防治妊娠高血压所致早产的临床研究[J].河北医药,2013,35(14):2171-2172.
[18] Committee on Obstetric Practice.Committee Opinion No 623:Em-ergent therapy for acute-onset,severe hypertension during pregnancy and the postpartum period[J].Obstet Gynecol,2015,125(2):521-525.
[19] Clark SM,Dunn HE,Hankins GD.A review of oral labetalol and nifedipine in mild to moderate hypertension in pregnancy[J].Semin Perinatol,2015,39(7):548-555.
