靶向药物尼妥珠单抗用于Ⅳ期结直肠癌根治术后患者维持治疗的疗效及预后分析
2018-03-09杨怀勇刘晓玲
艾 良 杨怀勇 刘晓玲
(1云南省肿瘤医院腹部外科 云南昆明 650100;2云南省肿瘤医院药剂科 云南昆明 650100;3昆明医科大学第一附属医院干疗科 云南昆明 650032)
结直肠癌是临床上常见的恶性肿瘤之一,在世界肿瘤发病率中位居第3位,死亡率为第4位,在我国结直肠癌发病率呈现逐年快速上升的趋势,已位于癌症谱第3位[1]。有资料显示,全球每年有130~140万例新增患者,其治疗方法主要以手术切除为主、辅以化疗和放疗的综合治疗[2]。但多数患者就诊时已处于肿瘤进展期,预后效果差,因此放化疗治疗成为结直肠癌患者治疗的一个重要手段[3]。但化疗药物的长时间使用,使患者体内累积的毒性增多,导致化疗的持续应用受到了限制[4-6]。因此,经化疗得到最佳效果后,选择低毒、有效的药物维持治疗是近年来结直肠癌的研究热点。国外有研究报道[7-9],选择尼妥珠单抗进行维持治疗,可以改善患者的疾病预后。鉴于此,本文旨在探讨靶向药物尼妥珠单抗用于Ⅳ期结直肠癌根治术后患者维持治疗的疗效以及对疾病预后的影响,以期为临床上化疗后结直肠患者的维持治疗方案提供参考,现报告如下。
1 资料与方法
1.1 一般资料 选取2010年1月至2012年6月本院收治的66例Ⅳ期结直肠癌患者作为研究对象,将入选的患者分为两组,A组为同意接受单药尼妥珠单抗作为维持治疗的患者(n=34),B组为未接受维持治疗而停药随访观察的患者(n=32)。A组中男性 18例,女性 16例;年龄 43~73岁,平均(58.32±2.94)岁;体力状况评分:0~1分 20 例,2 分 14 例;腺癌31例,黏液腺癌3例。B组中男性17例,女性15例;年龄 40~72 岁,平均(56.86±4.32)岁;体力状况评分:0~1分16例,2分16例;腺癌28例,黏液腺癌4例。两组患者在性别、年龄、病理组织学分型及疾病分期等一般资料差异均无统计学意义 (均P>0.05),具有可比性。本研究通过本院伦理委员会审核,所有患者在治疗前均知情并签署同意书。纳入标准:(1)病理诊断明确;(2)患者均未经任何类似药物治疗;(3)体力状况(performance status,PS)评分 0~2分,预计生存期>3个月。排除标准:(1)妊娠期妇女;(2)曾使用阿帕替尼靶向药物治疗胃癌的患者;(3)合并精神障碍的患者。
1.2 治疗方法[10]所有患者给予(FOLFOX/FOLFIRI/XELOX/XELIRI)的标准方案进行一线化疗。在结直肠癌病灶化疗取得最大缩小率后,A组患者接受单药尼妥珠单抗(尼妥珠单抗:批准文号:S20100023,厂家:上海中信国健药业股份有限公司)的维持治疗,采用静脉注射的方式,按照5 mg/kg体重每2 w给药1次,治疗至不能耐受或进展;B组患者未接受维持治疗而停药随访观察。
1.3 观察指标 (1)比较两组患者疗效,分级为完全缓解(complete response,CR),部分缓解(panial response,PR),疾病稳定(stable disease,SD)和疾病进展(progressive disease,PD)。 疗效评价标准[11]:①CR:结直肠癌病灶完全消失,且维持时间>1个月;②PR:结直肠病灶体积缩小>50%,且维持时间>1个月;③SD:结直肠病灶缩小<50%~增大<25%;④PD:结直肠病灶增大>25%或出现新的病灶。以(CR+PR)计算总体有效率,以(CR+PR+SD)计算疾病控制率(DCR)。(2)比较两组患者的3年无瘤生存率和5年总生存率[12]。(3)比较两组患者随访期间不良反应发生情况,不良反应包括肝功能异常、消化道反应、血液学毒性、血压升高、蛋白尿、手足综合征等[13]。
1.4 统计学方法 应用SPSS 17.0软件进行统计分析。计量资料以()表示,采用t检验进行组间比较;计数资料以[n(%)]表示,采用 χ2检验进行组间比较;采用Kaplan-Meier法进行3年无瘤生存率及5年总生存率的生存曲线分析,应用对数秩检验(log-rank test)计算生存曲线间的统计学差异。以P<0.05表示差异有统计学意义。

表1 两组实体肿瘤疗效比较[n(%)]

图1 两组无瘤生存率情况
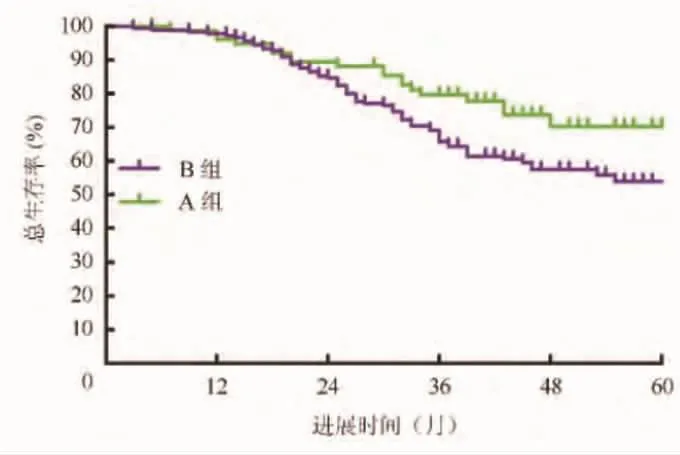
图2 两组总生存率情况

表2 两组不良反应发生情况比较[n(%)]
2 结 果
2.1 比较两组实体肿瘤疗效 A组的总有效率高于B组,组间差异有统计学意义(P<0.05);A组的疾病控制率高于B组,组间差异有统计学意义(P<0.05)。 见表 1。
2.2 比较两组生存情况 66例患者PFS为6.3~54.6个月, 中位 PFS为 34.2个月 (95%CI:27.4~41.0),A组3年无瘤生存率为61.00%,B组3年无瘤生存率为52.30%,与A组相比,B组患者的3年无瘤生存率显著降低(Log-rank P=0.032),见图1。66例患者OS为16.4~67.6个月,中位OS为46.3个月(95%CI:34.0~58.6),A 组 5年总生存率为 71.20%,B组5年总生存率为55.50%,与A组相比,B组患者的5年总生存率显著降低 (Log-rank P=0.049),见图2。
2.3 比较两组不良反应发生情况 主要不良反应包括肝功能异常、血液学毒性、血压升高、蛋白尿、手足综合征等,两组并发症总发生率差异无统计学意义(P >0.05)。 见表 2。
3 讨 论
结直肠癌是常见的消化道恶性肿瘤之一,具有较高的发病率和死亡率,严重影响着人民的生活质量和生命健康。原方案持续化疗直至疾病进展是结直肠癌化疗的传统理念,化疗可以改善结直肠癌患者的疾病预后,但随着多种细胞毒性化疗药物的使用,患者体内累积的毒性增多,药物的累积毒性使化疗的持续应用受到了限制。目前对于结直肠癌患者化疗获益后的后续维持治疗方案,仍然存在争议。Tournigand等[14]研究报道结直肠癌患者经过FOLFOX化疗后,再采用单药尼妥珠单抗进行维持治疗,与持续原化疗方案FOLFOX进行维持治疗相比,采用单药尼妥珠单抗的患者的不良反应发生率明显降低,还可以延长PFS和OS,明显改善患者的生活质量。也有研究发现[15],贝伐珠单抗进行“打打停停”的维持治疗方式,维持组的PFS和OS明显延长,用药安全性更好。
本文研究结果表明,采用靶向药物尼妥珠单抗维持治疗的A组患者总有效率高于不进行维持治疗的B组患者,采用靶向药物尼妥珠单抗维持治疗的A组患者的疾病控制率高于不进行维持治疗的B组患者,提示靶向药物尼妥珠单抗对Ⅳ期结直肠癌患者进行维持治疗的疗效显著。采用靶向药物尼妥珠单抗维持治疗的A组患者的3年无瘤生存率、5年总生存率均显著高于B组患者,提示靶向药物尼妥珠单抗对Ⅳ期结直肠癌患者进行维持治疗时更有助于改善患者疾病的预后。采用靶向药物尼妥珠单抗维持治疗的A组患者的总不良反应发生率与B组患者差异不显著,表明靶向药物尼妥珠单抗对Ⅳ期结直肠癌患者进行维持治疗时未增加不良反应发生率。
综上所述,靶向药物尼妥珠单抗用于Ⅳ期结直肠癌根治术后患者维持治疗的疗效较好,可提高3年无瘤生存率及5年总生存率,且未见增加不良反应发生率,但其确切疗效及安全性问题还需要更多大样本的临床研究、前瞻性研究来验证,值得进一步临床研究探讨。
[1]俞希虎,王磊.结直肠癌精准医疗的研究现状[J].中华实验外科杂志,2017,34(1):1-4.
[2]SIEGEL R, MA J, ZOU Z, et al.Cancer statistics,2014[J].CA Cancer J Clin,2014,64(1):9-29.
[3]杨林.化疗在结直肠癌中的地位及应用[J].实用肿瘤杂志,2013,28(1):15-19.
[4]张斌,刘慧燕.K-ras基因突变状态与西妥昔单抗/帕尼单抗治疗转移性结直肠肠癌疗效的系统评价[J].中国现代应用药学,2013,30(8):924-928.
[5]黄芳刘,超英.FOLFOX4方案与XELOX方案治疗转移性结直肠癌的疗效与不良反应分析[J].实用癌症杂志,2016,31(10):1675-1677.
[6]杨冬阳,黎莹,刘建化,等.晚期结直肠癌联合化疗后卡培他滨维持治疗的临床评价[J].南方医科大学学报,2013,33(12):1815-1818,1830.
[7]周勇,杨勇.两种同步放化疗方案对复发性结直肠癌患者生存时间及不良反应的影响[J].检验医学与临床,2017,14(11):1565-1567.
[8]LIU Y J, ZHU G P, GUAN X Y.Comparison of the NCICTCAE version 4.0 and version 3.0 in assessing chemoradiation-induced oral mucositis for locally advanced nasopharyngeal carcinoma[J].Oral oncol,2012,48(6):554-559.
[9]HONG K D, LEE S I, MOON H Y.The efficacy of oral tegafururacil as maintenance therapy following intravenous 5-fluorouracil chemotherapy in stage Ⅲ colon cancer[J].Hepato-gastroenterology,2012,59(113):104-107.
[10]ALDERTON G K.Metastasis:Epithelial to mesenchymal and back again[J].Nat Rev Cancer,2013,13(1):3-7.
[11]TSENG J Y,YANG C Y,LIANG S C,et al.Interleukin-17A modulates circulating tumor cells in tumor draining vein of colorectalcancersandaffectsmetastases[J].ClinCancerRes,2014,3(13):2162-2168.
[12]DIAZ-RUBIO E,GOMEZ-ESPANA A,MASSUTI B,et al.Firstline XELOX plus bevacizumab followed by XELOX plus bevacizumab or single-agent bevacizumab as maintenance therapy in patients with metastatic colorectal cancer: the phase Ⅲ MACRO TTD study [J].Oncologist,2012,17(1):15-25.
[13]WASAN H,MEADE A M,ADAMS R,et al.Intermittent chemotherapy plus either intermittent or continuous cetuximab for first-line treatment of patients with KRAS wildtype advanced colorectal cancer (COIN-B):a randomised phase 2 trial[J].Lancet Oncol, 2014, 15 (6):631-639.
[14]TOURNIGAND C,CERVANTES A,FIGER A,et al.OPTIMOX1:a randomized study of FOLFOX4 or FOLFOX7 with oxaliplatin in a stop-and-Go fashion in advanced colorectal cancer-a GERCOR study[J].Clin Oncol,2016,24(3):394-400.
[15]CHIBAUDEL B, MAINDRAULT-GOEBEL F, LLEDO G,et al.Final results of OPTIMOX2,a large randomized phase II study of maintenance therapy or chemotherapyfree intervals (CFI) after FOLFOX in patients with metastatic colorectal cancer (MRC):A GERCOR study[J].Clin Oncol,2017,25(18):4013-4014.
