2013-2015年南京地区34家医院乳腺癌内分泌治疗药物利用分析
2018-03-06潘祺琦
潘祺琦,赵 萍
(南京医科大学第一附属医院药学部,南京 210029)
乳腺癌是女性发病率最高的恶性肿瘤,在我国,每年有近20万女性被诊断出乳腺癌,尤其在大城市,乳腺癌的发病率逐年增加。但随着新的治疗策略和方法的普及,乳腺癌的死亡率正逐步下降[1]。在乳腺癌的综合治疗中,内分泌治疗占有重要的地位,规范的内分泌治疗是降低激素受体阳性乳腺癌患者肿瘤复发率及提高总生存率的重要手段。本文拟通过对南京地区34家医院2013-2015年乳腺癌内分泌治疗药物应用数据的回顾性统计、分析,以了解该地区这类药物的用药现状和发展趋势。
1 资料与方法
1.1一般资料 原始数据由江苏省医药科技情报研究所提供,来源于南京地区34家入网医院2013-2015年上报给“长江流域医院用药信息网”的购药数据。
1.2方法 运用Microsoft Excel2007软件对南京地区34家医院2013-2015年乳腺癌内分泌治疗药物的品种、用量、销售金额等进行统计、分析,采用限定日剂量(DDD)、用药频度(DDDs)、日均费用(DDC)、销售金额作为分析指标。DDD值取自WHO药物统计方法整合中心网站(http://www.whocc.no/atc_ddd_index)。DDDs=某药的年消耗量/相应的DDD值,DDDs越大药物的使用频度越高,反映临床对该药的选择倾向性大。DDC=某药的销售总金额/DDDs,反映平均每日的用药费用。乳腺癌内分泌治疗药物按其药理作用可分为抗雌激素药物[他莫昔芬(TAM)、托瑞米芬、氟维司群]、芳香化酶抑制剂(AI,如来曲唑、阿那曲唑、依西美坦)、黄体激素释放激素类似物(LH-RH-A,如戈舍瑞林、亮丙瑞林)、孕激素类(甲羟孕酮、甲地孕酮)药物。LH-RH-A、孕激素类药物因不作为乳腺癌内分泌治疗的一线药物推荐,且适应证不仅仅是乳腺癌内分泌治疗,因此本文未作统计分析。
2 结 果
2.1各年度乳腺癌内分泌治疗药物总销售金额及年增长率 乳腺癌内分泌治疗药物销售金额呈上升趋势,且年增长率逐年增加。抗雌激素药物年增长率趋于稳定,AI增幅逐年升高。两大类药物每年所占比例基本相似,见表1。
2.2各年度各种乳腺癌内分泌治疗药物销售金额情况 乳腺癌内分泌治疗药物销售金额排序各年度保持不变。AI阿那曲唑、来曲唑各年构成比稳定,两药的销售金额各年度均占总销售金额的70%以上。抗雌激素药物托瑞米芬销售金额构成比逐年小幅上升,TAM销售金额构成比逐年小幅下降,见表2。
2.3各年度乳腺癌内分泌治疗药物DDDs排序及DDC统计 乳腺癌内分泌治疗药物DDDs排序各年度也保持不变,且各种药物的DDDs均逐年升高。首个抗雌激素药TAM各年度DDDs一直以明显优势稳居榜首,说明TAM仍一直是临床应用最多的乳腺癌内分泌治疗药物。对比表2可见,由于TAM价格低廉,销售金额排序一直靠后,且从DDC来看,TAM逐年略有降低,托瑞米芬逐年略有升高,这可能导致托瑞米芬与TAM销售金额构成比的小幅变化。AI中阿那曲唑由于价格较高,金额排序一直稳居第一,但从DDDs可以看出,该类药物中来曲唑是临床选用倾向性最大的药物,其次为阿那曲唑,见表3。
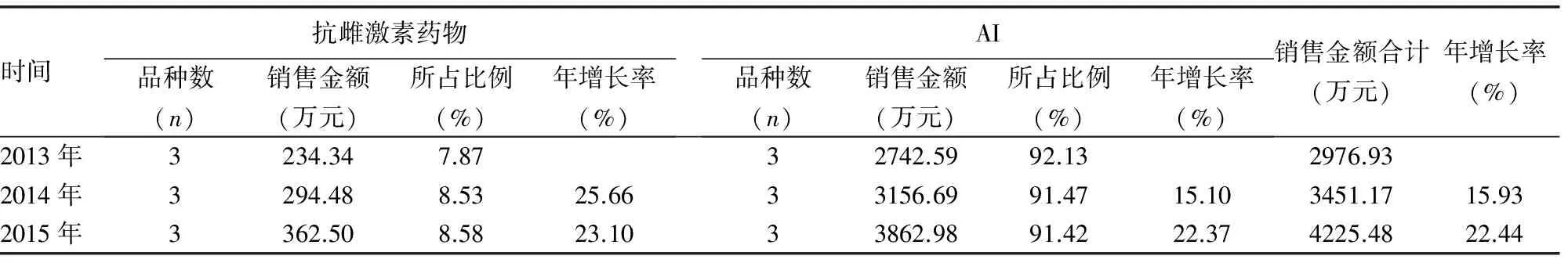
表1 2013-2015年南京地区乳腺癌内分泌治疗药物总销售金额、占比及年增长率
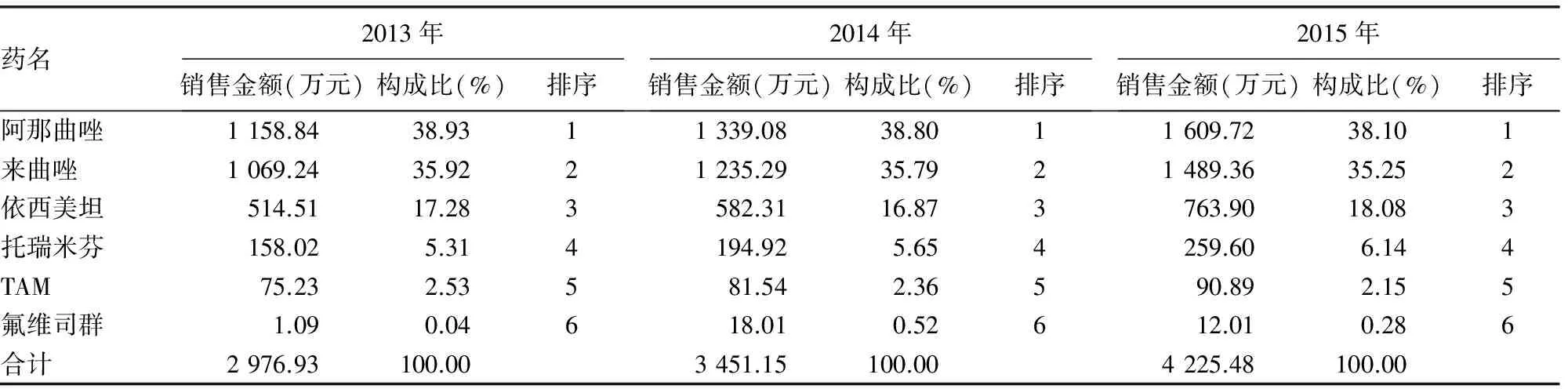
表2 2013-2015年南京地区乳腺癌内分泌治疗药物销售金额、构成比及排序
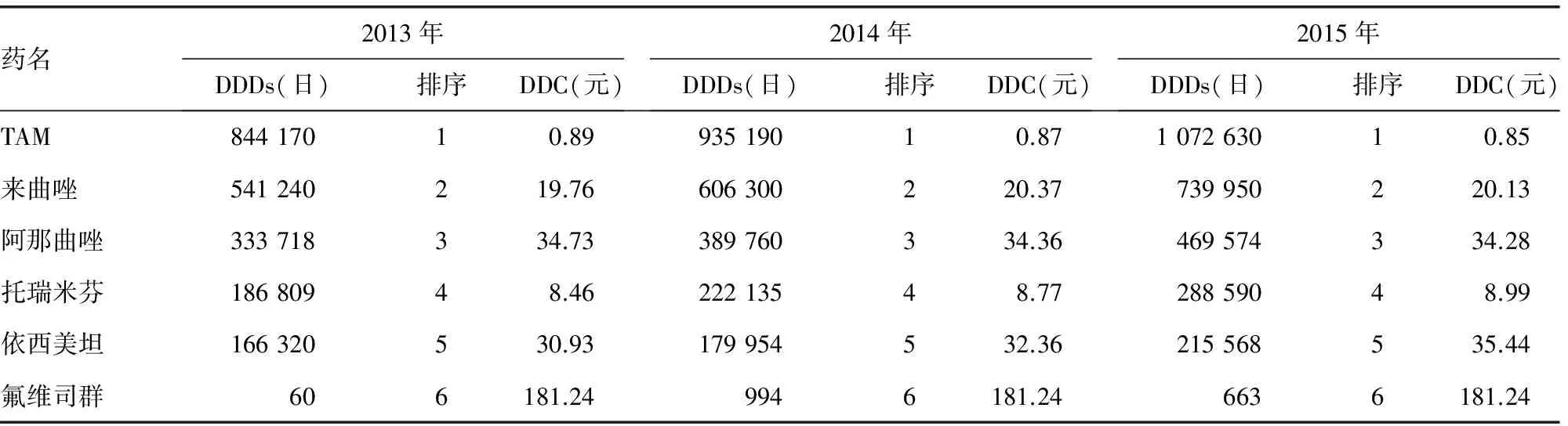
表3 2013-2015年南京地区乳腺癌内分泌治疗药物DDDs、排序及DDC
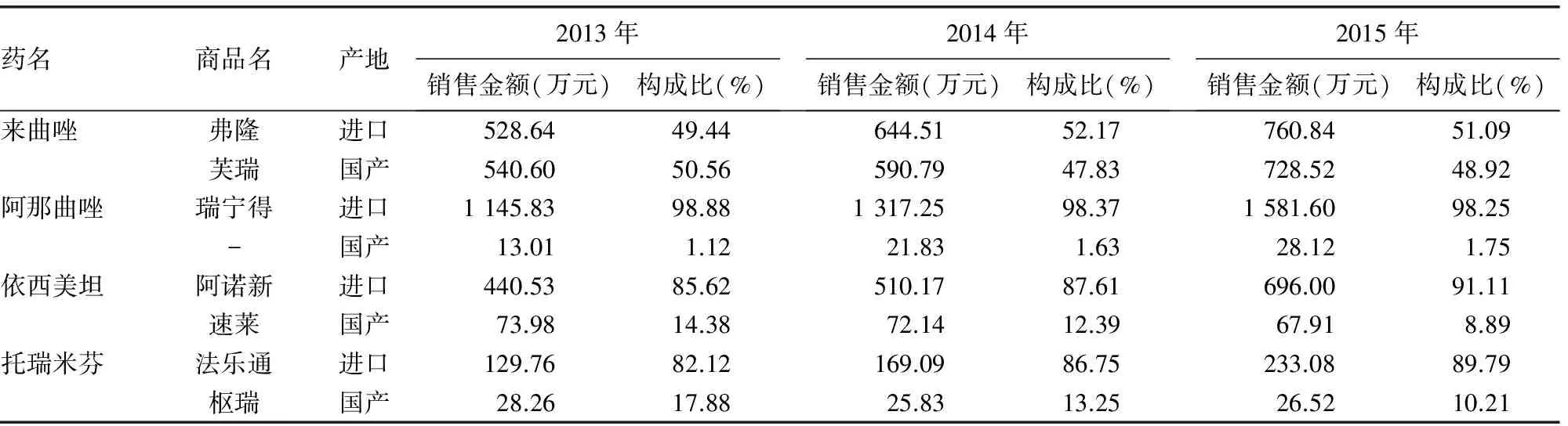
表4 2013-2015年南京地区乳腺癌内分泌治疗药物各原研药与仿制药销售金额及构成比

表5 2013-2015年南京地区乳腺癌内分泌治疗药物各原研药与仿制药DDDs、构成比及DDC
2.44种药物原研药与仿制药之间用药分析 来曲唑、阿那曲唑的原研药与仿制药的销售金额构成比及DDDs构成比各年基本保持不变,依西美坦、托瑞米芬原研药销售金额构成比及DDDs构成比逐年略有升高。原研药价格均高于仿制药,尤其是其中的3种AI,价格相差悬殊。仅有来曲唑的仿制药临床选用倾向性远高于原研药,而其他3种药物,临床更倾向于选用其原研药,尤其是阿那曲唑、托瑞米芬,原研药的DDDs大幅高于仿制药,且托瑞米芬的原研药DDDs仍在逐年升高。依西美坦的原研药2013年DDDs略高于仿制药,但到2015年,其原研药的DDDs构成比已是仿制药的2倍余。说明虽然原研药的价格高于仿制药,但除外来曲唑,临床更多地选用了该类药物的原研药,2013-2015年南京地区34家医院TAM均使用的是国产仿制药,氟维司群均使用的是原研药“芙仕得”,故无法进行这两种药品原研药与仿制药的比较分析。2013-2015年南京地区乳腺癌内分泌治疗药物各原研药与仿制药销售金额及构成比等见表4、5。
3 讨 论
乳腺癌属于激素依赖性肿瘤,在长期雌激素的刺激下会增加疾病复发和转移的风险。其内分泌治疗机制是改变激素依赖性肿瘤生长所需要的内分泌微环境,抑制癌细胞的生长增殖[2]。美国国立综合癌症网络(NCCN)乳腺癌临床实践指南及国家卫计委《乳腺癌诊疗规范》要求:雌激素受体(ER)、孕激素受体(PR)阳性的浸润性乳腺癌患者,不论其年龄、淋巴结状况或是否应用辅助化疗,都要考虑辅助内分泌治疗。
南京地区乳腺癌内分泌治疗药物各年销售金额及增幅逐年增长,除外乳腺癌的发病率逐年增加,也反映出乳腺癌内分泌药物治疗已被临床普遍认同和应用。TAM为首个用于临床的乳腺癌内分泌治疗药物,循证医学证据表明激素受体阳性乳腺癌患者使用TAM较不使用TAM可明显降低复发风险和死亡风险[3-4]。TAM由于疗效确定、耐受性良好、价格低廉,至今仍为临床选用最多的乳腺癌内分泌治疗药物。托瑞米芬为TAM的类似物,由于临床证据相对不足,一直被各指南推荐用于TAM不能耐受患者的二线治疗。
AI的问世使乳腺癌内分泌治疗药物有了更多的选择。对于绝经后激素受体阳性患者,AI的疗效已被证明优于TAM[5-6]。近年的临床试验表明绝经前激素受体阳性患者在卵巢功能抑制前提下,AI较TAM治疗有更大获益[7-8]。2016年版《NCCN指南》也新增推荐其可用于绝经前激素受体阳性的复发高风险患者。3年来,南京地区AI总DDDs各年均略高于抗雌激素药总DDDs,AI销售金额的增幅也逐年增加,表明AI已被临床接纳和认可,并且越来越受到青睐。目前,临床应用的阿那曲唑、来曲唑、依西美坦均属于第3代AI,有Meta分析表明,这3种AI在乳腺癌内分泌治疗疗效方面差异无统计学意义(P>0.05)[9-10];而发生心血管不良反应总例数及严重心血管不良反应总例数最多的是来曲唑,其次是依西美坦,最少的是阿那曲唑。而从表3来看,来曲唑一直是南京地区应用最多的AI,其次是阿那曲唑。可能由于来曲唑价格相对最能让患者接受,但需警惕其心血管不良反应。
关于乳腺癌内分泌治疗药物原研药与仿制药的临床等效性研究尚较少。从本文数据看,除外来曲唑,其他3种药物均是原研药占据了较大的市场份额,临床应用也更倾向于原研药。可能出于医生及患者对仿制药临床疗效的担心。胡莉荣等[11]研究表明来曲唑仿制药的经济效益优于原研药。其他药物在药物经济学方面尚缺乏相关研究。
综上所述,TAM由于价格低廉、疗效确定,仍为南京地区临床应用最多的药物。AI随着循证医学证据的增多,DDDs已赶超抗雌激素药物,并且销售金额增幅逐年增加,市场前景良好。来曲唑可能由于价格优势,是应用最多的AI。原研药所占市场份额及DDDs明显高于仿制药。南京地区乳腺癌内分泌治疗用药趋势与各个指南推荐相符,临床用药规范。
[1]中国乳腺癌内分泌治疗专家共识专家组.中国乳腺癌内分泌治疗专家共识(2015版)[J].中国癌症杂志,2015,25(9):755-759.
[2]张彦收,刘运江.乳腺癌内分泌治疗简史[J].中华医史杂志,2015,45(1):28-32.
[3]FACTORS A.Effects of adjuvant tamoxifen and of cytotoxic therapy on mortality in early breast cancer.An overview of 61 randomized trials among 28 896 women[J].N Engl J Med,1988,319(26):1692-1681.
[4]BUZDAR A.The place of chemotherapy in the treatment of early breast cancer[J].Br J Cancer,1998,78 Suppl 4:S16-20.
[5]CUZICK J,SESTAK I,BAUM M,et al.Effect of anastrozole and tamoxifen as adjuvant treatment for early-stage breast cancer:10-year analysis of the ATAC trial[J].Lancet Oncol,2010,11(12):1135-1141.
[6]COATES A S,KESHAVIAH A,THUERLIMANN B A,et al.Five years of letrozole compared with tamoxifen as initial adjuvant therapy for postmenopausal women with endocrine-responsive early breast cancer:Update of study BIG 1-98[J].J Clin Oncol,s2007,25(5):486-492.
[7]PAGANI O,REGAN M M,WALLEY B A,et al.Adjuvant exemestane with ovarian suppression in premenopausal breast cancer[J].N Engl J Med,2014,371(2):107-118.
[8]FRANCIS P A,REGAN M M,FLEMING G F,et al.Adjuvant ovarian suppression in premenopausal breast cancer[J].N Engl J Med,2015,372(5):436-446.
[9]AYDINER A.Meta-analysis of breast cancer outcome and toxicity in adjuvant trials of aromatase inhibitors in postmenopausal women[J].Breast,2013,22(2):121-129.
[10]ZHAO X H,LIU L,LI K,et al.Comparative study on individual aromatase inhibitors on cardiovascular safety profile:a network meta-analysis[J].Onco Targets Ther,2015,8(8):2721-2730.
[11]胡莉荣,樊帆,赵涛,等.国产与进口来曲唑的成本-效果分析[J].江西医药,2011,46(4):362-364.
