巨噬细胞移动抑制因子抗体对大鼠大肠异常隐窝病灶及大肠癌的影响
2018-03-06沈媛媛刘成霞王爱丽张冉冉
沈媛媛,刘成霞,王爱丽,程 凯,张冉冉
(滨州医学院附属医院:1.消化内科;2.甲状腺乳腺外科,山东滨州 256600)
大肠癌是常见的恶性肿瘤之一,严重威胁人类健康,早期发现大肠癌前病变是提高大肠癌治愈率的关键。异常隐窝病灶(aberrant crypt foci,ACF)是目前显微镜下可见的最小、最早的癌前病变[1],ACF数量与结直肠肿瘤发生有明显相关性[2]。因此,如何早期发现及治疗ACF成为研究的热点。研究表明,巨噬细胞移动抑制因子(macrophage migration inhibitory factor,MIF)作为一种传统的炎性因子,可直接影响细胞的分裂和诱导癌基因的恶性转化,是一个独特的促肿瘤发生细胞因子[3-4]。因此,本实验采用二甲基肼诱导大鼠ACF及大肠癌模型,在组织学水平探讨MIF的表达及MIF抗体对ACF及癌瘤数量的影响,分析MIF抗体在大肠癌癌变中的抑制作用。
1 材料与方法
1.1材料 实验动物:实验用Wistar大鼠100只,雌雄各半,5周龄左右,平均体质量70 g左右,购自山东鲁抗公司,生产许可证号SCXK鲁20130001。严格按照滨州医学院动物实验伦理委员会的条例执行。主要药物及试剂:二甲基肼、MIF抗体均由济南芯博生物科技有限公司生产,生产批号D161802、20415-1-AP。
1.2方法
1.2.1实验分组 所有大鼠在温度24 ℃、湿度50%左右的条件下饲养,喂以常规饲料,适应1周后,将其分为5组,每组20只。空白组(A组):每周腹腔内注射生理盐水1 mL/100 g。参照贾旭东等[5]方法建立动物模型,ACF对照组(B组):腹腔注射二甲基肼25 mg/kg及生理盐水1 mL/100 g,每周1次,连续12周;MIF抗体治疗ACF组(C组):腹腔注射二甲基肼25 mg/kg+生理盐水1 mL/100 g+MIF抗体400 μg/只,连续12周;大肠癌对照组(D组):腹腔注射二甲基肼25 mg/kg及生理盐水1 mL/100 g,每周1次,连续20周后;MIF抗体治疗大肠癌组(E组):腹腔注射二甲基肼25 mg/kg+生理盐水1 mL/100g + MIF抗体400 μg/只,连续20周。以上大鼠每周称体质量1次,并根据体质量改变生理盐水、二甲基肼剂量。
1.2.2大鼠ACF检查 实验第13周,选取A组大鼠10只及B、C组全部(n=20)大鼠用于ACF检查。10%水合氯醛麻醉,腹主动脉取血后断头处死大鼠,快速分离大肠并切下,参照BIRD[6]的方法固定标本和染色,用生理盐水冲洗肠内容物,将整根大肠铺平夹于两层滤纸之间,固定于100 mL/L中性缓冲甲醛溶液中,至少24 h。固定好的标本用2 g/L亚甲蓝染色3~5 min,立即在×40光学显微镜下观察并计数ACF数目。比较A、B、C 3组ACF数目变化。
1.2.3大鼠大肠癌检查 实验第21周,将A组剩余10只大鼠及D、E组全部(n=20)大鼠用10%水合氯醛麻醉,腹主动脉取血后断头处死,快速分离大肠并切下,纵向剖开,用生理盐水冲洗肠内容物,展开铺于玻璃板上,计算每只大鼠大肠肿瘤数目,最后用中性缓冲甲醛溶液固定。固定后,梯度乙醇脱水,石蜡包埋并5 mm切片,每组选取2张进行常规HE染色。
1.2.4ELISA及免疫组化检测 将各组血标本离心并取血液上清液,冻存于-80 ℃冰箱备用。在进行ELISA前将各组血液上清液复温,并按照ELISA试剂盒说明书检测MIF。将各组石蜡标本5 mm切片后,随机选取2张进行MIF免疫组化染色,严格按照说明书进行。以已知阳性结果作为阳性对照,PBS液作为阴性对照。

2 结 果
2.1MIF抗体对大鼠ACF的形成及大肠癌发生的影响 实验第13周,处死A组10只大鼠的大肠中无ACF形成,B、C组大鼠的大肠中均有ACF形成(图1A);B、C组大鼠的大肠ACF总数量分别为(115.20±14.12)、(52.40±7.35)个,C组的抑制率为54.50%,C组每只大鼠的大肠ACF总数量明显低于B组,两组比较差异有统计学意义(P<0.01)。实验第21周,处死A组10只大鼠的大肠中无大肠癌发生,D、E组大鼠的大肠中均有大肠癌形成(图1B);D组大鼠癌瘤总数目为27个,E组为14个;E组的抑制率为48.10%,与D组比较,E组的大鼠大肠癌发生率明显受抑制(P<0.01)。
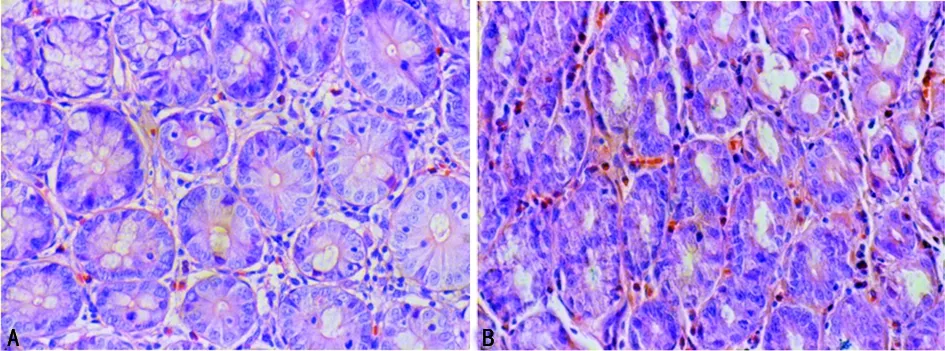
A:ACF;B:大肠癌
图1大鼠ACF及大肠癌形成HE染色(×40)
2.2MIF抗体对大鼠大肠癌癌变过程中MIF表达的影响 ELISA检测各组血清MIF表达水平,A、B、C、D、E组分别为(1.60±0.30)、(20.10±4.80)、(12.70±3.60)、(78.00±7.50)、(51.20±8.50)pg/mL;与A组比较,B、C、D、E组大鼠血清MIF表达水平均明显升高(P<0.01);B组MIF水平明显高于C组(P<0.01),D组MIF水平明显高于E组(P<0.01),D组MIF水平明显高于B组(P<0.01)。免疫组化法检测各组MIF表达,实验第13周,MIF在B、C组均有表达(图2A、B),且C组可明显抑制MIF表达;实验第21周,D组呈高表达(图2C),E组可明显抑制MIF表达(图2D),MIF在A组不表达(图2E)。
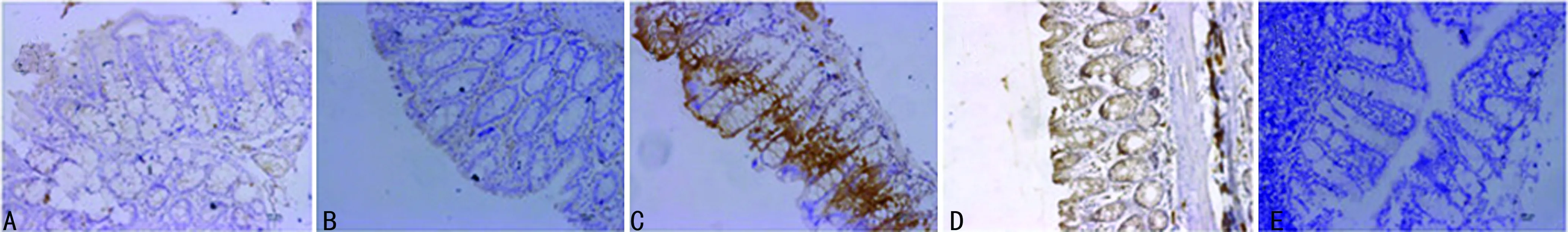
A:B组;B:C组;C:D组;D:E组;E:A组
图2免疫组化法检测各组大鼠MIF表达
3 讨 论
二甲基肼是一类经典的啮齿类致癌剂,在细胞、组织水平变化及肿瘤发生的分子机制方面与人类大肠癌癌变过程类似[7];自1987年BIRD[6]利用实体镜在大肠癌动物模型中首次发现了ACF,在随后一系列临床及动物研究中发现,ACF是大肠癌发病路径中,在显微镜下发现的最早的黏膜损伤,它的出现明显早于不典型增生及腺瘤,并在遗传、表观遗传、免疫组化和组织病理等方面的改变影响着肿瘤的发生,且ACF的数量与结直肠高危肿瘤[即直径1 cm及以上和(或)绒毛状、和(或)重度不典型增生、浸润癌]的发生有明显的相关性,因此它被称为最早的大肠癌前病变[8-9]。本实验证实了二甲基肼可诱导产生大鼠最早期癌前病变大肠ACF,并随用药时间增加建立大鼠大肠癌模型,这说明在大鼠大肠癌癌变过程中,ACF是目前最早发生的、显微镜下可见的最小的癌前病变,通过检测ACF数量可评价大肠癌癌变概率。
大肠肿瘤的发生、发展是一个多因素、多途径过程,目前,越来越多的研究集中于肿瘤微环境对肿瘤发生、发展的影响。MIF是1966年由BLOOM等[10]发现的一种淋巴因子,因其能减慢或抑制巨噬细胞的随机移动而得名,有激素样抗炎、免疫耐受的作用[11],近年来,发现MIF在结肠癌、肝癌、乳腺癌等多种肿瘤中的高表达,并通过信号通路CD74/CD44受体结合来活化细胞外信号调节ERK1/2 MAPK信号途径[12],并与CXCR2和CXCR4结合,抑制抑癌基因p53功能[3],发挥其在肿瘤增殖、分化等方面的作用。在大肠癌的相关研究中,目前已发现,向C26荷瘤小鼠注射抗MIF抗体后,可明显抑制肿瘤生长[13];在人正常大肠黏膜、大肠腺瘤和大肠癌组织及相应患者的血清中,MIF的表达依次增加,且与大肠癌的淋巴转移、肝转移密切相关[14]。因此,以MIF抗体作为大肠癌预防、治疗、防治转移及预后判断有着潜在的发展前景[15]。本实验研究发现,MIF抗体可以明显抑制ACF及大肠癌癌瘤数量,即在组织水平上说明了MIF抗体在大鼠从大肠癌早期癌至癌瘤形成的过程中发挥抑制作用。通过免疫组化和ELISA发现,大肠癌肠黏膜中MIF的表达明显高于早期癌变ACF模型肠黏膜的MIF表达,在一定意义上说明MIF参与了大肠癌癌变过程,应用MIF抗体后可明显抑制ACF和大肠癌模型中MIF的表达,在蛋白水平上进一步证实了MIF抗体在大肠癌癌变过程中的抑制作用。
综上所述,应用MIF抗体后能明显抑制ACF数量及大肠癌瘤体体积,并抑制MIF在血清及组织中的表达,这可能是MIF抗体能阻断大肠癌癌变的作用机制,在今后的研究中,需要在分子水平等方面进一步深入研究MIF抗体的作用机制,MIF可能会成为大肠癌早诊早治的新靶点。
[1]WARGOVICH M J,JIMENEZ A,MCKEE K,et al.Efficacy of potential chemopreventive agents on rat colon aberrant crypt formation and progression[J].Carcinogenesis,2000,(21):1149-1155.
[2]SEIKE K,KODA K,ODA K,et al.Assessment of rectal aberrant crypt foci by standard chromoscopy and its predictive value for colonic advanced neoplasms[J].Am J Gastroenterol,2006,101(6):1362-1369.
[3]JUNG H,SEONG H A,HA H.Critical role of cysteine residue 81 of macrophage migration inhibitory factor(MIF) in MIF-induced inhibition of P53 activity[J].J Biol Chem,2008,283(29):20383-20396.
[4]XU X D,WANG B,YE C S,et al.Overexpression of macrophage migration inhibitory factor induces angiogenesis in human breast cancer[J].Cancer Lett,2008,261(2):147-157.
[5]贾旭东,王伟,崔文明,等.饮茶对大鼠大肠变性隐窝病灶及大肠肿瘤的影响[J].卫生研究,2000,29(1):54-56.
[6]BIRD RP.Observation and quantification of aberrant crypts in the murine colon treated with a colon carcinogen:preliminary findings[J].Cancer Lett,1987,37(2):147-151.
[7]INAMINE M,SUZUI M,MORIOKA T,et al.Inhibitory effect of dietary monoglucosylceramide 1-O-beta-glucosyl-N-2′-hydroxyarachidoyl-4,8-sphingadienine on two different categories of colon preneoplastic lesions induced by 1,2-dimethylhydrazine in F344 rats[J].Cancer Sci,2005,96(12):876-881.
[8]CADERNI G,PEWELLI M G,CECCHINI F,et al.Enhanced growth of colorectal aberrant crypt foci in fasted/refed rats involves changes in TGF21 and P21CIP expressions[J].Carcinogenesis,2002,23(2):323-327.
[9]LUO L,SHEN G Q,STIFFLER K A,et al.Loss of heterozygosity in human aberrant crypt foci(ACF),a putative precursor of colon cancer[J].Carcinogenesis,2006,27(6):1153-1159.
[10]BLOOM B R,BENNETT B.Mechanism of a reaction in vitro associated with delayed-type hypersensitivity[J].Science,1966,153(3731):80-82.
[11]SUN B,NISHIHIRA J,SUZUKI M,et al.Induction of macrophage migration inhibitory factor by lysophosphatidic acid:relevance to tumor growth and angiogenesis[J].Int Moll Med,2003,12(4):633-641.
[12]BARON N,DEUSTER O,NOELKER C,et al.Role of macrophage migration inhibitory factor in primary glioblastoma multiforme cells[J].J Neurosci Res,2011,89(5):711-717.
[13]SHUN C T,LIN J T,HUANG S P,et al.Expression of macrophage migration inhibitory factor is associated with enhanced angiogenesis and advanced stage in gastric carcinomas[J].World J Gastroenterol,2005,11(24):3767-3771.
[14]何兴祥,李晓宇,郝元涛,等.巨噬细胞移动抑制因子与大肠癌肝转移的关系[J].中华普通外科杂志,2007,22(11):855-858.
[15]杨荣娇,王丽京,臧林泉,等.靶向巨噬细胞移动抑制因子的Sirna对小鼠大肠癌肝转移的影响[J].中华实验外科杂志,2011,28(9):1495-1497.
