个体化CT引导经皮肺穿刺对肺内占位病变活检的应用分析
2018-01-26张利锋张淑妙张占强庞志璐屈志刚
张利锋,张淑妙,韩 晶,张占强,庞志璐,屈志刚
(1.涿州市医院肿瘤科,涿州072750;2.保定市妇幼保健院妇瘤科,保定071000;3.涿州市医院呼吸内科,涿州072750;4.涿州市医院胸外科,涿州 072750)
CT引导经皮肺穿刺活检术近年来已广泛应用 于临床,是肺部占位性病变定性诊断中不可缺少的检查方法之一,对肺内占位病变的诊断及鉴别诊断具有重要的临床价值,以简便的方法获取病变组织从而为肺部恶性肿瘤临床治疗提供了必要的前提。在临床工作中根据具体患者及具体靶病灶自身特点,个体化选用适合的穿刺器械及引导方式能够进一步提高穿刺成功率,减少并发症的发生率。回顾自2012年5月-2016年12月共255例CT引导下经皮肺穿刺活检术的患者资料,按活检方式改进的时间节点分个体化前阶段及个体化后阶段,数据显示个体化后取材成功率明显提高、病理确诊率满意、并发症未增加,现总结报告如下。
1 资料与方法
1.1 一般资料 共255例患者,其中男性110例,女性145例,年龄32~82岁,平均48岁。靶病灶位于左肺130例,右肺113例,纵隔病变12例,其中肺外带172例,肺门部及纵隔病变83例。小于2.0 cm病灶 19 例,2.0~4.0 cm 病灶 59 例,4.0~6.0 cm 70 例,大于6.0 cm病灶107例。以上患者均不合并严重肺气肿、肺心病体位受限、严重出血倾向、不能控制的剧烈咳嗽、意识障碍不能配合等绝对穿刺禁忌证。1.2 术前准备 (1)严格掌握穿刺适应征及禁忌证。(2)血常规、术前感染筛查、出凝血时间等项目检测。(3)必要的呼吸功能训练、体位训练。大多数肺癌患者存在喘憋、咳嗽、气促、骨转移疼痛体位受限等症状,这些症状的存在对穿刺活检极为不利,甚至影响穿刺活检的进行,故在穿刺活检前需采取必要措施加以控制症状以确保穿刺活检顺利进行,如提前抗炎、化痰、镇咳、镇痛、抽取胸水及做好宣教鼓励患者予以配合等。(4)仔细分析现有影像学资料,提前规划靶病灶穿刺路径、规避脏器、大血管等。
1.3 活检方法 2012年5月-2014年5月期间活检病例102例,均使用16排螺旋CT引导,美国COOK公司生产的16G-18G同轴套管型半自动活检枪。2014年6月-2016年12月期间活检病例153例,穿刺前根据患者自身及靶病灶特点分为普通组及个体化组,凡符合(1)体型肥胖、胸壁厚(胸壁厚度大于 5 cm),(2)直径<2.0 cm 的小病灶,(3)中央型或纵隔病变,(4)与大血管关系密切病变,(5)靶病灶距离胸壁>10 cm,(6)需成角穿刺病例之一者为个体化组,对符合(1)、(2)者选用巴德全自动穿刺活检枪为主要条件,CT引导方式的选择为次要条件,如图 1a-d ;对符合(3)、(4)者在 CT 增强扫描引导下分步穿刺为主要条件,穿刺枪的选择为次要条件,如图1e-f;对符合(5)、(6)者选用COOK同轴套管型半自动活检枪并配合加用角度定位器为主要条件,CT引导方式的选择为次要条件,如图1g-h。

图1 肺内及纵隔占位病变穿刺活检CT影像
1.4 统计学分析 应用SPSS19.0统计软件对各组数据进行分析,计数资料采用χ2检验,以P<0.05表示差异有统计学意义。
2 结果
穿刺活检个体化前(2014年5月前)共102例,穿刺成功率为80.4%,总并发症发生率为25.4%,其中对符合个体化条件组穿刺成功率只有68.8%,详见表1。穿刺个体化后(2014年6月后)153例,成功取材137例,取材成功率达89.5%,总并发症为22.2%,其中个体化组穿刺成功率达92.6%,见表1、表2。
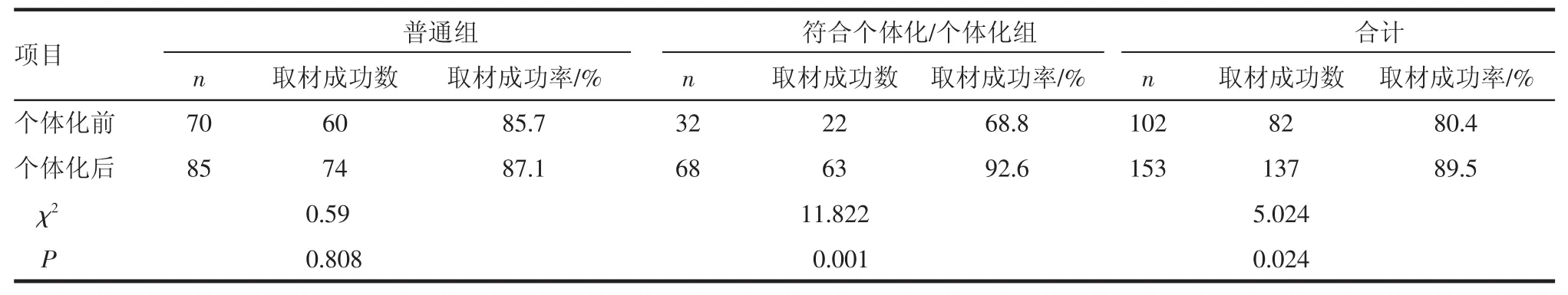
表1 穿刺活检个体化前后不同阶段不同组别取材成功率情况
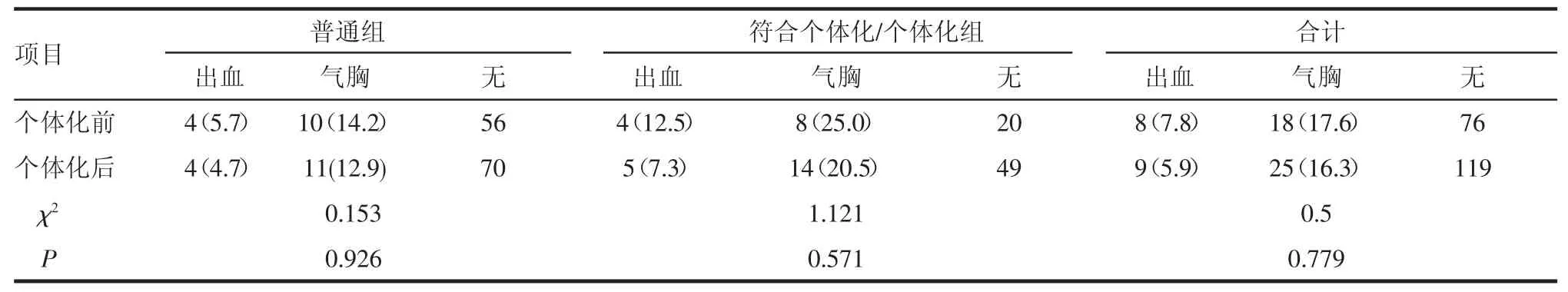
表2 穿刺活检个体化前后不同阶段不同组别并发症发生情况[n(%)]
3 讨论
3.1 CT引导经皮肺穿刺活检术的重要性 肺癌的发病率、死亡率近年来均居各类癌症首位,我国已成为名副其实的肺癌大国[1]。肺癌生物学特征较为复杂且具有较高的恶性程度,约80%的患者确诊时已为晚期,丧失了最佳治疗时机,其5年生存率不足15%[2]。随着近年来更多新药的研发、问世,更多新技术、新手段的采用,部分中晚期肺癌患者经过合理的精准治疗,生存期得到显著延长,合理的精准治疗需要明确的病理类型及分子生物学特征,病理是诊断的金标准。CT引导下经皮肺穿刺活检术是胸部介入放射学领域中重要的诊断技术,被公认为肺部疾病诊断及鉴别诊断的重要方法之一[3-4],是支气管镜检查的重要补充手段,其简便、微创、高效、安全,为肺恶性肿瘤的诊断及治疗提供重要支持。随着CT技术、病理检查技术和穿刺器械的不断改进,CT引导下经皮肺穿刺活检术的疾病诊断准确率也得到了大幅度提高[5],有报道称胸部疑难病灶穿刺活检诊断准确率为90%[6]。因每例患者的特殊性及靶病灶的不均一性势必存在一些难度大、危险性高、副损伤大的病例,如何在CT引导经皮肺穿刺活检这一成熟技术基础上进一步提高活检成功率,减少并发症发生率值得探讨。
3.2 个体化穿刺活检操作要点 (1)选取最利于穿刺且患者舒适的体位,因为只有患者给予配合才能
保证穿刺安全及取样成功。尽量垂直CT机床进针,这样更易把握进针距离和方向,提高穿刺成功率。(2)2%利多卡因逐层麻醉到胸膜,嘱患者屏气进针突破胸膜,但不要停留,以免患者呼吸时针尖线性划伤脏层胸膜。(3)一般选取2步到3步法进针至病灶边缘,如靶病灶距胸膜位置较深调整穿刺针方向时不要退出脏层胸膜外,以免反复穿透胸膜造成气胸,如靶病灶位于胸膜下调整进针方向时需退至胸膜外,勿在胸膜腔内调整进针方向。(4)可能情况下,尽可能经不张的肺组织进针而不经过正常肺组织可大大降低气胸的发生率[7]。(5)穿刺激发时手要稳,切割取材后退针要平顺。
3.3 个体化穿刺活检“因地制宜”提高活检成功率 个体化前在对体型肥胖、胸壁厚、胸壁肌肉发达的患者采用COOK活检枪切割取材时虽定位准确但常出现获取组织偏少或失败现象,分析其原因为COOK活检枪枪内簧细,激发后外套切割速度及力量偏低导致切割受阻取材失败;另针对肺内<2.0cm的病灶因靶病灶小,周围肺组织对其支撑力偏低而病灶又相对肺组织偏硬,使用COOK活检枪穿刺时需手动将针内芯推入靶病灶内然后激发针套前行切割,因该枪为半自动设计,缺点为手动推针芯速度偏慢,故常在推动针芯进入病灶时靶病灶被针芯顶偏在一侧,最终导致取材失败。活检个体化后针对符合上述条件病例首要条件为采用巴德全自动活检枪,该枪全自动设计,不需手动推针芯穿刺,弹射速度快、切割力量大、所切取组织完整,对符合上述条件患者尤为适用。肺中央型病变或纵隔病变由于位置较深且邻近肺门,穿刺的风险始终是无法回避的[8],个体化前对上述病例穿刺前常规参阅已有的增强CT片以观察靶病灶与肺门部血管、支气管的关系,而实际活检操作时均在平扫下进行,理论上可以按事先规划好的穿刺路径穿刺,规避肺门大血管及其分支、属支,穿刺活检时需在穿刺体位下重新定位、扫描,且由于体位、扫描条件、层厚均有可能不同,所得图像不能完全吻合,平扫信息量有限,肿块紧邻肺门部大血管及分支难以清楚显示区分,针尖方向,深度稍有偏差便可损伤血管导致出血进而导致穿刺失败。个体化后针对中央型病变及纵隔病变选择在CT增强扫描下分步进针穿刺,可有效规避大血管分支及属支,降低出血风险,提高活检成功率。针对靶病灶距离胸壁>10 cm及不能垂直进针的成角穿刺病例因皮肤定位进针点到靶病灶(靶点)距离偏远或最佳穿刺路径有肋骨、肩胛骨等遮挡需头脚、左右方向成角穿刺,徒手进针势必难以准确把握进针方向,而反复穿刺胸膜调整进针方向势必导致气胸发生率上升,一旦发生气胸则靶病灶相对位置改变,直接导致穿刺失败。进针次数与并发症呈正相关,避免不必要的多次进针,减少胸膜的损伤,能降低气胸发生[9]。个体化后针对上述病例首选COOK活检枪加角度定位器,活检时先用内针芯插入针套然后与角度定位器一并组合,组合后调整角度定位器进针长轴、皮肤进针点、靶点于一条直线上在CT引导下穿刺进针,当针尖到达靶病灶边缘时拆除角度定位器并退出针芯保持活检针外套不动,再插入穿刺枪手动推内芯激发取材。3.4 并发症及处理 气胸和出血是CT引导下经皮肺穿刺活检术最常见的并发症,其他并发症相对少见,如心包填塞、纵隔积气、空气栓塞和肿瘤播散种植等。研究表明,气胸和出血的发生与患者年龄、穿刺针的粗细、穿刺次数、穿刺部位、病灶大小、是否合并肺气肿、操作时间及操作者的熟练程度等有着密切的联系[10]。多中心系列报告显示肺活检穿刺后气胸发病率可达到27%~54%[11],其中大多数病例不需要处理,然而3%~15%的患者有持续增加的趋势,需要进行胸腔闭式引流[12];穿刺后肺出血的发生率大约 29%,而咯血只有 1.2%~5.0%[13-14],发生小量咳血时需予以镇静、止血治疗,发生大咯血时应立刻患侧卧位,防止血块引发窒息,应用垂体后叶素静点,予以药物止血等积极治疗措施。气胸大多发生在穿刺活检时或活检后1 h左右,但有个别病人会发生迟发性的气胸,我们在日常工作中应引起高度重视。文献报道年龄>60岁的患者多存在肺部病变如肺气肿、肺大泡、慢阻肺等,在穿刺过程中可能会增加气胸发生的可能性,穿刺路径越短则出现出血或咯血的情况会越少,这可能与穿刺针遇到血管的多少有关,穿刺深度越大则损伤的血管就越多,导致出血的概率就会增加[15]。另外在穿刺过程中要严格执行无菌操作。
综上所述,在临床工作中针对不同患者及靶病灶特点个体化选用不同特点穿刺器械及引导方式,术前评估客观准确,术中运用娴熟的穿刺技巧,术后仔细观察,出现并发症时处理快速准确,必然能进一步提高穿刺活检成功率并减少并发症的发生。
[1]中华医学会呼吸病学分会肺癌学组中国肺癌防治联盟.原发性支气管肺癌早期诊断中国专家共识(草案)[J].中华结核和呼吸杂志,2014,3(3):131
[2]杨浩.CT引导下经皮肺穿刺活检术在周围型肺癌诊断中的价值[J].基层医学论坛,2015,19(14):1942
[3] 周康荣.胸部颈面部CT[M].上海:上海医科大学出版社,1996:420
[4] 姚海泉,胡智斌,张鹏,等.CT导引下自动活检枪经皮肺穿刺活检的临床应用[J].中国中西医结合影像学杂志,2012,10(2):148
[5] 莫春明.CT引导下经皮肺穿刺活检术影响因素分析[J].中外医学研究,2013,11(14):51
[6] 陈良安,杨震,王平.肺癌早期诊断的新方法与评价[J].中华结核和呼吸杂志,2012,35(2):83
[7] Lima C D,Nunes R A,Saito E H,et a1.Results and complications of CT-guided transthoracic fine·needle aspirationbiopsy of pulmonary lesions[J].J Bras Pneumol,2011,37(2):209
[8] 王挺,赵振华,余月芳.CT导向下经中央型病变穿刺活检[J].放射学实践,2010,25(11):1279
[9] 贾丽涛,时高峰,李扬,等.CT引导下经皮肺穿刺活检并发症的预防及处理[J].河北医药,2016,38(13):2075
[10]刘斌,张洪,李月川.增强CT引导下经皮肺穿刺活检术的应用研究[J].天津医药,2015,4(34):429
[11]Collings C L,Westcott J L,Banson N L,et al.Pneumothorax and dependentversus nondependentpatientposition afterneedle biopsyof the lung[J].Radiology,1999,210(1):59
[12]Wu C C,Maher M M,Shepard J A.Complications of CT-guided percutaneousneedle biopsyof the chest:prevention and management[J].AJR Am J Roentgenol,2011,196(6):678
[13]Lucidarme O,Howanh N,Finet J F,et al.Intrapulmonary lesions:Percutaneous automateed biopsy with a detachabie,18-gauge,coaxialcutting needle[J].Radiology,1998,207(3):759
[14] ManhireA,CharigM,Clelland C,etal.Guidelinesfor radiologicallyguided lung biopsy[J].Thorax,2003,58(11):920
[15]蒋杨,潘江锋,董科,等.CT引导下经皮肺穿刺活检的临床应用及其并发症影响因素[J].中国医师导报,2014,11(18):52
