磷酸西他列汀片的质量控制
2018-01-26张金芬周禹宏李继彬邢正英房志仲
张金芬,周禹宏,李继彬,邢正英,房志仲
(天津医科大学药学院,天津市临床药物关键技术重点实验室,天津300070)
糖尿病(diabetes mellitus,DM)是一种以慢性高血糖为特征的代谢紊乱性疾病,可累及全身各个系统,诱发严重的并发症,危害人体健康。其中,90%以上为 2 型糖尿病(type 2 diabetes mellitus,T2DM)[1-2]。研究表明,2型糖尿病的发病呈逐渐加重的流行趋势[3]。传统的治疗2型糖尿病的药物主要为双胍类药物二甲双胍、磺脲类药物格列本脲、TZD类药物罗格列酮、格列奈类药物瑞格列奈等,其副作用如体质量减轻、低血糖、恶心呕吐、水肿等限制了其在临床上的使用[4]。故开发和研究新型抗糖尿病药物对治疗糖尿病具有重要意义。近年来,随着人类对糖尿病发病机制的深入研究,发现了一些具有降血糖作用的新靶点[5-6],二肽基肽酶-4(DPP-4)即为其中1种,DPP-4可使具有血糖下调作用的胰升糖素样肽-1(GLP-1)及糖依赖性胰岛素释放肽(GIP)裂解失活,随之研发出的DPP-4抑制剂可通过选择性地抑制DPP-4,减少二者在体内的失活,延长内源性的GLP-1及GIP的活性作用时间,促进胰岛B细胞分泌胰岛素的同时降低胰高血糖素的浓度,通过双途径发挥降血糖的作用。磷酸西他列汀为首个治疗2型糖尿病的DPP-4抑制剂[7],近年来广泛用于治疗2型糖尿病[8]。已有研究表明,磷酸西他列汀治疗2型糖尿病效果十分理想[9-10]。作为一种新型抗糖尿病药物,磷酸西他列汀具有血糖依赖性,降糖作用适中,在增加胰岛素分泌的同时不会发生低血糖,有效减轻饥饿感等优势,且无恶心呕吐、水肿及增加体质量等副作用[11-14]。本课题对自制的磷酸西他列汀片进行了质量控制方面的研究,摸索高效液相色谱法条件,建立自制制剂中主药的质量控制方法。同时参照欧洲药典[15],建立磷酸西他列汀片溶出度的有效测定方法。
1 材料与方法
1.1 试药 供试品:磷酸西他列汀片(自制);参比制剂:磷酸西他列汀片(捷诺维®杭州默沙东制药有限公司,批号:L030511);对照品:磷酸西他列汀(武汉远程共创科技有限公司,批号:20160808);甲醇(天津康克德科技有限公司,色谱纯);其他试剂均为市售分析纯;蒸馏水(自制)。
1.2 仪器 高效液相色谱仪(美国Spectra-Physics);柱温箱(Model100,天津市威仪科技发展有限公司);Anastar色谱工作站(天津奥特赛恩斯仪器有限公司);RCZ-8A智能溶出仪(北京宏昌信科技有限公司);电子分析天平(天津博达宏力科技发展有限公司);80-2B型台式离心机(苏州裕宸仪器有限公司);TS-6A型超声波清洗器(常州华冠仪器有限公司);酸度计PHS-25(上海精密科学仪器有限公司);U-3310分光光度计(天美科技有限公司TECHCOMPLIMITED)。
1.3 方法
1.3.1 色谱条件 TIANHE®KromasilC18色谱柱(200 mm×4.6 mm,5 μm);流动相为甲醇-0.1%HClO4=45∶55;检测波长 λ=205nm;流速为 0.8mL/min;柱温为25℃;进样量20 μL。
1.3.2 溶液制备 (1)对照品溶液的制备:精密称取磷酸西他列汀对照品12.87 mg至50 mL量瓶中,加入流动相溶解并定容,摇匀即得储备液;精密量取2 mL上述储备液置于10 mL量瓶中,流动相稀释并定容,摇匀即得磷酸西他列汀对照品溶液。(2)供试品溶液的制备:取3片自制样品研磨均匀,精密称取99.61 mg至50 mL量瓶中,流动相超声溶解后定容,摇匀;2 000 r/min离心5 min,上清液采用微孔滤膜过滤,精密移取续滤液2 mL至10 mL量瓶中,流动相稀释并定容,摇匀,即得供试品溶液。(3)阴性对照品溶液的制备:按照自制制剂处方制备不含磷酸西他列汀的空白制剂,按照上述供试品溶液的制备方法制成阴性对照品溶液。
1.3.3 专属性试验 分别吸取“1.3.2”项下配制的对照品溶液及阴性对照品溶液各20 μL进样,按照“1.3.1项下”的色谱条件进行测定并记录色谱图。
1.3.4 线性关系考察 精密称取磷酸西他列汀对照品64 mg至100 mL量瓶中,适量流动相超声溶解后稀释至刻度,摇匀,即得0.64 mg/mL的磷酸西他列汀对照品储备液;使用移液管精密量取上述对照品储备液 0.1、0.7、0.9、1.0、1.1、1.3 和 1.5 mL 至 10 mL量瓶中,流动相稀释至刻度,摇匀,即得6.4、44.8、57.6、64、70.4、83.2 和 96 μg/mL 的对照品溶液。取上述溶液20 μL,按照“1.3.1项下”的色谱条件进行测定并记录其色谱图,对其峰面积进行线性回归。
1.3.5 精密度试验 (1)重复性试验:按照“1.3.1项下”供试品溶液的制备方法对同一批样品进行处理得到样品溶液,重复进样6次,按照“1.3.1项下”色谱条件进行测定,计算峰面积的RSD。(2)中间精密度:在不同的检查日期,采用不同的分析仪器,不同的试验人员,按照“重复性试验”方法测定,计算峰面积的RSD。
1.3.6 稳定性试验 取“1.3.2项下”配制的对照品溶液,分别于第 0、4、8、12、24 h 进样,按照“1.3.1 项下”色谱条件进行测定,计算峰面积的RSD。
1.3.7 准确度试验 (1)对照品储备液的配制:精密称取磷酸西他列汀对照品64 mg至100 mL量瓶中,适量流动相超声溶解后定容,摇匀,静置待用;(2)全辅料储备液的配制:将辅料(5片量)按照处方比例混合均匀,取285 mg至100 mL量瓶中,流动相超声溶解后定容,摇匀,离心,取上清液,静置待用;(3)分别精密量取上述全辅料储备液1.0 mL,再分别量取上述对照品储备液0.8、1.0和1.2 mL置10 mL量瓶中,流动相稀释至刻度,摇匀,即得80%、100%、120%的回收率待测溶液;按照“1.3.1项下”色谱条件进样,每个浓度平行测定3次,记录色谱图,计算主药的加入浓度与检验浓度,并求出回收率。
1.3.8 含量测定 根据“1.3.2项下”供试品溶液的制备方法对自制的3批样品进行处理得到样品溶液,进样,按照“1.3.1项下”色谱条件进行测定,采用外标一点法计算磷酸西他列汀浓度。
1.3.9 溶出度测定
1.3.9.1 溶出介质的配制:蒸馏水煮沸脱气;0.01mol/L HCl:取0.9 mL浓盐酸至1 000 mL纯水中,搅拌使混合均匀,即得;PBS4.5:精密称取磷酸二氢钾7.8g于适量纯水中,超声使其完全溶解后,加纯水至1 000mL,搅拌使均匀,即得;PBS 6.8:分别精密称取磷酸二氢钾6.804 5 g、氢氧化钠0.944 g于适量纯水中,超声使其完全溶解后,加纯水至1 000 mL,搅拌使均匀,即得。
1.3.9.2 溶出度测定方法及线性关系考察:分别精密称取磷酸西他列汀12.87 mg至4个100 mL量瓶中,纯水、0.01 mol/L HCl、PBS 4.5、PBS 6.8 分别作溶剂,超声使溶解完全,定容,摇匀,即得对照品储备液;分别精密量取上述对照品储备液0.5、0.7、0.9、1.0、1.1、1.3和1.5 mL至10 mL量瓶中,各溶剂稀释并定容,摇匀,按照紫外分光光度法,于205 nm波长下测定其吸光度,平行测定3次,记录其吸光度,对其吸光度进行线性回归。
1.3.9.3 对照品溶液的配制:分别精密量取“1.3.9.2”项下4种对照品储备液各1 mL至10 mL量瓶中,各溶剂稀释并定容,摇匀,按照紫外分光光度法,于205 nm波长下测定其吸光度,平行测定3次,记录其吸光度。
1.3.9.4 参比制剂溶出度测定:取磷酸西他列汀片4片,分别记录其片重,按照《中国药典》四部附录溶出度测定Ⅰ法,采用浆法,50 r/min,温度:(37±0.5)℃,分别以纯水、0.01 mol/L HCl、PBS 4.5、PBS 6.8 各 1 000 mL 为溶出介质,于第 5、10、15、20、30、45和60 min取溶出液10 mL,过滤,取续滤液1 mL至10 mL量瓶中,溶出介质稀释并定容,按照紫外分光光度法,于205 nm波长下测定其吸光度,平行测定3次,记录其吸光度值,同时补加等量恒温介质;按对照品溶液的浓度及吸光度值计算参比制剂各时间点的取样浓度及累积溶出度,绘制累积溶出度曲线。
1.3.9.5自制制剂溶出度测定:取自制制剂4片,分别记录其片重,按照《中国药典》四部附录溶出度测定Ⅰ法,采用浆法,50 r/min,温度:(37±0.5)℃,分别以纯水、0.01 mol/L HCl、PBS 4.5、PBS 6.8 各 1 000 mL为溶出介质,于第 1、3、5、10、15 和 60 min 取溶出液10 mL,过滤,取续滤液2 mL至10 mL量瓶中,溶出介质稀释并定容,按照紫外分光光度法,于205 nm波长下测定其吸光度,平行测定3次,记录其吸光度值,同时补加等量恒温介质;按对照品溶液的浓度及吸光度值计算自制制剂各时间点的取样浓度及累积溶出度,绘制累积溶出度曲线,计算自制制剂与参比制剂的累积溶出度相似因子f(2)。
2 结果
2.1 专属性试验色谱图 见图1。在“1.3.1项下”的色谱条件下,主药色谱图不受辅料影响,表明采用该色谱条件进行含量测定时专属性良好。
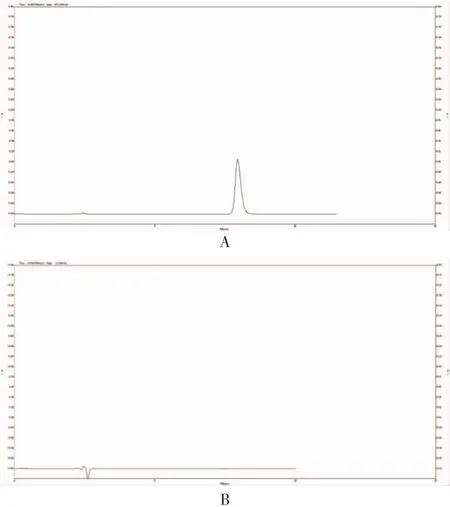
图1 专属性试验Fig 1 Specific test
2.2 线性关系考察结果 以磷酸西他列汀的峰面积(A)对浓度(C)作线性回归的标准曲线,得到线性方程为 A=22968.4427C-3504.03,r=0.999 8,表明磷酸西他列汀浓度在6.4~96 μg/mL的浓度范围内,其浓度与峰面积呈良好的线性关系。
2.3 精密度试验结果 磷酸西他列汀重复性试验的RSD为0.94%(n=6);中间精密度试验的RSD为0.77%(n=6),表明精密度良好。
2.4 稳定性试验结果 磷酸西他列汀稳定性试验的RSD为0.60%,表明磷酸西他列汀在24 h内稳定性良好。
2.5 回收率试验结果 如表1所示,自制磷酸西他列汀片中西他列汀的平均回收率为100.74%,RSD为0.46%,符合要求。
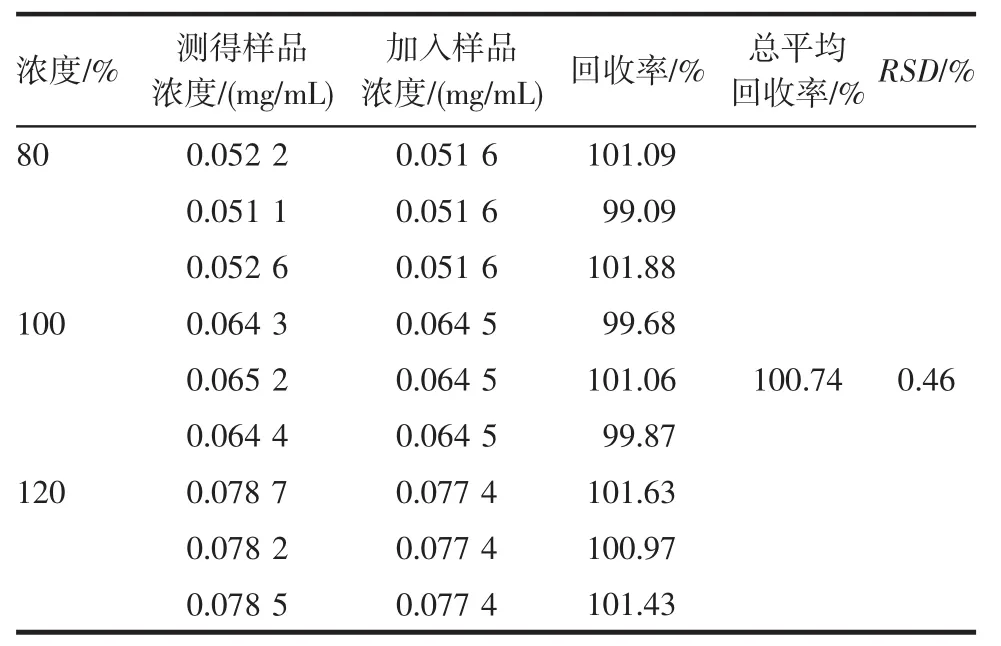
表1 磷酸西他列汀的回收率试验Tab 1 The recovery tests of sitagliptin phosphate
2.6 含量测定结果 3批样品中磷酸西他列汀的含量测定结果见表2。
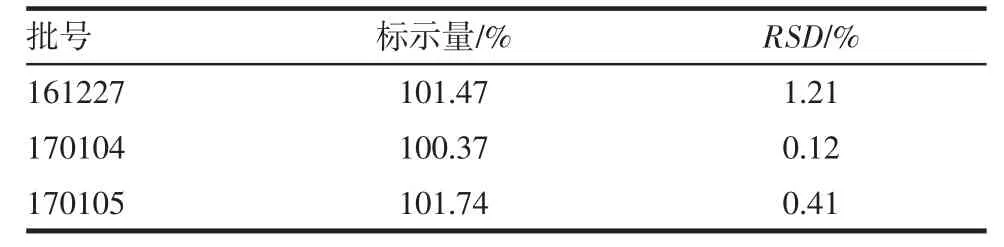
表2 磷酸西他列汀的含量测定结果Tab 2 Content determination of sitagliptin phosphate
2.7 溶出度试验结果
2.7.1 线性考察结果 分别以磷酸西他列汀的吸光度(Abs)对浓度(C)作线性回归的标准曲线,得到4个线性方程分别为:水,y=42.8286x+0.0340,r=0.9995;HCl,y=37.9714x+0.1086,r=0.999 6;PBS 4.5,y=41.9286x+0.0417,r=0.999 8;PBS 6.8,y=42.3429x+0.0450,r=0.999 9。表明磷酸西他列汀浓度在5~15 μg/mL的浓度范围内,其浓度与吸光度呈良好的线性关系。
2.7.2 累积溶出度曲线 绘制自制磷酸西他列汀片与参比制剂在4种溶出介质中的溶出曲线,计算累积溶出度,结果见图2~5。自制制剂与参比制剂的累积溶出度在4种溶出介质中的相似因子f(2)分别为64、87、63、59,均大于 50。表明自制制剂与参比制剂具有相似的溶出行为,自制制剂溶出良好。
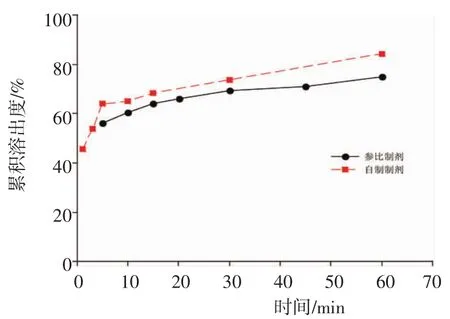
图2 自制磷酸西他列汀片与市售磷酸西他列汀片在水中的溶出曲线Fig 2 The dissolution profile of sitagliptin phosphate tablets and control agents in H2O
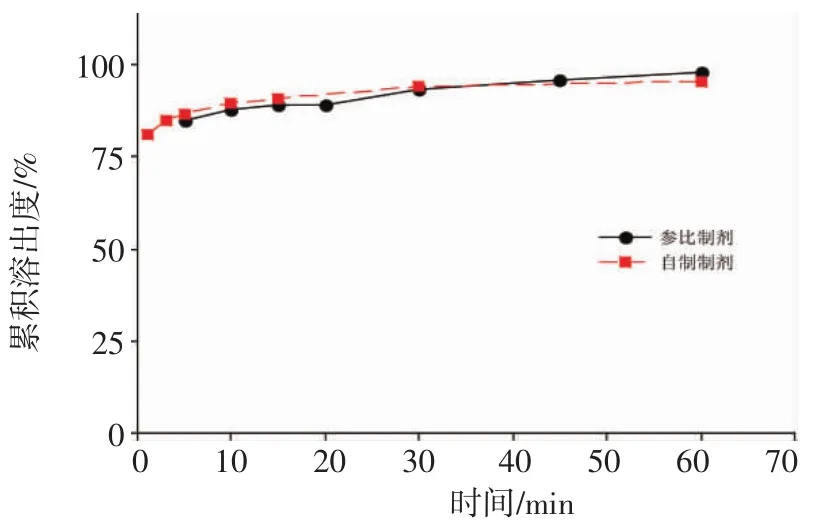
图3 自制磷酸西他列汀片与市售磷酸西他列汀片在0.01 mol/L HCl中的溶出曲线Fig 3 The dissolution profile of sitagliptin phosphate tablets and control agents in 0.01 mol/L HCl
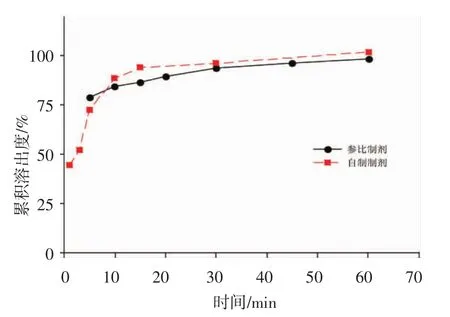
图3 自制磷酸西他列汀片与市售磷酸西他列汀片在PBS4.5中的溶出曲线Fig 3 The dissolution profile of sitagliptin phosphate tablets and control agents in PBS 4.5
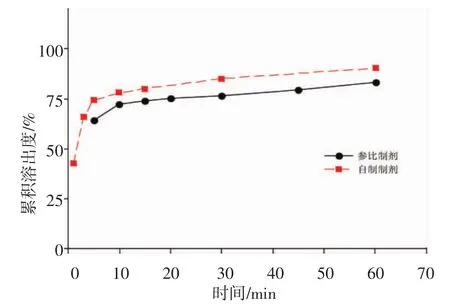
图4 自制磷酸西他列汀片与市售磷酸西他列汀片在PBS6.8中的溶出曲线Fig 4 The dissolution profile of sitagliptin phosphate tablets and control agents in PBS 6.8
3 讨论
3.1 色谱条件的筛选 经查阅欧洲药典及美国药典[16]得到磷酸西他列汀含量测定的色谱条件为:流动相乙腈-1.36 g/L磷酸二氢钾-磷酸缓冲液(磷酸调 pH 为 2.0)(15∶85),流速 1.0 mL/min,柱温 30 ℃,检测波长为205 nm。考虑到此流动相其盐溶液部分pH为2.0过酸,可能会对色谱柱损害,故不予考虑。查阅相关文献[17]得磷酸西他列汀含量测定的色谱条件为:甲醇-0.1%高氯酸 (32∶68),流速1.0 mL/min,柱温30℃,检测波长268 nm。将磷酸西他列汀对照品在上述色谱条件下进行进样分析,其主峰保留时间约30 min,保留时间过长,多次更改甲醇-0.1%高氯酸比例及流速调整主峰保留时间,考察柱温对色谱峰的影响,同时将磷酸西他列汀对照品按照紫外分光光度法在200~350 nm波长范围内进行全波长扫描,确定其最大吸收波长。最终得到磷酸西他列汀含量测定的色谱条件为:流动相甲醇-0.1%高氯酸(45∶55),流速 0.8 mL/min,柱温为 25 ℃,检测波长为205 nm。
3.2 供试品溶液的制备方法 试验中我们调整甲醇-0.1%高氯酸比例制备供试品溶液,按照上述色谱条件于0、4、8、12和24 h进样,观察其主峰峰面积变化,考察其稳定性,发现磷酸西他列汀在甲醇-0.1%高氯酸任何比例的溶液中都较稳定,其RSD值均小于2.0%,且进样分析时色谱峰峰形好。为方便实验操作,故采用流动相作为磷酸西他列汀稀释液溶解药品。
3.3 溶出方法的选择 经查阅欧洲药典得磷酸西他列汀片的溶出方法为:转速50 r/min,溶出介质0.01 mol/L HCl(1 000 mL),溶出时间30 min。查阅其他相关资料得磷酸西他列汀片的溶出方法为:转篮法,转速100 r/min,溶出介质水(900 mL),溶出时间30 min。为了更好地考察磷酸西他列汀在不同pH条件下的溶出行为,我们采用水、0.01 mol/L HCl、PBS4.5及PBS6.8作为4种溶出介质;考虑到人体胃肠道的生理环境及蠕动速度,拟定转速为50r/min。最终得到磷酸西他列汀片的溶出方法为:浆法,转速 50 r/min,溶出介质水、0.01 mol/L HCl、PBS4.5 及PBS6.8(1 000 mL),溶出时间 60 min。
3.4 溶出样品溶液的配制 为使试验操作简便易行,试验中我们采用紫外分光光度法进行溶出样品溶液的测定。由于采用紫外分光光度法测定样品溶液的吸光度时,以样品溶液的吸光度度数在0.3~0.7之间为宜,试验中我们通过尝试确定将溶出样品溶液的浓度稀释5倍,使其吸光度度数在0.3~0.7之间。
[1] American Diabetes Association.Diagnosis andclassification of diabetes mellitus[J].Diabetes Care,2013,36(Suppl 1):S67
[2] 胡洁,安富荣.西格列汀治疗2型糖尿病的临床研究进展[J].医药导报,2013,32(6):760
[3] 汪会琴,胡如英,武海滨,等.2型糖尿病报告发病率研究进展[J/OL].浙江预防医学,2016,28(1):37
[4] 万科,蒋世茂.2型糖尿病患者药物治疗的研究进展[J].临床合理用药杂志,2017,10(19):166
[5] 王小彦,王玉丽,徐为人.近几年治疗糖尿病热点靶点的研究进展[J].药物评价研究,2012,35(1):42
[6] 刘永贵,解学星,吴疆,等.治疗2型糖尿病的新靶点药物研究进展[J].现代药物与临床,2015,30(2):222
[7] 许菁,王玉丽,徐为人,等.治疗2型糖尿病的新型药物西他列汀[J].中国药物与临床,2007,7(11):861
[8] Aune T,Norat P,Romundstad L J,et al.Breastfeeding and the maternal risk of type 2 diabetes:A systematic review and doseresponse meta-analysis of cohort studies[J].Nutr Metab Cardiovasc Dis,2014,24(2):107
[9] 张鹏.磷酸西格列汀在2型糖尿病中的应用研究[J].中国现代药物应用,2017,11(13):105
[10]向群.西格列汀治疗2型糖尿病的效果观察[J].临床合理用药杂志,2017,10(8):37
[11]Barnett A.DPP-4 inhibitors and their potential role inthe management of type 2 diabetes[J].J Clin Pract,2006,60(11):1454
[12]Van C,Dyck K,Yi B,et al.Single dose of MK-0431,an inhibitorof dipeptidyl peptidase-IV,raise active GLP-1 levels without causinghypoglycaemia in healthy subjects[J].Diabetes,2005,54:493
[13]Herman G,Hanefeld M,Wu M,et al.Effect of MK-0431,a dipeptidyl peptidaseⅣ (DPPⅣ)inhibitor,on glycaemic control after 12 weeks in patients with type 2 diabetes[J].Diabetes,2005,54:541
[14]Nauck M A,Meininger G,Sheng D,et al.Efficacy and safety of thedipeptidyl peptidase-4 inhibitor,sitagliptin,comparedto the sulphonylurea glipizide in patients with type 2diabetes inadequately controlled on metformin alone:a randomised,double-blind,noninferiority trial[J].Diabetes Obes Metab,2007,9(2):194
[15]欧洲药典论坛.Pharmeuropa 26.3[S].2014:357
[16]美国药典.United States Pharmacopoeia[S].2016:5852
[17]孙旭,汤瑶,闻镍,等.RP-HPLC法测定人血浆中磷酸西他列汀药物含量[J].中国药事,2009,23(8):758
