心脏超声参数积分系统对慢性左心室收缩功能减低心力衰竭患者一年再入院的风险评估
2017-12-21翟春晓王晓军余永明王艺丹徐良栋丛晓申晓倩李虹梁英郝恩魁
翟春晓,王晓军,余永明,王艺丹,徐良栋,丛晓,申晓倩,李虹,梁英,郝恩魁
临床研究
心脏超声参数积分系统对慢性左心室收缩功能减低心力衰竭患者一年再入院的风险评估
翟春晓,王晓军*,余永明,王艺丹,徐良栋,丛晓,申晓倩,李虹,梁英,郝恩魁
目的: 本研究旨在建立并使用心脏超声参数积分系统(超声积分系统)对慢性左心室收缩功能减低(LVSD)心力衰竭(心衰)患者进行1年再入院风险评估。 方法: 收集并整理我院2007-01至2016-01期间连续9年慢性LVSD患者412例,以1年内再入院为本研究终点。412例患者常规超声心动图检查数据包括 2007-01至2014-12用于建立超声积分系统280例,2015-01至2016-01用于超声积分系统的验证132例。依据采集的7项指标并分组:(1)左心室内径: 0 组(n=290)和1 组(n=122);(2)二尖瓣反流: 0 组(n=203)、1 组(n=138)和 2 组(n=71);(3)三尖瓣反流: 0 组(n=302)、1 组(n=90)和 2 组(n=20);(4)LVEF: 0 组(n=272)和 1 组(n=140);(5)肺动脉收缩压: 0 组(n=282)和 1 组(n=130);(6) 心包积液: 0 组(n=347 )和1 组(n=65);(7)胸腔积液: 0组(n=261)、1组(n=86)和2组(n=65)。使用COX回归分析对超声参数进行筛查,并通过风险因子(HR)计算超声积分系统权重值,利用超声积分系统对LVSD患者1年内再入院进行分析,并与传统超声参数进行受试者工作特征(ROC)曲线分析比较。最后通过验证数据集对超声积分系统进行验证。 结果:超声积分系统分值如下:左心室内径>60 mm=1分,三尖瓣反流1组=1分,三尖瓣反流2组=3分,二尖瓣反流1组=2分,二尖瓣反流2组=4分,胸腔积液1组=2分,胸腔积液2组=3分,心包积液=1分。超声积分系统COX回归分析发现,不同组间LVSD患者1年内再入院率的HR分别为1.552、3.347、4.562,组间比较差异有统计学意义(P<0.05)。超声积分系统的预测能力采用ROC曲线下面积(AUC)进行评价(建模数据: 70.0%,95%CI:0.640~0.761;验证数据:70.4%,95%CI:0.616~0.792),最佳积分阈值为 4 分。 结论:超声积分系统能够很好的预测LVSD患者 1年再入院风险,并优于传统单项超声参数。
超声心动描记术;心室功能障碍,左; COX回归分析
(Chinese Circulation Journal, 2017,32:1194.)
心力衰竭(心衰)是各种心脏疾病的终末阶段,左心室收缩功能减退(LVSD)是心衰最常见病因(约占60%),随着我国人口老龄化, LVSD心衰的患病率逐年上升,预后差和再入院率较高,反复再入院占据了大量的医疗资源,给家庭及社会带来了沉重的经济负担[1]。有研究表明,慢性心衰30天、1年的再入院率分别为22%、63%,防止高频再入院可改善患者预后及控制医疗成本[2,3]。有研究提出临床积分系统,有助心衰早期诊断、预后评估,但大多数指标为主观指标[4,5]。与临床其他指标相比,心脏超声参数是客观、量化、稳定的指标,对LVSD心衰患者的预后及长期再入院预测有更好的作用。超声心动图现已成为预测、管理LVSD心衰患者的一项重要手段[6,7]。本研究旨在通过建立心脏超声参数积分系统(超声积分系统)分析和预测LVSD心衰患者1年再入院风险。
1 资料与方法
临床资料: 选取2007-01至2016-01我院因LVSD心衰急性发作入院患者433例,其中失访21例,共随访412例(95.15%),以 1 年内再次心衰入院作为终点,共225例患者发生终点事件。以2007-01至2014-12的280例患者用于建立超声积分系统[其中男性160例(57%),平均年龄(69±12)岁,1年内再入院156例(56%)]。以2015-01至2016-01的132例患者用于超声积分系统的验证[其中男性72例(55%),平均年龄(71±13)岁,1年内再入院69例(52%)]。
纳入标准:(1)患者因心衰急性发作入院,符合典型心衰症状的临床表现; (2)左心室射血分数(LVEF)<50%;(3)诊断为缺血性心肌病或扩张性心肌病。
排除标准:(1)其后发生了急性心肌梗死;(2)急性心肌炎、先天性心脏病、酒精性心脏病、慢性阻塞性肺疾病;(3)心脏瓣膜病;(4)原发性心包积液。入院后行常规生化血液检查,超声心动图检查于病情稳定3天后进行。412例患者在随诊1年时,发生再入院的纳入和排除标准同前。
治疗方法:根据美国心脏病学会(ACC)/ 美国心脏协会(AHA)美国 2007 年心衰指南为治疗方案。院内治疗:以强心苷类药物、利尿剂和血管活性药物为主, 同时应用血管紧张素转换酶抑制剂(ACEI)/血管紧张素Ⅱ受体拮抗剂(ARB)、β 受体阻滞剂和螺内酯,保持水电解质稳定,配合支持疗法,如果合并感染,配合使用药敏试验的抗生素,治疗时间为7~10 天。院外治疗:药物为主,如洋地黄、利尿剂、螺内酯、ACEI/ARB 和 β 受体阻滞剂,2~4 周门诊复查。
超声心动图检查及分组:412例患者入院后,症状初步缓解后3天行超声心动图检测 , 采集的7项指标及分组:(1)左心室内径:①0 组(n=290):左心室内径≤ 60 mm;② 1 组(n=122): 左心室内径>60 mm。(2)二尖瓣反流:① 0 组(n=203): 反流束面积/ 左心房面积 <19%;② 1 组(n=138):20% ≤反流束面积 / 左心房面积≤ 40%;③2组(n=71):反流束面积 / 左心房面积> 41%。(3)三尖瓣反流:①0 组(n=302):反流束面积 / 左心房面积 <19%;② 1 组(n=90):20% ≤反流束面积 / 左心房面积≤ 40%;③2 组(n=20):反流束面积 / 左心房面积> 41%。(4)LVEF:① 0组(n=272):LVEF ≥ 35%;② 1组(n=140):LVEF < 35%。(5)肺动脉收缩压:① 0组(n=282):肺动脉收缩压≤50mmHg(1mmHg=0.133 kPa);②1 组(n=130):肺动脉收缩压>50 mmHg。(6)心包积液:①0组(n=347 ):无心包积液;②1 组(n=65):有心包积液。(7)胸腔积液:①0组(n=261):无胸腔积液;②1组(n=86):一侧胸腔积液;③2组(n=65):双侧胸腔积液。
随访:2007-01 至 2016-01 期间通过住院和门诊病历和电话访谈对412例患者进行随访,每3个月在门诊或电话联系进行评估,再入院事件以再次因心衰入院。

2 结果
各组患者平均1年内再入院时间比较(表1):(1)左心室内径组内间比较(P=0.004)、二尖瓣反流组内比较(P=0.000)、三尖瓣反流组内比较(P=0.000)、胸腔积液组内比较(P=0.003)、心包积液组内比较(P=0.001)、肺动脉收缩压组内组间比较(P=0.004),患者 1 年内再入院时间均呈下降趋势,差异均有统计学意义。(2)LVEF 组内间比较(P=0.784),患者1年内再入院时间差异无统计学意义。
多项超声参数COX回归分析(表2):结果显示左心室内径、三尖瓣反流、二尖瓣反流、胸腔积液、心包积液是LVSD患者1年内再入院的独立危险因素。
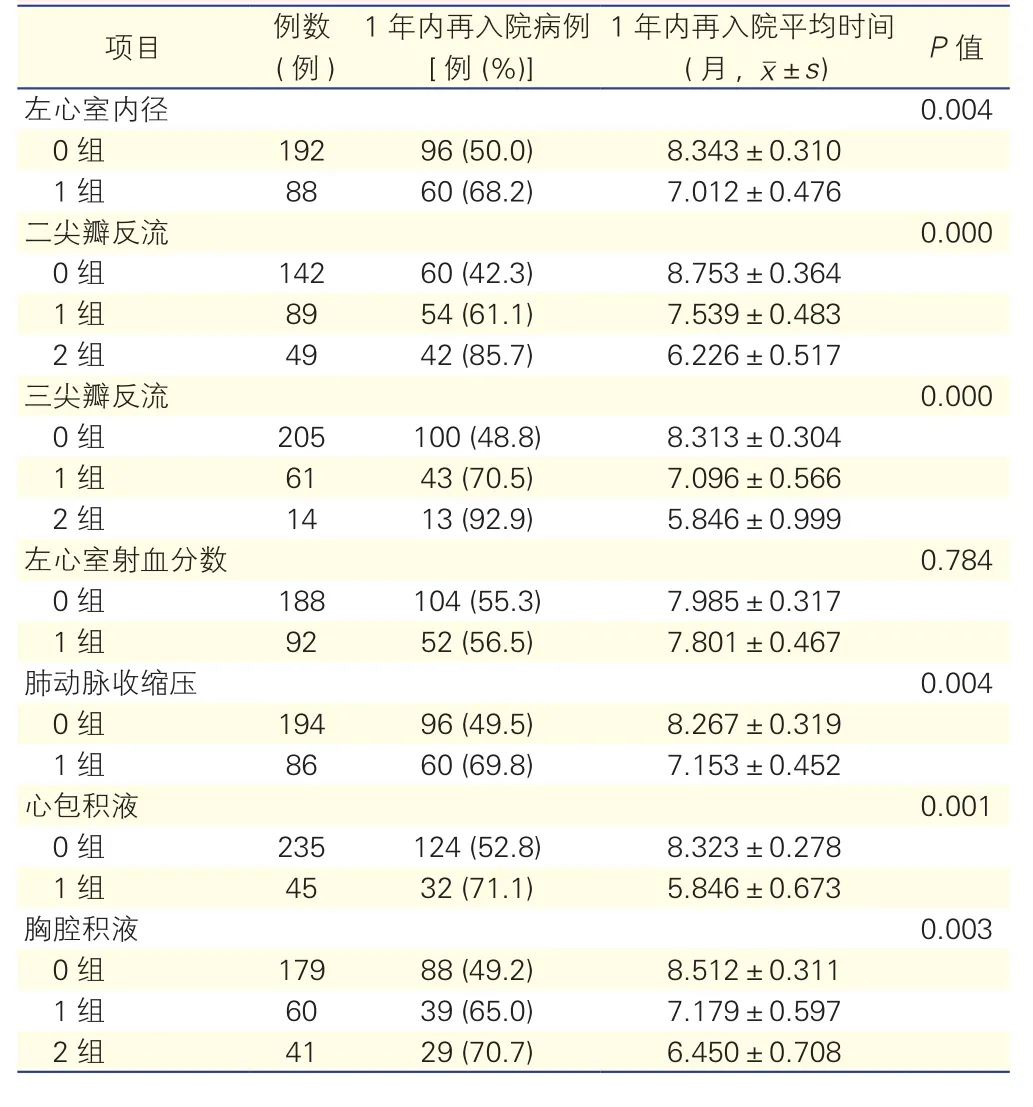
表1 280例(建模)患者在不同组别中平均1年内再入院时间比较(log-rankα=0.05)

表2 多项超声参数COX回归分析
超声积分系统建立与评价:根据对有意义参数进行多因素COX回归分析确定的HR,HR-1代表与对照组(0组)相比增加的1年内再入院风险率,将左心室内径的HR-1设定为1分,其他相关变量的HR-1以左心室内径为参照转换为相应的整数。超声积分系统的分值范围是0~12,其中左心室内径> 60 mm =1分,三尖瓣反流1组=1分,三尖瓣反流2组=3分,二尖瓣反流1组=2分,二尖瓣反流2组=4分,胸腔积液1组=2分,胸腔积液2组=3分,心包积液=1分。超声积分系统四分类Kaplan-Meier生存曲线(图1)。
超声积分系统COX回归分析: 采用 COX回归分析结果显示,不同组间LVSD患者1年内再入院率有显著差异:超声积分系统(1组vs 0组)[HR=1.552,95% CI:1.066~2.259,P=0.022), 超声积分系统(2组 vs 0组 ) [HR=3.374,95% CI:2.161~5.185,P=0.000),超声积分系统(3组 vs 0组)[HR=4.562,95%CI:2.517~8.269,P=0.000)。
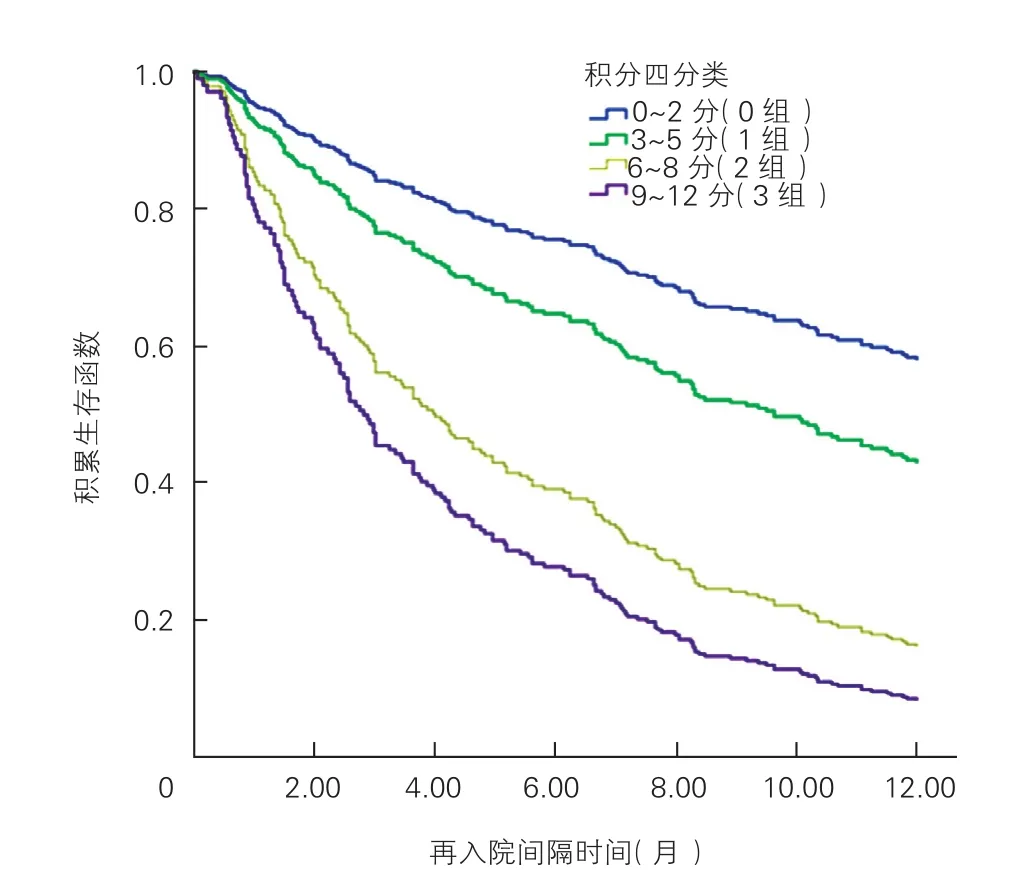
图1 超声积分系统四分类Kaplan-Meier生存曲线
ROC曲线分析(图2): 结果表明超声积分系统的 AUC 为 70.0%,95%CI:0.640~0.761,最佳积分阈值为4分。

图2 超声积分系统和各项超声参数对280例患者1年内再入院预测的受试者工作特征曲线
1年内再入院预测结果(表3):用 ROC 曲线分析超声积分系统和各项超声参数对280例患者1年内再入院特异性及敏感性均高于单项超声指标。
超声积分系统验证:使用超声积分系统对132例验证病例的超声指标进行赋值,并绘制ROC曲线与建模数据曲线比较(图3),结果显示验证数据模型AUC为70.4%,95%CI:0.616~0.792,最佳积分阈值为4分。以上结果与建模数据评价结果相似,说明系统预测性能良好,可有效预测LVSD患者预后。

表3 用ROC曲线分析超声积分系统和各项超声参数对280例患者1年内再入院预测结果

图3 验证数据和建模数据预测1年内再入院的受试者工作特征曲线
3 讨论
许多因素可增加LVSD患者心衰再入院风险,目前已证实的再入院高危因素有年龄>80岁、缺血性心衰、液体潴留、低钠血症、肾功能衰竭史、血肌酐≥1.5 mg/dl、B型利钠肽≥1023.90 ng/L等[8-12],这些因素的出现提示患者可能需要再次入院接受治疗,通过有意义的预测指标对再入院高危因素早期识别尤为必要。
随着床旁超声和便携式超声设备的推广,超声心动图检查作为一个简便、可靠的评估手段被广泛应用于LVSD患者的临床筛查、诊断和治疗。近年来,已有多项研究使用心脏超声参数对LVSD患者血流动力学进行评估,并对预后和再入院进行预测分析[8,13-15],公认的超声参数有二尖瓣反流、三尖瓣反流、肺动脉收缩压、LVEF等,这些指标对LVSD患者短期再入院预测有重要价值。有研究认为预测LVSD患者1年内再入院的心脏超声参数指标包括二尖瓣反流、三尖瓣反流、心包积液,其中二尖瓣反流、心包积液为1年内再入院的独立危险因素[16]。但是以上几种指标是相互独立的,彼此权重不同,其特异性和敏感性不高。本研究将多项心脏超声参数指标综合分析,计算各自的权重来建立超声积分系统,旨在对LVSD患者的一年内再入院风险评估做出更好的评价,通过此系统进行出院评估,制定全面的出院计划和门诊随诊,有利于降低LVSD患者的再入院率。
另外,对不同方法间的ROC曲线和AUC值的比较分析结果表明,超声积分系统对心衰患者1年内再入院的风险评估效果明显优于单项指标,其准确性和敏感性均有显著提高,具有较高的临床实用价值和理论研究意义。另一方面,由于在超声积分系统的设计中,各参数权重的设定依赖于人工经验,这对系统的稳定性和泛化能力产生消极影响。随着数据挖掘与机器学习技术的不断发展,利用机器学习算法建立心衰生存预测模型,对心衰患者进行预后评估,逐渐成为心衰研究的热点[17]。在未来的研究中,我们将利用机器学习与数据挖掘算法,评估参数的重要性,融合多超声参数,进一步优化超声系统,建立超声参数与心衰之间的映射关系。因此,超声心动图是可以有输出各种有效数据的基础,有助于疾病预测、筛查、诊断、治疗评估,能提供大量有效、可靠原始数据,对LVSD患者1年内再入院风险评估、生存分析评估有重大价值和挖掘潜力。未来随着人工智能发展,以该数据平台为主,结合其他体系指标,比如肾功能指标,有望构建心衰早期筛查、风险评估的计算机模型和精准医疗平台。
总之,超声心动图可以提供丰富的临床有效数据,为LVSD的预测、筛查、诊断、治疗和预后评估提供大量信息。本文基于超声心动图建立的超声积分系统,对LVSD患者1年内再入院的风险进行评估,具有重要的临床应用价值。但由于影响心衰患者预后的因素较多,为提高预测模型的准确性和适用性,有必要融合多指标体系,进一步开展多中心大样本量研究,以构建更适合临床心衰患者的预后评估系统。
[1] 中华医学会心血管病学分会, 中华心血管病杂志编辑委员会. 中国心力衰竭诊断和治疗指南2014. 中华心血管病杂志, 2014, 42:98-122.
[2] Tuppin P, Cuerq A, de Peretti C, et al. Two-year outcome of patients after a first hospitalization for heart failure: A national observational study. Arch Cardiovasc Dis, 2014, 107: 158-168.
[3] Thavendiranathan P, Yingchoncharoen T, Grant A, et al. Prediction of 30-day heart failure-specific readmission risk by echocardiographic parameters. Am J Cardiol, 2014, 113: 335-341.
[4] Levy WC, Mozaffarian D, Linker DT, et al. The seattle heart failure model: prediction of survival in heart failure. Circulation, 2006, 113:1424-1433.
[5] Pocock SJ, Ariti CA, McMurray JJ, et al. Predicting survival in heart failure: a risk score based on 39372 patients from 30 studies. Eur Heart J, 2013, 34: 1404-1413.
[6] O' Halloran L, McAdam B, Morgan K, et al. Readmission rates among cardiology inpatients with echocardiography abnorm alities associated with heart failure. Ir J Med Sci, 2016, 185: 717-722.
[7] Dokainish H, Zoghbi WA, Lakkis NM, et al. Incremental predictive power of B-type natriureticpeptide and tissue Doppler echocardiography in the prognosis of patients with congestive heart failure. J Am Coll Cardiol, 2005, 45: 1223-1226.
[8] Giamouzis G, Kalogeropoulos A, Georgiopoulou V, et al.Hospitalization epidemic in patients with heart failure: risk factors,risk prediction, knowledge gaps, and future directions. J Card Fail,2011, 17: 54-75.
[9] 刘暐, 林英, 张福春. 158例慢性心力衰竭患者一年再住院的影响因素分析. 中国循环杂志, 2009, 24: 352-355.
[10] Gheorghiade M, Abraham WT, Albert NM, et al. Relationship between admission serum sodium concentration and clinical outcomes in patients hospitalizedfor heart failure: an analysis from the OPTIMIZEHF registry. Eur Heart J, 2007, 28: 980-988.
[11] Rodríguez-Artalejo F, Guallar-Castillón P, Herrera MC, et al. Social network as a predictor of hospital readmission and mortality among older patients with heart failure. J Card Fail, 2006, 12: 621-627.
[12] 赵玉清, 袁桂莉, 张进顺, 等. 和肽素联合N末端B型利钠肽原评估慢性心力衰竭患者预后的价值. 中国循环杂志, 2014, 29: 275-278.
[13] Prakash R, Horsfall M, Markwick A, et al. Prognostic impact of moderate or severe mitral regurgitation (MR) irrespective of concomitant comorbidities: a retrospective matched cohort study. BMJ Open, 2014, 4: e004984.
[14] Agha SA, Kalogeropoulos AP, Shih J, et al. Echocardiography and risk prediction in advanced heart failure: incremental value over clinical markers. J Card Fail, 2009, 15: 586-592.
[15] Shalaby A, Voigt A, El-Saed A. Usefulness of pulmonary artery pressure by echocardiography to predict outcome in patients receiving cardiac resynchronization therapy heart failure. Am J Cardiol, 2008,101: 238-241.
[16] 王晓军, 丛晓, 申晓倩, 等. 采用超声心动图参数分析和预测慢性左心室射血分数降低心力衰竭患者1年内再入院风险. 中国循环杂志, 2016, 31: 142-145.
[17] Panahiazar M, Taslimitehrani V, Pereira N. Using EHRs and machine learning for heart failure survival analysis. Stud Health Technol Inform, 2015, 216: 40-44.
Risk Assessment of Echocardiography Parameter Scoring System for 1 Year Re-admission in Patients With Left Ventricular Systolic Dysfunction
ZHAI Chun-xiao, WANG Xiao-jun, YU Yong-ming, WANG Yi-dan, XU Liang-dong, CONG Xiao, SHEN Xiao-qian, LI Hong,LIANG Ying, HAO En-kui.
Department of Clinical Medical School, Weifang Medical College, Weifang (261053), Shandong, China
HAO En-kui, Email: haoenkui@sdu.edu.cn
Objective: To establish an echocardiography parameter scoring system for assessing the risk of 1 year re-admission in patients with left ventricular systolic dysfunction (LVSD).
Methods: A total of 412 chronic LVSD patients treated in our hospital from 2007-01 to 2016-01 were studied and the end point event was 1 year re-admission. The data included in 280 patients from 2007-01 to 2014-12 for establishing the scoring system and 132 patients from 2015-01 to 2016-01 for verifying the system. Based on 7 echocardiography parameters,the patients were divided into 7 sets of groups:①Left ventricular diameter (LVD): Group0, n=290 and Group1, n=122;②Mitrial regurgitation (MR): Group0, n=203, Group1, n=138 and Group2, n=71; ③Tricuspid regurgitation (TR): Group0,n=302, Group1, n=90 and Group2, n=20;④LVEF: Group0, n=272 and Group1, n=140;⑤Pulmonary artery systolic pressure: Group0, n=282 and Group1, n=130; ⑥Hydropericardium: Group0, n=347 and Group1, n=65; ⑦Hydrothorax:Group 0, n=261, Group1, n=86 and Group2, n=65. The parameters were identified by COX regression analysis, weighted value of scoring system was calculate by hazard ratio (HR), predictive value for1 year re-admission was assess by ROC curve and finally, scoring integration was verified by validation data group.
Results: The integration score was calculated as follows: LVD>60mm=1 point; TR: Group1=1 point and Group2=3 points; MR: Group1=2 points and Group2=4 points; Hydrothorax: Group1=2 points and Group2=3 points;Hydropericardium=1 point. COX regression analysis indicated that for 1 year re-admission: HR=1.552 in Group1 vs Group0,HR=3.374 in Group2 vs Group0 and HR=4.562 in Group3 vs Group0, all P<0.05. The AUC of ROC for establishing the data was 70.0% (95% CI 0.640-0.761) and for verifying the data was 70.4% (95% CI 0.616-0.792); the best integration score was 4 points.
Conclusion: Echocardiography parameter scoring system may better predict the risk of 1 year re-admission in LVSD patients which is superior to single echocardiography parameter.
Echocardiography; Ventricular dysfunction, left; COX regression analysis
2014 年山东省科技发展计划(2014GSF118187)
261053 山东省潍坊市,潍坊医学院 临床医学院( 翟春晓 ) ;山东大学附属千佛山医院 心内科(王晓军、李虹、梁英、郝恩魁); 山东大学(余永明、王艺丹);德州市人民医院 急诊科(徐良栋);济南市中心医院 心内科(丛晓);烟台毓璜顶医院 神经外科监护室(申晓倩)
翟春晓 硕士研究生 研究方向为心力衰竭基础和临床研究 Email:zhaichunxiao123@126.com 通讯作者:郝恩魁 Email:haoenkui@sdu.edu.cn*为共同第一作者
R541.4
A
1000-3614(2017)12-1194-05
10.3969/j.issn.1000-3614.2017.12.013
2017-02-07)
(编辑:梅平)
