穿膜肽修饰紫杉醇和他莫昔芬脂质体中主药含量测定
2017-11-30*
*
1.北京石油化工学院制药工程系,北京 102617;2.辽宁中医药大学药学院,辽宁 大连 116600
穿膜肽修饰紫杉醇和他莫昔芬脂质体中主药含量测定
居瑞军1程岚2彭效明1王腾1李翠清1王娇2李学涛2*
1.北京石油化工学院制药工程系,北京 102617;2.辽宁中医药大学药学院,辽宁 大连 116600
目的测定穿膜肽(TAT)修饰的紫杉醇和他莫昔芬脂质体中的主药含量。方法采用薄膜分散法和硫酸铵梯度法制备穿膜肽修饰紫杉醇和他莫昔芬脂质体;通过高效液相色谱法测定脂质体中紫杉醇和他莫昔芬的含量。结果TAT修饰的空白脂质体对主药含量的测定无干扰;TAT修饰的紫杉醇和他莫昔芬脂质体中紫杉醇和他莫昔芬分别在0.13~1.3μg和0.16~1.6μg范围内线性关系良好,回收率均在97%以上,RSD均小于1.0%,精密度的相对标准偏差均小于2.0%;脂质体中紫杉醇的平均含量为23.6μg/mL,他莫昔芬的平均含量为8.6μg/mL。结论所建立的HPLC方法准确可靠、简便快速、重复性好,可用于TAT修饰紫杉醇和他莫昔芬脂质体的质量控制。
穿膜肽;紫杉醇;他莫昔芬;脂质体;高效液相色谱法;含量测定
脂质体具有类似生物细胞的结构,作为药物载体进入体循环后,可通过其粒径效应进入血管通透性显著增强的肿瘤病灶处,进而提高抗肿瘤药物的治疗指数,降低药物的治疗剂量,减少药物的毒副作用[1]。紫杉醇(Paclitaxel,PTX)提取于红豆杉科短叶红豆杉(TaxusBrevifolia),属二萜类生物碱,为白色结晶性粉末,不溶于水,易溶于氯仿、丙酮等有机溶剂[2-3]。其抗癌作用机理是在细胞增殖期的G2期,抑制纺锤体和纺锤丝的形成,从而抑制有丝分裂,阻止癌细胞的增殖。目前紫杉醇除了治疗乳腺癌、卵巢癌、非小细胞肺癌等恶性肿瘤以外,其临床适应证还扩大到子宫癌、肺癌、食管癌、前列腺癌及直肠癌等十几种癌症,被认为是迄今人类发现的最有效的抗癌药物[4]。有些肿瘤在经历化疗后,仍难免复发,其中一个重要的原因就是肿瘤细胞对化疗药物产生了多药耐药性(Multidrug Resistance, MDR),是指肿瘤细胞接触一种抗肿瘤药物后,产生对多种结构不同的、作用机制各异的其他抗肿瘤药的耐药性[5]。他莫昔芬(Tamoxifen, TAM)又名三苯氧胺,是第一代选择性雌激素受体调节剂[6],临床上常用其来抑制肿瘤细胞的多药耐药,并且具有毒副作用小、能透过血脑屏障的优点[7]。穿膜肽(Transcription Activator,TAT)是一类不超过30个氨基酸,并能够穿透细胞膜进入细胞质甚至细胞核而不损坏细胞膜结构的小分子多肽[8]。TAT具有能够透过肿瘤细胞,降低不良反应、提高利用率等特点,常用于提高治疗肿瘤药物的靶向性[9-10]。
1 仪器与材料
1.1 仪器 Y220电子分析天平(日本岛津公司);电热恒温水浴锅(上海医疗器械五厂);RE-52AA旋转蒸发器(上海亚荣生化仪器厂);DF2101S集热式恒温加热磁力搅拌器(河南巩义予华仪器厂);KQ3200超声波清洗器(江苏昆山超声设备公司);JY92-2D超声波细胞捣碎机(宁波新芝生物科技股份有限公司);MD34透析袋(上海百赛生物技术有限公司,截留分子量12000~14000);PHS-25型pH计(上海精密科学仪器公司雷磁仪器厂);岛津20AT液相色谱仪(日本岛津公司,UV检测器,岛津色谱工作站)。
1.2 材料 卵磷脂(EPC,日本NOF公司);胆固醇(Chol,日本NOF公司);聚乙二醇-二硬脂酰磷脂酰乙醇胺(PEG2000-DSPE,相对分子质量2800.5,批号:B10206,日本精化株式会社NFC);聚乙二醇-二硬脂酰磷脂酰乙醇胺-N-羟基琥珀酰亚胺-穿膜肽(PEG2000-DSPE-TAT,辽宁中医药大学药剂实验室合成);他莫昔芬(批号:MB5257,大连美仑生物技术有限公司);紫杉醇(批号:SO802A,大连美仑生物技术有限公司);Sephadex G-50(上海华蓝化学科技有限公司)。
2 方法与结果
2.1 脂质体的制备[11]精密称取卵磷脂(EPC)、胆固醇(Chol)、PEG2000-DSPE、PEG2000-DSPE-TAT、紫杉醇和他莫昔芬适量,溶解于氯仿-甲醇(3∶1)中,40 ℃水浴旋转蒸发,减压干燥除去有机试剂,在圆底烧瓶底部及内壁形成一层薄薄的均匀脂膜。加入适量硫酸铵溶液水化,设置超声工作时间为10 s,间歇时间为10 s,全程时间为10 min,保护温度为20 ℃,功率为200 W,超声结束后逐渐形成带有微弱蓝色荧光的半透明液体。然后将超声波粉碎后的脂质体溶液通过孔径为400nm,200nm的聚碳脂膜各挤压3次,制得TAT修饰紫杉醇和他莫昔芬脂质体。
2.2 TAT修饰紫杉醇和他莫昔芬脂质体中主药含量测定
2.2.1 供试品溶液的制备 精密量取TAT修饰紫杉醇和他莫昔芬脂质体样品溶液1mL,置10mL容量瓶中,加入甲醇超声破乳,并定容至刻度,过0.45μm的微孔滤膜1次,取续滤液即得。
2.2.2 对照品溶液的制备 精密称取PTX对照品1.30mg,置10mL容量瓶中,加乙腈定容至刻度,超声使溶解,制备成0.13mg/mL的紫杉醇对照品溶液。精密称取他莫昔芬对照品1.60mg,加甲醇定容至刻度,超声使溶解,制备成0.16mg/mL的他莫昔芬对照品溶液。
2.2.3 空白溶液的制备 制备方法见“2.1”,不加入紫杉醇和他莫昔芬即得空白脂质体。精密量取空白脂质体1mL,置10mL容量瓶中,加入甲醇超声使溶解,并定容至刻度,过0.45μm的微孔滤膜一次,取续滤液即得。
2.2.4 色谱条件[12]及系统适应性 紫杉醇测定色谱条件:色谱柱:C18色谱柱(250mm×4.6mm,5μm,月旭科技(上海股份有限公司));流动相:A:乙腈-甲醇(26∶23),B:水,A:B(70∶30);流速:1.0mL/min;柱温:30 ℃;进样量:20μL;检测波长:233nm。
他莫昔芬测定色谱条件:色谱柱:迪马公司C18柱(250mm×4.6mm,5μm);流动相:甲醇-0.5 %三乙胺水溶液(92∶8);流速:1.0mL/min;柱温:30℃;进样量:20μL;检测波长:254nm。
取紫杉醇对照品溶液,空白脂质体溶液和TAT修饰紫杉醇和他莫昔芬脂质体溶液,按照上述色谱条件分别进样分析,用HPLC法检测,记录色谱图见图1。由图知空白脂质体中的辅料和试剂对主药的含量测定无影响。
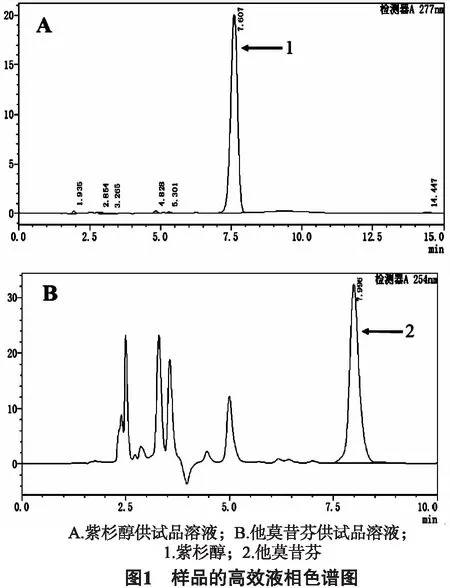
2.2.5 方法学考察
2.2.5.1 标准曲线的建立 分别取紫杉醇与他莫昔芬的对照品溶液,按照上述色谱条件测定紫杉醇与他莫昔芬的色谱峰面积A值,并以质量M(ng)为横坐标,对其相应的色谱峰面;积A值进行线性回归,求得标准曲线。得到紫杉醇的回归方程为Y=116.78X+4150.8(r2=0. 9996),表明紫杉醇在0.13~1.3 μg范围内线性关系良好;他莫昔芬的回归方程为Y=2971.8X+17099(r2=0.9999),表明他莫昔芬在0.16~1.6 μg范围内线性关系良好。
2.2.5.2 精密度实验 取浓度为0.13 mg/mL的紫杉醇对照品溶液,按照上述色谱条件,进行5次分析。同法测得他莫昔芬的峰面积。计算得紫杉醇峰面积的RSD为0.14 %,他莫昔芬峰面积的RSD为0.10 %,表明仪器的精密度良好。
2.2.5.3 重复性实验 取同一样品,按“2.2.1”项下方法制备,进行5次分析,结果紫杉醇重复性试验的RSD为0.06 %,他莫昔芬重复性试验的RSD为0.20 %,表明该方法重复性良好。
2.2.5.4 稳定性实验 取同一样品,按照上述色谱条件,室温下放置,在0、2、4、8、12、24h进行测定,分别进行6次分析并计算相应的RSD值,结果紫杉醇稳定性试验的RSD为0.20 %,他莫昔芬稳定性试验的RSD为0.11 %,表明样品溶液在24 h内稳定性良好。
2.2.5.5 加样回收率实验 精密量取空白脂质体1 mL置10mL容量瓶中,分别加入0.020、0.026、0.031mg/mL的紫杉醇对照品溶液1mL,每种浓度平行操作3次,加入甲醇超声破乳,并定容至刻度。按照上述的色谱条件,用HPLC法检测,测定并记录紫杉醇的峰面积,脂质体中紫杉醇的平均加样回收率符合要求。同法精密量取空白脂质体1mL置10mL容量瓶中,分别加入0.006、0.008、0.010mg/mL的他莫昔芬对照品溶液1mL,每种浓度平行操作3次,测定并记录他莫昔芬的峰面积,脂质体中他莫昔芬的平均加样回收率符合要求。结果见表1。
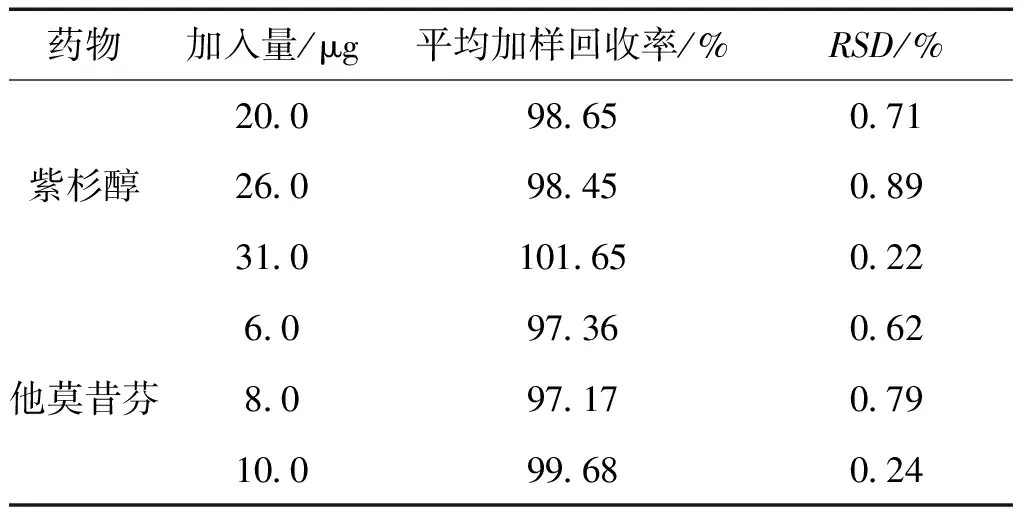
表1 加样回收率考察结果 (n=3)
2.2.6 主药含量测定 精密量取TAT修饰紫杉醇和他莫昔芬脂质体1.0 mL,按“2.2.1”项下制备方法进行操作,照上述色谱条件,用HPLC法检测,记录色谱峰面积,分别计算紫杉醇和他莫昔芬的样品含量和RSD值。结果见表2。

表2 脂质体中药物含量
3 讨论
为了增强药物的靶向性、延长药物在体内滞留时间、增强疗效、降低毒副作用,将TAT作为靶向配体修饰在脂质体表面,提高脂质体的靶向作用;将TAM包裹在脂质体双分子层中,起到抑制肿瘤细胞的多药耐药作用,以提高抗肿瘤药物的敏感度;PTX作为抗肿瘤药物被包封在脂质体双分子层中,起到抑制肿瘤细胞增殖的作用。
实验系统适应性的高效液相色谱图显示,在高效液相色谱法测定脂质体中紫杉醇和他莫昔芬的含量过程中,应用的辅料对实验结果无干扰,方法专属性强。方法学考察的实验结果表明采用此法测定脂质体中紫杉醇和他莫昔芬的含量,分别在0.13~1.3μg和0.16~1.6μg范围内线性关系良好,回收率均在98%以上,RSD均小于1%,精密度的相对标准偏差均小于2%,符合要求。
[1] 谭静净,程岚,李学涛.中心组合设计-效应面法优化长春碱亲水基修饰阳离子脂质体的处方[J].中草药,2012,43(9):1742-1745.
[2]沈征武.紫杉醇研究进展[J].化学进展,1997(1):1-13.
[3]吴秀兰.天然抗癌药物紫杉醇的研究进展[J].中国野生植物资源,2014,33(5):42-60.
[4]余响华.植物细胞工程技术生产紫杉醇研究进展[J].西北植物学报,2013,33(6):1279-1284.
[5]巫蒙,王梅.肿瘤多药耐药性产生机制及其逆转的研究现状[J].当代医学,2011(21):26-28.
[6]谢清.大鼠脑出血早期应用他莫西芬的治疗作用[J].中国临床神经科学,2012,20(5):481-487.
[7]何伟亮.他莫西芬对人脑多形性胶质母细胞瘤BT-325细胞抑制作用的研究[J].中华临床医师杂志,2013,7(5):2056-2059.
[8]何吉文.肿瘤靶向性细胞穿膜肽的固相合成及体外活性研究[J].南方医科大学学报,2011,31(2):201-204.
[9]袁端锋.穿膜肽TAT和脑肿瘤靶向肽T7双修饰脂质体的制备和体外靶向性评价[J].药学学报,2015,50(1):104-110.
[10]张丽.穿膜肽在肿瘤靶向治疗中的应用[J].肿瘤防治研究,2015,42(10):1043-1048.
[11]赵锐.抗癌植物药紫杉醇研究进展与动态[J].中草药,2009,40(7):1172-1174.
[12]刘玉华,李太平.高效液相色谱法测定枸橼酸他莫昔芬的含量[J].色谱,1995,13(6):483-484.
DeterminationofContentofTATModifiedPaclitaxelPlusTamoxifenLiposomes
JU Ruijun1CHENG Lan2PENG Xiaoming1WANG Teng1LI Cuiqing1WANG Jiao2LI Xuetao2*
1.Department of Pharmaceutical Engineering, Beijing Institute of Petrochemical Technology,Beijing 102617,China; 2.School of Pharmacy, Liaoning University of Traditional Chinese Medicine, Dalian 116600,China
ObjectiveTo measure main component contents of TAT modified paclitaxel plus tamoxifen liposomes.MethodsThe TAT modified paclitaxel plus tamoxifen liposomes were prepared by a thin-film dispersion method followed by an ammonium sulfate gradient method. The contents of paclitaxel and tamoxifen in the liposomes were measured via a HPLC method.ResultsUnder the established chromatographic condition, the TAT modified blank liposomes had no interference on the determination of drugs. The paclitaxel and tamoxifen were 0.13~1.3 μg and 0.16~1.6 μg in good linear ranges; recovery rates were over 97%,RSDof recovery rates were less than 1.0%,RSDof precision tests were less than 2.0%. The average content of paclitaxel and tamoxifen in the TAT modified paclitaxel plus tamoxifen liposomes were 23.6 μg/mL and 8.6 μg/mL, respectively.ConclusionThe established HPLC method was simple, precise, replicable, and can be used for the quality control of TAT modified paclitaxel plus tamoxifen liposomes.
TAT; Paclitaxel; Tamoxifen; Liposomes; HPLC; Content Determination
国家自然基金(81673603, 81541081);辽宁省自然基金(2014020046);辽宁省教育厅重点实验室项目(LZ2015053)。
居瑞军(1986-),男,汉族,博士研究生,讲师,研究方向为药物新制剂与新剂型。E-mail:juruijun@bipt.edu.cn
李学涛(1979-),男,汉族,博士研究生,教授,研究方向为新型给药系统。 E-mail: lixuetao1979@163.com
R284.1
A
1007-8517(2017)21-0013-03
2017-09-18 编辑:邓佳丽)
