分子机器概述及目前发展现状
2017-11-10郭建初

在生物体中,分子马达起到将化学能转化为机械能的作用,是生物体宏观运动和微观生理活动的基础。为了研究生物体的本质,人们尝试使用人工合成的分子机器来实现分子马达的全部或部分功能。本文从分子机器的3个基本特征出发,首先,介绍了分子机器的组成模块与运动方式,并对各种能量来源进行了对比;其次,对转动开关、分子肌肉、分子泵和分子装配线这几种特定功能的分子机器进行了分析;最后,对目前的发展现状进行了总结与展望。
背景介绍
在复杂的生物体中,无论是外在的宏观运动还是微观的细胞活动都离不开分子马达(molecular motors)的作用。分子马达是一类可以运动的蛋白,它们可以从ATP等分子中获得能量,并把获得的化学能转化为机械能,从而驱动生物体的活动。至今所发现的分子马达可分为3个不同的家族:肌球蛋白(myosins)家族、驱动蛋白(kinesins)家族和动力蛋白(dyneins)家族,它们为肌肉收缩、细胞分裂、物质运输等提供了基本的动力来源[1]。
由于这些生物体内的分子马达的基础都是单个的蛋白分子,因而人们希望能够通过完全的人工合成制备分子机器,实现这些生物体分子马达的部分功能,从而对生物体的本质有更加深入的认识[2]。在宏观世界中,“机器”是指具有一些运动模块的物体,它们可以通过消耗能量来完成一些特定的任务。类似的分子机器是指具有3种基础的功能的一些分子:1)具有可活动的部分;2)消耗能量;3)可以完成特定的
工作[3]。
关于人工分子机器的研究已有近30年的历史,人们设计并合成出了形式各样的分子机器,实现了转动、伸缩、运输、催化、装配等各种功能。本文从分子机器的3个基本特征出发,从组成模块、能量来源和实现功能3个方面,对分子机器的基本原理和发展现状进行了简要的介绍。
组成模块和运动方式
在一个分子机器中,要实现其他能量到机械能的转变,从而具备一定的功能,能够活动的组成模块是必不可少的部分。这种能够活动的组成模块的运动方式包括以化学键为基础的分子构型构象变化和以分子间作用力为基础的空间位置变化。
图1展示了可以用于分子机器的各种活动模块和它们对应的运动方式。在各种组成模块中,最基础也是应用最多的是碳碳单键的旋转,分子的各个部分以它为旋转轴,进行相对的转动。除了碳碳单键以外,三明治结构的π-金属化合物(如二茂铁[4])也可以作为旋转轴使用。除了单键旋转以外,如果想要在分子中引入光敏特性,在光照的时候发生分子异构,常常在分子机器中引入双键,双键在光照时可以发生顺反异构造成弯曲运动,从而能够使分子机器进行光响应。在构建光响应的分子机器时,偶氮苯和二苯乙烯被广泛的使用。与此同时,二芳基乙烯和螺吡喃由于可以在光照条件下通过周环反应而开环和关环,同样可以进行弯曲运动,因而也被用于光响应的分子机器。第三类组成模块是轮烷类的分子,它由中心的哑铃形分子和套在上面的环状分子组成。通常哑铃形分子上有多个作用位点可以和环状分子发生相互作用,而两端的阻碍又使得环状分子无法脱离,因而环状分子会在外界刺激下在多个作用位点间往复运动。第四类组成模块是索烃类分子,由相互嵌套的两个环状分子组成,可以进行一个环相对于另一个环的旋转运动。
能量来源
在研究的开始阶段,由于热能的无处不在和施加方便,人们普遍使用热能来作为分子机器的能量来源。但使用热能来驱动分子机器时,很难对分子层面的旋转和平移进行控制,这是热能最大的缺陷。为了对分子机器中的运动获得更好的控制,有必要在人工分子机器中引入一些对化学能、电能、光能、磁能等除了热能之外的能量有刺激响应性的模块,作为分子运动精细控制的基础。
因为可逆化学反应的广泛存在,化学能被认为是最具有吸引力的一种能量来源,其中酸碱中和被广为应用,如图2(a),冠醚(DB24C8)和一个二级铵离子可以形成较强的氢键从而得到精确的1:1复合物,这个复合物在离子中心的质子被去掉后又会立刻分解,从而实现了对pH的刺激响应性[5]。但使用化学能时,会在反应过程中不可逆的产生化学废料,随着废料浓度的不断升高,反应的效率会迅速下降并最终停止。为了避免化学废料的产生,人们把注意力转移到了只进行电子转移或构象变化的化学反应上。如图2(b),CBPQT4+离子和联吡啶衍生物(viologens)离子还原条件下可以形成相互穿插的三自由基、三正电荷的复合物;氧化环境中,又会由于强的库仑排斥作用而解离[6]。尽管这类氧化还原反应可以通过添加化学物质驱动,我们也可以在电极表面利用电化学来驱动反应的进行,从而在电极和分子机器间只有电子的迁移。除了电能之外,光能是最方便的一种驱动分子机器的能量来源,只要分子机器中包含光响应基团即可。例如,反式偶氮苯会和反式α-环糊精形成包络复合物。在紫外光的影响下,反式偶氮苯会进行异构化生成顺式的异构体,从而使络合物发生解离[7]。
特定功能的分子机器
在分子机器的研究之初,就是为了模拟生物体内的分子马达的一种或多种功能。因而在实现了分子机器的基本运动之后,人们便利用各种运动模块和对于外界能量的刺激响应性,来实现特性的功能,包括分子开关、分子肌肉、运输器、装配线等等,下面对它们进行简要的介绍。
转动开关
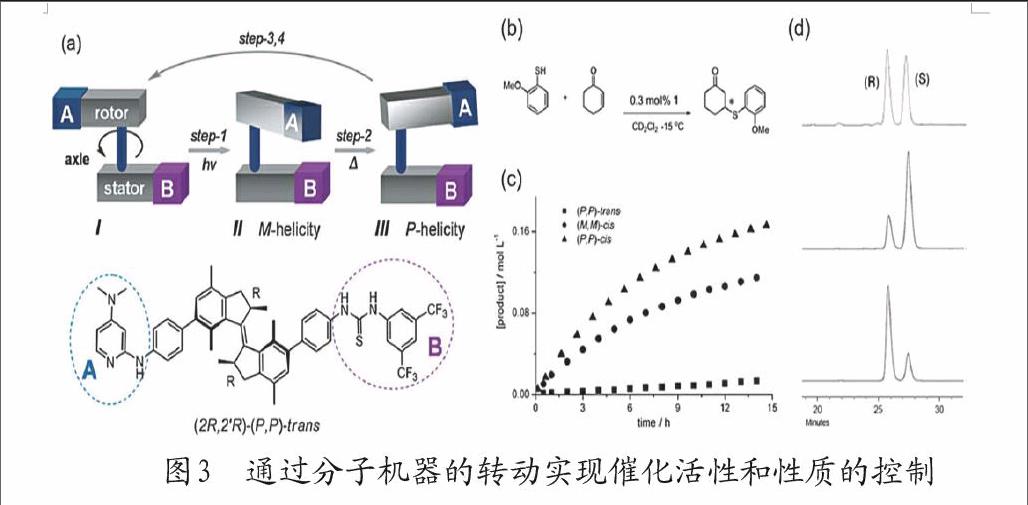
酶和人工合成的不对称催化劑可以在催化反应时进行立体化学控制,大多数时候可以得到单一的手性异构体。但是这些不对称催化剂只能得到某一种手性产物,很难改变其手性倾向得到另一种手性的产物。Feringa等人[8],通过将不对称催化剂和光驱动的分子机器相结合,可以同时做到控制催化剂的活性和产物手性的控制。他们设计的催化剂如图3(a)所示,主要由转动部分A和固定部分B组成,A、B两部分协同发挥催化作用,可以催化迈克尔加成反应的进行。在A和B处于反式结构时,催化活性很低,且几乎没有手性选择性。对反应体系进行光照或加热,可以推动分子机器中双键的旋转,且光照和加热可以分别得到M型和P型两种异构体。M型和P型分子中,A、B两部分相隔较近,由于两者之间的协同作用可以发挥出较高的催化活性,且M和P型分子可以分别特异性地得到一种手性产物,实现了对产物手性构型的控制。
分子肌肉
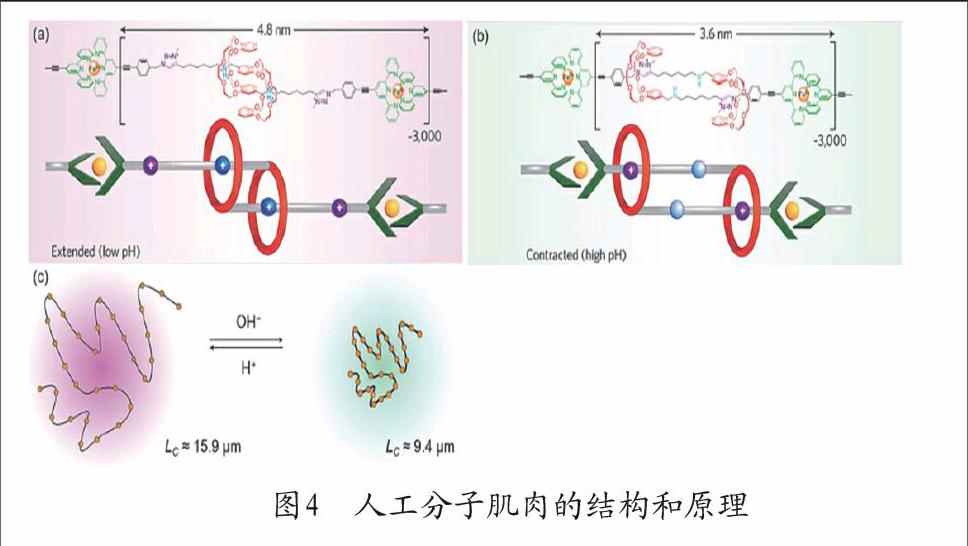
由于肌球蛋白是生物体内分子马达非常重要的一类,它驱动了生物体肌肉的收缩和伸展,因而人们在研究人工分子机器时对人工分子肌肉进行了广泛的探索。其中最为成功的是Buhler和Giuseppone等人[9]的研究成果,他们利用了-CH2NH2+CH2-中心和冠醚(24冠8)的识别来实现了分子的伸缩。他们设计的分子如图4所示,单个分子是一个哑铃型,一端通过三联吡啶和Fe3+形成络合物从而实现了多个分子在一端的动态连接;另一端连接一个冠醚,并且临近的两个分子的冠醚环相互嵌套,从而在分子的另一端进行连接。在分子的链状部分,在两个不同的地方嵌入了三唑环和胺,三唑环和胺在酸性环境下都会带正电荷从而和冠醚因异性电荷而相互吸引,有较强的相互作用。在较低的pH时,两者都会带正电,但胺处电荷密度较高,因而冠醚会优先与胺作用,此时分子处于伸长状态;在较高的pH时,胺的正电荷会先失去,只留下三唑环上的正电荷,此时冠醚只能和三唑环作用,分子处于收缩状态。也就是说,通过调控体系的pH,可以实现人工分子肌肉较为明显的伸缩。对于使用了3 000个重复单元的超分子链,酸性环境中可以比碱性环境中伸长6μm。
分子泵
在生物体中,物质输运是分子马达的另一个非常重要的作用领域,通过动力蛋白实现了氧气、营养物质、离子等在全身的運输。而人工合成分子泵,主要困难在于如何实现运输的单向性,防止分子机器的反向运输。
2012年,Credi等人[10]实现了可控的链状分子单向穿过一个环,为日后真正实现分子泵打下了良好的基础。他们首先使用冠醚(DB24C8)作为环状分子,用来穿过冠醚的分子由偶氮苯和一个烷基链组成,烷基链上有一个铵离子作为识别位点S,末端连接一个位阻较大的环戊烷作为截止位点D。初始状态时,偶氮苯处于反式构型,分子位阻较小,可以穿过冠醚环,从而使得铵离子识别位点S和冠醚能够相互作用,得到一个能量比较低的稳定状态。接下来,由于截止位点D的影响,继续前进将面临较大的能垒。为了防止分子从冠醚中反向穿出,向体系施加光照从而使得偶氮苯的双键发异构化变为顺式结构。顺式结构的偶氮苯具有非常大的位阻,从而阻止了分子反向穿出的可能。接下来,向体系中加入K+以减弱冠醚和识别位点S的相互作用,在热运动的作用下,分子就只能继续往右穿出冠醚,从而实现了分子对于一个环的单向穿过。
分子装配线
在生物体中,实时都在进行着DNA的转录,RNA的翻译。氨基酸在核糖体中,根据RNA携带的密码子信息,按次序连接生成多肽,进而得到具有各种功能的蛋白。核糖体就可以看成生物体内合成蛋白的装配线。
人工合成的分子装配线的一个典型例子是Harada等
人[11]在2011年的工作。作者使用了轮烷状的环糊精作为δ-戊内酯连续开环聚合的催化剂和装配线。其中,β-环糊精可以固定、活化戊内酯,并且使戊内酯开环以起到聚合催化剂的作用。将一个α-环糊精和之前的β-环糊精连接在一起,就组成了一个人工的分子装配线,既可以在其内部发生开环聚合,也可以对活性位点提供保护从而避免了副反应的发生。这样一个分子装配线最终可以达到95%的转化率,并且得到的高分子链的数均分子量可以达到16 500。
总结与展望
本篇文章从生物体内的分子马达引入,对分子机器的原理和目前发展现状进行了简要的介绍。
首先,介绍了单键旋转、双键异构化、轮烷往复运动、索烃相对转动这四种基本的分子机器组成模块和运动方式;然后,对热能、化学能、电能和光能这几种能量来源进行了对比和分析;最后,针对分子机器实现的特定功能,介绍了转动开关、分子肌肉、分子泵和分子装配线的设计、原理和发展现状。
从上面的介绍中可以看到,分子机器目前的研究已经取得了长足的进步,可以实现一些基本的功能,对未来的进一步发展奠定了良好的基础;但相比于生物体内的分子马达而言还处在比较初级的阶段,功能还比较单一且难以对运动的过程进行精确的控制。未来可以从能量来源的多样化、更加精确地控制等方面入手,并且结合使用多种运动模块,实现更加复杂的功能。
参考文献
[1]Veigel,C.,Schmidt,C.F.,Nat.Rev.Mol.Cell Bio.2011,12(3):163.
[2]Kinbara,K.,Aida,T.,Chem.Rev.2005,105(4):1377-1400.
[3]Cheng,C.,Stoddart,J.F.,ChemPhysChem 2016,17(12):1780-1793.
[4]Muraoka,T.,Kinbara,K.;Aida,T.,Nature 2006,440(7083):512.
[5]Ashton,P.R.,Ballardini,R.,Balzani,V.,et al.J.Am.Chem.Soc,1998,120(46),11932-11942.
[6]Trabolsi,A.,Khashab,N,Fahrenbach,A.C.,et al.,Nat.Chem,2010,2(1):42-49.
[7]Harada,A.,Accounts Chem.Res.2001,34(6):456-464.
[8]Wang,J,Feringa,B.L.,Science 2011,331(6023):1429-1432.
[9]Bruns,C.J,Stoddart,J.F.,Nat.Nanotechnol.2013,8(1):9-10.
[10]Baroncini,M.,Silvi,S.,Venturi,M.,et al.,Angew.Chem.Int.Edit.2012,51(17):4223-4226.
[11]Takashima,Y,Osaki,M,Ishimaru,Y,et al.,Angew.Chem.Int.Edit.2011,50(33):7524-7528.
(作者简介:郭建初,清华大学附属中学永丰学校。)
