2-氯烟酸构筑的六核铜配合物:合成、晶体结构和性质研究
2017-11-03徐涵潘兆瑞
徐涵,潘兆瑞
(1.黄山学院化学化工学院,安徽黄山245041;2.南京晓庄学院环境科学学院,江苏南京211171)
2-氯烟酸构筑的六核铜配合物:合成、晶体结构和性质研究
徐涵1,潘兆瑞2
(1.黄山学院化学化工学院,安徽黄山245041;2.南京晓庄学院环境科学学院,江苏南京211171)
在水热反应条件下,合成了一个新的六核配合物Cu6L6(2,2′-bipy)4(H2O)2(L=2-氯烟酸,2,2′-bipy=2,2′-联吡啶),经元素分析、红外、热重、单晶衍射表征了化合物。配合物为单斜晶系,P21/n空间群,分子量Mr=1980.97,a=1.2023(3)nm,b=1.9801(4)nm,c=1.7244(4)nm,α=90.00°,β=109.256(3)°,γ=90.00°,V=3.8757(14)nm3,Z=2,Dc=1.880g·cm-3,F(000)=2196,S=1.085,R1=0.0978,ωR2=0.2227。配合物中6个铜离子通过2-氯烟酸和2,2′-联吡啶桥联成有六核铜单元。
2-氯烟酸;六核铜单元;晶体结构
0 引言
金属配合物不仅具有新颖的结构,而且在光、电、磁性、气体存储等方面都具有潜在的应用价值[1-3],因此,合成具有一定结构和功能的配合物具有十分重要的意义,近年来取得了化学工作者的关注。除此之外,pH值、阴离子、反应温度、有机溶剂等对形成配合物也起着重要的作用[4-6]。与无机物和有机小分子相比,金属-有机配合物存在着很多优点,因为有机配体与金属离子构造配位聚合物形成不同的结构,并且金属离子可以表现出不同的配位方式。许多刚性羧酸类配体被广泛应用于合成结构和性质新颖的配合物[7-9],2-氯烟酸是有很强的配位能力羧酸配体,吡啶环上的氮原子和环外的都能与金属离子以多种连接方式配位。
本文以2-氯烟酸和2,2′-联吡啶为混合配体,在水和甲醇组成的反应介质中,与Cu(NO3)2·3H2O反应,用水热法合成了新的配合物Cu6L6(2,2′-bipy)4·(H2O)2,并对其进行元素分析、红外、热重、单晶衍射等相关表征。
1 实验部分
1.1 试剂与仪器
FTIR仪(VECTOR-22 Bruker公司),Bruker Smart Apex CCD衍射仪(Bruker公司),TGA-7型热分析仪(美国Perkin-Elmer公司),PERkin Elmer 240C elemental Analyzery元素分析仪、Bruker D8 ADVANCE型X-射线粉末衍射仪(Cu Kα,λ=0.154178nm)。
1.2 Cu6L6(2,′-bipy)4(H2O)2的合成
将溶有12mg(0.05mmol)的Cu(NO3)2·3H2O水溶液(5mL)同溶有8mg(0.05mmol)的2-氯烟酸配体的甲醇(5mL)混合均匀,置入25mL反应釜中,在120℃烘箱中反应3天,以每小时2℃的温度逐渐降至室温,得到深蓝色块状晶体。然后将晶体分离并用乙醚洗净,在空气中干燥。FTIR(KBr固体压片ν/cm-1):3341(s,br),1638(s),1554(s),1420(s),1389(m),1286(m),768(m),702(m),608(m)cm-1。元素分析(%,按C76H54Cl6Cu6N14O14计算,括号内为计算值)C,46.10(46.04);N9.84(9.89);H2.70(2.73)。
1.3 Cu6L6(2,2′-bipy)4(H2O)2晶体结构的测定
选取外观完好,0.30mm×0.26mm×0.24mm的深蓝色块状晶体,采用Bruker Smart Apex CCD单晶衍射仪,使用经过石墨单色器单色化的Mo Ka衍射(λ=0.071073nm),以φ-ω扫描方式,在室温下,在2.06°<θ<25.00°的范围内应用Smart程序收集10835个衍射数据,其中独立衍射点4546个(Rint=0.0553),I>2σ(I)的可观测衍射点3079个。
2 结果和讨论
2.1 红外光谱分析
以KBr为基质,在4000-400cm-1范围内测定了配合物的红外光谱。从图1中可以看出,配合物Cu6L6(2,2′-bipy)4(H2O)2在3341cm-1附近有一宽吸收峰,表明配合物中含有结晶水,与元素分析结果一致,且O-H的伸缩振动向低波数方向移动,表明Cu6L6(2,2′-bipy)4(H2O)2结构中有氢键存在。强的1638cm-1和1554cm-1峰,为配位后羧基伸缩振动特征峰,羧基配位后,其峰也向低波数方向移动。1420cm-1,1389cm-1,1286cm-1为苯环的骨架伸缩振动。768cm-1,702cm-1,608cm-1为苯环上C-H的面内弯曲振动。
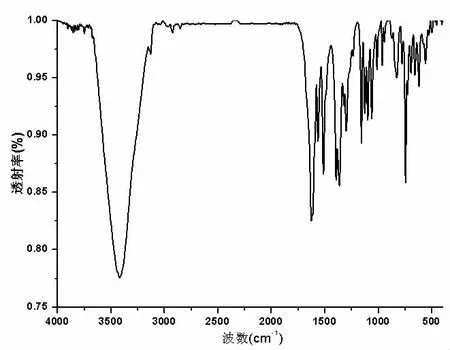
图1 配合物Cu6L6(2,2′-bipy)4(H2O)2的红外光谱图
2.2 配合物的晶体结构
Cu6L6(2,2′-bipy)4(H2O)2的主要的键长和键角列于表1。配合物Cu6L6(2,2′-bipy)4(H2O)2属单斜晶系,P21/n。X-射线单晶体结构表明,配合物的不对称单元中包含3个CuII离子,3个L配体,2个2,2′-bipy以及一个配位水分子。Cu1,Cu2,Cu3采取不同的配位模式(图2),Cu1和Cu2为六配位的变形八面体配位构型,与Cu1配位的1个氧原子,2个氯原子和3个氮原子分别来自2个L配体和1个2,2′-bipy配体。与Cu2配位1个氧原子,2个氮原子和3个氯原子分别来自3个L配体。Cu3的空间几何构型为五配位的变形四方锥构型,与Cu3配位的1个氯原子,2个氧原子和2个氮原子分别来1个L配体,1个2,2′-bipy配体和1个配位水分子。Cu-O,Cu-N和Cu-Cl的键长分别在1.913(6)-2.234(6)Å,1.972(6)-2.044(7)Å和1.901(6)-2.730(6)Å范围内,这些键长都在正常键长范围内。4个L配体中的氯原子通过桥联的方式连接2个Cu1和2个Cu2形成了[Cu4Cl4]含8个原子的环状结构。
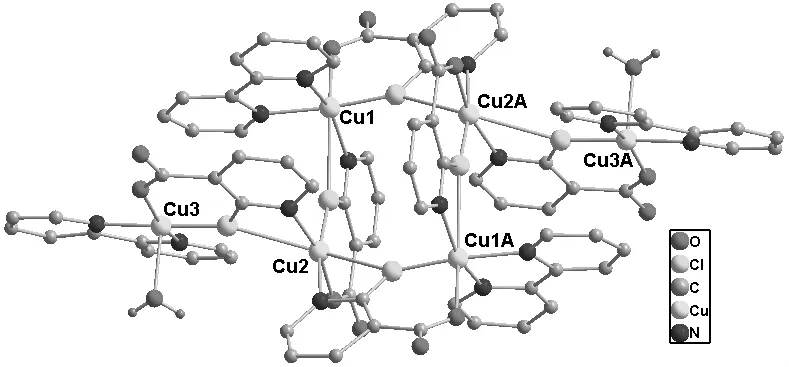
图2 配合物分子的结构图(椭球几率50%)
配位水和相邻六核铜单元中的羧基氧原子之间形成分子间氢键O(7)–H(7B)O(2),氢键的作用使得配合物的不同结构单元相互连接,构筑成一维链状结构(图3)。
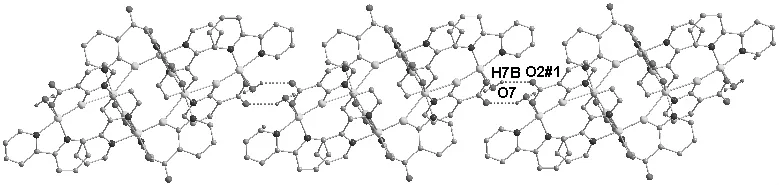
图3 配合物的氢键图
2.3 配合物的热重分析
为了考察配合物的热稳定性,在25-700℃的温度范围内对化合物进行了热重分析(图4)。热重分析显示从室温到170℃内没有失重,说明该化合物具有较好的热稳定性,高于170℃时,随着有机配体的分解,框架发生坍塌而快速失重。

表1 标题化合物的主要键长和键角
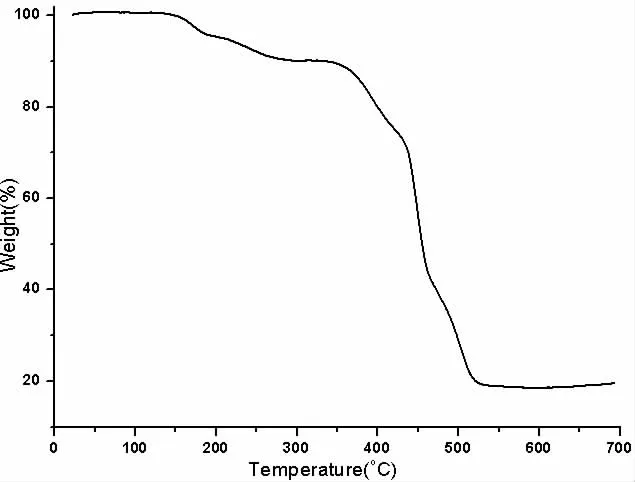
图4 配合物的热重曲线
2.4 Cu6L6(2,2′-bipy)4(H2O)2的粉末X射线衍射分析
图5为配合物Cu6L6(2,2′-bipy)4(H2O)2的粉末XRD图谱,配合物实验测定的PXRD图和它的单晶结构分析模拟的PXRD图能很好的吻合,证实了所合成的配合物是均一的纯相,并且在室温下稳定。
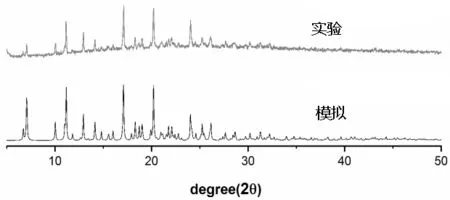
图5 配合物Cu6L6(2,2′-bipy)4(H2O)2的XRD图谱
3 结论
将硝酸铜、2,2′-联吡啶和2-氯烟酸混合,水热法合成了一个新的六核配合物Cu6L6(2,2′-bipy)4·(H2O)2,并对其进行了结构分析和表征。铜离子采取不同的配位模式,六核铜单元通过O(7)–H(7B)O(2)分子间氢键,形成一维链结构。
[1]Zhang D,Li G S,Peng Y and Li L P.Synthesis of a Ternary Thiostannate with 3D Channel Decorated by Hydronium for High Proton Conductivity[J].Inorg Chem,2017,56(1):208-212.
[2]Qin L,Chen H Z,Lei J,Wang,Y Q,Ye T Q and Zheng H G.A(3,6)-Connected Metal–Organic Framework with pyr Topology and Highly Selective CO2Adsorption[J].Crystal Growth&Design,2017,17(1):16-18.
[3]Wang Q,Jiang J J,Zhang M X and Bai J F.A HomochiralPorousMetal-OrganicFrameworkforHighly Enantioselective Heterogeneous Asymmetric Catalysis[J].J.Am.Chem.Soc.,2005,127:8940-8941.
[4]肖伯安,陈水生.由芳香羧酸和含氮配体构筑的两个金属锌配合物的合成、晶体结构和荧光性质[J].无机化学学报,2017,33(2):347-353.
[5]顾文君,顾金忠.由半刚性三羧酸配体构筑的一维和二维钴(II)配位聚合物的合成、晶体结构及磁性质[J].无机化学学报,2017,33(2):227-236.
[6]Ji H Y,Li X M,Xu D H,Zhou Y S,Zhang L J,Zuhar Z and Yang S W.Synthesis,Structure,and Photoluminescence of Color-Tunable and White-Light-Emitting Lanthanide Metal–Organic Open Frameworks Composed of AlMo6(OH)6OPolyanion and Nicotinate[J].Inorg Chem,2017,56(1):156-166.
[7]Gao X X,Liu M S,Lan J W,Liang L,Zhang X and Sun JM.LewisAcid–BaseBifunctionalCrystalswitha Three-Dimensional Framework for Selective Coupling of CO2and Epoxides under Mild and Solvent-Free Conditions[J].Crys Growth&Des,2017,17(1):51-57.
[8]Shi Z Q,Guo Z J and Zheng H G.Two luminescent Zn(II)metal-organicframeworksforexceptionallyselective detection of picric acid explosives[J].Chem.Commun.,2015,51:8300-8303.
[9]Three different metal-organic frameworks derived from a one-pot crystallization and their controllable synthesis[J].Chem.Commun.,2015,51:8338-8341.
A Hexanuclear CuII Complex Assembled with 2-Chloronicotiante:Its Synthesis,Crystal Structure and Property
Xu Han1,Pan Zhaorui2
(1.School of Chemistry and Chemical Engineering,Huangshan University,Huangshan 245041,China;2.School of Environmental Science,Nanjing Xiaozhuang University,Nanjing 211171,China)
A new coordination compound Cu6L6(2,2′-bipy)4(H2O)2(L=2-chloronicotinate,2,2′-bipy=2,2′-bipyridine)is prepared by solvothermal synthesis and characterized by elemental analysis,IR,TG and X-ray crystallography.The compound crystallizes in monoclinic crystal system with space group P21/n,Mr=1980.97,a=1.2023(3)nm,b=1.9801(4)nm,c=1.7244(4)nm,α=90.00°,β=109.256(3)°,γ=90.00°,V=3.8757(14)nm3,Z=2,Dc=1.880g.cm-3,F(000)=2196,S=1.085,R1=0.0978 and ωR2=0.2227.In the compound,six CuII ions are connected by L and 2,2′-bipy ligands to form a hexanuclea CuII unit.
2-chloronicotinate;hexanuclear CuII unit;crystal structure
O614.121
A
1672-447X(2017)05-0033-004
2017-05-15
安徽省教育厅自然科学研究项目(KJHS2017B05)
徐涵(1980-),山东潍坊人,硕士,黄山学院化学化工学院讲师,研究方向为配合物。
责任编辑:胡德明
