miR-125b对急性白血病细胞HL-60增殖与凋亡的影响及相关机制
2017-10-13冀林华马晓静尹启超
罗 伟 冀林华 耿 惠 马晓静 马 婕 尹启超 刘 媛 崔 森
(青海大学附属医院血液科,青海 西宁 810001)
miR-125b对急性白血病细胞HL-60增殖与凋亡的影响及相关机制
罗 伟 冀林华 耿 惠 马晓静 马 婕 尹启超 刘 媛 崔 森
(青海大学附属医院血液科,青海 西宁 810001)
目的探讨miR-125b对急性白血病(AL)细胞人早幼粒白血病细胞(HL)-60增殖与凋亡的影响及相关机制。方法利用LipofectamineTM2000脂质体将miR-125b inhibitor,miR-125b NC转入白血病细胞HL-60中,RT-PCR法检测miR-125b表达,四甲基偶氮唑盐(MTT)法检测细胞活力,流式细胞术分别检测细胞凋亡及细胞周期变化,Western印迹检测细胞中细胞周期蛋白(Cyclin)A1,CyclinD1,Bax,Bcl-2蛋白表达及细胞外调节蛋白激酶(ERK)磷酸化水平。结果与miR-125b NC比较,miR-125b inhibitor组miR-125b inhibitor表达下调,细胞活力降低,细胞凋亡率提高,细胞周期阻滞在G1期,CyclinA1,Bcl-2及p-ERK表达下调,CyclinD1及Bax表达上调(均P<0.01)。结论miR-125b inhibitor能显著抑制白血病细胞HL-60增殖,诱导细胞凋亡,可能与下调ERK磷酸化水平有关。
miR-125b;白血病;HL-60;增殖;凋亡
急性白血病(AL)是一种因为造血干细胞恶性克隆,骨髓中原始细胞和幼稚细胞异常增殖并使正常造血功能受抑制的恶性血液肿瘤〔1〕。AL根据受累的细胞系可分为急性髓系细胞白血病(AML)和急性淋巴细胞白血病(AML),前者约占AL的80%~90%。miRNA是一类高度保守的长度约21~23 nt的非编码小RNA分子,能够靶向结合于靶基因的mRNA 3′非翻译区,抑制靶基因的转录或降解靶基因,进而调控下游基因的表达,参与机体发育、免疫调控、肿瘤的发生发展〔2〕。研究表明miR-125b在AML患者中高表达,治疗后表达降低,复发后表达又升高,且同时过表达miR-125b能促使白血病细胞急性早幼粒细胞白血病细胞株(NB4)及人早幼粒白血病细胞(HL-60)过度增殖,反义寡核苷酸干扰miR-125b表达能有效抑制白细胞增殖〔3~5〕,但具体作用未知。本研究将进一步探讨miR-125b对白血病细胞HL-60增殖与凋亡的影响及相关机制。
1 材料和方法
1.1试剂与仪器 兔抗人CyclinA1、CyclinD1、Bax、Bcl-2、GAPDH单克隆抗体均购自美国Cell Signal Technology公司;兔抗人细胞蛋白调节激酶(ERK)1/2,p-ERK1/2多克隆抗体均购自美国Abcam公司;四甲基偶氮唑盐(MTT),DMEM培养基均购自美国Gibco公司;辣根过氧化物酶标记山羊抗兔IgG(H+L),二喹啉甲酸(BCA)蛋白浓度测定试剂盒均购自南通碧云天生物技术有限公司,Annexin V-FITC/PI流式双染试剂盒,细胞周期检测试剂盒均南京凯基生物技术有限公司;trizol试剂盒,一步法RT-PCR试剂盒,LipofectamineTM2000均购自美国Invitrogen公司;miR-125b inhibitor,miR-125b NC均购自广州锐博生物技术有限公司;DYCZ-25D型双垂直电泳仪,DYCZ-25D型转印电泳仪均购自北京六一生物科技有限公司;ChemiDocTM XRS凝胶成像系统购自美国伯乐公司;FACSCalibur流式细胞仪购自美国BD公司;MK3酶标仪购自美国Thermo公司。
1.2细胞株 L-60购于中国科学院细胞库,用含有10%胎牛血清的DMEM培养基来培养,细胞每隔2 d左右以1∶3的比例进行传代,并选取对数生长期的细胞用于后续的实验研究。
1.3RT-PCR检测细胞中miR-125b的表达 当HL-60细胞生长达到50%左右,利用LipofectamineTM2000脂质体将miR-125b inhibitor及miR-125b NC转染到HL-60细胞中,6 h后换液,继续培养48 h,利用胰蛋白酶消化细胞,再根据Trizol试剂盒提取细胞总的RNA,并检测总RNA纯度,通过一步法RT-PCR试剂盒将RNA逆转录成cDNA,并将cDNA进行扩增,最后用琼脂糖凝胶电泳检测扩增产物。miR-125b上游引物:5′-CGGGATCCCCAGATACTGCGTATGTGTG-3′,下游引物:5′-CCGCTCGAGG TCACCTGATCCCATCTAAC-3′,GAPDH上游引物:5′-AGCCACA TCGCTCAGACA-3′,下游引物:5′-TGGACTCCACGACGTACT-3′。
1.4MTT法检测HL-60细胞活力 将HL-60细胞接种到96孔板,培养24 h后,利用LipofectamineTM2000脂质体将miR-125b inhibitor及miR-125b NC转染到HL-60细胞中,继续培养48 h后,加入20 μl的MTT(终浓度为5 mg/ml),继续培养4 h,将96孔板中的上清液小心吸取并舍弃,再加入150 μl二甲基亚砜,震荡使结晶物溶解,于酶标仪波长560 nm处测OD值,细胞凋亡率=(miR-125b inhibitor组OD值-空白组OD值)/(miR-125b NC组OD值-空白组OD值)×100%。
1.5Annexin V-FITC/PI法检测HL-60细胞凋亡情况 将HL-60细胞接种到6孔板,培养24 h后,利用LipofectamineTM2000脂质体将miR-125b inhibitor及miR-125b NC转染到HL-60细胞中,继续培养48 h后,miR-125b inhibitor组及miR-125b NC组分别收集1×105/ml个细胞,再将500 μl的结合缓冲液加入细胞中并吹打混匀后,接着将5 μl的Annexin V-FITC及5 μl的PI按顺序加入已混合均匀的细胞中,继续吹打混匀,并在室温条件下避光孵育10 min,于1 h内在流式细胞仪上进行细胞凋亡分析。
1.6流式细胞术检测细胞周期 miR-125b inhibitor组及miR-125b NC组分别收集1×105/ml个细胞,再加入5 μl的Rnase(终浓度为10 mg/ml),吹打混匀后,在37℃条件下孵育1 h,再次加入PI染液,吹打混匀并于室温避光孵育30 min,于1 h内在流式细胞仪进行细胞周期检测分析。
1.7Western印迹检测细胞中CyclinA1,CyclinD1,Bax,Bcl-2及p-ERK蛋白的表达 HL-60细胞培养、转染同1.5,在冰浴条件下将6孔板中细胞刮下来,离心收集细胞,并加入细胞裂解液,裂解30 min,离心获得的上清液即是总蛋白。接着利用BCA试剂盒测定蛋白浓度。蛋白煮沸10 min进行变性,取约30 ng的蛋白样品上样,进行十二烷基苯磺酸钠凝胶电泳1~2 h,后湿法转膜30~50 min。5%脱脂奶粉封闭1 h,一抗溶液(兔抗人CyclinA1、CyclinD1、Bax、Bcl-2、GAPDH单克隆抗体,稀释度1∶100;兔抗人ERK1/2、p-ERK1/2多克隆抗,稀释度为1∶200)孵育,4℃过夜;二抗溶液〔辣根过氧化物酶标记山羊抗兔IgG(H+L)〕室温孵育1~2 h。于凝胶成像系统中曝光。用“Quantity one”软件统计各抗体条带灰度值。
1.8统计学方法 应用SPSS17.0软件进行t检验。
2 结 果
2.1miR-125b inhibitor转染的验证 miR-125b NC及miR-125b inhibitor转染HL-60细胞48 h后,经RT-PCR实验发现,miR-125b inhibitor组中miR-125b表达量(0.18±0.02)显著低于miR-125b NC组(0.96±0.09)(P<0.01),说明miR-125b inhibitor转染成功。见图1。
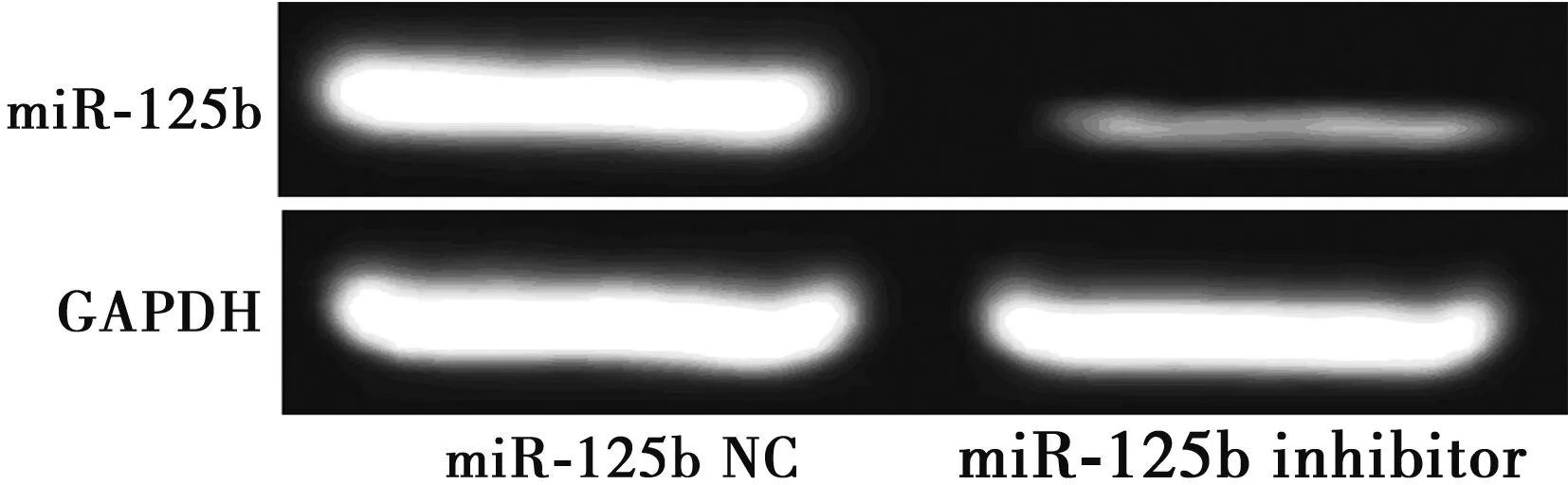
图1 miR-125b转染的验证
2.2miR-125b inhibitor对HL-60细胞活力的影响 miR-125b NC及miR-125b inhibitor转染HL-60细胞24、48、72、96 h后,经MTT实验发现,HL-60细胞活力均显著降低(P<0.01),且在48 h细胞活力适于后续实验研究,因此选择48 h作为后续细胞转染时间。见表1。
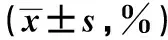
表1 miR-125b inhibitor对HL-60细胞的抑制率
与miR-125b NC组比较:1)P<0.01,下表同
2.3miR-125b inhibitor对HL-60细胞凋亡及细胞周期的影响 miR-125b NC及miR-125b inhibitor转染HL-60细胞48 h后,经流式细胞术实验发现,miR-125b inhibitor组细胞凋亡率显著高于miR-125b NC组(P<0.01);细胞周期G1期明显比miR-125b NC组延长,说明miR-125b inhibitor使HL-60细胞周期阻滞在G1期。见表2。
2.4miR-125b inhibitor对HL-60细胞中细胞周期及细胞凋亡相关蛋白表达的影响 miR-125b NC及miR-125b inhibitor转染HL-60细胞48 h后,经Western印迹实验发现,与miR-125b NC组比较,miR-125b inhibitor组CyclinA1、Bcl-2表达量下调,Bax及CyclinD1表达量上调(均P<0.01)。见图2,表3。
2.5miR-125b inhibitor对HL-60细胞中(p-ERK)水平的影响 miR-125b NC及miR-125b inhibitor转染HL-60细胞48 h后,经Western印迹实验发现,miR-125b inhibitor组中p-ERK表达量(0.18±0.02)显著低于miR-125b NC组(0.49±0.05)(P<0.01)。见图3。
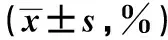
表2 miR-125b inhibitor对HL-60细胞凋亡及细胞周期的影响
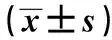
表3 miR-125b inhibitor对HL-60细胞中细胞周期及细胞凋亡相关蛋白表达的影响
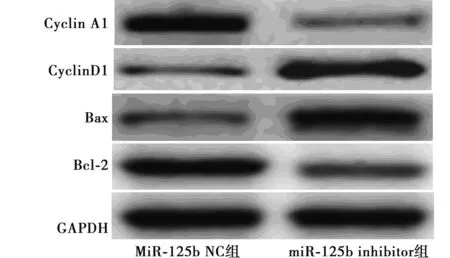
图2 miR-125b inhibitor对HL-60细胞中细胞周期及细胞凋亡相关蛋白表达的影响
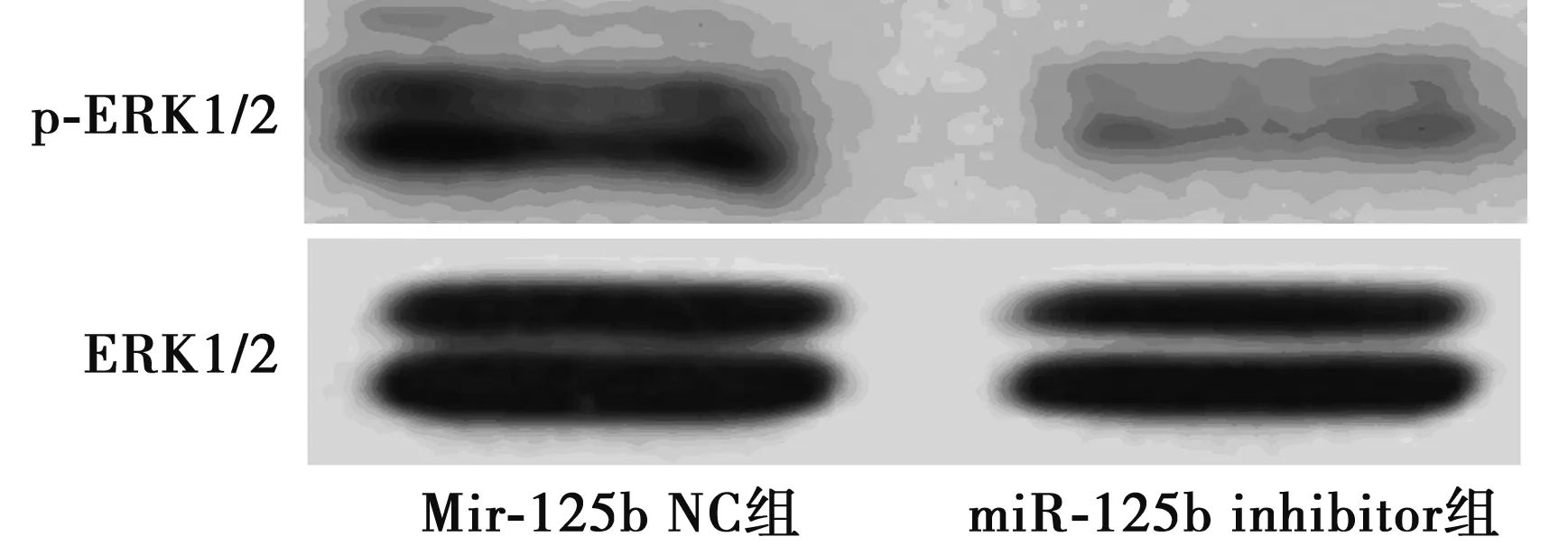
图3 miR-125b inhibitor对HL-60细胞p-ERK水平的影响
3 讨 论
miR-125b是秀丽线虫Line-4的同源基因,有两个前体成员,分别为miR-125b-1和miR-125b-2,且研究显示AML中主要的成熟miR-125b来源于miR-125b-1,另外miR-125b-1位于人类染色体11号的脆性区域,提示miR-125b在AML发生中发挥着重要作用〔6〕。而且Bousquet等〔7〕研究发现AML中miR-125b表达异常,且高表达的miR-125b能通过增加小鼠外周血液中白细胞的数量来直接诱导白血病的发生。王丽娜等〔4〕研究表明儿童急性早幼粒细胞白血病患者中miR-125b高表达,缓解后降低,复发后又升高。谢晶晶等〔3〕研究也表明在儿童AML患者中miR-125b高表达。上述研究充分说明了miR-125b在AML中起着癌基因的作用,且又有学者研究发现过表达miR-125b能促使白血病细胞NB4及HL-60过度增殖,反义寡核苷酸干扰miR-125b表达能有效抑制白细胞增殖〔4,5〕。但是具体的作用机制未知。本研究结果表明miR-125b inhibitor能显著降低HL-60细胞活力,并诱导细胞凋亡,与刘晓丹等〔5〕研究一致。而肿瘤细胞的凋亡受限来源于细胞的恶性克隆,细胞周期的不可控制,因此调控细胞周期点成为众多抗癌药物的作用靶点〔8〕。另外本研究结果表明miR-125b inhibitor能延长G1期,缩短G2期,进而使细胞周期阻滞在G1期,使细胞复制停滞于DNA合成的前期,从而抑制HL-60细胞的恶性增殖,此结果也与miR-125b inhibitor在慢性淋巴细胞K562中的作用一致〔9〕。
细胞的凋亡受细胞凋亡相关基因的严格调控,其中研究最为广泛的是Bcl-2蛋白家族,其中Bcl-2是常见的抑凋亡蛋白,能与促凋亡蛋白Bax形成异二聚体,阻断凋亡信号的传递,促进细胞的存活。Bax能自身形成二聚体,将凋亡信号传递给Caspase 3家族,最终导致细胞凋亡。而细胞凋亡受限制源自于细胞增殖的不可控制,即细胞周期的不可控制。其中CyclinA1及CyclinD1是与细胞周期S和G1期密切相关的细胞周期蛋白,其中CyclinA1对于S期的驱动具有重要作用,而CyclinD1在G1期开始合成并达到高峰,能与CDK4/CDK6形成复合物,进而作用于底物,促使转录起始因子E2F进行转录,推动与DNA合成有关的基因进行转录,从而促使G1期向S期转变。因此通过调控细胞凋亡相关蛋白及细胞周期相关蛋白,能显著的调控细胞的凋亡与增殖,本研究结果表明miR-125b inhibitor能显著下调CyclinA1及Bcl-2表达,上调Bax及CyclinD1表达。
细胞的凋亡、增殖、分化及细胞周期调控受多种信号通路的调控,MAPK/ERK信号通路就是其中的一种〔10〕。EKR是此信号通路的关节调控点,包括5个亚族(ERK1~5),其中EKR1和ERK2研究的最为彻底,能通过自身磷酸化并将信号传递给下游基因进而调控细胞的生命过程。且研究还显示ERK在AML中被高度激活,miR-125b在头颈部肿瘤中的作用机制与MAPK信号通路密切相关〔11〕。本研究结果表明miR-125b inhibitor对EKR表达量影响不大,但能显著的下调p-ERK,提示miR-125b inhibitor能通过下调p-EKR水平进而诱导HL-60细胞凋亡,并抑制细胞增殖。
1Saultz JN,Garzon R.Acute myeloid leukemia:a concise review〔J〕.J Clin Med,2016;5(3):E33.
2朱明霞,克晓燕.MicroRNA在淋巴细胞发育分化及淋巴系统恶性肿瘤发生中的作用〔J〕.中国实验血液学杂志,2012;20(4):1014-9.
3谢晶晶,陈 捷,翁丹丹.微小r-125b在初发急性髓系白血病中的表达情况及临床意义〔J〕.中国卫生检验杂志,2016;26(10):1433-5.
4王丽娜,黄礼彬,梁燕妮,等.MiR-125b对儿童典型急性早幼粒细胞白血病的影响〔J〕.中国实用儿科杂志,2014;29(11):849-54.
5刘晓丹,徐 令,檀卫平,等.MiR-125b在儿童AML中的表达及其反义寡核苷酸对白血病细胞的作用〔J〕.中国病理生理杂志,2012;28(4):738-41.
6Ribeiro J,Sousa H.MicroRNAs as biomarkers of cervical cancer development:a literature review on miR-125b and miR-34a〔J〕.Mol Biol Rep,2014;41(3):1525-31.
7Bousquet M,Harris MH,Zhou B,etal.MicroRNA miR-125b causes leukemia〔J〕.Proc Natl Acad Sci U S A,2010;107(50):21558-63.
8刘厚广,刘 卓,姜 颖,等.细胞周期蛋白与黑色素瘤的研究进展〔J〕.中国地方病防治杂志,2015;30(1):30-3.
9Li Q,Wu Y,Zhang Y,etal.MiR-125b regulates cell progression in chronic myeloid leukemia via targeting BAK1〔J〕.Am J Transl Res,2016;8(2):447-59.
10Sun Y,Liu W Z,Liu T,etal.Signaling pathway of MAPK/ERK in cell proliferation,differentiation,migration,senescence and apoptosis〔J〕.J Recept Signal Transduct Res,2015;35(6):600-4.
11李华梅,曾意茹,陈福雄,等.磷酸特异化流式细胞术检测骨髓白血病细胞磷酸化信号蛋白的实验研究〔J〕.中国实验血液学杂志,2011;19(5):1176-9.
〔2017-04-11修回〕
(编辑 袁左鸣)
R557
A
1005-9202(2017)19-4731-04;
10.3969/j.issn.1005-9202.2017.19.018
罗 伟(1977-),男,硕士,副主任医师,副教授,硕士生导师,主要从事血液病学研究。
