低剂量阿帕替尼单药在晚期乳腺癌末线治疗中的临床疗效观察
2017-07-14赵艳凤温福刚
赵艳凤 温福刚 李 彬 刘 君 刘 建
(鞍山市肿瘤医院肿瘤内科,辽宁 鞍山 114000)
低剂量阿帕替尼单药在晚期乳腺癌末线治疗中的临床疗效观察
赵艳凤 温福刚 李 彬 刘 君 刘 建
(鞍山市肿瘤医院肿瘤内科,辽宁 鞍山 114000)
抗血管生成治疗;阿帕替尼;晚期乳腺癌;末线治疗
根据GLOBOCAN数据显示,乳腺癌已成为全球女性发病率最高的癌症。全球每年新发病例138.4万,约45.8万死于乳腺癌[1]。4%~6%乳腺癌初诊时即为转移性乳腺癌,而早期患者中接受辅助治疗的30%~40%可进一步发展为转移性乳腺癌,5年生存率约20%[2]。晚期乳腺癌通常是不可治愈的,研究表明乳腺癌是一种血管依赖性疾病。因此,在晚期乳腺癌治疗中,抗血管生成靶向治疗越来越广泛地受到关注。血管内皮生长因子(VEGF)及其血管内皮生长因子受体(VEGFR)介导的信号传导通路在调控肿瘤血管生成过程中发挥着极其重要的作用。虽然抗血管生成靶向治疗不断有新的药物和新的方案被运用于临床,但都应用于一线或二线,且为联合治疗,并没有明确的总生存期的延长。本文报道了3例晚期乳腺癌患者末线治疗中应用单药低剂量阿帕替尼的病例,在使用阿帕替尼治疗后,病情得到了不同程度的控制,患者生存期和生活质量均得到一定程度的提高,显示出低剂量阿帕替尼单药具有潜在的治疗晚期乳腺癌的临床价值。
1 病案摘要
病例1:患者女性,62岁,住院号:0000476440。2010年1月行“左乳腺癌改良根治术”,术后病理:乳腺浸润性导管癌,淋巴结7/9。免疫组化:ER(+)<25%,PR(-),C-erbB-2(+)。术后行辅助化疗:CEF方案3个周期,多西他赛方案3个周期。后行辅助放疗,来曲唑内分泌治疗。2013年12月经CTMRI影像学检查诊断“乳腺癌术后肝多发转移”,一线化疗行多西他赛+顺铂化疗6个周期,疗效PR。后他莫昔芬口服。2015年3月肝内病灶进展,二线化疗行多西他赛+希罗达化疗6个周期,疗效SD。后希罗达维持治疗。2016年2月MRI提示右侧小脑转移,给予小脑转移病灶调强放疗。患者ECOG评分2分。5月初开始口服阿帕替尼治疗425 mg,1次/天。1个月后复查病情疗效PR,继续阿帕替尼口服,目前仍病情稳定。用药期间主要不良反应3级高血压、2级手足皮肤反应,尿蛋白(+),1级乏力,少量咳血,对症处理后好转。阿帕替尼向下调整剂量为283 mg/d(3日2粒)口服,目前仍维持治疗,不良反应可耐受。患者目前病情稳定,无进展生存期PFS为7个月。
病例2:患者女性,62岁,住院号:0000479787。2006年7月行“右乳腺癌根治术”,术后病理:右乳导管浸润癌,淋巴结3/8。免疫组化:ER(+)<5%,PR(+)40%,C-erbB-2(+)。术后行辅助化疗:CEF方案6个周期。未行内分泌治疗。2013年12月影像学检查诊断“乳腺癌术后双肺多发转移”,复查免疫组化报ER(+)70%,PR(+)25%,HER-2(0),Ki67 5%。一线化疗行多西他赛+顺铂化疗4个周期,疗效SD。后阿那曲唑口服。2015年6月彩超、MRI等影像学提示肝脏多发转移,骨多发转移,行肝病灶穿刺病理:ER(-),PR(+5%),CerbB-2(-)、CA153(+),Heppar(-),CDX-2(-),NapsinA(-),支持乳腺癌肝转移。二线化疗行长春瑞滨+希罗达化疗2个周期,疗效PD。三线化疗行吉西他滨单药5个周期,化疗3个周期后复查疗效SD,化疗5个周期后复查疗效PD。行四线治疗草酸铂化疗5个周期联合阿帕替尼口服425 mg,1次/天,化疗2个周期复查疗效PR,化疗4个周期复查疗效持续PR。阿帕替尼继续口服,每2个月复查,目前病情持续PR状态,患者一般状态良好,ECOG评分1分。用药期间主要不良反应1级乏力,尿蛋白(3+),少量咳血,2级高血压、1级手足皮肤反应,无腹泻,阿帕替尼降至212.5 mg/d口服,尿蛋白(2+),高血压口服降压药可控。目前仍维持单药阿帕替尼口服,不良反应可耐受。患者目前病情稳定,无进展生存期PFS长达12个月。
病例3:患者女性,61岁,住院号:0000487736。2013年1月行“左乳腺癌根治术”,术后病理:左乳浸润癌,淋巴结1/7。免疫组化:ER(-),PR(+)>15%,C-erbB-2(-)。术后行辅助化疗:CEF方案6个周期。未行内分泌治疗。2013年9月影像学检查诊断“乳腺癌术后左锁骨上淋巴结、纵膈淋巴结转移”,左锁骨上淋巴结穿刺病理癌。一线化疗行长春瑞滨+希罗达化疗6个周期,疗效PR。锁骨上区淋巴结、纵膈淋巴结放疗,并希罗达维持口服。2015年1月出现左胸壁肿物,穿刺病理转移癌。免疫组化:CK(+),ER(-),PR(-),Vimentin(-),C-erbB-2(1+)。二线化疗行紫杉醇+顺铂化疗6个周期,疗效SD。同时行转移病灶姑息放疗,疗效PR。后来曲唑口服。2015年12月病情进展,出现双肺多发转移,三线化疗行吉西他滨+替吉奥2个周期,疗效PD。行四线化疗FOLFOX4方案3个周期,疗效PD。患者体质下降,ECOG评分2分,2016年3月10日开始阿帕替尼口服425 mg,1次/天,1个月后复查疗效PR,继续阿帕替尼口服。用药期间主要不良反应高血压3级,2级乏力,尿蛋白(3+),无出血、腹泻及手足皮肤反应,对症处理后好转,阿帕替尼调整剂量为212.5 mg/d口服。2016年8月患者病情进展,给予最佳支持治疗,9月26日临床死亡。无进展生存期PFS为5个月,总生存OS为6.5个月。
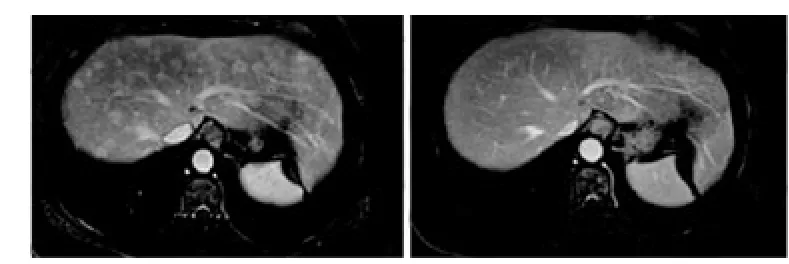
图1 应用阿帕替尼前后肝脏影像学对比
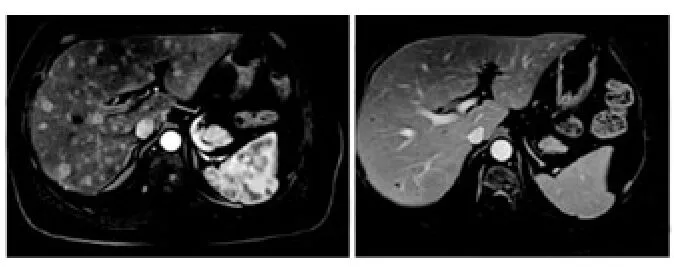
图2 应用阿帕替尼前后肝脏影像学对比
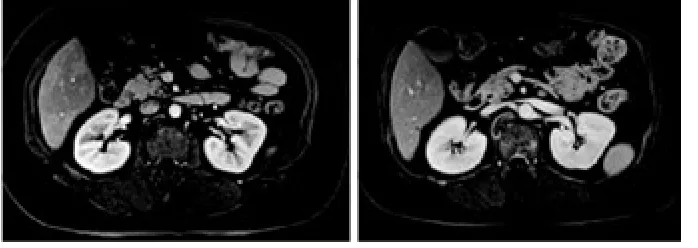
图3 应用阿帕替尼前后肝脏影像学对比
典型病例2影像学情况,患者女性,61岁。ECOG:1分。诊断:右乳腺癌术后复发Ⅳ期rT0N0M1,肝转移,肺转移,骨转移。治疗:阿帕替尼为6线治疗,PFS长达12个月,目前为持续维持PR状态。患者应用阿帕替尼425 mg/d后出现3级高血压,蛋白尿+++,口服降压药及对症处理给予下调剂量至阿帕替尼212.5 mg/d,仍然有效。应用阿帕替尼前后肝脏影像学对比。见图1~图3。
2 讨 论
乳腺癌是导致妇女死亡最常见的恶性肿瘤之一,病死率居女性各类恶性肿瘤的首位[3]。既往的抗血管生成治疗都为一线或二线的联合治疗,且没有明确的总生存期的延长。对这3例患者均为晚期乳腺癌多线治疗后,没有更好的治疗选择,尝试使用单药阿帕替尼治疗,考虑到患者多周期化疗后耐受期可能偏差,给予低剂量425 mg/d口服,由于不能耐受的不良反应剂量进一步下调低至212.5 mg/d,临床上仍然有效,病情均得到不同程度的控制。与胃癌中常规剂量850 mg/d相比,低剂量阿帕替尼在末线乳腺癌中有效,有明显的临床优势,值得进一步探索。此3例晚期乳腺癌患者,我们尝试应用低剂量阿帕替尼临床上有效,无进展生存期5~12个月,其中2例仍在随访中,分别服药7和12个月。可见低剂量阿帕替尼单药治疗晚期乳腺癌末线治疗的患者初步显示有效。
在乳腺癌的抗血管生成治疗中既往研究较多的有贝伐单抗及小分子酪氨酸激酶抑制剂。贝伐珠单抗是一种人源化单克隆抗体,通过竞争性结合VEGF来阻断胞内酪氨酸激酶激活进而阻断下游信号的促进血管生成。在晚期乳腺癌的治疗中贝伐单抗最具代表意义的临床试验是E2100[4]和AVADO[5]。两个实验不同程度的延长无进展生存,也提高了客观缓解率,但总生存期并没有显著改善。此外,Bergh等报道小分子酪氨酸激酶抑制剂舒尼替尼(Sunitinib)联合化疗治疗进展期乳腺癌患者疗效的一个Ⅲ期临床试验结果,同样显示了PFS提高了,但总生存期并无改善。综上所述,尽管以贝伐单抗为代表的抗血管生成治疗应用于晚期乳腺癌具有一定的价值,但所有相关数据显示并不能获得明确的OS获益。而对于三线或以上的关于抗血管生成治疗的相关数据少之又少,多线治疗后体质的下降,联合用药毒性增加,都使我们进一步思考:寻找一种有效低毒的药物控制病情进展,那么单药抗血管生成治疗用于末线的晚期乳腺癌是否可行呢,值得我们进一步临床探索。
阿帕替尼是一种小分子VEGFR酪氨酸激酶抑制剂,它特异性地竞争细胞内VEGFR-2的ATP结合位点,阻断下游信号转导,从而抑制肿瘤血管生成,抑制肿瘤生长[4]。Ⅰ期临床研究结果显示,阿帕替尼对多种肿瘤具有抗肿瘤活性,包括胃癌,结肠直肠癌和乳腺癌等[4]。由于阿帕替尼在胃癌的Ⅲ期临床试验中显示出良好的生存获益,2014年10月被CFDA批准上市用于晚期胃腺癌或胃-食管结合部腺癌三线或三线以上的治疗。目前尚未批准用于治疗其他恶性肿瘤,但是已在多种实体瘤中已开展临床试验。有关阿帕替尼的最佳给药剂量、用药终点的探索、不良反应的类型和程度以及有关防治措施等,都需要进一步密切观察和积累证据。
阿帕替尼在晚期乳腺癌中亦有试验证明有应用的前景及价值。阿帕替尼在转移性三阴性乳腺癌患者Ⅱ期研究中,56例可评价的患者中,中位PFS及OS分别是3.3和10.6个月[5]。ORR[CR)+PR)]为10.7%,临床获益率为25%。至随访结束时有2例患者疗效评价为持续PR状态,并且其PFS长达14.7个月及30个月。在非三阴晚期乳腺癌患者的一项Ⅱ期临床研究中,入组38例患者在研究中接受阿帕替尼中位治疗4个周期,中位随访10.1个月[6]。结果显示中位PFS及OS分别为4.0个月和10.3个月,36例可评价的患者中,ORR为16.7%,疾病控制率(DCR)为66.7%。研究结果[5]中推荐阿帕替尼的剂量为500 mg/d。这3个病例主要特点是针对晚期乳腺癌多线治疗后的,不适用当前标准治疗的末线治疗患者,化疗内分泌治疗已经耐药,体质相对偏弱,选择了阿帕替尼单药,且从低剂量开始425 mg,1次/天口服,有2例3级高血压,2例蛋白尿+++均向下调整剂量。3例患者病情均得到了有效的控制,其中2例仍为持续PR状态,患者明显受益。我们应用阿帕替尼的不同之处在于,与胃癌中标准剂量(850 mg/d)及上述乳腺癌中500 mg/d相比,阿帕替尼应用剂量更低,重要的是仍然有效。由此可见,低剂量阿帕替尼单药在晚期乳腺癌末线治疗中安全,有效,耐受性好。那么,阿帕替尼在晚期乳腺癌末线治疗中单药最低有效剂量,最佳应用剂量以及联合用药是否会增加疗效等,都需要更多的数据及实验来证明。
综上所述,低剂量单药阿帕替尼在晚期乳腺癌的治疗中初步观察到有一定的疗效,且安全性良好,尤其是多线治疗后的晚期乳腺癌患者中有很好的临床受益,今后我们期待有更多更好的试验进一步探讨该药治疗晚期乳腺癌的机制,并扩大样本量进行临床试验,获得最佳的药物使用剂量和方法。阿帕替尼在多线治疗后的晚期乳腺癌治疗中可能具有重大而深远的意义。阿帕替尼重新燃起我们对晚期乳腺癌思考,对于多线治疗后的晚期乳腺癌,低剂量阿帕替尼单药临床有效可行。对于阿帕替尼而言,在乳腺癌的故事中,这是新的开始,我们期待着!
[1] Jemal A,Bray F,Center MM,et al.Global cancer statistics[J].CA Cancer J Clin,2011,61(2):69-90.
[2] Cardoso F,Fallowfield L,Costa A,et al.Locally recurrent or metastatic breast cancer:ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up[J].Ann Oncol,2011,22(Suppl 6):vi25-30.
[3] Anderson BO,Shyyan R,Eniu A,et al.Breast cancer in limitedresource countries:an overview of the breast health global initiative 2005 guidelines[J].Breast J,2006,12(Suppl 1):S3-S15.
[4] Li J,Zhao X,Chen L,er al.Safety and pharmacokinetics of novel selective vascular endothelial growth factor receptor-2 inhibitor YN968D1 in patients with advanced malignancies[J/OL].BMC Cancer,2010,10[2016-02-22].http://link.springer.com/article/10. 1186/1471-2047-10-529.
[5] Hu X,Zhang J,Xu B,et al.Multicenter phaseⅡstudy of apatinib,a novel VEGFR inhibitor in heavily pretreated patients with metastatic triple-negative breast cancer[J].Int J Cancer,2014,135(8):1961-1969.
[6] Hu X,Cao J,Hu W,et al.Multicenter phaseⅡstudy of apatinib in non-triple-negative metastatic breast cancer[J].BMC Cancer,2014, 14(1):820.
R737.9
B
1671-8194(2017)17-0210-02
