ESI-Q-TOF-MS/MS用于碳青霉烯类抗生素及其中间体质谱裂解机理研究
2017-07-05孙子晴肖钦钦梁现蕊
苏 凤,孙子晴,肖钦钦,梁现蕊
(1.浙江工业大学 绿色制药协同创新中心,浙江 杭州 310014;2.浙江工业大学 药学院,浙江 杭州 310014)
ESI-Q-TOF-MS/MS用于碳青霉烯类抗生素及其中间体质谱裂解机理研究
苏 凤1,2,孙子晴1,2,肖钦钦1,2,梁现蕊1,2
(1.浙江工业大学 绿色制药协同创新中心,浙江 杭州 310014;2.浙江工业大学 药学院,浙江 杭州 310014)
采用电喷雾-四极杆-飞行时间串联质谱(ESI-Q-TOF-MS/MS),在正离子模式下,对美罗培南等碳青霉烯类抗生素及其合成中间体共8种化合物的裂解规律进行了探讨.实验结果显示碳青霉烯类抗生素在该质谱条件下易形成[M+H]+离子,其合成中间体则易观察到[M+Na]+离子.该8种化合物裂解途径相似,主要为分子内脱羧基反应、四元内酰胺环裂解反应及侧链结构中C—S键的裂解反应.
碳青霉烯类抗生素;电喷雾-四极杆-飞行时间串联质谱(ESI-Q-TOF-MS/MS);裂解规律
1976年,默克公司的科学家在筛选能作用于细胞壁生物合成的抑制剂过程中,从卡特利链霉菌(Streptomycescattleya)发酵液中分离得到一种具有广谱、强力抗菌活性的碳青霉烯类抗生素硫霉素(thienamycin),在随后的几十年里,人们通过对硫霉素的结构改造,陆续开发出一系列碳青霉烯类抗生素,它是治疗危重感染的常用抗菌药物之一[1].近年来,运用胶束毛细管电泳色谱法[2]、毛细管区带电泳法[3]和高效液相色谱法[4-7]等对碳青霉烯类抗生素厄他培南、美罗培南等及其有关物质进行了广泛的研究.质谱联用(LC-MS,GC-MS等)技术已成为快速、准确鉴定药物中杂质的较佳方法[8-14],在药物定性鉴别、杂质研究、体内代谢物研究和中药复杂组分分析等领域都发挥着越来越重要的作用.目前常用的质谱技术主要有高分辨率质谱(HRMS)和多级质谱(MSn).对于HRMS,以飞行时间(TOF)质谱为例,因其可以提供精确到小数点后4~6位的相对分子质量,使得仪器分辨率和相对分子质量的精确度得到提高,同时也可以获得相应碎片离子的元素组成及分子式.由于高分辨质谱的精确性,使得其在化合物结构鉴定方面有着较广泛的应用[15-19].MSn可以提供丰富的碎片离子信息以及裂解信息,利用得到的数据可以推测出药物及其杂质的裂解模式,进而结合已有的知识鉴定出未知化合物的结构,在杂质分析和控制方面具有重要作用.
目前已有关于碳青霉烯类抗生素美罗培南、厄他培南杂质谱裂解机理的报道[20-23],但未见对该类抗生素及其相关合成中间体质谱裂解规律的系统总结.对厄他培南、美罗培南、比阿培南和多尼培南及其4种合成中间体(保护美罗培南、MAP、4AA水解物和4AA氧化物)进行ESI-ITMSn,ESI-QTOF-MS/MS分析和研究,发现了该类化合物的质谱裂解规律,为碳青霉烯类抗生素及其有关物质结构解析和定量分析提供科学依据.
1 实验部分
1.1 主要试剂与仪器
Micro TOF QⅡ质谱仪,德国Bruker公司:配有电喷雾(ESI)离子源,Compass数据处理系统,自动进样器.
乙腈(HPLC纯),德国Merck公司;质谱校正液(CF3COONa),阿拉丁试剂有限公司;实验用水,自制超纯水;样品溶液配制,分别取少量厄他培南、美罗培南、比阿培南、多尼培南、MAP、保护美罗培南、4AA水解物和4AA氧化物用一定比例的水-乙腈-10%甲酸的混合溶液溶解样品后进样.碳青霉烯类抗生素结构式为8种碳青霉烯类抗生素及其合成中间体化合物均由浙江海翔制药有限公司提供,纯度99%以上,其结构式如表1所示.


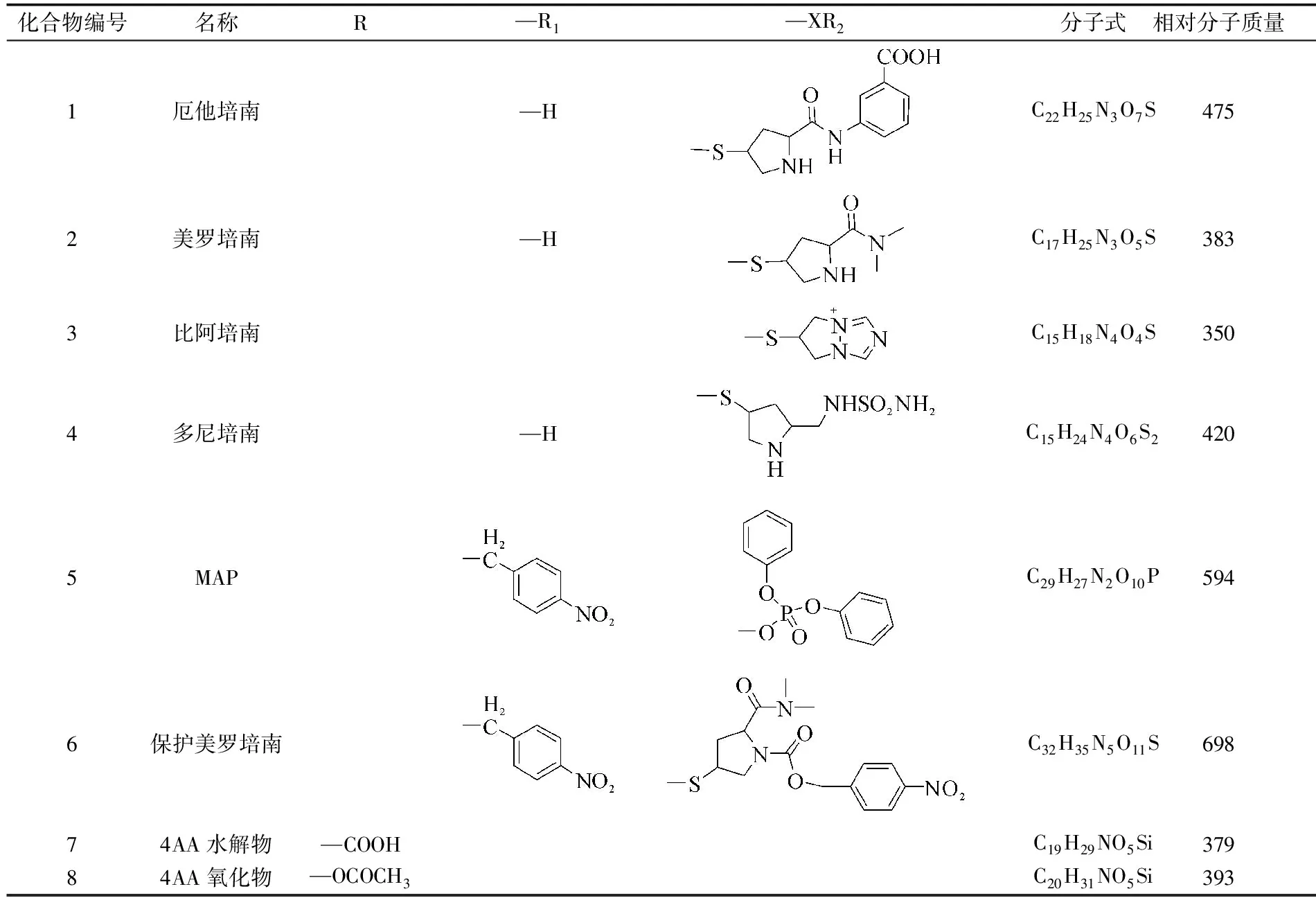
表1 碳青霉烯类抗生素及其合成中间体的结构Table 1 The structures of carbapenems antibiotics and its synthetic intermediates
1.2 质谱分析条件
电喷雾(ESI)离子源;ESI源电压500 V;毛细管电压4 500 V;雾化气体液氮;雾化气压力0.4 Bar;氮气温度180 ℃;氮气流速4.0 L/min;碰撞气体氩气;进样速度180 μL/h;在正离子模式下先进行一级质谱全扫描,m/z为50~1 500,再将得到的待测物的准分子离子[M+H]+或[M+Na]+作为母离子进行二级质谱分析,以用于化合物裂解规律的研究.
2 结果与讨论
2.1 8种化合物的一级全扫描质谱
采用电喷雾离子源,在正离子检测模式下,对8种化合物进行一级质谱全扫描分析,检测结果列于表2.其中4种碳青霉烯类抗生素易观察到[M+H]+准分子离子峰,而4种碳青霉烯类抗生素的合成中间体不易形成[M+H]+的准分子离子峰,而易得到[M+Na]+准分子离子峰.
表2 8种化合物的一级质谱数据
Table 2 The MS data of carbapenems antibiotics and its synthetic intermediates
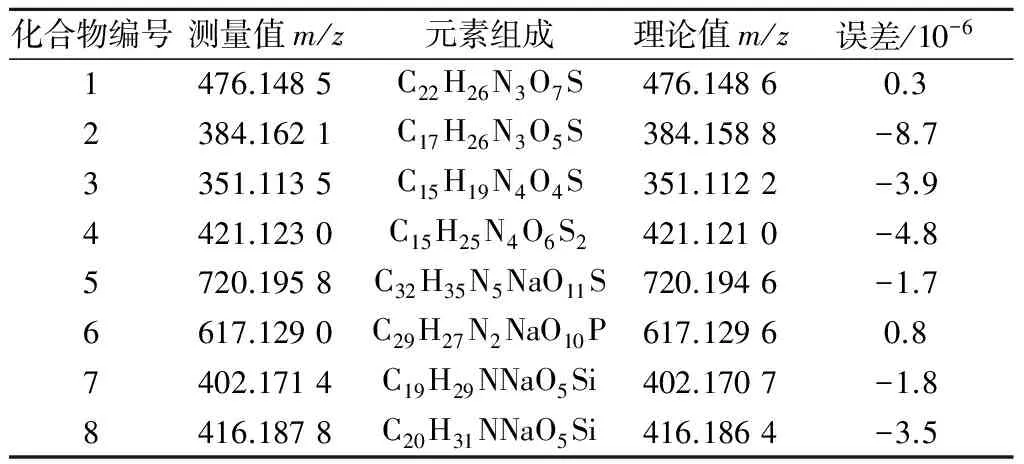
化合物编号测量值m/z元素组成理论值m/z误差/10-61476.1485C22H26N3O7S476.14860.32384.1621C17H26N3O5S384.1588-8.73351.1135C15H19N4O4S351.1122-3.94421.1230C15H25N4O6S2421.1210-4.85720.1958C32H35N5NaO11S720.1946-1.76617.1290C29H27N2NaO10P617.12960.87402.1714C19H29NNaO5Si402.1707-1.88416.1878C20H31NNaO5Si416.1864-3.5
2.2 化合物1~6的MS/MS分析及裂解规律研究
对化合物1~6的准分子离子进行MS/MS分析,所得到的主要产物离子的精确质量数如表3所示,该6种化合物因结构中都具有碳青霉烯类抗生素的母环结构,表现出了相似的裂解途径.
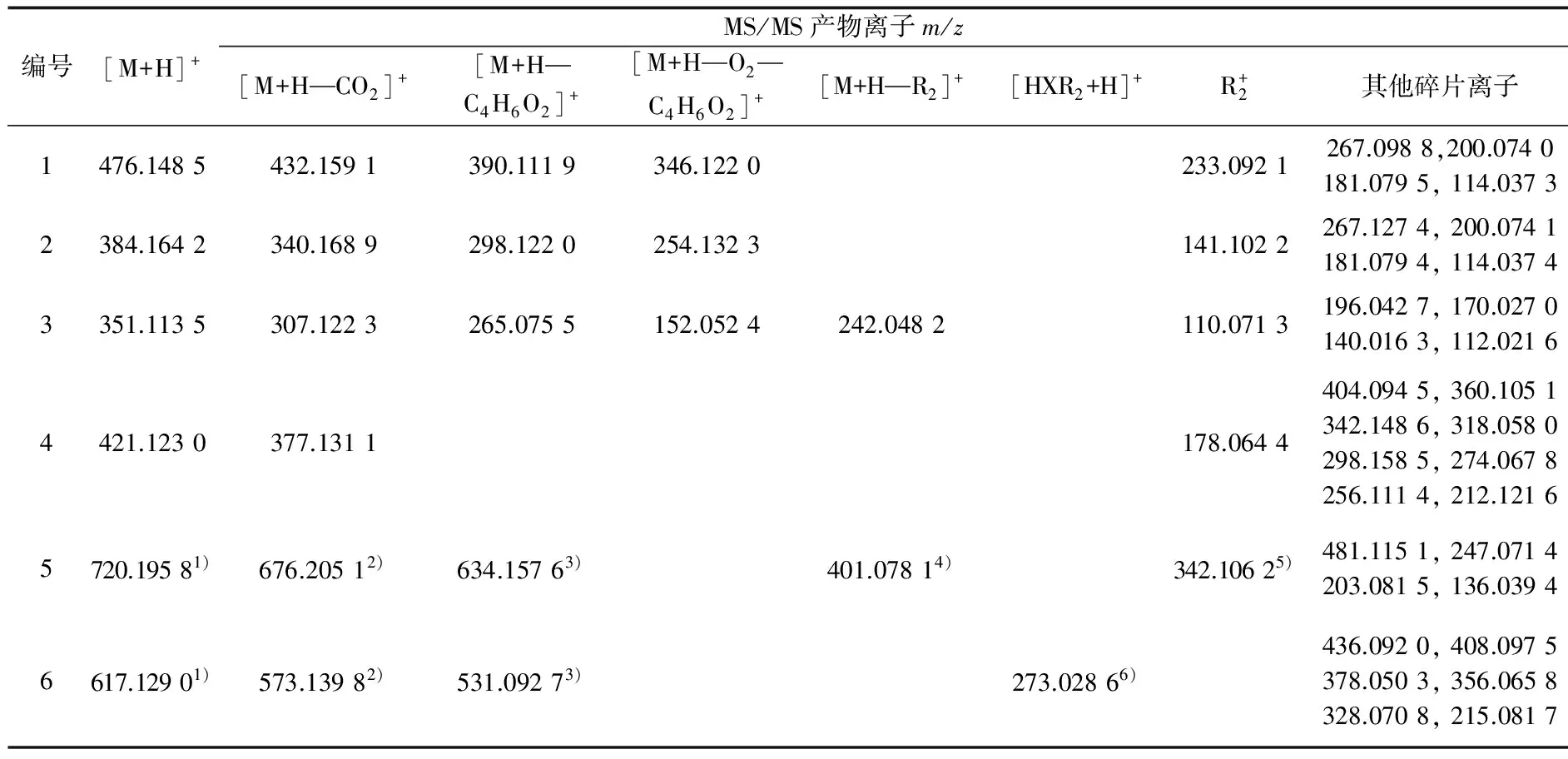
表3 化合物1~6的[M+H]+离子在ESI-Q-TOF-MS/MS谱图中的主要产物离子Table 3 Major product [M+H]+ions from ESI-Q-TOF-MS/MS spectrum of compounds 1~6
注:1) [M+Na]+ion;2) [M+Na—CO2]+ion;3) [M+Na—C4H6O2]+ion;4) [M+Na—R2+H]+ion;5) [R2—H+Na]+ion;6) [HXR2+Na]+ion.
厄他培南[M+H]+准分子离子(m/z=476)在正离子模式下,所得到的MS/MS扫描图可看到4种主要碎片离子:m/z为432,390,346和233,同时还可以看到一些相对丰度较低的碎片离子m/z为267,200,181和114.准分子离子m/z=432与准分子离子m/z=476相比减少了44 u,该子离子可能是由母核上的羧基发生脱羧反应失去一分子CO2所得到.离子m/z=390与准分子离子m/z=476相比减少了86 u,该碎片离子的形成可能是因四元内酰胺环发生[2,2]逆Diels-Alder反应而产生的,包含酰胺键断裂和C5—C6单键的断裂.离子m/z=346可能是由离子m/z=390再发生脱羧反应失去一分子CO2得到,该中间体侧链R2基团如果发生酰胺键断裂脱去一分子对氨基苯甲酸后,再脱去一分子CO即生成离子m/z=181.离子m/z=114的形成可分a,b和c三种途径:途径a为[M+H]+(m/z=476)准分子离子先脱去一分子CO2,再脱去侧链,最后失去86 u形成;途径b为[M+H]+(m/z=476)准分子离子先失去一分子C4H6O2(相对分子质量86 u),再脱去一分子CO2(相对分子质量44 u),最后脱去侧链形成;途径c为[M+H]+准分子离子发生母核与侧链之间的断裂,形成侧链互补离子对m/z=233和m/z=244,而离子m/z=244易再脱去一分子CO2形成较稳定的m/z=200离子峰.离子m/z=200再失去一分子C4H6O2得到离子m/z=114.对于子离子m/z=267,其并未得到一个确定的分子组成,说明该信号可能是由(Ⅰ),(Ⅱ)元素组成不同的两种离子混合而成的.美罗培南因侧链结构与厄他培南相差较小,其[M+H]+的裂解途径与厄他培南相似,不同的是其m/z=267离子有确定的元素组成(Ⅰ),化合物1,2 [M+H]+的可能的裂解途径为

比阿培南和多尼培南[M+H]+的裂解途径稍有不同,主要区别在于比阿培南侧链结构中的氮杂双环结构易发生C—N键断裂脱去一个三氮五元杂环,其[M+H]+可能的裂解途径为

保护美罗培南[M+Na]+准分子离子(m/z=720)二级质谱得到的碎片离子主要有m/z为342,634,203,481,247和136.子离子m/z=634与相对丰度较低的子离子m/z=676的断裂与厄他培南相似,分别由准分子离子m/z=720失去一分子CO2和C4H6O2得到.离子m/z=634再发生酯基C—O单键断裂脱去一分子对硝基苯甲醇生成离子m/z=481.[M+Na]+准分子离子再经厄他培南途径c发生母核与侧链之间的断裂,形成侧链互补离子对m/z=342和m/z=401.离子m/z=247是由离子m/z=342先脱去一分子NH(CH3)2后,再脱去一分子CO后所得,在这个过程中同时发生了Na-H交换.离子m/z=247失去一分子CO2得到离子m/z=203,然后再丢掉氮杂环后形成离子m/z=136.
MAP[M+Na]+准分子离子(m/z=720)二级质谱得到的碎片离子主要有m/z=531,m/z=356和一些相对丰度较低的碎片离子.离子m/z=378可能是由MAP[M+Na]+准分子离子先失掉C4H6O2生成离子m/z=531,该中间体再发生酯基C—O单键断裂脱去一分子对硝基苯甲醇所得.离子m/z=573可能是由准分子离子m/z=720脱去一分子CO2而得到,该中间体可再连续脱去一分子NO2、一分子苯酚和苯正离子后得到离子m/z=356,该离子再丢失一分子CO后生成离子m/z=328.另一方面,离子m/z=573也可先脱去一分子对硝基甲苯形成离子m/z=436,再脱去一分子CO2后形成m/z=408.而m/z=215离子的形成可分三种途径,都为失去一分子CO2,一分子C4H6O2和碎片离子m/z=273,同时也发生了Na-H交换反应,只是裂解顺序不同而已.MAP[M+Na]+可能的裂解途径为

2.3 化合物7,8的[M+Na]+MS/MS分析及裂解规律研究
对4AA氧化物[M+Na]+准分子离子(m/z=416)进行二级质谱分析,也得到丰富的碎片离子峰.[M+Na]+准分子离子四元内酰胺环上C-4位乙酰氧基可能产生Ⅰ,Ⅱ,Ⅲ和Ⅳ四种断裂方式.途径Ⅰ为四元内酰胺环上C-4位发生脱乙酰氧基反应,若O与邻位H结合,则丢掉一分子乙酸形成离子m/z=356,若与Na结合,则丢掉一分子乙酸钠形成离子m/z=334,而m/z=334碎片离子由于C-3位基团上杂原子O的强电负性易使分子内发生电子重排反应生成离子m/z=159.途径Ⅱ为在四元内酰胺环上C-4位乙酰氧基上发生甲基重排脱去一分子CO,再发生H重排脱去一分子HCHO后,再脱去1-叔丁基-二甲基-硅醇,四元内酰胺环内发生脱羰基反应,最后生成离子m/z=198.途径Ⅲ为在四元内酰胺环上C-4位乙酰氧基上发生酯基C—O键断裂失去一分子CH2=C=O,脱去1-叔丁基-二甲基-硅醇,脱去苯甲基醚等连续断裂反应形成离子m/z=134.途径Ⅳ为C-4位乙酰氧基发生分子内重排后脱去一分子CO2,该中间体四元内酰胺环的支链乙基再发生C—O键断裂后,若O与邻位H结合,则丢掉1-叔丁基-二甲基-硅醇后生成离子m/z=240,若与Na结合,则丢掉1-叔丁基-二甲基-硅醇钠形成m/z=218.4AA氧化物[M+Na]+可能裂解途径为
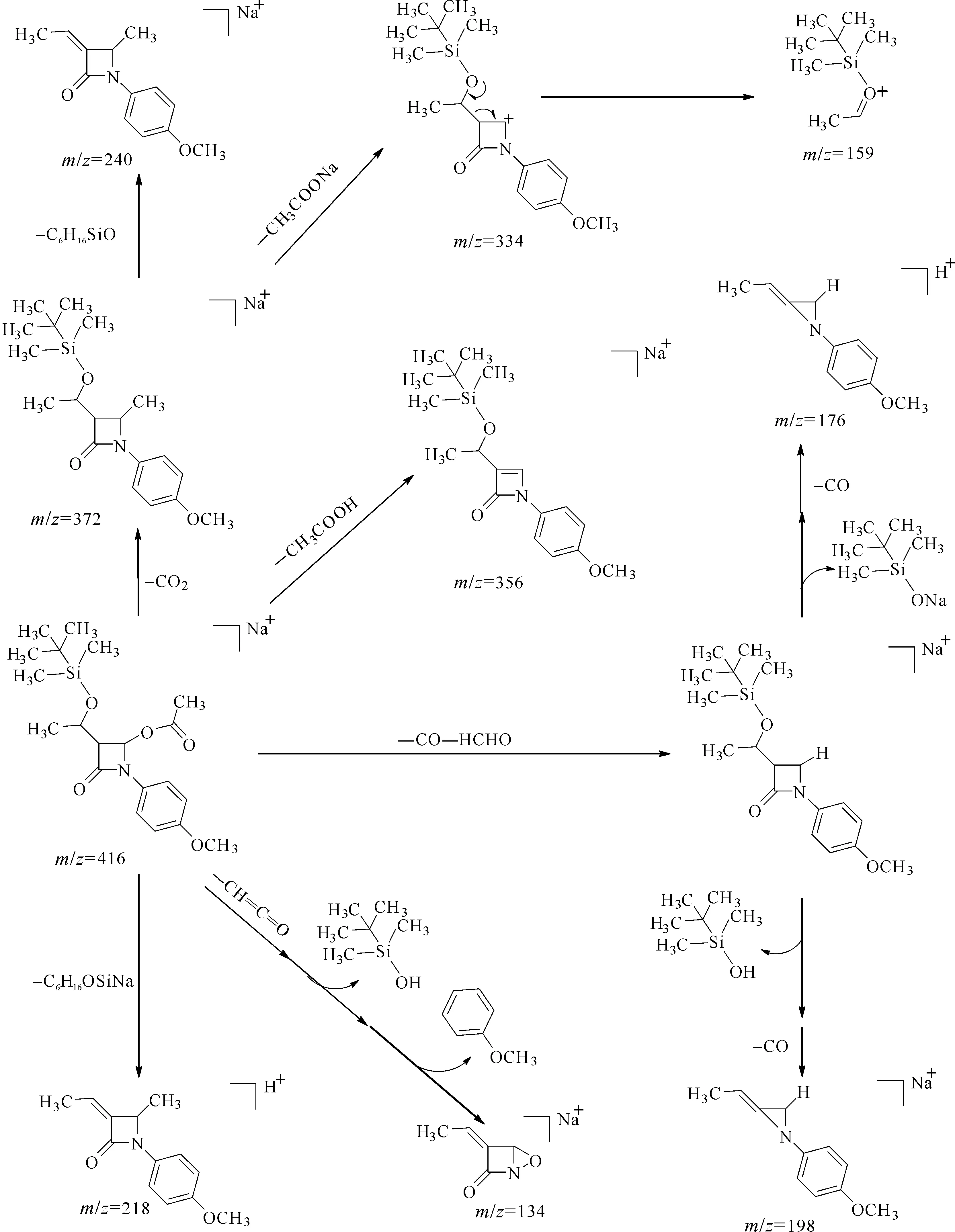
4AA水解物[M+Na]+的裂解方式与4AA氧化物相似,不同的是4AA水解物可发生四元内酰胺环C2—N1和C3—C4键断裂而开环形成碎片离子m/z=202.4AA水解物和4AA氧化物[M+Na]+MS/MS产生的主要碎片离子的分子式、精确质量数和误差如表4所示.

表4 化合物7,8的[M+Na]+离子在ESI-Q-TOF-MS/MS谱图中的主要产物离子Table 4 Major product [M+Na]+ ions from ESI-Q-TOF-MS/MS spectrum of compounds 7, 8
3 结 论
笔者应用电喷雾-四级杆-飞行时间串联质谱(ESI-Q-TOF-MS/MS)技术,研究了几种典型的碳青霉烯类抗生素及其合成中间体的裂解途径.发现该类抗生素在正离子检测模式下,主要以[M+H]+准分子离子峰形式存在,而其合成中间体主要以[M+Na]+准分子离子峰形式存在.二级质谱实验结果表明:无论该类化合物以何种准分子离子形式存在,其二级质谱裂解方式都具有相似的裂解途径或模式,主要为分子内脱羧基反应(途径C)、四元内酰胺环裂解反应(途径A)及侧链结构中C—S键的裂解(途径B)反应.
[1] 胡付品,朱德妹.KPC型碳青霉烯酶研究进展[J].中国感染与化疗杂志,2008,11(1):76-80.
[2] MICHALSKA K, PAJCHEL G, STEFAN T. Different sample stacking strategies for the determination of ertapenem and its impurities by micellar electrokinetic chromatography in pharmaceutical formulation[J]. Journal of chromatography A, 2009, 1216(14): 2934-2942.
[3] TANIGUCHI S, HAMASE K, KINOSHITA A, et al. Simple and rapid analytical method for carbapenems using capillary zone electrophoresis[J]. Journal of chromatography B, 1999, 727(1/2): 219-225.
[4] MUSSON D G, BIRK K L, KITCHEN C J, et al. Assay methodology for the quantitation of unbound ertapenem, a new carbapenem antibiotic, in human plasma[J]. Journal of chromatography B, 2003, 783(1): 1-9.
[5] NRIROGI R V, KANDIKERE V N, SHRIVATAVA W, et al. Quantification of faropenem in human plasma by high-performance liquid chromatography[J]. Arzneimittelforschung, 2005, 55(22): 762-766.
[6] GAO S W, CHEN X, TAO H, et al. Determination of faropenem in human plasma and urine by liquid chromatography-tandem mass spectrometry[J]. Biomed chromatogr, 2008, 22(1): 5-12.
[7] LEGRAND T, CHHUN S, REY E, et al. Simultaneous determination of three carbapenem antibiotics in plasma by HPLC with ultraviolet detection[J]. Journal of chromatography B, 2008, 875(2): 551-556.
[8] XIA M, HANG T J, ZHANG F, et al. The stability of biapenem and structural identification of impurities in aqueous solution[J]. Journal of pharmaceutical and biomedical analysis, 2009, 49(4): 937-944.
[9] SAJONZ P, NATISHAN T K, WU Y, et al. Preparation, isolation, and characterization of dimeric degradation products of the 1β-methylcarbapenem antibiotic, ertapenem[J]. Journal of liquid chromatography & related technologies, 2001, 24(5): 2999-3015.
[10] SUN C, WU J M, PAN Y J. Characterization of novel hydrolysis products of carbapenems by electrospray ionization mass spectrometry[J]. Rapid commun in mass spectrometry, 2009, 23(19): 3205-3212.
[11] MENDZE A, CHAGASTELLES P, PALMA E, et al. Thermal and alkaline stability of meropenem: degradation products and cytotoxicity[J]. International journal of pharmaceutics, 2008, 350(1/2): 95-102.
[12] 李祖光,国明,聂晶,等.直接进样杆在线衍生GC-MS测定阿司匹林中的水杨酸[J].浙江工业大学学报,2014,42(1):67-72.
[13] 曹慧,林珍珍,陈小珍,等.固相萃取-气相色谱/三重四级杆质谱法同时分析蔬菜中的50种农药残留量[J].浙江工业大学学报,2012,40(3):279-283.
[14] 李祖光,孟微微,王芳,等.超声微波协同水蒸气蒸馏-GC/MS分析生姜挥发油化学成分[J].浙江工业大学学报,2013,41(6):614-619.
[15] WU Z J, FANG D M, HAN D, et al. Analysis of sesterterpenoids fromAspergillusterreususing ESI-QTOF and ESI-IT[J]. Phytochemical analysis, 2010, 21(4): 374-383.
[16] JIN Y, ZHANG X L, SHI H, et al. Characterization of Cglycosyl quinochalcones inCarthamustinctoriusL. by ultraperformance liquid chromatography coupled with quadrupole-time-of-flight mass spectrometry[J]. Rapid commun in mass spectrometry, 2008, 22(3): 1275-1287.
[17] BIJTTEBIER S K, HONDT E, HERMANS N, et al. Unravelling ionization and fragmentation pathways of carotenoids using orbitrap technology: a first step towards identification of unknowns[J]. Journal of mass spectrometry, 2013, 48(6): 740-754.
[18] YANG M, LU Z Q, YU K, et al. Studies on the fragmentation pathways of ingenol esters isolated fromEuphorbiaesulausing IT-MSn and Q-TOF-MS/MS methods in electrospray ionization mode[J]. International journal of mass spectrometry, 2012, 323: 55-62.
[19] BUSE J, EAI B, VERRALL R E, et al. Tandem mass spectrometric analysis of novel diquaternary ammonium gemini surfactants and their bromide adducts in electrospray-positive ion mode ionization[J]. Journal of mass spectrometry, 2011, 46(10): 1060-1070.
[20] CORNELISEC A, XIAO Y, XIN X, et al. Elucidation of fragmentation mechanisms involving transfer of three hydrogen atoms using a quadrupole time-of-flight mass spectrometer[J]. Journal of mass spectrometry, 2001, 36(5): 575-579.
[21] ZHAO Z X, QIN X Z, REED R A. Identification by LC/MSn of degradates of a novel carbapenem antibiotic in an aqueous matrix [J]. Journal of pharmaceutical and biomedical analysis, 2002, 29(1/2): 173-181.
[22] 王晓雪,赫军,崔刚,等.碳青霉烯类抗生素的电喷雾质谱裂解规律分析[J].中国药房,2014,25(45):4295-4296.
[23] LI J, ZHANG D S, CHONG XM, et al. Influence of substituent groups at the 3-position on the mass spectral fragmentation pathways of cephalosporins[J]. Rapid commun in mass spectrometry, 2010, 24(14): 2143-2150.
(责任编辑:朱小惠)
Fragmentation pathways of carbapenems antibiotics and their intermediates using electrospray ionization quadrupole time-of-flight mass spectrometry
SU Feng1,2, SUN Ziqing1,2, XIAO Qinqin1,2, LIANG Xianrui1,2
(1. Collaborative Innovation Center of Green Pharmaceuticals, Zhejiang University of Technology, Hangzhou 310014, China;2. College of Pharmaceutical Sciences, Zhejiang University of Technology, Hangzhou 310014, China)
The fragmentation pathways of carbapenem antibiotics and their intermediates were investigated by electrospray ionization quadrupole time-of-flight tandem mass spectrometry (ESI-Q-TOF-MS/MS) in positive mode. The experimental results showed that carbapenem antibiotics gave the prominent [M+H]+ions, while the intermediates yielded prominent [M+Na]+ions. All the eight compounds shared similar cleavage pathways, which involved the decarboxylation reaction, [2,2]-trans-Diels-Alder cleavage within the quaternary lactam ring, and the carbon-sulphur bond cleavage reaction.
carbapenems antibiotics; electrospray ionization quadrupole time-of-flight mass spectrometry (ESI-Q-TOF MS/MS); fragmentation pathways
2017-03-23
苏 凤(1983—),女,浙江临安人,研究实习员,研究方向为药物结构鉴定以及杂质分离分析,E-mail:sufeng@zjut.edu.cn.
R248.1
A
1674-2214(2017)02-0070-07
