乙氧氟草醚的1H、13C NMR全归属
2017-04-18梁向晖毛秋平钟伟强
梁向晖 毛秋平 钟伟强
(华南理工大学化学与化工学院,广州510640)
乙氧氟草醚的1H、13C NMR全归属
梁向晖 毛秋平 钟伟强
(华南理工大学化学与化工学院,广州510640)
乙氧氟草醚是含氟二苯醚类广谱、高效除草剂,关于其核磁共振(NMR)波谱数据全归属的研究未见报道,本实验应用一维(1D)和二维(2D)NMR技术,包括1H NMR、13C NMR、DEPT135、1H-13C HMBC、1H-13C HSQC、1H-1H COSY及19F NMR等,对乙氧氟草醚的1H、13C NMR数据进行了全归属,并讨论了19F对1H和13C NMR谱的影响;为含氟二苯醚类除草剂的核磁共振表征提供指导。
乙氧氟草醚 除草剂 核磁共振 结构归属
乙氧氟草醚(Oxyfluorfen)又称乙氧醚割草醚,属氟二苯醚类除草剂,商品名有果尔、草枯特、杀草狂等。该产品于1975年美国罗门哈斯公司最先开发出来,分子式为C15H11ClF3NO4,相对分子量为361.70,不饱和度Ω=9,其结构式如图1所示。乙氧氟草醚的除草活性比相应的除草醚高5~10倍,为杀草丹的16.32倍。乙氧氟草醚使用范围广,杀草谱广,持效期长,亩用量少,活性高,可与多种除草剂复配使用。该除草剂使用方便,既可芽前处理,又可芽后处理,且毒性较低[13]。目前对乙氧氟草醚的研究主要涉及剂型、除草活性、环境行为及残留分析等[4,5],而关于其核磁共振(NMR)波谱数据全归属的研究未见报道。NMR波谱数据在分析未知或已知化合物的结构、探讨结构与活性的相互作用关系,以及区分异构体等方面具有重要的指导作用[6,7]。因此,本实验利用NMR分析技术对乙氧氟草醚结构进行表征,测定其一维(1D)和二维(2D)NMR谱,包括1H NMR、13C NMR、DEPT135、1H-13C HMBC、1H-13C HSQC、1H-1H COSY和19F NMR谱等,对该化合物的1H和13C NMR信号进行了详细归属,对含氟二苯醚类除草剂的结构分析具有一定的参考价值。

图1 乙氧氟草醚结构式
1 实验部分
1.1 主要试剂、样品及仪器
1H NMR、13C NMR、DEPT135、1H-1H COSY、1H-1H NOESY、1H-13C HSQC、1H-13C HMBC、19F NMR实验均在Bruker AVANCE III 400型超导NMR谱仪上完成,采用BBFO-5mm多核宽带探头和内径为5mm的NMR样品管(ST-500,NORELL)。乙氧氟草醚购买于百灵威公司;CDCl3(氘化率为99.8%,CIL,含0.03%TMS)购自青岛腾龙微波科技有限公司。
1.2 实验条件
样品溶于CDCl3,以TMS为内标.实验温度为(298.0±0.1)K,1H和13C NMR的工作频率分别为400.13MHz和100.61MHz,谱宽分别为8223.7Hz和24038.5Hz.DEPT135采用仪器自带的标准脉冲序列deptsp135,谱宽为16 129.0Hz.2DNMR实验包括梯度场1H-1H COSY、1H-13C HSQC、1H-13C HMBC及19F NMR等,均采用标准脉冲序列。1H-1H COSY的F2(1H)和F1(1H)维谱宽均为5341.9Hz,采样数据点阵t2×t1=2048× 128;1H-13C HSQC和1H-13C HMBC的F2(1H)和F1(13C)维谱宽分别为5330.5Hz和16667.8Hz,采样数据点阵t2×t1=1 024×256;1H-13C HMBC的F2(1H)和F1(13C)维谱宽分别为5208.3Hz和22347.8Hz,采样数据点阵t2×t1=2048 ×128。
2 结果与讨论
2.1 1DNMR谱分析
从1H NMR谱(图2)可以看出,在高场δ4.15和δ1.49分别有一组四重峰和三重峰,面积比为2∶3,前者为被甲基裂分的亚甲基信号,后者为被亚甲基裂分的甲基峰信号,归属于乙基(-CH2CH3)信号峰;在δ7.92~δ6.46出现六组信号,且面积比为1∶1∶1∶1∶1∶1,归属于6个苯环上的氢的信号峰;且谱图中存在4组d峰和2组dd峰。13C NMR谱(图3)可以发现,出现四组由于受到三氟甲基的耦合作用而裂分为四重峰的峰,位移分别为123.059(-CF3,JC-F=272.07Hz)125.56(C-5,3JC-F=3.60Hz),128.47(C-4,2JC-F=33.43Hz),128.57(C-3,3JC-F=3.71Hz)。DEPT135谱(图4)可知存在1个甲基、1个亚甲基、6个次甲基的峰。从19F NMR谱(图5)可看出有一个很强单峰,该峰为三氟甲基峰。

图2 乙氧氟草醚的1H NMR谱
1H-NMR数据分析(400M,CDCl3):1.492(3H,CH3,t,7.2Hz),4.150(2H,CH2,q,7.2Hz),6.459(1H,H-6’,dd,9.01Hz。,2.42Hz),6.709(1H,H-2’,d,2.42Hz),7.218(1H,H-6,d, 8.51Hz),7.591(1H,H-5,dd,8.51Hz,1.61Hz),7.799(1H,H-3,d,1.61Hz),7.918(1H,H-5’,d,9.04Hz)

图3 乙氧氟草醚的13C NMR谱
13C-NMR数据分析(100M,CDCl3):14.37(-CH3)65.72(-CH2-),103.73(C-2’),108.05(C-6’),121.84(C-6),123.059(-CF3,JC-F=272.07Hz)125.56(C-5,3JC-F=3.60Hz),127.09(C-2),128.09(C-5’),128.47(C-4,2JC-F=33.43Hz),128.57(C-3,3JC-F=3.71Hz),135.50(C-4’),153.49(C-1),154.80(C-3’),160.76(C-1’)。
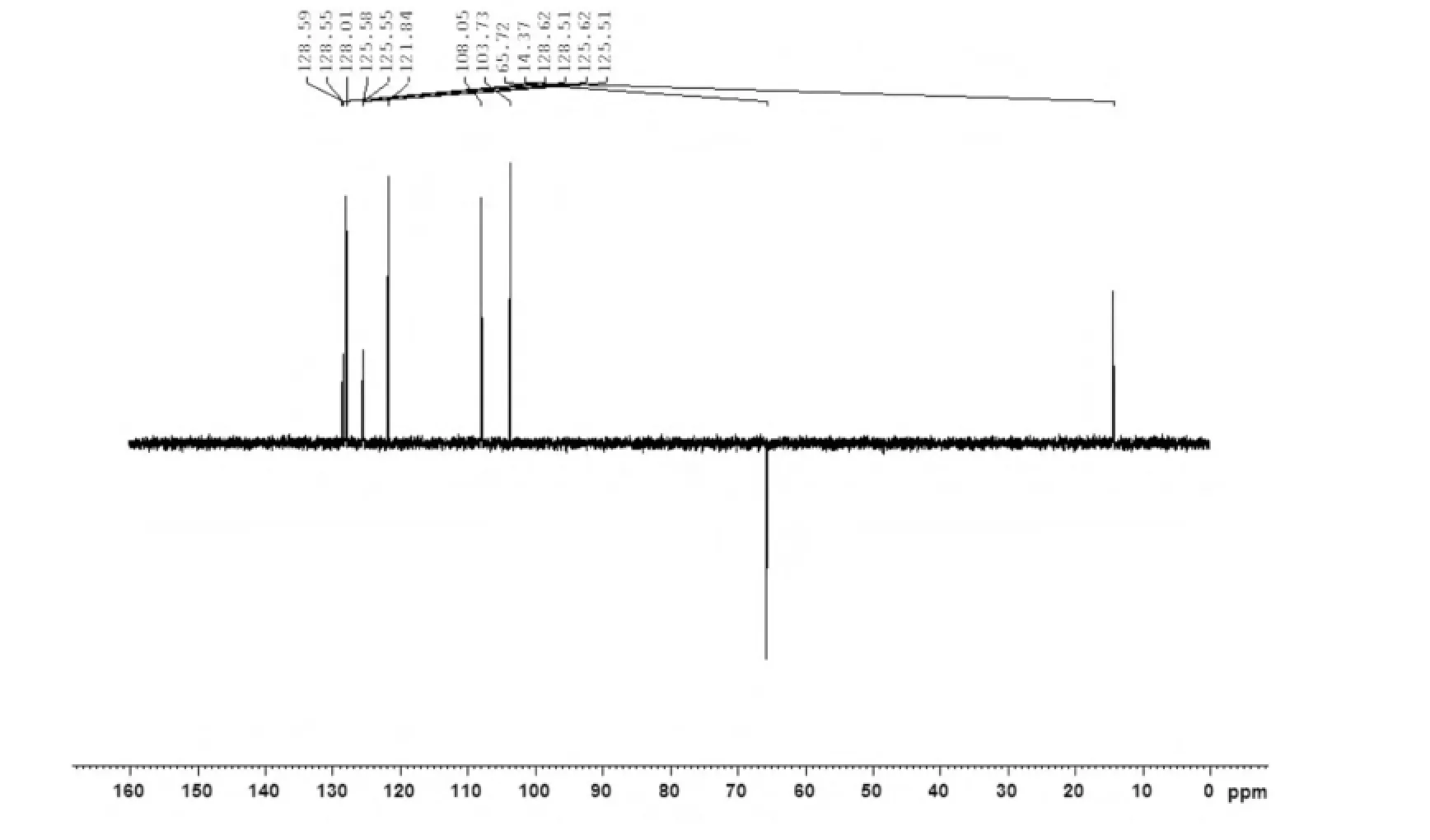
图4 乙氧氟草醚的DEPT 135谱

图5 乙氧氟草醚的19F-NMR谱
2.2 2DNMR谱分析
从1H-1H COSY谱(图6)可以看出:H5’和H6’是同一个苯环上相邻,互相裂分成d峰,H5和H6两个氢也是同一个苯环上相邻,互相裂分成d峰。6.459(1H,H-6’,dd,9.01Hz。,2.42Hz),7.918(1H,H-5’,d,9.04Hz)6.709(1H,H-2’,d,2.42Hz)及7.218(1H,H-6,d,8.51Hz),7.591(1H,H-5,dd,8.51Hz,1.61Hz),7.799(1H,H-3,d,1.61Hz)。H5’由于受到拉电子基(NO2)与苯环形成π-π共轭,使苯环电子云密度降低,δ值低场移动。
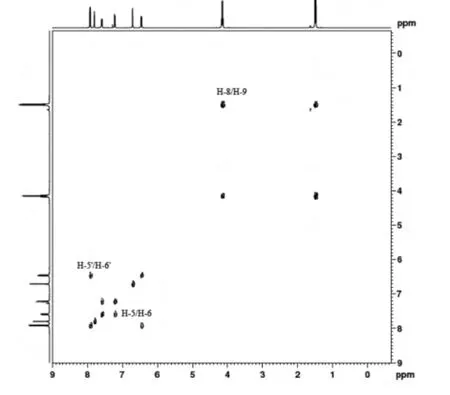
图6 乙氧氟草醚的1H-1H COSY谱
HSQC谱(图7),其HSQC数据统计归属见表1。由图7及表1可以看出,C3和C5被裂分成四重峰,表明C3和C5均处于三氟甲基的邻位。而H3的化学位移往低场偏移较多,且为d峰,说明H3是处在苯氧基间位,且其邻位连着三氟甲基。

图7 乙氧氟草醚的HSQC谱
HMBC谱(图8、图9),其HMBC数据统计归属见表1。由图8、图9及表1可以看出,H8和C3’存在远程相关,同时C3’与H2’、H5’存在远程相关。C1’与H2’、H5’、H6’存在远程相关。C1’与H3、H5、H6存在远程相关,表明C1’与苯氧醚相连,C3’与乙氧基相连,C4’与硝基相联,C1与H3、H5、H6存在远程相关,表明C1与苯氧醚相连。从碳谱中得知C3和C5分别为四重峰(q峰),说明C3和C5中间的C4连有三氟甲基(-CF3);同时C4与H3、H5、H6存在远程相关。而H3的化学位移往低场偏移较多,且为d峰,表明H3应该处在苯氧基间位,且其邻位连着三氟甲基。
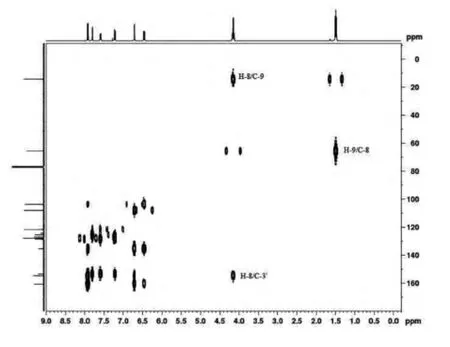
图8 乙氧氟草醚的HMBC谱
乙氧氟草醚的1H NMR和13C NMR信号全归属结果见表1。由上面分析知,H3、H5和H6在同一个苯环上;H2’、H5’与H6’在同一个苯环上。从1HNMR中6个芳氢的化学位移可以看出:相对于苯环氢的化学位移,H2’和H6’往高场移动,表明该苯环上连有给电子基,即乙氧基(-OCH2CH3),形成p-π共轭,使苯环的电子云密度增大,δ值向高场位移;而H5’往较低场移动,且在六个芳氢中化学位移最大,因而其所在的苯环上有一个强的吸电子基,即硝基(-NO2),由于π-π共轭,使苯环的电子云密度降低,δ值向低场位移[8]。
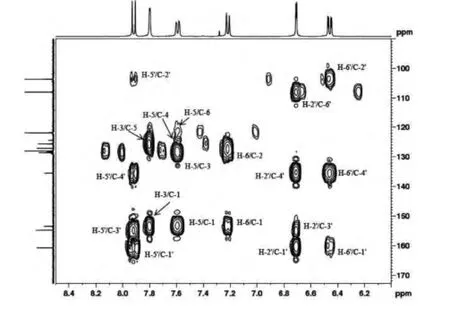
图9 乙氧氟草醚的HMBC低场放大图谱
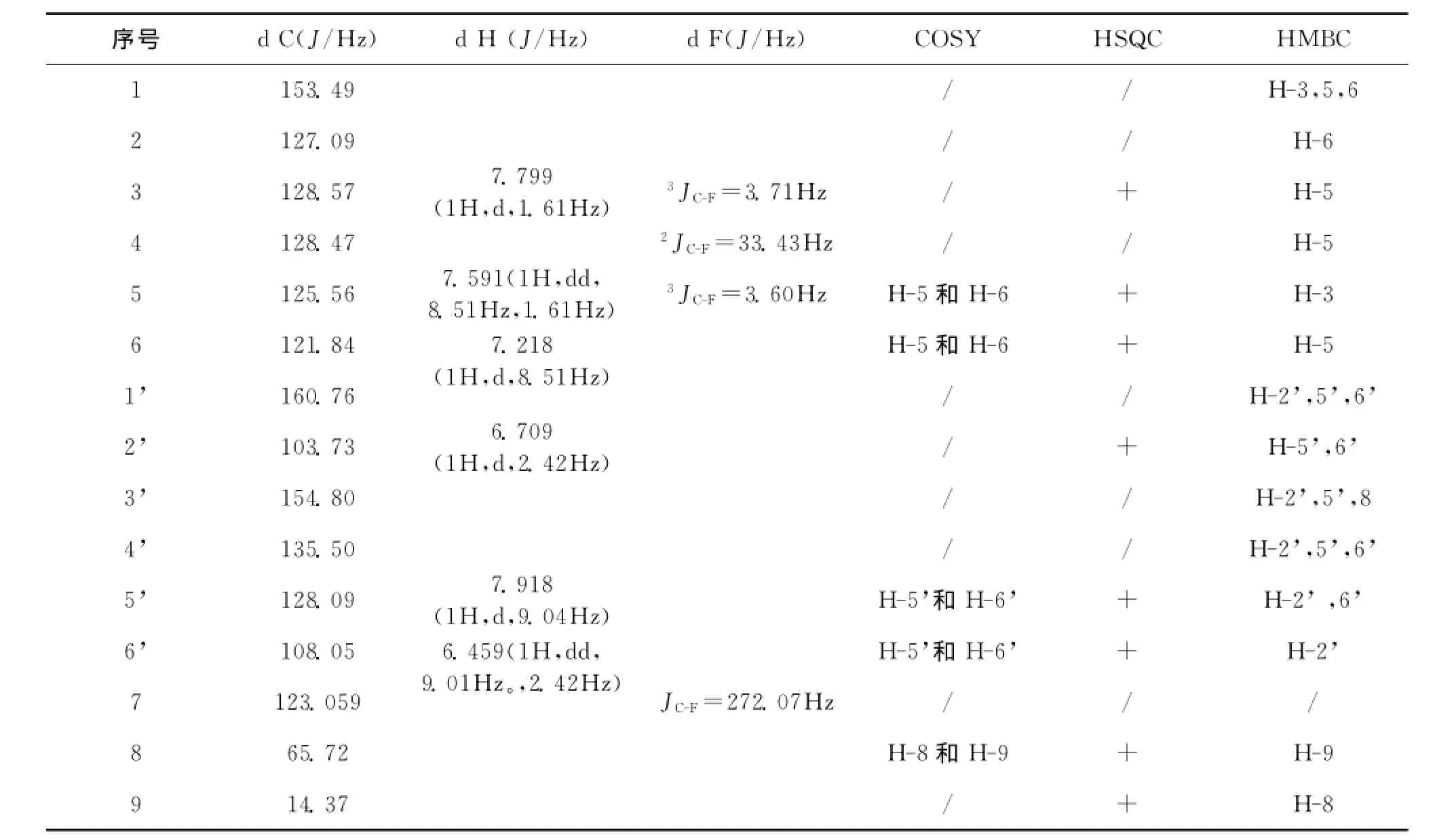
表1 乙氧氟草醚的NMR信号全归属
3 结论
运用1D和2DNMR技术对乙氧氟草醚进行了NMR测试,分析和归属了乙氧氟草醚所有的1H和13C NMR信号。应用该分析技术及波谱学数据,为含氟二苯醚类除草剂的NMR结构表征提供技术指导。
[1]邓延岗,易芬远,韦茂春,等.30%丁草胺·乙氧氟草醚水乳剂防除甘蔗田杂草药效试验[J].甘蔗糖业,2014,1:20-23.
[2]侯新玲,郭志刚,郭振营,等 .乙氧氟草醚与莠灭净混剂防治玉米田杂草的室内活性配方筛选[J].安徽农业科学,2016,(03):183-184.
[3]齐萌,王亚楠,康占海,等.14%噁草酮·乙氧氟草醚乳油对棉花田杂草的防效及安全性[J].农药,2014,(05):361-362.
[4]Saha Ajoy,Bhaduri Debarati,Pipariya Ashvin,et al.Behaviour of pendimethalin and oxyfluorfen in peanut field soil:effects on soil biological and biochemical activities[J].Chemistry and Ecology,2015,31(6):550-566.
[5]Ramalingam Sathya Priya,Chinnagounder Chinnusamy,Perumal Manickasundaram,et al.Evaluation of new formulation of oxyfluorfen(23.5%EC)for weed control efficacy and bulb yield in onion[J].American Journal of Plant Sciences,2013,4(4):890-895.
[6]魏玉海,姚志敏,凤晓博,等 .苯氧菌胺及其Z-异构体的NMR数据全归属[J].现代农药,2014,13(1):19-21.
[7]Ferney Betancourt Cardozo,Eliseo Avella Moreno,Carlos Alexander Trujillo.Structural Characterization of Unfractionated Asphalts by1H NMR and13CNMR.Energy Fuels,2016,30(4):2729-2740.
[8]孟令芝,龚淑玲,何永炳.有机波谱分析(3版)[M].武汉:武汉大学出版社,2010:97-98.
Assignment of1H and13C chemical shifts of oxyfluorfen.
Liang Xianghui,Mao Qiuping,Zhong Weiqiang
(School of Chemistry and Chemical Engineering,South China University of Technology,Guangzhou510640,China)
Oxyfluorfen is one kind of fluorinated biphenyl ether derivatives,which can be used as a highly efficient herbicide with broad spectrum.This research focuses on analyzing the NMR spectroscopy data of oxyfluorfen since it has not been reported before.1H and13C chemical shifts of oxyfluorfen were assigned using 1Dand 2DNMR techniques including1H NMR,13C NMR,DEPT135,and19F NMR,and the effect of19F on1H and13C NMR spectrums was discussed.This paper can provide a guidance for NMR characterization of fluorinated biphenyl ether herbicides.
oxyfluorfen;herbicide;NMR;structural assignment
10.3936/j.issn.1001-232x.2017.01.013
2016-09-29
华南理工大学校级教研教改项目(Y9160640);华南理工大学探索性实验教学项目(Y1160050)
梁向晖,女,1972年出生,高级实验师,主要从事有机分析专业,E-mail:liangxh@scut.edu.cn。
