含有芳杂环片段的喹诺酮类化合物的设计、合成与体外抗病毒活性
2017-04-15李宵宁殷金秋柴芸李玉环高荣梅刘明亮
李宵宁,殷金秋,柴芸,李玉环,高荣梅,刘明亮
含有芳杂环片段的喹诺酮类化合物的设计、合成与体外抗病毒活性
李宵宁*,殷金秋*,柴芸,李玉环,高荣梅,刘明亮
目的设计合成一系列含有芳杂环片段的喹诺酮类化合物,并评价其体外抗人类巨细胞病毒(HCMV)和抗单纯疱疹病毒 1 型(HSV-1)活性。
喹诺酮类; 化学技术,合成; 抗病毒药;疱疹病毒 1 型,人; 巨细胞病毒
人类巨细胞病毒(human cytomegalovirus,HCMV)是疱疹病毒家族中的重要成员,可引起人类巨细胞病毒感染[1]。单纯疱疹病毒 1 型(herpes simplex virus 1,HSV-1)则是引起口腔和面部损伤的主要病原体,也是疱疹性脑炎的最常见病因[2]。目前常用的抗 HCMV/HSV-1 药物均为病毒 DNA聚合酶抑制剂,因安全性问题和口服生物利用度低等使其临床应用受到很大限制[3],而近年不断出现的交叉耐药毒株则使其治疗方案复杂化[4],故寻找和研发新型抗病毒药物势在必行[5]。
喹诺酮是目前临床广泛使用的一类广谱、高效、低毒的一线抗感染化疗药物,主要用于治疗由细菌感染引起的系统性疾病[6]。近 10 余年来,科学家对喹诺酮进行了卓有成效的结构改造,发现这类化合物除抗菌之外还具有多种“非经典”生物活性,并筛选得到若干有苗头的候选物[7]。其中,第 1 个喹诺酮抗肿瘤药物沃萨罗辛(voreloxin,拓扑异构酶 II 抑制剂)[8]和第 1 个喹诺酮抗AIDS 药物埃替格韦(elvitegravir,HIV-1 整合酶抑制剂)[9]已分别于 2009 年和 2012 年被美国FDA 批准上市。
多名学者对 6-氨基喹诺酮的抗病毒构效关系(SAR)进行了系统研究[10-12]。其中,代表物WC5[13-14](14c)对人类疱疹病毒家族中的 HCMV具有高度的选择性[15],且与更昔洛韦(GCV)表现出协同作用[16]。本文以 WC5 为先导物,在对其 C7位改造的基础上,对母核的 N1、C6 和 C8 位分别修饰,设计合成一系列含有芳杂环片段的喹诺酮类化合物,并初步评价其抗病毒活性,以期获得对HCMV 和(或)HSV-1 具有抑制活性的化合物,为下一步设计合成活性喹诺酮类化合物奠定基础。
1 材料与方法
1.1 材料
1.1.1 主要仪器 梅特勒 MP-70 熔点仪为瑞士梅特勒-托利多公司产品;Mass Express 2.1.243 和Micromass Autospec Ultima-TOF 型质谱仪分别为美国 Advion 公司和 Waters 公司产品;Mercury-400 MHz 和 Inova-500 MHz 型核磁共振仪为美国 Varian 公司产品。
1.1.2 主要试剂 阳性对照药 GCV 和阿昔洛韦(ACV)分别购于美国 Sigma-Aldrich 公司和湖北科益制药厂;色谱用薄层层析硅胶 H 为青岛海洋化工厂产品;其他试剂和溶剂均为市售化学纯或分析纯,根据需要经无水干燥处理后使用。
1.2 方法
1.2.1 化学合成 以 2-氯苯并噁唑(1a)和 2-溴苯并噻唑(1b)为原料,依次经与 N-Boc-哌嗪亲核取代和脱保护基可分别制得侧链化合物 2-哌嗪基苯并噁唑(2a)和 2-哌嗪基苯并噻唑(2b)[17](图 1)。
按照合成喹诺酮的常规操作[18-19],6 个母核羧酸酯(8~13)很容易由相应的羧酸(3~7)依次经酰氯化、与丙二酸二乙酯缩合、部分水解并脱羧、与原甲酸三乙酯缩合、亲核取代及环合分别制得(图 2)。
基于我们合成喹诺酮类化合物的成功经验[20-22],羧酸酯 8 与上述合成的侧链化合物 2a、2b 以及国内有商品供应的 1-(2-吡啶基)哌嗪(2c)、1-(3-吡啶基)哌嗪(2d)和 1-(4-吡啶基)哌嗪(2e)直接缩合,接着依次经酯水解和硝基还原得目标物 14;喹诺酮母核 9~11 则需先经螯合活化,然后与侧链化合物缩合,最后水解即得 15~17;萘啶酮母核 12 和 13 可直接与侧链化合物缩合后水解即得 18 和 19(图 3)。
1.2.2 CPE 法测定体外抗病毒活性 HCMV 和HSV-1 病毒株分别为 HCMV AD-169 株(ATCC VR538)和 HSV-1 F 株(ATCC VR733),病毒宿主分别为人胚胎成纤维细胞(MRC-5)和非洲绿猴肾(Vero)细胞,阳性对照药分别为 GCV 和 ACV。目标化合物用 DMSO 配成浓度为 20 mg/ml 的母液,检测时用培养液稀释浓度为 200 μg/ml,然后进行 3 倍稀释,共 8 个稀释度。试验时,MRC-5细胞和 Vero 细胞分别种 96 孔培养板,24 h 后分别感染 AD-169(100 TCID50)和 HSV-1(100 TCID50),吸附 2 h,弃病毒液,加入含有不同稀释度样品及阳性对照药的维持液,同时设细胞对照孔和病毒对照孔,待病毒对照组病变程度(CPE)达 4+时观察各组 CPE,用 Reed-Muench[23]法分别计算目标化合物对 HCMV 和 HSV-1 的药物半数有毒浓度(TC50)和药物对病毒半数抑制浓度(IC50)。

图1 侧链化合物 2a、2b 的合成Figure 1 Synthesis of compounds 2a and 2b

图2 喹诺酮母核羧酸酯 8~13 的合成Figure 2 Synthesis of compounds 8-13

图3 目标化合物 14~19 的合成Figure 3 Synthesis of target compounds 14-19
2 结果
2.1 目标化合物的合成
共合成目标化合物 22 个(包括 WC5),其结构(图 4)均经1H-NMR、13C-NMR 和 MS 确证,部分化合物还经 HRMS 进一步确证。
2.2 抗病毒活性
2.2.1 抗 HCMV 活性 由表 1 可见,目标物 17和 18b 对 HCMV 有抑制作用[IC50分别为(17.26 ± 1.85)μg/ml 和(11.14 ± 1.69)μg/ml],但明显弱于先导物 WC5(14c)[IC50:(1.27 ± 0.44)μg/ml]和对照药 GCV[IC50:(0.025 ± 0.005)μg/ml],其余目标物在无毒浓度下均未测出 IC50。
2.2.2 抗 HSV-1 活性 由表 1 可见,9 个目标物(14d、15d、16c、16d、17、18b、18d、18e、19)在无毒浓度下对 HSV-1 显示抑制作用,其中目标物 19 的活性[IC50:(2.18 ± 0.30)μg/ml]仅略弱于先导物 WC5[IC50:(1.68 ± 0.25)μg/ml],两者均弱于对照药 ACV[IC50:(0.63 ± 0.09)μg/ml]。
3 讨论
作为抗 HCMV 候选物,6-氨基喹诺酮 WC5具有全新作用机制(直接阻滞病毒 IE2 蛋白转录活性[15]),被认为在对付耐药病毒感染方面可能具有重要意义[14]。作者借鉴喹诺酮的抗菌 SAR,以WC5 为先导物,对其母核的四个位置(N1、C6、C7、C8)进行结构改造,设计合成了一系列含有芳杂环片段的喹诺酮类化合物。由体外活性数据可见:①活性结果大多不如预期,仅部分化合物表现出体外抗病毒活性,故其 SAR 难以总结;②所有对 HCMV 有抑制作用的化合物(17、18b)也同样显示出抗 HSV-1 活性,但两者之间并无直接相关性;③WC5 不仅对 HCMV 具有抑制作用,而且对 HSV-1 显示相似的活性,但对 Vero 细胞毒性大(TC50:22.22 μg/ml)及选择性差(SI:13.23)。
值得注意的是,N1 位为 (1S,2R)-2-氟环丙基(第四代喹诺酮西他沙星的 N1 位取代基)的喹诺酮 17 对 HCMV 和 HSV-1 均有抑制作用,且对两种细胞的毒性均小于 WC5,而 N1 位为(1S,2R)-2-氟环丙基的萘啶酮 19 对 HSV-1 显示良好活性(尽管其细胞毒性较大)。据此,我们认为,很有必要对 1-[(1S,2R)-2-氟环丙基]喹诺酮/萘啶酮的 C6、C7 和 C8 位进行结构修饰,以期筛选出活性更强和毒性更小的化合物。事实上,本课题组已经开始相关的化学合成工作,结果值得期待。

图4 目标化合物 14~19 的结构Figure 4 Structures of target compounds 14-19
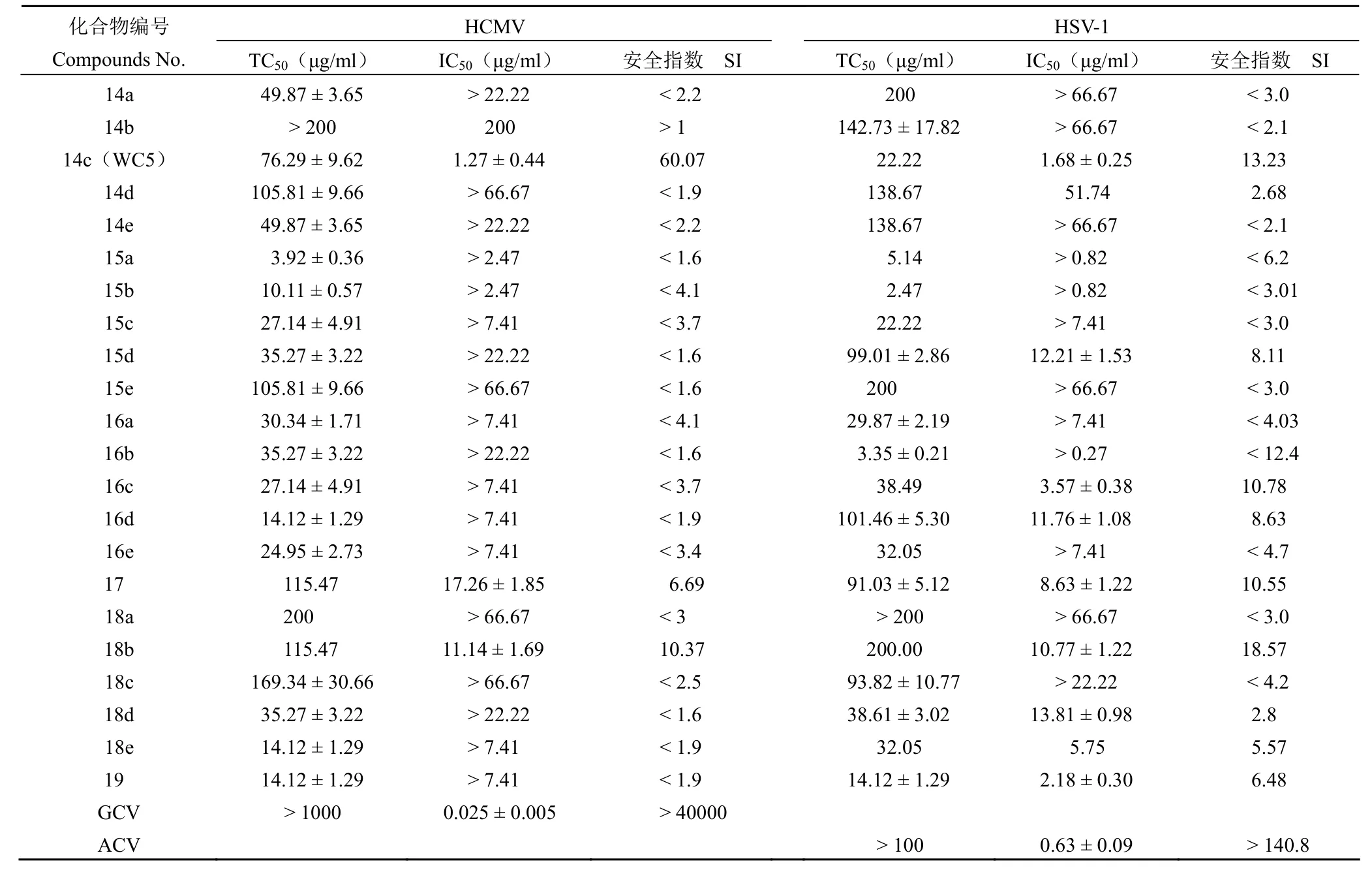
表1 目标化合物 14~19 的抗病毒活性Table 1 Antiviral activity of target compounds 14-19
参考文献
[1]Meshesha MK,Bentwich Z,Solomon SA,et al.In vivo expression of human cytomegalovirus (HCMV) microRNAs during latency.Gene,2016,575(1):101-107.
[2]Rahn E,Petermann P,Thier K,et al.Invasion of herpes simplex virus type 1 into murine epidermis:an ex vivo infection study.J Invest Dermatol,2015,135(12):3009-3016.
[3]Yaghobi R,Geramizadeh B,Zamani S,et al.The molecular and antigenic tissue impact of viral infections on liver transplant patients with neonatal hepatitis.Int J Organ Transplant Med,2011,2(3):108-115.
[4]Schreiber A,Härter G,Schubert A,et al.Antiviral treatment of cytomegalovirus infection and resistant strains.Expert Opin Pharmacother,2009,10(2):191-209.
[5]De Clercq E.A cutting-edge view on the current state of antiviral drug development.Med Res Rev,2013,33(6):1249-1277.
[6]Liu ML,Wang JX,Guo HY.Progress of activity against mycobacteria of quinolones and it's structure-activity relationships.Chin J Pharm,2008,39(12):933-941.(in Chinese)刘明亮,王菊仙,郭慧元.喹诺酮抗分枝杆菌活性及其构效关系研究进展.中国医药工业杂志,2008,39(12):933-941.
[7]Feng LS,Liu ML.Advances of quinolone derivatives in nonclassical bioactivities.J Int Pharm Res,2010,37(2):139-143.(in Chinese)冯连顺,刘明亮.喹诺酮类药物的结构修饰及“非经典”生物活性研究进展.国际药学研究杂志,2010,37(2):139-143.
[8]Lv K,Feng LS,Liu ML,et al.Advances of quinolones as potent antitumor agents and the structure-activity relationships.Chin J Pharm,2010,41(6):456-463.(in Chinese)吕凯,冯连顺,刘明亮,等.喹诺酮抗肿瘤活性及构效关系研究进展.中国医药工业杂志,2010,41(6):456-463.
[9]Feng LS,Wang J,Liu ML,et al.Advances of quinolones potent HIV inhibitors and their structure-activity relationships.Chin J Pharm,2011,42(11):840-850.(in Chinese)冯连顺,王健,刘明亮,等.喹诺酮抗HIV活性及其构效关系的研究进展.中国医药工业杂志,2011,42(11):840-850.
[10]Stevens M,Balzarini J,Tabarrini O,et al.Cell-dependent interference of a series of new 6-aminoquinolone derivatives with viral (HIV/CMV) transactivation.J Antimicrob Chemother,2005,56(5):847-855.
[11]Tabarrini O,Stevens M,Cecchetti V,et al.Structure modifications of 6-aminoquinolones with potent anti-HIV activity.J Med Chem,2004,47(22):5567-5578.
[12]Massari S,Daelemans D,Barreca ML,et al.A 1,8-naphthyridone derivative targets the HIV-1 Tat-mediated transcription and potently inhibits the HIV-1 replication.J Med Chem,2010,53(2):641-648.
[13]Cecchetti V,Parolin C,Moro S,et al.6-aminoquinolones as new potential anti-HIV agents.J Med Chem,2000,43(20):3799-3802.
[14]Massari S,Mercorelli B,Sancineto L,et al.Design,synthesis,and evaluation of WC5 analogues as inhibitors of human cytomegalovirus Immediate-Early 2 protein,a promising target for anti-HCMV treatment.ChemMedChem,2013,8(8):1403-1414.
[15]Mercorelli B,Muratore G,Sinigalia E,et al.A 6-aminoquinolone compound,WC5,with potent and selective anti-human cytomegalovirus activity.Antimicrob Agents Chemother,2009,53(1):312-315.
[16]Loregian A,Mercorelli B,Muratore G,et al.The 6-aminoquinolone WC5 inhibits human cytomegalovirus replication at an early stage by interfering with the transactivating activity of viral immediate-early 2 protein.Antimicrob Agents Chemother,2010,54(5):1930-1940.
[17]Hofer S,Kratschmar DV,Schernthanner B,et al.Synthesis and biological analysis of benzazol-2-yl piperazine sulfonamides as 11β-hydroxysteroid dehydrogenase 1 inhibitors.Bioorg Med Chem Lett,2013,23(19):5397-5400.
[18]Liu ML,Sun LY,Wei YG,et al.Synthesis of tosufloxacin p-tosylate.Chin J Pharm,2003,34(4):157-158.(in Chinese)刘明亮,孙兰英,魏永刚,等.托氟沙星对甲苯磺酸盐的合成.中国医药工业杂志,2003,34(4):157-158.
[19]Qi JJ,Li SY,Liu ML,et al.Synthesis of sparfloxacin.Chin J Pharm,2001,32(9):387-389.(in Chinese)戚建军,李树有,刘明亮,等.司帕沙星的合成工艺研究.中国医药工业杂志,2001,32(9):387-389.
[20]Liu H,Huang J,Wang J,et al.Synthesis,antimycobacterial and antibacterial evaluation of l-[(1R,2S)-2-fluorocyclopropyl]fluoroquinolone derivatives containing an oxime functional moiety.Eur J Med Chem,2014,86:628-638.
[21]Zhang YB,Feng LS,You XF,et al.Synthesis and in vitro antibacterial activity of 7-(3-alkoxyimino-4-methyl-4-methylaminopiperidin-1-yl)-fluoroquinolone derivatives.Arch Pharm (Weinheim),2010,343(3):143-151.
[22]Chai Y,Wan Z,Wang B,et al.Synthesis and in vitro antibacterial activity of 7-(4-alkoxyimino-3-amino-3-methylpiperidin-1-yl) fluoroquinolone derivatives.Eur J Med Chem,2009,44(10):4063-4069.
[23]Fu JH.Practical experiment technology of virology.Jinan:Shandong Science and Technology Press,2001:61.(in Chinese)傅继华.病毒学实用实验技术.济南:山东科学技术出版社,2001:61.
Design,synthesis and in vitro antiviral activity of quinolones containing a heteroaromatic moiety
LI Xiao-ning,YIN Jin-qiu,CHAI Yun,LI Yu-huan,GAO Rong-mei,LIU Ming-liang
ObjectiveTo design and synthesize a series of novel quinolones containing a heteroaromatic moiety,and evaluate their in vitroantiviral (HCMV and HSV-1) activity.MethodsTarget compounds were synthesized through nucleophilic substitution of N-heteroaromaticpiperazines with different quinolone cores.Their structures were characterized by1H-NMR,13C-NMR,MS and HRMS.In vitro antiviral (HCMV and HSV-1) activity of the compounds was evaluated by CPE assay.ResultsTwenty-two compounds including WC5 were synthesized in this study.Some compounds were found to have inhibition against HCMV and/or HSV-1.Compound 19 [IC50:(2.18 ± 0.30) μg/ml]is slightly less active than WC5 [IC50:(1.68 ± 0.25) μg/ml]against HSV-1.ConclusionThe study enriches the structure activity relationship of quinolone against HCMV/HSV-1,which lays the foundation for the future design of novel quinolones with potent activity.
Quinolones; Chemistry techniques,synthetic; Antiviral agents; Herpesvirus 1,human; Cytomegalovirus
LIU Ming-liang,Email:lmllyx@126.com
国家自然科学基金青年科学基金(81502923)
100050 北京,中国医学科学院北京协和医学院医药生物技术研究所有机化学室
刘明亮,Email:lmllyx@126.com
2017-01-16
*同为第一作者
10.3969/j.issn.1673-713X.2017.02.003
方法N-芳杂环基哌嗪与喹诺酮母核化合物通过亲核取代反应制备目标物,其结构经1H-NMR、13C-NMR、MS 和HRMS 确证。CPE 法测定所有目标物对细胞的 TC50及对HCMV 和 HSV-1 的 IC50值。
结果合成了 22 个喹诺酮类化合物(包括先导物 WC5)。部分目标物对 HCMV 和(或)HSV-1 有抑制作用,其中化合物 19 对 HSV-1 的 IC50为(2.18 ± 0.30)μg/ml,略弱于 WC5 的(1.68 ± 0.25)μg/ml。
结论丰富了喹诺酮类化合物抗病毒构效关系,并为下一步设计合成活性喹诺酮类化合物奠定基础。
Author Affiliation:Department of Medicinal Chemistry,Institute of Medicinal Biotechnology,Chinese Academy of Medical Sciences & Peking Union Medical College,Beijing 100050,China
