蒿甲虚热清颗粒的制备及其含量测定方法研究
2017-04-10王远苹余楚钦林华庆
王远苹,余楚钦 ,杨 怡,林华庆
(广东药科大学·广东省药物新剂型重点实验室,广东 广州 510006)
·实验研究·
蒿甲虚热清颗粒的制备及其含量测定方法研究
王远苹,余楚钦 ,杨 怡,林华庆
(广东药科大学·广东省药物新剂型重点实验室,广东 广州 510006)
目的建立同时测定蒿甲虚热清颗粒中丹皮酚、葛根素含量的高效液相色谱法。方法药材提取液作为黏合剂,采用流化床一步制粒。采用YMC-Pack ODS-A C18色谱柱(250mm×4.6mm,I.D.S-5 m,12 nm);柱温为35℃;流动相为甲醇(A)-水(B)-0.2%磷酸溶液(C),梯度洗脱;流速为1 m L/min;检测波长为274 nm;进样体积为 10 L。结果 丹皮酚和葛根素进样量分别在0.418~1.464 g和0.608~2.126 g范围内与峰面积线性关系良好(r=0.999 5);精密度、稳定性、重复性试验结果的 RSD均不超过3%;加样回收率分别为98.64% ~103.84%,98.98% ~102.99%,RSD分别为1.93%,1.74%(n=6)。结论 该制备工艺简单可行,含量测定方法简便、准确、重复性好,可用于蒿甲虚热清颗粒的质量控制。
蒿甲虚热清颗粒;一步制粒;高效液相色谱法;丹皮酚;葛根素;含量测定
蒿甲虚热清颗粒由青蒿、醋鳖甲、葛根、丹皮等8味药材组方,源于《温病条辨·卷三下焦篇》中青蒿鳖甲汤,经剂型改良而得[1]。青蒿鳖甲汤是治疗瘟病后期阴虚发热的代表方剂[2-4],主要有解热、抗炎、镇静、抗病原微生物等作用。蒿甲虚热清颗粒原制备工艺包括提取、浓缩、喷雾干燥、湿法制粒等步骤,以药材提取液作为黏合剂,采用流化床制粒,将传统湿法制粒中混合、制粒、干燥3个步骤一次完成,同时省略原工艺中喷雾干燥的步骤,提高生产效率。原质量标准采用2015年版《中国药典(一部)》中丹皮酚和葛根素的高效液相色谱(HPLC)法分别测定其含量[5],操作烦琐,检测耗时,且目前暂无同时测定丹皮酚与葛根素的方法,本研究中建立了同时测定丹皮酚、葛根素含量的HPLC法,可用于蒿甲虚热清颗粒的质量控制。现报道如下。
1 仪器与试药
1.1 仪器
OTREA1型流化床(瑞士 Niro-Aeromatic有限公司);UltiMate 3000型高效液相色谱仪(戴安中国有限公司);RV8型旋转蒸发仪(IKA,德国艾卡仪器设备有限公司);BS224S型电子分析天平(Sartorius,德国赛多利斯科学仪器有限公司);CP2250型电子分析天平(Sartorius,德国赛多利斯科学仪器有限公司);SK7200LHC超声仪(IKA,德国艾卡仪器设备有限公司);TGL-20B离心机(上海安亭科学仪器厂);MA35快速水分测定仪(广州市博勒泰贸易有限公司)。
1.2 试药
青蒿、醋鳖甲、葛根、牡丹皮等(广州至信中药饮片厂有限公司,批号为150301);乳糖(德国美剂乐沃斯堡牛奶房两合公司,批号为L1411);共聚维酮S630(ISP Technologies INC,批号为ML200083795);葛根素对照品(中国食品药品检定研究院,批号为110751-201514,纯度为95.5%);丹皮酚对照品(中国食品药品检定研究院,批号为110708-200505,纯度为98%)。水(屈臣氏蒸馏水),甲醇(Fisher)、磷酸(天津市科密欧化学试剂有限公司,批号为20131217)均为色谱纯。
2 方法与结果
2.1 蒿甲虚热清颗粒的制备
2.1.1 提取工艺
醋鳖甲粉碎后煎煮2次,煎煮液过滤,滤液合并,备用;按处方工艺量取青蒿、葛根等6味药材煎煮2次,煎煮液过滤,滤液合并,备用;牡丹皮先采用水蒸汽蒸馏提取,分别收集蒸馏液和煎煮液,药渣再次提取,煎煮液过滤,滤液合并,备用。合并上述所有水煎滤液,减压浓缩至密度为 1.1~1.2 g/m L(25℃),高速离心,取上清液,备用。丹皮蒸馏液加入适量氯化钠,4℃冷藏24 h,滤过,得丹皮酚结晶物,晾干,备用。
2.1.2 流化床制粒[6-7]
取丹皮酚结晶物溶于95%乙醇溶液,配制含4.25%丹皮酚和1%共聚维酮的溶液,备用。取乳糖180 g过80目筛,置流化床物料槽内,于50℃流化状态下预热约10min,顶喷喷入备用药材提取液248 g,制粒。将含药颗粒于60℃流化干燥至水分低于4%后,继续顶喷喷入备用丹皮酚溶液20g,40℃流化干燥,控制水分在3%~5%,整粒。优化后的流化床制粒工艺技术参数见表1。

表1 流化床工艺技术参数
2.2 含量测定方法的建立
2.2.1 色谱条件与系统适用性试验
色谱柱:YMC-Pack ODS-A C18柱(250 mm× 4.6 mm,I.D.S-5μm,12 nm);流动相:甲醇(A)-水(B)-0.2%磷酸溶液(C)[8-11],梯度洗脱,洗脱条件见表2;流速:1 m L/min;柱温:35℃;检测波长:274 nm;进样量:10μL。理论板数按丹皮酚峰计应不少于6 000,按葛根素峰计应不少于3 000,分离度均应大于2.5。各成分基线分离良好,色谱图见图1。

表2 梯度洗脱条件
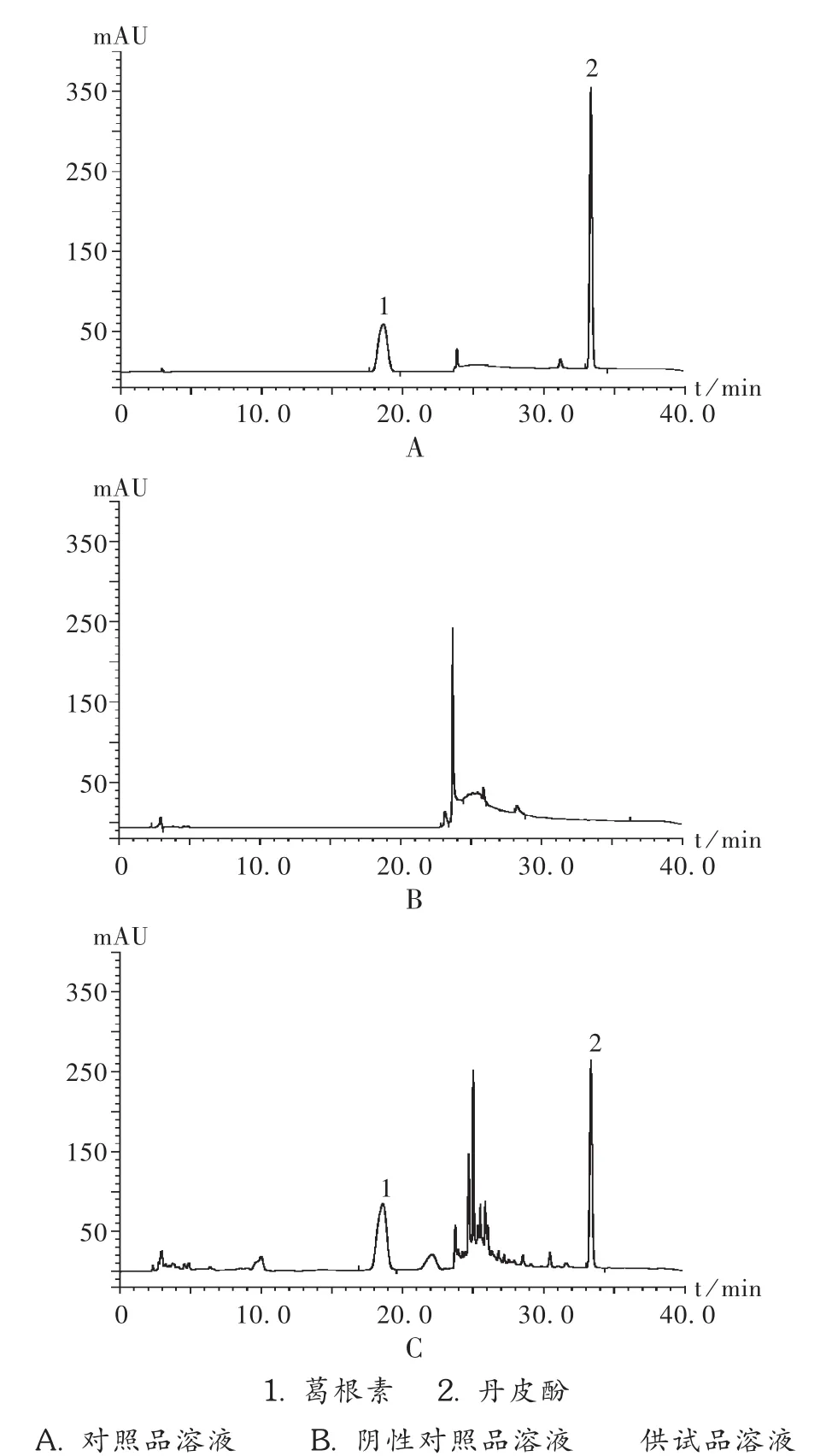
图1 高效液相色谱图
2.2.2 溶液制备
丹皮酚对照品贮备液:取丹皮酚对照品约10 mg,精密称定,置25 mL容量瓶中,加适量甲醇超声5 min溶解并定容,摇匀,即得。
葛根素对照品贮备液:取葛根素对照品约15 mg,精密称定,置25 m L容量瓶中,加适量甲醇超声5 min溶解并定容,摇匀,即得。
混合对照品溶液:分别称取丹皮酚对照品、葛根素对照品适量,加甲醇溶解,制成每1m L约含丹皮酚、葛根素分别为0.06,0.09mg的混合对照品溶液。
供试品溶液:取适量蒿甲虚热清颗粒,研细,取粉末约2 g,精密称定,置20m L容量瓶中,加入适量甲醇超声5min溶解并定容,摇匀,滤过,取续滤液,即得。
阴性对照品溶液:取不含葛根、丹皮酚药材的浸膏提取液依法流化床制粒,取制备好的颗粒,研细,取粉末约2 g,精密称定,置20 mL容量瓶中,加入适量甲醇超声5 min溶解并定容至刻度,摇匀,滤过,取续滤液,即得。
2.2.3 方法学考察
线性关系考察:分别精密量取上述对照品贮备液1.0,1.5,2.0,2.5,3.0,3.5m L,置20 mL容量瓶中,用甲醇稀释并定容至刻度,摇匀,即得。按拟订色谱条件进样测定,记录色谱图,分别以丹皮酚和葛根素的质量浓度(X)为横坐标,以峰面积(Y)为纵坐标,进行线性回归,用最小二乘法计算回归方程。结果见表3。
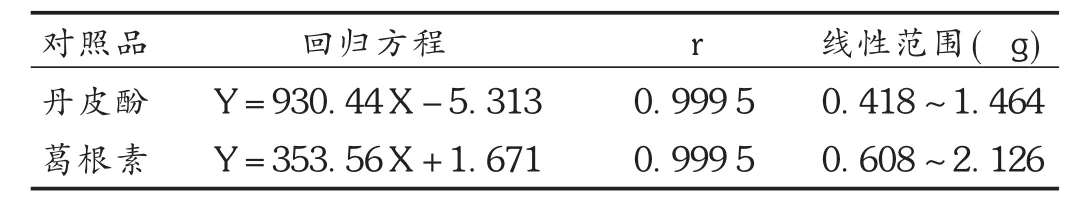
表3 线性关系考察结果
精密度试验:取混合对照品溶液,按拟订色谱条件进样6次,测定。结果丹皮酚和葛根素的 RSD分别为0.48%,0.59%(n=6),表明仪器精密度良好。
稳定性试验:取同一批(批号为160503)样品,依法制备供试品溶液,分别于0,2,4,6,8,10,12,24 h时,按拟订色谱条件进样测定,记录丹皮酚和葛根素的色谱图,记算峰面积。结果丹皮酚和葛根素的 RSD分别为0.94%,0.70%(n=8),表明供试品溶液在24 h内基本稳定。
重复性试验:精密称取同一批(批号为160503)样品适量,依法平行制备供试品溶液6份,按拟订色谱条件分别进样测定,记录色谱图。结果丹皮酚和葛根素的RSD分别为2.75%,2.35%(n=6),表明方法重复性良好。
加样回收试验:分别精密称取同一批(批号为160503)样品适量,依法平行制备6份供试品溶液,分别精密量取5m L置10 mL容量瓶中,分别精密加入丹皮酚对照品贮备液0.7mL和葛根素对照品贮备液1.5mL,用甲醇稀释至刻度,摇匀。按拟订色谱条件进样测定,记录色谱图,计算回收率,结果见表4。
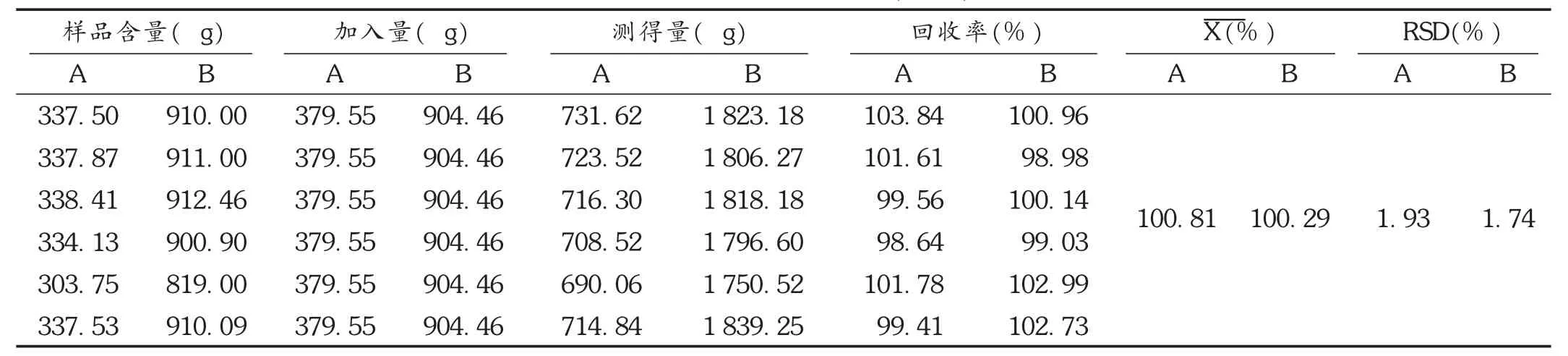
表4 加样回收试验结果(n=6)
2.2.4 样品含量测定
精密称取3批(批号分别为160503,160505,160506)样品,依法制备供试品溶液,按2.2项下色谱条件进样测定,分别计算葛根素和丹皮酚的含量。结果见表5。

表5 样品含量测定结果(mg/g,n=3)
3 讨论
青蒿鳖甲汤始见于清代叶天士《临症指南案·卷五·温热·热陷血分王案》,温病学家吴鞠通在叶天士基础上规范用量[12]。吴鞠通所著《温病条辨卷二·中焦篇·湿热,卷三·下焦篇·风热》中均有记载,两方略有不同,对于发热症候,只要具备“夜热早凉,退热无汗”的症状,无论阴虚症状轻重,皆可用青蒿鳖甲汤加减用量治疗[3,12]。青蒿鳖甲汤广泛用于临床各科发热症候的病症治疗,疗效良好,但传统汤剂体积较大,味苦,携带服用不方便,且易发霉发酵,不易于长期存贮和大量制备。目前,青蒿鳖甲汤的中成药只有片剂1种,蒿甲虚热清颗粒在青蒿鳖甲汤基础上进行剂型创新,采用颗粒剂,方便医患使用。
本研究中对蒿甲虚热清颗粒的原工艺上进行改进,直接用药材提取液作为黏合剂,采用流化床制粒,将传统湿法制粒中混合、制粒、烘干的过程一步完成,缩短操作时间,提高生产效率,且整个操作过程在同一密闭容器中完成,减少物料损失和外源污染[13]。流化床制粒所得颗粒与原产品比较,粒度分布更均匀[6]。本研究中所采用方法减少了药材提取液喷雾干燥的步骤,避免提取物经长时间高温处理,降低产品中有效成分的损失。原工艺将丹皮酚溶于乙醇后直接喷洒在颗粒表面,在存放过程中丹皮酚部分挥发,含量下降。在丹皮酚乙醇溶液中加入共聚维酮,增加溶液的黏性,使丹皮酚更易黏附在颗粒表面,同时共聚维酮在颗粒表面形成一层膜,将丹皮酚包裹其中,更好地保护丹皮酚,使其不易挥发,提高丹皮酚在颗粒中的稳定性,解决了原工艺制得颗粒丹皮酚含量不稳定的问题。
蒿甲虚热清颗粒中丹皮酚和葛根素同时测定方法的建立尚属首次。《中国药典(一部)》中丹皮酚、葛根素检测波长分别为274 nm和360 nm,本研究中考察了丹皮酚、葛根素在274 nm波长处均有较好吸收,故本方法选择274 nm作为检测波长,使这2种成分能同法检测。本研究中选择甲醇-水-0.2%磷酸溶液为流动相,梯度洗脱,既兼顾了丹皮酚、葛根素定量所需的参数要求,又确保了前一次进样的样品能完全洗脱,不会对后一次进样的样品产生影响,同时,使丹皮酚、葛根素分别达到较好的分离度。同法检测可减少样品处理步骤,缩短检测时间,提高检测效率。
综上所述,蒿甲虚热清颗粒与原青蒿鳖甲汤相比,药物稳定性显著提高,方便携带和保存,利于患者使用。本研究在原工艺基础上改良出更简单可行的制备工艺,同时通过新辅料和制剂手段增加丹皮酚在制剂中的稳定性,该工艺方法可用于工业化生产。所建立的HPLC法可同时测定丹皮酚和葛根素的含量,简便、可靠,提高检测效率,可用于蒿甲虚热清颗粒的质量控制。
[1]江 涛,唐春萍,曾昭智,等.蒿甲虚热清颗粒解热作用及机制研究[J].广东药学院学报,2010,26(4):384-387.
[2]朱建光 .浅析青蒿鳖甲汤及其临床应用[J].光明中医,2008,3(9):1391-1392.
[3]常会峰,李仁廷.青蒿鳖甲汤治疗阴虚热郁型癌性发热的疗效观察[J].现代中医药,2013,33(4):27-28.
[4]余锦秀.青蒿鳖甲汤临床应用研究进展[J].中医临床研究,2012,4(15):118-119.
[5]国家药典委员会.中华人民共和国药典(一部)[M].北京:中国医药科技出版社,2015:172,333.
[6]刘旭海,陶 松,何华山,等.流化床制粒设备的制药探讨[J].江西中医药,2011,42(5):76-78.
[7]宫传波.流化床技术代替传统制粒技术项目可行性研究[D].北京:北京化工大学,2015.
[8]高新彪,孙 磊,乔善义,等.牡丹皮HPLC指纹图谱研究[J].中草药,2013,44(7):900-904.
[9]高锦红.牡丹皮中丹皮酚含量的测定[J].湖北农业科学,2013,52(3):669-671.
[10]杨树平,韩立军,朱金卫,等.葛渣总黄酮提取及葛根素含量测定[J].食品科学,2011,32(14):303-306.
[11]李 标,张 锴,曹文丁,等.高效液相色谱法测定山楂叶中金丝桃苷的含量[J].中国药业,2003,12(12):37-38.
[12]王佳雯,翟永松,王满元,等.《温病条辨》青蒿鳖甲汤现代药理及临床应用研究进展[J].实用中医内科杂志,2016,30(7):95-98.
[13]高丹丹,刘哲鹏,陈 岚,等.流化床一步制粒法的工艺优化[J].应用化工,2011,40(1):176-178.
Preparation and Content Determ ination M ethod of Haojia Xureqing G ranules
Wang Yuanping,Yu Chuqin,Yang Yi,Lin Huaqing
(Guangdong Provincial Key Laboratory of Advanced Drug Delivery,Guangdong Pharmaceutical University,Guangzhou,Guangdong,China 510006)
Ob jective To simultaneously determinate the content of paeonol and puerarin in Haojia Xureqing Granules with high performance liquid chromatography method.Improve the efficiency of production and testing.M ethods The fluidized bed was used to make granules with the herbal extract as binder.HPLC was performed on the column of YMC-Pack ODS-A C18(250 mm×4.6 mm, I.D.S-5μm,12 nm)with mobile phase of methanol(A)-water(B)-0.2% phosphoric acid solution(C),at flow rate of 1.0 m L/min, in gradient elution,column temperature was 35℃,the injection volume was 10μL,and determine wavelength was 274 nm.Resu lts Paeonol and pueraria were in good linear relationship(r=0.999 5)in the range of 0.418μg-1.464μg,0.608μg-2.126μg;the RSD of precision,reproducibility tests and the stabilities were no more than 3%.The scopes of sample recovery rate were 98.64%-103.84%(RSD=1.93%,n=6),98.98%-102.99%(RSD=1.74%,n=6).Conclusion The preparation technology is simple and feasible,the content determination method is simple,accurate and reproducible,and can be used for the quality control of the Haojia Xureqing Granules.
Haojia Xureqing Granules;one-step granulating method;HPLC;paeonol;puerarin;content determination
R286.0;R284.1
A
1006-4931(2017)03-0008-04
2016-10-07;
2016-11-08)
10.3969/j.issn.1006-4931.2017.03.003
广东省科技计划项目[2013B021800080]。
王远苹(1991-),女,硕士研究生在读,研究方向为中药剂型,(电子信箱)yuanpingwang@163.com。
余楚钦,高级工程师,大学本科,研究方向为药物新剂型,(电子信箱)pn333@163.com。
