Cu-Fe/凹凸棒石硫化氢吸附剂常温再生性能
2017-04-07张智宏
魏 燕, 张智宏, 李 敏
(常州大学 石油化工学院, 江苏 常州 213164)
Cu-Fe/凹凸棒石硫化氢吸附剂常温再生性能
魏 燕, 张智宏, 李 敏
(常州大学 石油化工学院, 江苏 常州 213164)
采用共沉淀法制备了用于脱除H2S的Cu-Fe/凹凸棒石负载型吸附剂(Cu-Fe/ATP)。在固定床反应器上考察了再生温度、再生气速对吸附H2S后的Cu-Fe/ATP再生性能的影响,采用XRD、XPS、FT-IR和N2吸附-脱附对吸附H2S前后及再生后Cu-Fe/ATP吸附剂进行表征。结果表明,Cu-Fe/ATP吸附剂在常温下吸附H2S生成Fe1-xS 和CuS,再生后生成单质S以及少量的Fe2(SO4)3。单质S和Fe2(SO4)3在吸附剂孔道中聚集,使吸附剂比表面积和孔体积减小。采用无水乙醇浸渍再生吸附剂,可以回收单质硫,有效提高吸附剂再生率。吸附H2S后的Cu-Fe/ATP 吸附剂最佳再生温度和气体流量为50℃、150 mL/min;吸附剂进行3次吸附H2S-再生循环,累积硫容达到29.52%,硫回收总量为253 mg/g。
吸附剂; 常温; 再生; 硫回收
H2S是一种高刺激性剧毒气体,在工业生产过程中,低浓度的H2S也能引起设备、管道腐蚀和催化剂中毒。干法脱硫由于其设备和操作简单、能耗低,被广泛用于低浓度含硫气体的处理。所用的固体吸附剂以金属氧化物为主,如氧化锌、氧化锰、氧化铜和氧化铁。随着环保意识的增强,人们希望其可以再生重复使用,以减少资源浪费和二次污染。吸附剂的再生行为日益引起人们的关注[1-3]。
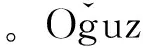
氧化铁资源丰富,价格低廉,人们逐渐关注氧化铁吸附剂的常温再生性能。Wang等[10]将氧化铁吸附剂在室温空气中暴露24 h后,用液氨浸渍吸附剂,有效提高再生性能,并回收单质硫,累计硫容达到50%,但此法需在液氨条件下操作。李澜等[11]在50℃、空气流量0.8 L/min下再生氧化铁吸附剂,再生后生成S单质,但未涉及其回收问题。通常所说的氧化铁是铁的各种氧化物的统称,其种类繁多,活性各异。现在工业应用中的氧化铁吸附剂,操作空速不高(100~3000 h-1),活性组分各不相同,脱硫性能差别较大,使用场合存在局限性。因此,制备在高空速下以氧化铁为主的吸附剂并研究其再生性能,具有积极的理论和工业意义。
笔者采用共沉淀法制备了Cu-Fe/凹凸棒石(Cu-Fe/ATP)可再生吸附剂,在0~100℃空气中再生吸附H2S后的吸附剂,采用无水乙醇萃取回收S单质,考察了再生工艺条件对吸附剂再生性能的影响,研究了吸附剂在硫化再生过程中活性物及孔隙结构的变化,并初步探索了其再生机理。
1 实验部分
1.1 原料与试剂
凹凸棒石(ATP),购于江苏南大紫金科技基团有限公司,镁、钙、硅、铁、铝质量分数分别为9.32%、0.52%、35.86%、5.15%、6.03%;氯化铁(FeCl3·6H2O)、硫酸铜(CuSO4·5H2O)、碳酸钠(Na2CO3), AR,购于上海国药化学试剂有限公司;N2和H2S混合气体,购于常州京华气体有限公司。
1.2 吸附剂的制备
将ATP配成10%的浆液。FeCl3·6H2O和CuSO4·5H2O按质量比10 配制成0.1 mol/L的溶液,与0.1 mol/L Na2CO3溶液并流加入ATP浆液中,控制反应终点pH值为8。搅拌老化30 min,抽滤,用去离子水洗涤至中性,烘干,200℃焙烧,制得Cu-Fe/ATP吸附剂。测定负载前后溶液中残留的Fe3+、Cu2+的含量,计算Cu-Fe/ATP的Fe、Cu负载量,得出Fe负载量为31.45%,Cu负载量为2.77%(均为质量分数)。
1.3 吸附剂的表征
采用日本理学D/max2500PC型X射线仪进行XRD表征,铜靶,管电压40 kV,管电流100 mA,步进0.02°。
采用赛默飞世尔公司ESCALAB 250Xi型X射线光电子能谱仪进行XPS表征,最佳空间分辨率20 μm,能量分辨率小于0.50 eV,灵敏度500 cps。
采用岛津FTIR-8400S光谱仪进行FT-IR表征。将干燥的吸附剂和KBr一起研磨成粉,压片测定,波谱范围7800~350 cm-1,分辨率大于0.85 cm-1。
采用ASAP2010C表面孔径吸附仪测定N2吸附-脱附等温线,比表面分析范围>0.001 m2/g,孔径的分析范围0.35~500 nm。
1.4 吸附剂脱除H2S性能评价
采用固定床反应装置评价吸附剂脱除H2S的性能,如图1所示。将0.1500 g吸附剂装入U型管中,在20℃、气体流量30 mL/min的条件下,通入N2和H2S混合气体,H2S的质量浓度为600 μg/L。采用上海天美科学仪器有限公司GC7890FP型气相色谱仪检测出口H2S浓度,火焰光度检测器(FPD),气化温度323 K,色谱柱温度323 K,检测器温度393 K,检测精度4×10-10。按式(1)计算吸附剂穿透硫容。
(1)

1.5 吸附剂空气再生率的测定
吸附剂经过空气再生后,用25 mL热无水乙醇浸渍24 h,用荧光定硫仪测定乙醇中硫含量;将浸渍后的吸附剂烘干,按1.4进行脱硫性能评价,按式(2)计算其再生率R。
(2)
式(2)中,Si为第i次再生后吸附剂的硫容,%;S0为吸附剂的初始硫容,%。
2 结果与讨论
2.1 Cu-Fe/ATP吸附剂的表征结果
2.1.1 XRD
图2为新鲜、吸附H2S和再生Cu-Fe/ATP吸附剂的XRD谱。由图2可以看出,凹凸棒土负载活性组分后,其衍射峰的位置没有改变,只是强度变弱,说明负载Cu、Fe后ATP结构没有发生变化。

图2 新鲜、吸附H2S和再生Cu-Fe/ATP吸附剂的XRD谱Fig.2 XRD patterns of fresh, H2S adsorbed and regenerated Cu-Fe/ATP
新鲜Cu-Fe/ATP吸附剂没有检测到活性组分的衍射峰,这可能是由于活性组分在ATP表面呈高度分散状态。Cu-Fe/ATP吸附剂吸附H2S后,在15.42°、16.81°、20.21°、25.88°、31.14°、61.98°出现了Fe1-xS的特征衍射峰[12],说明吸附剂中的活性组分与H2S反应后生成了多硫化物。再生Cu-Fe/ATP 吸附剂的Fe1-xS的衍射峰明显减弱,在23.08°出现了单质S 的衍射峰[13],说明吸附剂经过空气再生后将铁硫化物还原为铁氧化物,并生成了单质S。
吸附剂再生后,用乙醇浸渍再生吸附剂,分离得到的溶液除去乙醇后得到的固体物的XRD谱示于图3。其衍射峰与PDF#08-0247卡片中硫单质的标准谱图吻合,表明吸附剂用空气再生后生成了单质S。通过无水乙醇浸渍可回收单质S。
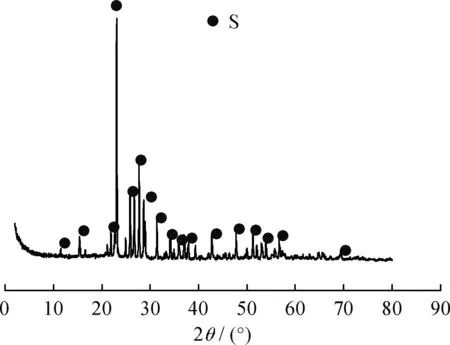
图3 再生Cu-Fe/ATP吸附剂乙醇浸渍所得固体物的XRD谱Fig.3 XRD pattern of the solid from ethanol solution after leaching regenerated Cu-Fe/ATP
2.1.2 XPS
将新鲜、吸附H2S以及再生Cu-Fe/ATP吸附剂进行XPS分析,以确定上述过程中Fe和Cu存在的状态,图4、5分别为它们的Cu 2p和Fe 2pXPS分峰拟合图。
由图4可以看出,新鲜Cu-Fe/ATP吸附剂在942.2 eV处可以观察到强震激伴峰,在电子结合能在935.1 eV出现Cu 2p3/2峰,说明吸附剂中的Cu元素以Cu2+的形式存在,对应Cu(OH)2;吸附H2S后Cu-Fe/ATP中的Cu 2p3/2XPS经过分峰拟合的电子结合能分别为932.3 eV和934.6 eV,对应CuS/Cu(OH)2;而与吸附H2S的Cu-Fe/ATP相比,再生后Cu-Fe/ATP吸附剂的Cu 2p3/2峰变化不大,但是CuS/Cu(OH)2由0.89/0.11变为0.87/0.13,说明吸附剂再生后,部分CuS转变为Cu(OH)2。
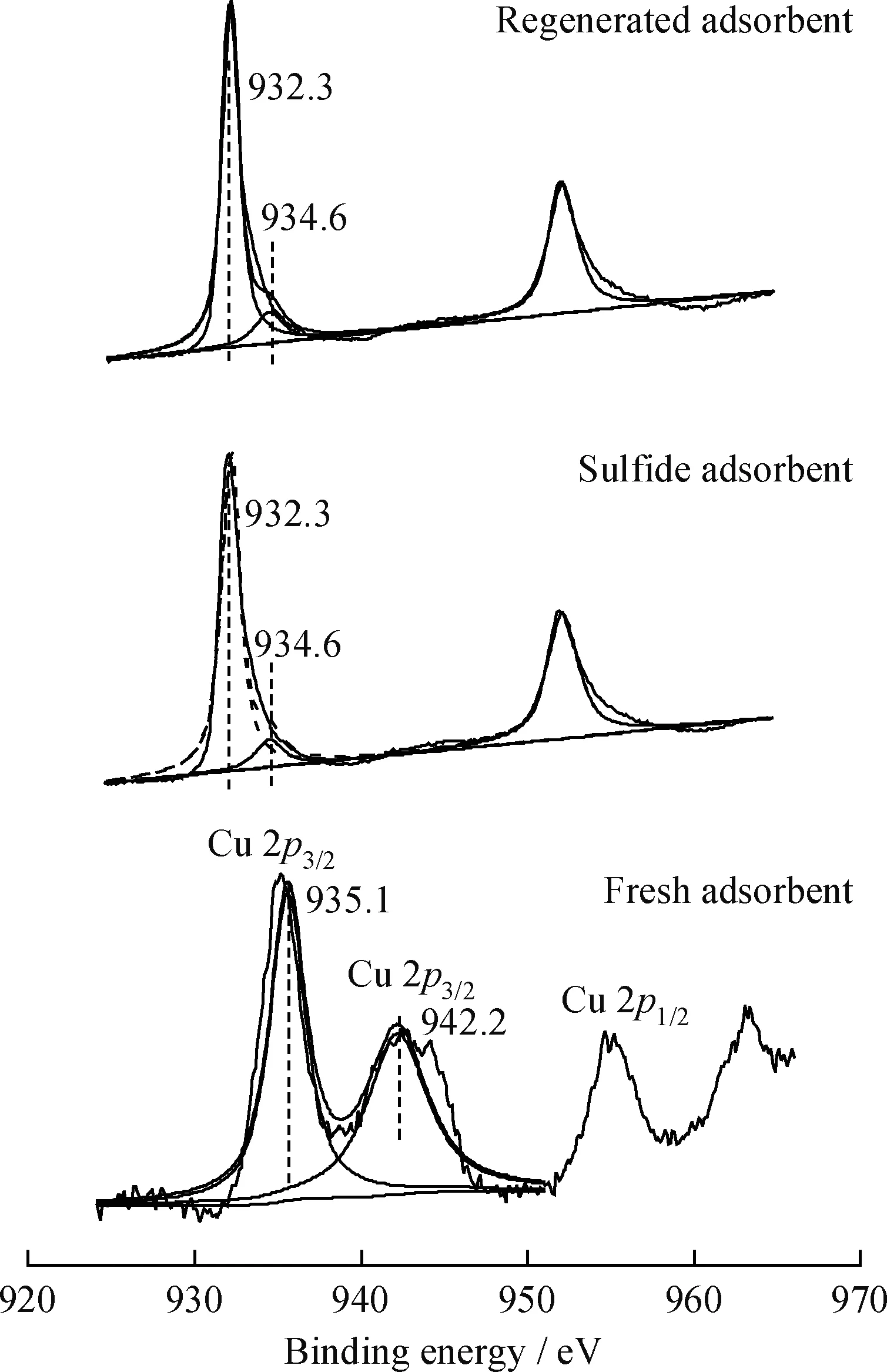
图4 新鲜、吸附H2S和再生Cu-Fe/ATP 吸附剂的Cu 2p XPS分峰拟合图Fig.4 Cu 2p XPS fitted curves of fresh,H2S adsorbed and regenerated Cu-Fe/ATP
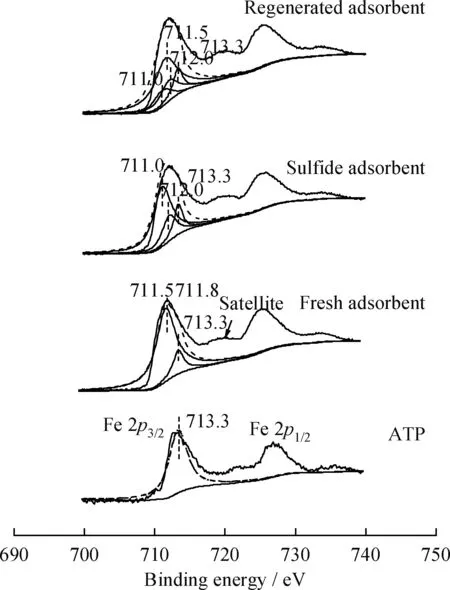
图5 新鲜、吸附H2S和再生Cu-Fe/ATP吸附剂的Fe 2p XPS分峰拟合图Fig.5 Fe 2p XPS fitted curves of fresh,H2S adsorbed and regenerated Cu-Fe/ATP
由图5可见,载体ATP的Fe 2p3/2的结合能为713.3 eV,归属于ATP中八面体络合结构中Fe3+-O。Fe2O3的Fe 2p3/2和Fe2p1/2的结合能为709.2 eV和722.6 eV[14],存在13.4 eV的能量偏差,新鲜Cu-Fe/ATP 吸附剂中Fe 2p3/2和Fe 2p1/2的峰位向高结合能偏离2.6 eV,结合能分别为711.8 eV和725.2 eV,并出现明显的卫星峰,可能是因为加入Cu2+后Fe-Cu之间形成了弱的相互作用,提高了Fe2O3的分散性,使得表面金属和载体的接触面变大,载体对金属的拉电子作用增强。经过分峰拟合,新鲜吸附剂在711.5 eV的位置对应Fe3+-O的电子结合能[15],吸附H2S后吸附剂中的Fe 2p3/2峰的电子结合能分别为711.0 eV和712.0 eV,分别对应Fe3+-S和Fe2(SO4)3的结合能[12]。说明在吸附H2S过程中发生了Fe3+-O+H2S→Fe3+-S+Fe2(SO4)3。计算各峰的面积可知,新鲜吸附剂中活性Fe3+的比例占Fe总含量的85.23%;吸附H2S后,产物Fe3+-S中活性Fe3+质量分数为62.84%,结合XRD谱可以说明Cu-Fe/ATP吸附剂与H2S反应的主要硫化产物为Fe1-xS。再生后吸附剂的Fe2O3中Fe3+质量分数为57.22%,占新鲜吸附剂中活性Fe3+含量的67.14%,说明用空气可以有效再生Cu-Fe/ATP 吸附剂。
2.1.3 FT-IR
Cu-Fe/ATP吸附剂吸附H2S前后及再生后的FT-IR谱示于图6。
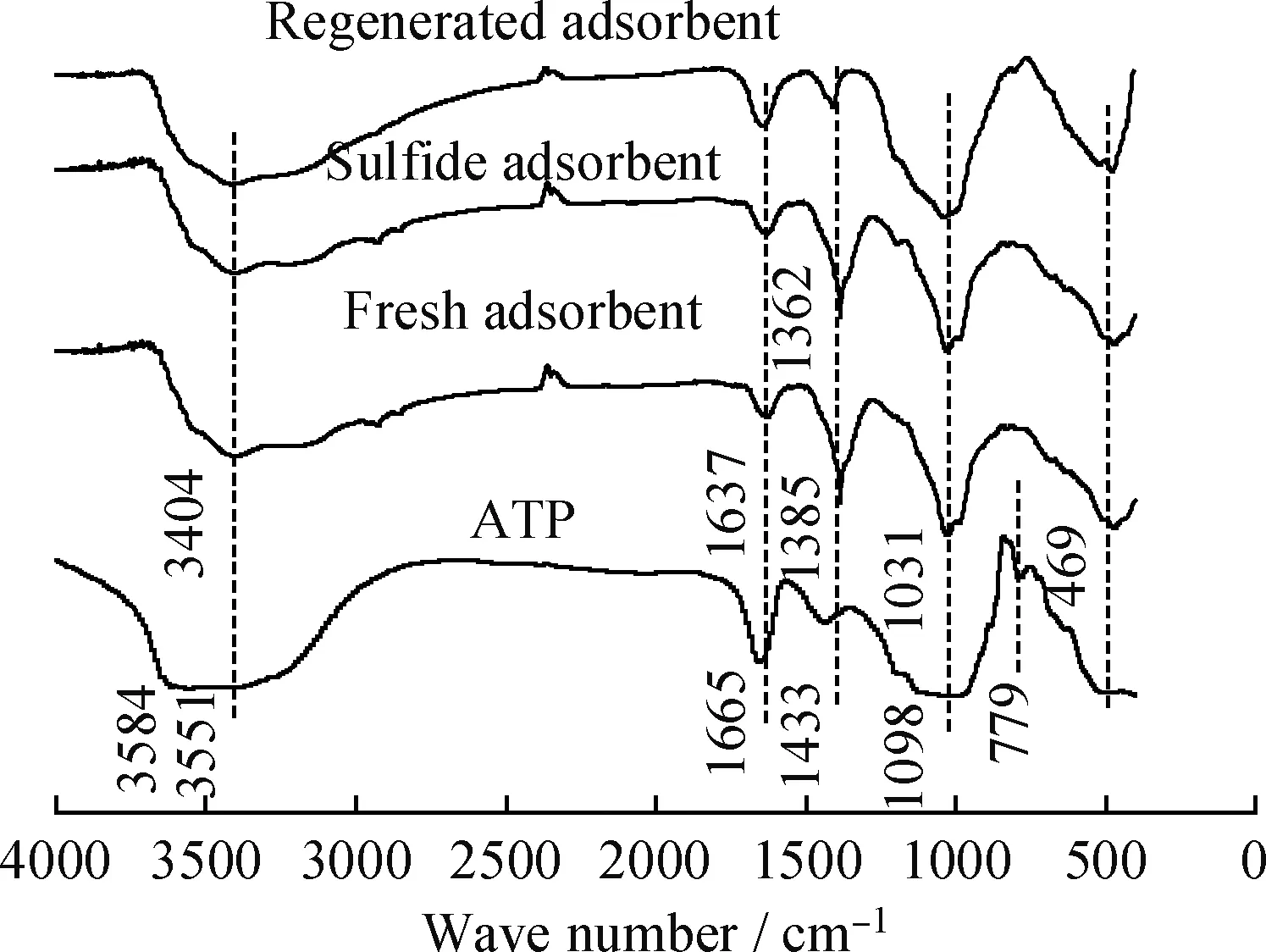
图6 Cu-Fe/ATP吸附剂吸附H2S前后及再生后的FT-IR谱 Fig.6 FT-IR spectra of the fresh, H2S adsorbed and regenerated Cu-Fe/ATP

2.1.4 比表面积和孔结构
图7和图8为新鲜、吸附H2S和再生Cu-Fe/ATP吸附剂的N2吸附-脱附等温线和孔径分布,根据BET法计算得出结果列于表1。从图7看出,三者的N2吸附-脱附等温线均为典型的IV型吸附等温线,从滞后环的形状来看,吸附剂的孔分布比较均匀。由图8可以看出,吸附剂的孔径分布在1~4 nm 之间。从表1可见,吸附H2S的吸附剂的比表面积、孔半径和孔体积均较新鲜剂的减小。主要是因为Fe—O键长0.2050 nm,Fe—S键长为0.2470 nm,S原子占据Fe2O3中的O原子位,吸附剂失去脱硫性能[18],反应所处的孔道变窄,孔半径变小。吸附剂再生时,O原子取代S原子,是1个扩孔的过程,因此再生吸附剂的比表面积和孔结构有所改善;但再生产物单质硫在吸附剂孔道中聚集,孔径和比表面积很难恢复到初始的孔结构状态。无水乙醇浸渍后,吸附剂的比表面积、平均孔半径、累积孔体积均有所增加,但是与新鲜吸附剂相比,比表面积仍下降了17.4 %,说明再生过程吸附剂的结构发生了变化,无水乙醇浸渍单质S可以改善其孔结构,恢复其活性中心。
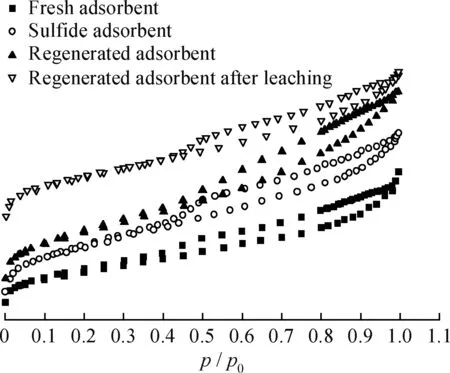
图7 新鲜、吸附H2S和再生Cu-Fe/ATP的N2吸附-脱附等温线Fig.7 N2 adsorption-desorption isotherms of fresh,H2S adsorbed and regenerated
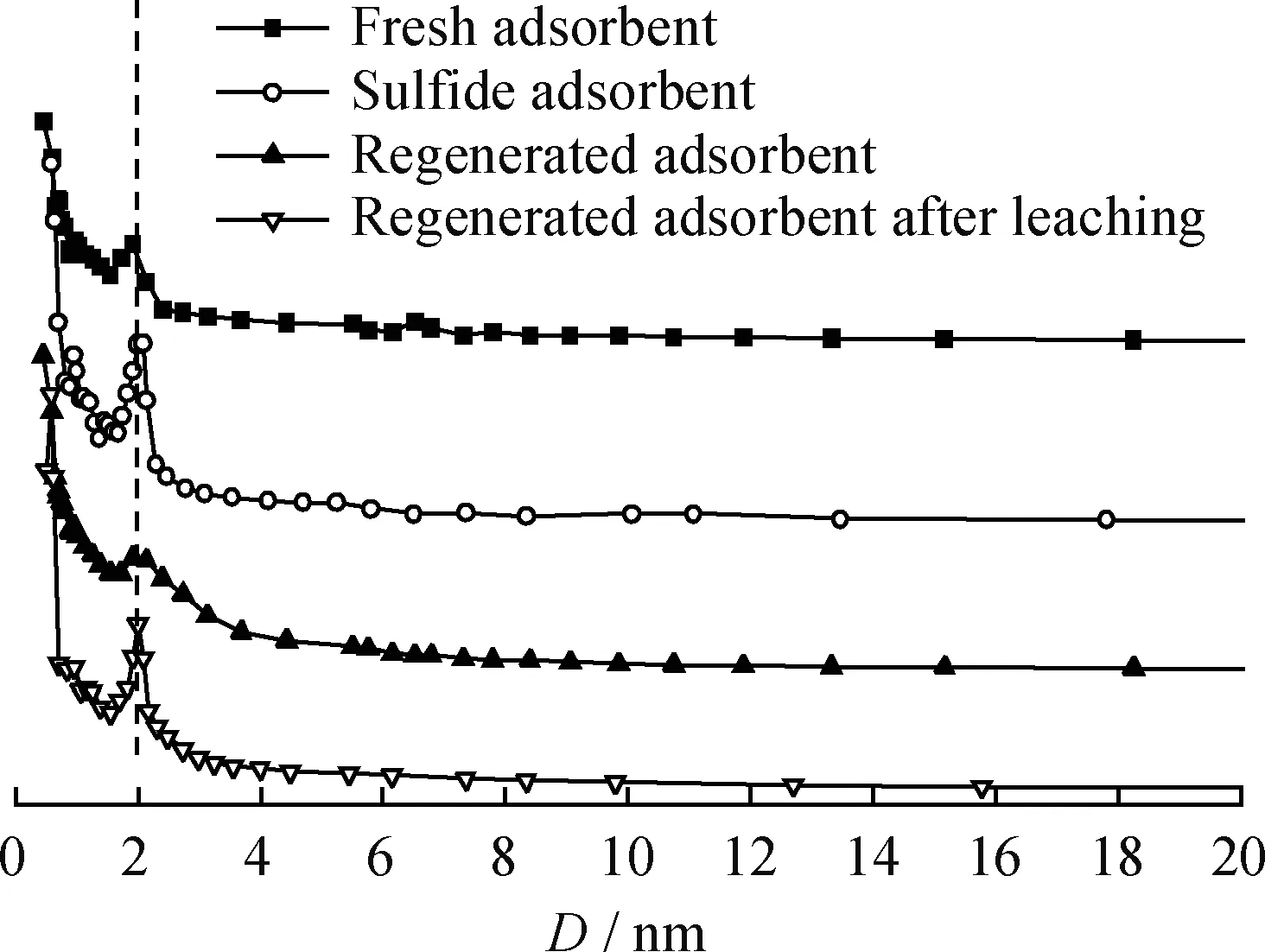
图8 新鲜、吸附H2S和再生Cu-Fe/ATP吸附剂的孔径分布Fig.8 Pore size distributions of fresh,H2S adsorbed and regenerated
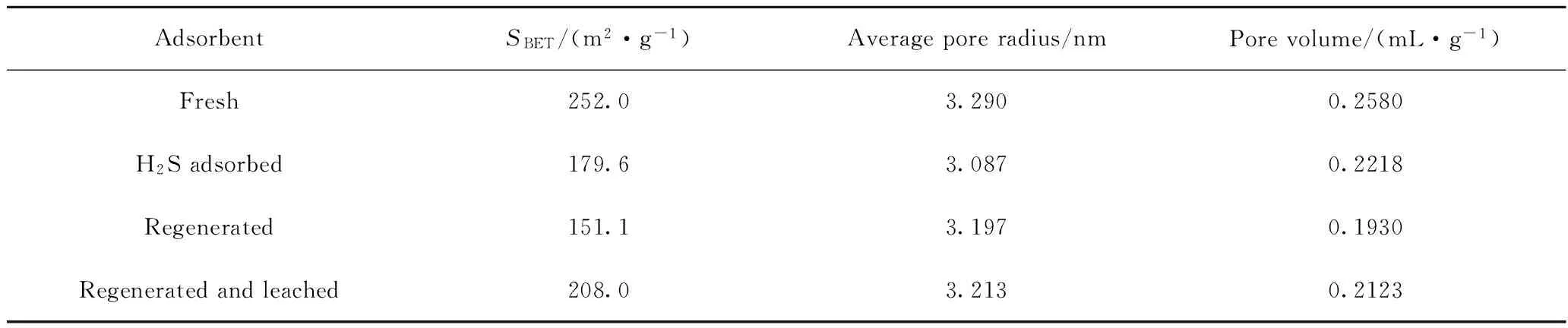
AdsorbentSBET/(m2·g-1)Averageporeradius/nmPorevolume/(mL·g-1)Fresh252.03.2900.2580H2Sadsorbed179.63.0870.2218Regenerated151.13.1970.1930Regeneratedandleached208.03.2130.2123
2.2 再生温度和气体流量对Cu-Fe/ATP吸附剂再生的影响
2.2.1 再生温度的影响
在含氧气氛中,常温氧化铁吸附剂再生反应为强放热反应,温度对吸附剂的再生有很大的影响。将粒度为710~850 μm的吸附H2S后的Cu-Fe/ATP吸附剂在流速150 mL/min的空气中再生,测定不同再生温度下Cu-Fe/ATP吸附剂的二次吸附H2S穿透曲线和再生率,结果示于图9和图10。
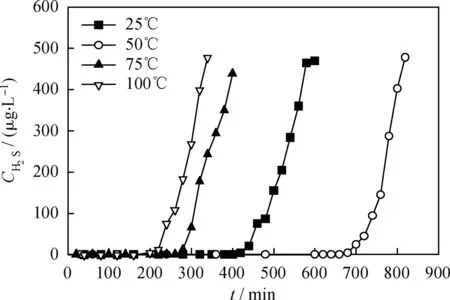
图9 不同温度再生后Cu-Fe/ATP吸附剂的二次吸附H2S穿透曲线Fig.9 Breakthrough curves for adsorbing H2S of Cu-Fe/ATP after regeneration at different temperatures

图10 再生温度对Cu-Fe/ATP吸附剂再生率的影响Fig.10 Effect of temperature on regeneration rate of Cu-Fe/ATP adsorbent
可以看出,当再生温度为50℃时,吸附剂的二次脱硫穿透时间最长,为700 min,再生率为66.12%。当再生温度为25℃,穿透时间缩短,再生率下降;当温度超过50℃时,随着温度的升高,再生率也降低,50℃是最佳的再生温度。再生温度较低时,反应速率小,导致再生不完全,二次脱硫活性下降;升高再生温度虽然可以提高再生速率,但在空气气氛中,Cu-Fe/ATP吸附剂的再生为放热反应,高温不利于反应的进行。
2.2.2 气体流量的影响
在50℃时,不同气体流量下粒度为710~850 μm 的吸附H2S后的Cu-Fe/ATP吸附剂空气中再生后的二次脱硫穿透曲线及再生率示于图11和图12。可以看出,在150 mL/min空气流速下,吸附剂的再生率最高,继续增大气体流量,再生率反而下降。在气-固反应过程中,反应过程要受到内扩散和外扩散两方面的阻力,气体流量较小即空速较低时,受外扩散的影响,再生不很充分,而增大气体流量可以消除外扩散的影响[19],提高再生速率。但再生反应为放热过程,增大气体流量,会提高单位时间内与吸附剂反应的气体的浓度,容易导致吸附剂局部温度太高而引起吸附剂烧结,造成再生率下降。

图11 不同气体流量下再生后Cu-Fe/ATP吸附剂的二次吸附H2S穿透曲线Fig.11 Breakthrough curves for adsorbing H2S of Cu-Fe/ATPafter regeneration at different gas velocities

图12 再生气体流量对Cu-Fe/ATP吸附剂再生率的影响Fig.12 Effect of gas flow on regeneration rate of Cu-Fe/ATP
2.3 Cu-Fe/ATP吸附剂吸附H2S的重复使用性能
吸附H2S后的Cu-Fe/ATP吸附剂在室温下流量为150 mL/min的空气中再生。再生Cu-Fe/ATP吸附剂在25℃、H2S气体流量为30 mL/min的条件下吸附脱除H2S,结果示于图13和14。Cu-Fe/ATP吸附剂再生循环硫容及再生率列于表2。由图13可以看出,吸附剂经过再生,再用乙醇浸渍处理后,进行下一次吸附脱硫实验,其穿透时间增长,再生率明显提高。由图14可以看出,一次再生后吸附剂的穿透时间约为新鲜吸附剂的50%,在随后的2次再生后的吸附剂的穿透时间依次递减,但减小幅度变缓。由表2可以看出,新鲜吸附剂的硫容为15.14%,经过多次再生后,吸附剂的硫容和再生率的变化与穿透时间的变化趋势一致,吸附剂的累积穿透硫容为29.52%。可见,经过空气再生的Cu-Fe/ATP 吸附剂可以再利用,降低生产成本。
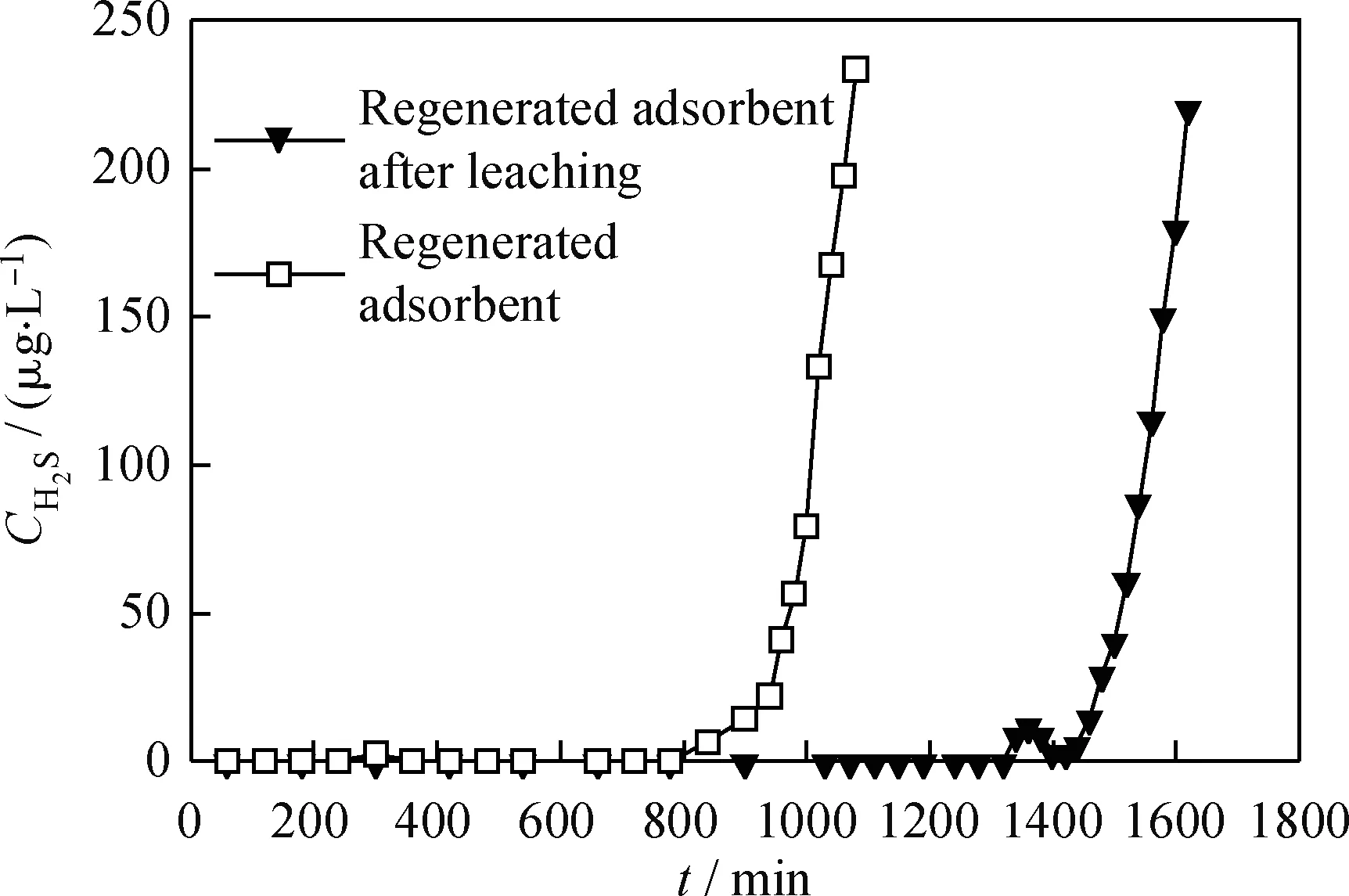
图13 再生后Cu-Fe/ATP吸附剂的吸附H2S穿透曲线Fig.13 Breakthrough curves for adsorbing H2S of regenerated Cu-Fe/ATP
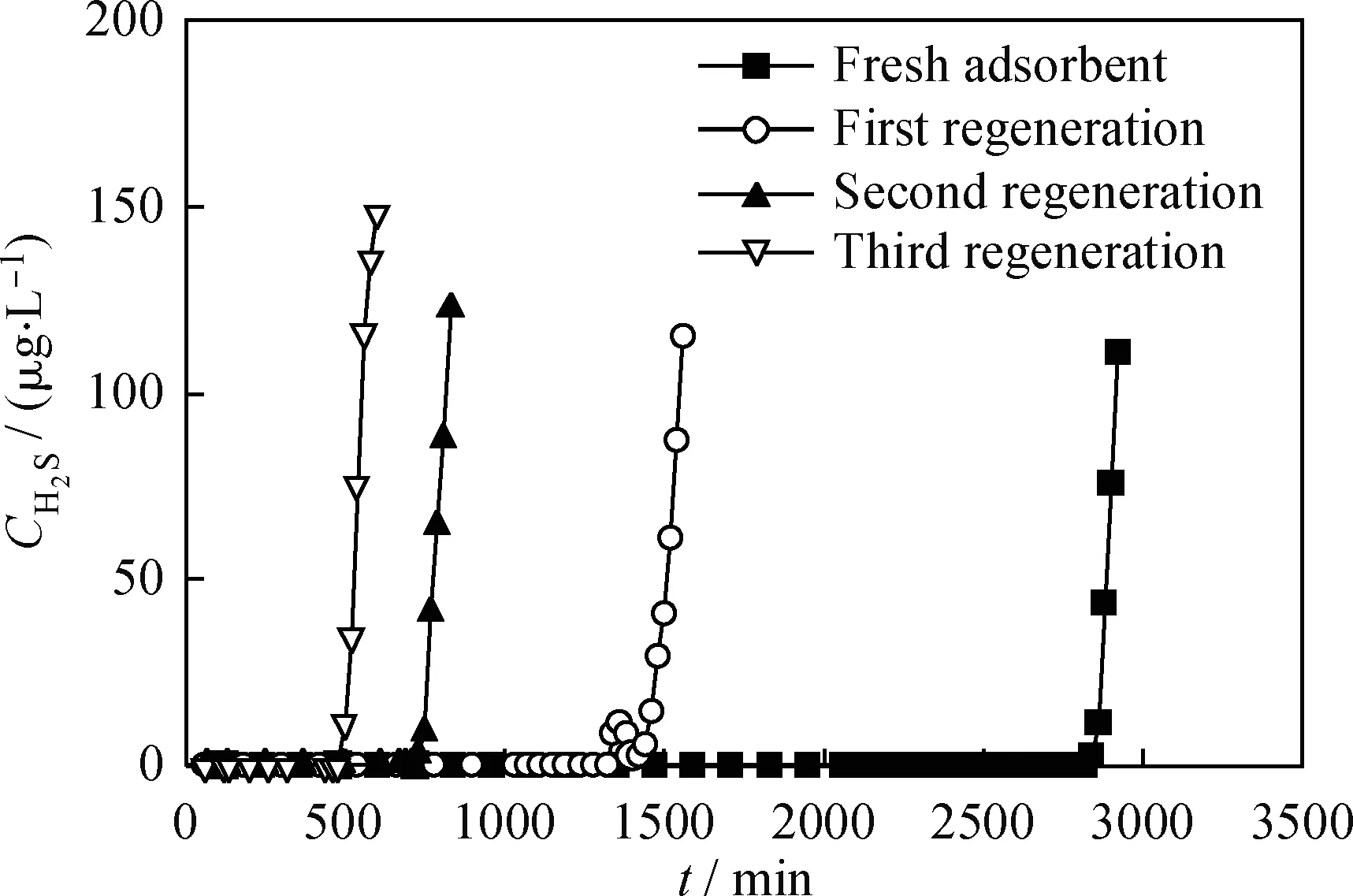
图14 Cu-Fe/ATP吸附剂的吸附-再生循环使用的H2S穿透曲线Fig.14 Breakthrough curves for adsorbing H2S of Cu-Fe/ATP in adsorption-regeneration cycles

AdsorbentS/%R/%mS/mgFresh15.14—0Firstregenerated7.5649.9343.06Secondregenerated4.0726.8831.40Thirdregenerated2.7518.1614.09
3 结 论
(1)采用共沉淀法制备的Cu-Fe/ATP吸附剂的活性组分为Fe2O3和Cu(OH)2,吸附H2S后形成了Fe1-xS和CuS,在常温空气中再生后生成了单质S和少量的Fe2(SO4)3。
(2)再生后生成的单质硫在吸附剂孔道中聚集,使比表面积和孔体积减小,导致再生率较低;采用热无水乙醇浸渍再生后吸附剂,可以有效改善再生吸附剂的孔结构,并回收单质S,实现资源的有效利用。
(3)Cu-Fe/ATP吸附剂在室温下固定床反应器中吸附H2S,然后在空气气氛中再生,3次再生累计穿透硫容为29.52%,再生温度和再生气体流量对Cu-Fe/ATP吸附剂的再生性能影响较大,在50℃、150 mL/min气体流量下再生,吸附剂的再生率最高达到66.12%。
[1] LING L X, HAN P D, WANG B J, et al. DFT study on the regeneration mechanism of ZnO surface during the desulfurization of H2S[J].Fuel Processing Technology, 2013, 109(9): 49-56.
[2] HUANG Z B, LIU B S, WANG F, et al. Performance of Zn-Fe-Mn/MCM-48 sorbents for high temperature H2S removal and analysis of regeneration process[J].Applied Surface Science, 2015, 353(1): 1-10.
[3] WAMG B J, SONG J J, NIU X Q. The regeneration mechanisms of sulfurizedα-Fe2O3surfaces under O2atmosphere: A density functional theory study[J].Fuel Processing Technology, 2014, 128(1): 238-250.
[4] VINCENT G, DAVID C, ARNAUD B, et al. Innovative low temperature regenerable zinc based mixed oxide sorbents for synthesis gas desulfurization[J].Fuel, 2015, 140(1): 453-461.
[5] WANG J, LIANG B, PARNAS R. Manganese-based regenerable sorbents for high temperature H2S removal[J].Fuel, 2013, 107(9): 539-546.
[7] WHITE J D,GROVE-JR F R, Harrison D P. Elemental sulfur production during the regeneration of iron oxide high-temperature desulfurization sorbent[J].Catalysis Today, 1998, 40(1): 47-57.
[8] XIE W, CHANG L P, WANG D H, et al.Removal of sulfur at high temperatures using iron-based sorbents supported on fine coal ash[J].Fuel, 2010, 89(4): 868-873.
[9] LIU B S, WEI X N, ZHAN Y P, et al. Preparation and desulfurization performance of LaMeOx/SBA-15 for hot coal gas[J].Applied Catalysis B: Environmental, 2011, 102(1): 27-36.
[10] WANG G H, FANG D M, CHUANG K T. A sulfur removal and disposal process through H2S adsorption and regeneration: Ammonia leaching regeneration[J].Process Safety and Environmental Protection, 2008, 86(4): 296-302.
[11] 李澜, 赵秋萍, 陈俊伊, 等. 负载氧化铁凹凸棒石脱硫剂的制备及再生工艺[J].石油学报(石油加工), 2013, 29(3): 487-493. (LI Lan, ZHAO Qiuping, CHEN Junyi, et al. Preparation of iron oxide supported attpulgite desulfurizer and its regeneration process[J].Acta Petrolei Sinica(Petroleum Processing Section), 2013, 29(3): 487-493.)
[12] LI Y, VANSANTEN R A, WEBER T. High-temperature FeS-FeS2solid-state transitions: Reactions of solid mackinawite with gaseous H2S[J]. Journal of Solid State Chemistry, 2008, 181: 3151-3162.
[13] WANG Z Y, CAI X L, ZHANG Z B. Separation and enrichment of elemental sulfur and mercury from hydrometallurgical zinc residue using sodium sulfide[J].Trans Nonferrous Met Soc China, 2015, 25(2): 640-646.
[14] BALOURIA V, KUMAR A, SAMAMTA S, et al.Nano-crystalline Fe2O3thin films for ppm level detection of H2S[J].Sensors and Actuators B: Chemical, 2013, 181(5): 471-478.
[15] GROSVENOR A P, KOBE B A, BIESINGER M C, et al.Investigation of multiplet splitting of Fe 2pXPS spectra and bonding in iron compounds[J].Surface and Interfact Analysia, 2004, 36(12): 1564-1574.
[16] QIZ G, YE H M, XU J, et al.Synthesis and characterizations of attapulgite reinforced branched poly(butylenes succinate) nanocomposites[J].Colloids and Surfaces A: Physicochemical and Engineering Aspects, 2013, 436(35): 26-33.
[17] XU Y Y, YANG S, ZHANG G Y, et al. Uniform hematiteα-Fe2O3nanoparticles: Morphology, size-controlled hydrothermal synthesis and formation mechanism[J].Mater Lett, 2011, 65(12): 1911-1914.
[18] SONG J J, NIU X Q, LING L X.A density functional theory study on the interaction mechanism between H2S and theγ-Fe2O3(0001) surface[J].Fuel Processing Technology, 2013, 115(2): 26-33.
[19] MA Z W, ZHENG X R, CHANG L P, et al.Desulfurization kinetics of ZnO sorbent loaded on semi-coke support for hot coal gas[J].Journal of Natural Gas Chemistry, 2012, 21(5): 556-562.
Regeneration Performance at Room Temperature of Cu-Fe/Attapulgite Adsorbent for H2S
WEI Yan, ZHANG Zhihong, LI Min
(SchoolofPetrochemicalEngineering,ChangzhouUniversity,Changzhou213164,China)
The Cu-Fe/attapulgite (Cu-Fe/ATP) adsorbent for H2S removal was prepared by using coprecipitation method. The effects of regeneration temperature and gas flow rate on regeneration performance of H2S-adsorbed Cu-Fe/ATP adsorbent were investigated in a fixed-bed at room temperature. The fresh, H2S-adsorbed and regenerated Cu-Fe/ATP samples were characterized by XRD, XPS, FT-IR and N2-physical adsorption. The results showed that the H2S was adsorbed on Cu-Fe/ATP first, then transferred to Fe1-xS and CuS at room temperature, and the sulfur species mainly existed in the form of elemental sulfur and a litter ferric sulfate after the air regeneration, due to which the surface area and pore volume of Cu-Fe/ATP reduced. By the leaching of elemental sulfur from regenerated Cu-Fe/ATP adsorbent with ethanol as solvent, the elemental sulfur could be recovered and the regeneration ratio could be improved. The best regeneration conditions for Cu-Fe/ATP adsorbent were temperature of 50℃ and gas flow of 150 mL/min, under which the accumulated sulfur capacity of 29.52% were obtained, and the total sulfur recovery reached 253 mg/g after three times of H2S adsorption-regeneration cycle.
adsorbent; ambient temperature; regeneration; sulfur recovery
2016-04-22
江苏省产学研前瞻项目(BY2014037-10)资助
魏燕,女,硕士研究生,从事环境中污染物的检测和净化研究
张智宏,女,教授,主要从事环境中污染物的检测和净化研究,E-mail:zzhfine@163.com
1001-8719(2017)02-0234-08
X701.3
A
10.3969/j.issn.1001-8719.2017.02.007
