博路定和其他抗乙肝病毒核苷酸类药物治疗HBeAg阳性慢性乙型肝炎疗效和安全性的Meta分析
2017-03-15吴梅花严国鸿王小燕郑小娟陈肖虹肖钦
吴梅花,严国鸿,王小燕,郑小娟,陈肖虹,肖钦
(1.福建中医药大学附属人民医院药剂科,福建 福州 350004;
2.厦门大学附属中山医院药剂科,福建 厦门 361004)
博路定和其他抗乙肝病毒核苷酸类药物治疗HBeAg阳性慢性乙型肝炎疗效和安全性的Meta分析
吴梅花1,严国鸿1,王小燕2,郑小娟1,陈肖虹1,肖钦1
(1.福建中医药大学附属人民医院药剂科,福建 福州 350004;
2.厦门大学附属中山医院药剂科,福建 厦门 361004)
目的:评价博路定和其他抗乙肝病毒核苷酸类药物对核苷初治的乙型肝炎e抗原(HBeAg)阳性慢性乙型肝炎(CHB)患者的疗效和安全性。方法:计算机检索PubMed、Mestre、中国期刊全文数据库(CNKI)、中文科技期刊数据库(VIP)、万方数据库(建库至2015年10月)公开发表的有关博路定和其他抗乙肝病毒核苷酸类药物对核苷初治的HBeAg阳性CHB患者疗效的随机对照试验(RCTs),并追查已获文献的参考文献。由两名研究者独立筛选文献,提取数据,按照改良后Jadad评分标准进行质量评价。采用RevMan5.2软件进行Meta分析。结果:最终纳入11个RCTs,共2326例患者。Meta分析结果显示,治疗48周时,博路定组在血清丙氨酸氨基转氨酶(ALT)复常率[OR=1.42,95%CI(1.17,1.73)],HBeAg转阴率[OR=1.35,95%CI(1.08,1.69)]方面均显著高于ADV组,差异有统计学意义(P<0.05)。博路定和其他抗乙肝病毒核苷酸类药物组在血清乙型肝炎病毒(HBV)-DNA转阴率[OR=1.36,95%CI(0.80,2.32)]和不良反应发生率[OR=1.08,95%CI(0.60,1.93)]方面比较,差异无统计学意义(P>0.05)。结论:核苷初治的HBeAg阳性CHB患者治疗48周时,博路定促使ALT复常和清除HBeAg方面的疗效均优于其他抗乙肝病毒核苷酸类药物,但在降低血清HBV-DNA、安全性方面相似。
博路定;抗乙肝病毒核苷酸类药物;慢性乙型肝炎;Meta分析
慢性乙型肝炎(Chronic Hepatitis B,CHB)是世界上高发病率和高死亡率的疾病之一,是严重危害我国人民健康的慢性传染病之一[1]。乙型肝炎病毒(hepatitis B virus,HBV)是慢性乙型肝炎者发生肝硬化、肝癌的主要因素,抗病毒治疗是CHB治疗的关键。目前,用于抗乙肝病毒的药物主要为核苷(酸)类药物如恩替卡韦,拉米夫定,阿德福韦酯和替比夫定等。
博路定(恩替卡韦)由Bristol-Myers Squibb(美国百时美施贵宝公司)2005年获美国食品药品监督管理局(Food and Drug Administration,FDA)批准上市,2006年引进我国销售,是一种具有很强的抗HBV作用的核苷类似物,具有疗效好、耐药率低、不良反应小、安全性高等优点,近年在乙型肝炎的抗病毒治疗中被广泛使用并作为首选药物之一。但对于大多数消费者而言,博路定价格昂贵[2],而其他抗乙肝病毒核苷酸类药物价格相对较低廉,且患者也表现出了一定的临床疗效。为进一步明确进口药博路定与其他抗乙肝病毒核苷酸类药物在疗效和安全性方面的差异,对博路定与其他抗乙肝病毒核苷酸类药物治疗HBeAg阳性慢性乙型肝炎(CHB)的随机对照试验(RCTs)进行Meta分析,以期为临床提供更为可靠的循证医学证据。
1 资料与方法
1.1 检索策略
采用主题词和关键词结合的方式,通过计算机检索“PubMed”“Metstr”(建库至2015年7月),检索词为“Chronic hepatitis B”“Entecavir”“Clinical trial”“Chinese”“Baraclude”“Chronic hepatitis B”“Randomized controlled trials”。以“慢性乙型肝炎”“临床试验”“恩替卡韦”“国产”“博路定”等关键词在中国期刊全文数据库、万方医学数据库、维普医药信息资源系统,检索年限均从建库至2015年7月,并检索近3年来国内外有关慢性乙型病毒性肝炎治疗的学术会议及论文集,并严格按纳入和排除标准筛选。
1.2 纳入和排除标准
纳入标准:①研究设计:RCTs;②研究人群:核苷初治的HBeAg阳性CHB患者,诊断符合我国2011年《慢性乙型肝炎防治指南》[3]的诊断标准;③干预措施:博路定剂量为0.5 mg/d,疗程至少为48周。
排除标准:①仅有摘要无全文的文献资料以及数据不完整无法利用的文献;②恩卡替韦联合其他药物治疗的文献,未采用进口或合资恩卡替韦做对照的文献以及综述性的文献;③重复发表的文献,雷同文献;④综述、短篇报道、自身对照试验以及不能提供全文的文献;⑤有其他肝炎病毒感染或人类免疫缺陷病毒感染,以及有酒精性、自身免疫性肝炎或肝癌以及肝移植患者的研究文献。
1.3 数据提取
由两名研究者独立按照纳入排除标准筛选文献,提取数据,对存在分歧的地方通过讨论及参考原始文献解决。提取的信息包括:患者性别、年龄、样本数、疗程、研究结果、方法学特征(随机序列的产生、分配隐藏、盲法、退出和失访)。
1.4 结局判定及定义
主要结局指标包括治疗48周时血清HBV-DNA转阴率、丙氨酸氨基转氨酶(ALT)复常率、血清HBeAg转阴率。血清HBV-DNA转阴指血清HBVDNA 检测不到(PCR法)或低于检测下限。ALT复常指血清ALT恢复正常,血清HBeAg转阴指血清HBeAg检测不到。次要结局指标为治疗期间不良反应的发生率。
1.5 质量评价
由两名研究者独立按照改良后的Jadad评分标准[4]对纳入的研究进行质量评价,内容包括随机序列的产生、分配隐藏、盲法、退出和失访。随机序列的产生:①恰当:计算机产生的随机数字或类似方法(2分);②不清楚:随机试验但未描述随机分配的方法(1分);③不恰当:采用交替分配的方法如单双号(0分)。分配隐藏:①恰当:中心或药房控制分配方案、或用序列编号一致的容器、现场计算机控制、密封不透光的信封或其他使临床医生和受试者无法预知分配序列的方法(2分);②不清楚:只表明使用随机数字表或其他随机分配方案(1分);③不恰当:交替分配、病例号、星期日数、开放式随机号码表、系列编码信封以及任何不能防止分组的可预测性的措施(0分);④未使用(0分)。盲法:①恰当:采用了完全一致的安慰剂片或类似方法(2分);②不清楚:试验陈述为盲法,但未描述方法(1分);③不恰当:未采用双盲或盲法不恰当,如片剂和注射剂比较(0分)。撤出与退出:①描述了撤出或退出的数目和理由(1分);②未描述撤出或退出的数目或理由(0分)。Jadad 评分1~3分为低质量研究,4~7分为高质量研究。
1.6 统计学分析
采用Cochrane 协作网提供的RevMan5.2软件进行Meta分析,采用相对危险度(Relativerisk,RR)和95%置信区间(CI)为合并统计量。纳入研究结果间的异质性采用χ2检验。当各研究结果间存在统计学同质性时(P>0.10,I2<50%),采用固定效应模型进行Meta分析;当各研究结果间存在统计学异质性时(P<0.10,I2>50%),则分析异质性的来源,必要时采用亚组分析;若各研究结果间存在统计学异质性而无临床异质性时,采用随机效应模型进行Meta分析。采用假设检验验证多个同类研究的合并统计量是否有统计学意义,当P<0.05时,则为有统计学差异。
2 结果
2.1 一般资料
文献检索结果初检索出文献695篇,去重后获得文献654篇,通过阅读标题和摘要排除明显不符的文献后获得38篇,仔细阅读全文后获得文献11篇,最终纳入Meta分析文献11篇[5-15]。文献筛选流程见图1。
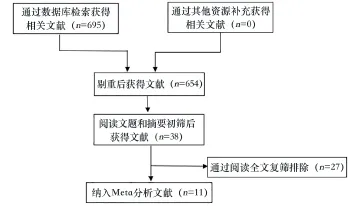
图1 文献筛选流程
纳入文献特征及质量评价11篇文献中,其中1篇为来自国外的多中心研究[14],其余均来自中国。11项研究均提及随机化,但未描述随机化的方法;所有研究均未描述分配隐藏的方案;5项研究[5,10,12,14-15]为开放性研究,其余未描述是否实施盲法;3项研究[6,8,13]描述退出和失访情况。纳入研究的基本特征和质量评价。见表1。
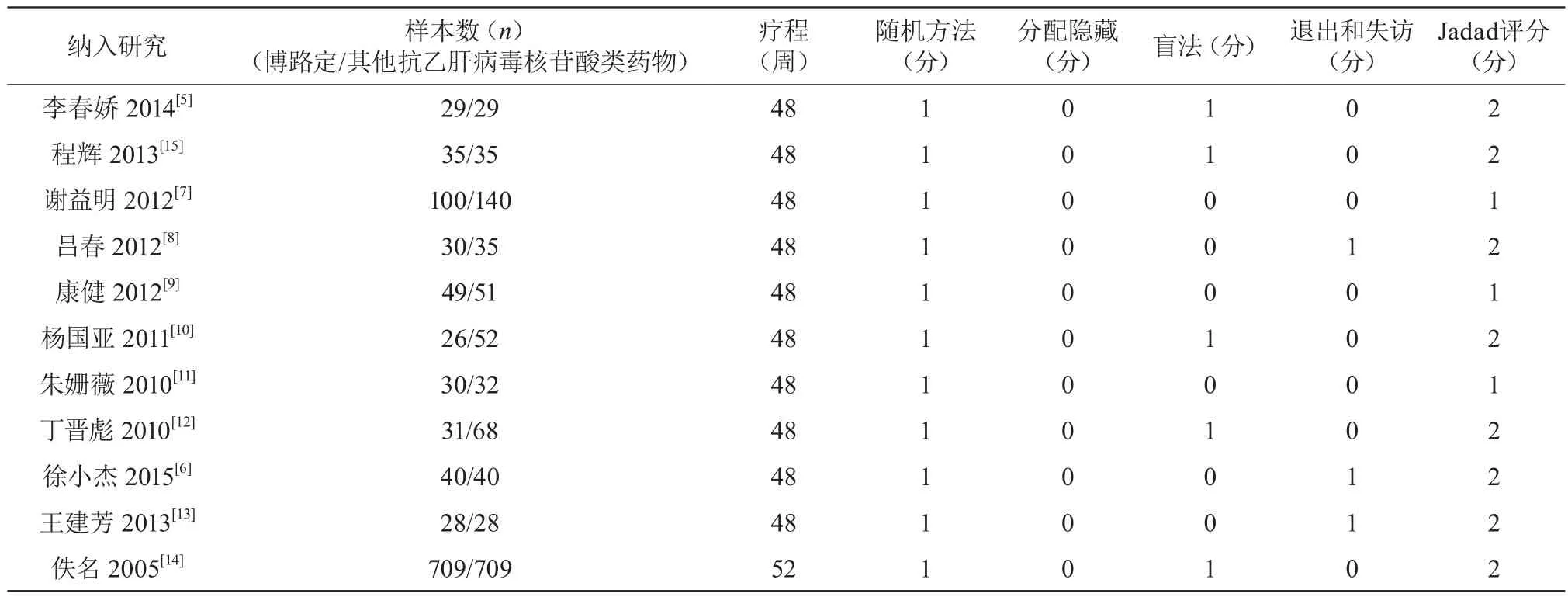
表1 纳入研究的一般资料
2.2 Meta分析结果
2.2.1 血清HBV-DNA转阴率比较11篇文献[5-15]报道了治疗48周时血清HBV-DNA转阴率,异质性检验结果为P<0.000 01,I2=80%,各研究间显示存在统计学异质性,故采用随机效应模型。Meta分析结果为OR=1.36,95% CI(0.80,2.32),P=0.25,无统计学差异,见图2。结果显示,治疗48周时,分别使用博路定和其他抗乙肝病毒核苷酸类药物治疗后,血清HBV-DNA转阴率的差异无统计学意义。
2.2.2 血清ALT复常率比较有10项文献[5-6,8-15]报道了治疗48周后的血清ALT复常率,异质性检验结果为P=0.95,I2=0%,各研究间无统计学异质性,采用固定效应模型。Meta分析结果为OR=1.42,95% CI(1.17,1.73),P=0.000 4,有统计学差异,见图3。结果显示,治疗48周时,博路定组血清ALT复常率显著高于其他抗乙肝病毒核苷酸类药物组。
2.2.3 血清HBeAg转阴率比较有9项文献[5-6,8-13,15]报道了治疗48周后血清HBeAg转阴率,异质性检验结果为P=0.83,I2=0%,各研究间无统计学异质性,采用固定效应模型。Meta分析结果分别为OR=1.42,95% CI(1.01,2.01),P=0.04,有统计学差异,见图4。结果显示,治疗48周时,博路定组血清HBeAg转阴率显著高于抗乙肝病毒核苷酸类药物组。
2.2.4 不良反应发生率比较有5项文献[6,8-10,12]报道了治疗期间不良反应发生率,异质性检验结果为P=0.84,I2=0%。各研究间无统计学异质性,采用固定效应模型。Meta分析结果为OR=1.08,95% CI(0.60,1.93),P=0.81,无统计学差异,见图5。结果显示,治疗期间,博路定组不良反应发生率与抗乙肝病毒核苷酸类药物组无显著差异。
2.2.5 发表偏倚和敏感性分析以OR为指标,绘制博路定和其他抗乙肝病毒核苷酸类药物对ALT复常率的漏斗图,详见图6。结果显示图形不对称,提示存在一定的发表偏倚。安全性研究由于纳入文献数量较少,不能通过漏斗图的方法评价研究的偏倚。

图2 博路定和其他抗乙肝病毒核苷酸类药物对血清HBV-DNA转阴率比较

图3 博路定和其他抗乙肝病毒核苷酸类药物对ALT复常率比较

图4 博路定和其他抗乙肝病毒核苷酸类药物对HBeAg转阴率比较

图5 博路定和其他抗乙肝病毒核苷酸类药物不良反应发生率比较
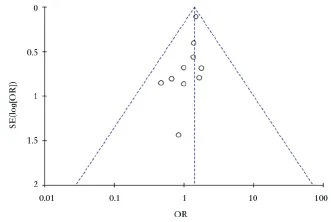
图6 博路定和其他抗乙肝病毒核苷酸类药物对ALT复常率漏斗图
3 讨论
目前,CHB的治疗目标主要是抗HBV病毒,通过持续抑制HBV病毒复制,减少HBV突变,延缓疾病进展为失代偿性肝病、肝硬化或肝癌[16]。博路定是一种新型碳2'-脱氧鸟苷化合物,是鸟嘌呤核苷类似物,临床试验结果表明,博路定在抗HBV感染中,特别是对于基因突变的拉米夫定耐药株疗效显著[17]。
本研究对11篇文献的Meta分析结果显示,核苷初治的HBeAg阳性CHB患者治疗48周时,同疗程博路定组与其他抗乙肝病毒核苷酸类药物的ALT复常率、血清HBeAg阴转率有显著差异,而HBV-DNA阴转率以及不良反应的发生均无显著差异。
乙肝抗病毒治疗是一个长期的过程,然而调查显示[18],仍有近1/4的患者在服药过程中出现自行停药、间断服药(月漏服3次以上)、隔日服药和未发现病毒耐药但换药现象。近六成患者有长期接受抗病毒治疗的医疗费用带来的经济压力,仅有三成患者经济上可承担两年以上的治疗。所以抗病毒治疗必须尽量减少患者经济负担,不能坚持规范的抗病毒治疗,不仅达不到治疗效果,还可能引发病毒变异而导致病情恶化。因此博路定虽然价格较贵且具有强效抑制病毒及e抗原的较高转化率,但已有包括拉米夫定、阿德福韦和恩替卡韦在内的多个口服抗病毒药物也能有效抑制乙肝病毒,医生及患者应根据具体病情及其自身的经济情况,选择能够做到长期坚持规范服用的药物。
本研究的局限性为纳入研究的方法学质量较低,无研究描述随机化的方法及是否实施分配隐藏。漏斗图分析提示存在一定的发表偏移。为加强证据的可靠性,还需要大样本、设计严谨,长期随访的多中心临床随机对照试验,以便进一步验证博路定在治疗HBeAg阳性CHB患者疗效上的优势。
[1] Lok AS.Chronic hepatitis B[J].N Engl J Med,2002, 346 (22):1682-1683.
[2] 刘士敬.恩替卡韦是治疗乙肝的首选药物[J].求医问药,2010,27(11):18-19.
[3] 中华医学会肝病学分会、感染病学分会.慢性乙型肝炎防治指南[J].中华肝脏病杂志,2005,13(12):881-891.
[4] Jadad AR,Moore RA,Carroll D,et al.Assessing the quality of reports of randomized clinical trials:is blinding necessary[J].Control Clin Trials,1996,17(1):1-12.
[5] 李春娇,夏丽珍,张金付.恩替卡韦分散片治疗慢性乙型肝炎的临床疗效观察[J].海峡药学,2014,26(1):110-112.
[6] 徐小杰,任自力,黄磊.恩替卡韦与拉米夫定治疗e抗原阳性慢性乙型病毒性肝炎的临床研究[J].中国临床药理学杂志,2015,31(14):1363-1365.
[7] 谢益明,朱建荣,周文光.进口与国产恩替卡韦治疗慢性乙型肝炎成本-效果分析[J].医学理论与实践,2012,25(19):2438-2439.
[8] 吕春,张梅芹.恩替卡韦分散片治疗HBeAg阳性慢性乙型肝炎的疗效观察[J].医学理论与实践,2012,25(6):663-664.
[9] 康健,马德强,张银华.恩替卡韦治疗HBeAg阳性慢性乙型肝炎患者疗效和安全性评价[J].临床内科杂志,2012,29(8):551-552.
[10] 杨国亚,张玉琴,陈科,等.恩替卡韦分散片初始治疗慢性乙型肝炎52例临床分析[J].中国医药指南,2011,9(36):371-373.
[11] 朱姗薇.恩替卡韦分散片治疗HBeAg阳性慢性乙型肝炎近期效果观察与经济学分析[J].华北国防医药,2010,22(6):529-530.
[12] 丁晋彪,李跃旗,周越塑,等.恩替卡韦分散片治疗慢性乙型肝炎临床研究[J].传染病信息,2010,23(3):168-171.
[13] 王建芳.国产恩替卡韦与进口恩替卡韦的疗效分析[J].实用医技杂志,2013,20(3):334-335.
[14] Entecavir(baraclude) for chronic hepatitis b[J].Med Lett Drugs Ther,2005,47(1210):47-48.
[15] 程辉,张建,袁宇慧.恩替卡韦分散片治疗慢性乙型肝炎临床研究[J].医学信息,2013,27(18):161.
[16] Choe WH,Hong SP,Kim BK,et al.Evolution of hepatitis B virus mutation during entecavir rescue therapy in patients with antiviral resistance to lamivudine and adefovir[J]. Antivir Ther,2009,14(7):985-993.
[17] 姚光粥,任红,王宝恩,等.恩替卡韦治疗拉米夫定失败的慢性乙型肝炎患者多中心随机双盲对照临床研究[J].肝脏,2005,10(1):2-4.
[18] 公培强.我国慢性乙型肝炎治疗现状、近况及对策[EB/ OL].(2010-02-01)[2016-06-20].http://blog.renren.com/ share/222856454/1535394745.
本文编辑:马宏宇
Meta-analysis of Curative Effects and Safeties of Baraclude Versus Other Nucleoside Drugs for Treatment of HBeAg-positive Chronic Hepatitis B
Wu Mei-hua1, Yan Guo-hong1, Wang Xiao-yan2, Zheng Xiao-juan1, Chen Xiao-hong1, Xiao Qin1
(1. Department of Pharmacy, People’s Hospital Affliated to Fujian University of Traditional Chinese Medicine, Fujian Fuzhou 350004, China; 2. Department of Pharmacy, Zhongshan Hospital Affliated to Xiamen University, Fujian Xiamen 361004, China)
Objective:To evaluate the curative effects and safeties of baraclude and other nucleotide drugs for treatment of HBeAg positive chronic hepatitis B (CHB) resistant to nucleosides.Methods:Randomized controlled trials (RCTs) of baraclude and other nucleotide drugs for treatment of HBeAg positive chronic hepatitis B (CHB) resistant to nucleosides published in PubMed, Mestre, CNKI, Chinese Science and Technology Periodical Database (VIP) and ChinaInfo (from the establilshment to October 2015) were searched, of which the references were traced. The literatures were screened by two researchers independently, from which data were extracted and evaluated for quality according to the modifed Jadad scoring criteria. Meta-analysis was performed by using RevMan5.2 software.Results:A total of 11 RCTs were screened, which 2326 patients were included. Meta-analysis showed that the normalization rate of serum alanine aminotransferase (ALT) [(OR = 1.42, 95% CI (1.17,1.73)] and negative conversion rate of HBeAg [(OR = 1.35, 95% CI (1.08,1.69)] in baraclude group 48 weeks after treatment were signifcantly higher than those in ADV group (P < 0.05). However, the negative conversion rate of HBV-DNA [(OR = 1.36, 95% CI (0.80,2.32)] and the adverse reaction rate [(OR = 1.08, 95% CI (0.60,1.93)] in baraclude groupshowed no signifcant difference with those in other nucleoside drug groups (P > 0. 05).Conclusion:The curative effect of baraclude was superior to other nucleoside drugs in promoting the normalization of ALT and clearance of HBeAg, while showed no signifcant difference in decreasing serum HBV DNA level and in safety.
Baraclude; Nucleoside Drugs Against Hepatitis B Virus; Chronic Hepatitis B; Meta-analysis
R512.6+2
A
10.3969/j.issn.2096-3327.2017.01.005
2016 - 06 - 23
吴梅花,女,硕士,药师。研究方向:临床药学。通讯作者E-mail:xiaojiang0809@126.com
