茶皂素的提取及其溶液的表面性质
2016-11-24毛雷霆齐亚会孙振东
毛雷霆,齐亚会,孙振东,曾 强,严 峰
(1.中石化节能环保工程科技有限公司,山东东营 257026;2.天津工业大学环境与化学工程学院,天津 300387)
茶皂素的提取及其溶液的表面性质
毛雷霆1,齐亚会2,孙振东1,曾 强1,严 峰2
(1.中石化节能环保工程科技有限公司,山东东营 257026;2.天津工业大学环境与化学工程学院,天津 300387)
采用醇提法提取油茶饼粕中的茶皂素,考察了溶液pH值和电解质浓度对茶皂素表面张力和表面扩张模量的影响.结果表明:pH值升高,临界胶束浓度增大,表面扩张模量下降;电解质的加入对茶皂素的表面张力和临界胶束浓度影响不太,但会破坏表面活性剂分子在溶液表面上的氢键作用,从而降低表面扩张模量.在中性条件下茶皂素的表面扩张模量较大,可达200 mN/m以上,这可能是茶皂素泡沫稳定的主要原因.
茶皂素;表面活性剂;表面张力;临界胶束浓度;表面扩张模量
油茶饼粕是由油茶籽、山茶籽等油茶种子压榨制油之后的副产物.近年来,随着我国油茶经济的迅速发展,油茶饼粕的产量持续增加,但在农村地区油茶饼粕通常被作为废弃物处理.研究表明,油茶饼粕中富含茶皂素、维生素、蛋白质及多糖等多种有益物质[1],对油茶饼粕进行废物利用不仅可以保护环境,同时还可带来巨大的经济效益和社会效益.目前对油茶饼粕的资源化利用主要集中在对茶皂素的提取研究上.
茶皂素是一种五环三萜类糖苷化合物[2],主要由糖体(亲水性)、苷元和有机酸(疏水性)3部分组成,亲水基与疏水基通过醚键连接.由于分子结构中同时具有亲水基和疏水基,因此茶皂素具有表面活性,是一种性能良好的天然表面活性剂,被广泛应用于日用化工、农药、纺织、采油及采矿等行业[3].
关于茶皂素的提取已经有大量文献报道,但目前的研究主要集中于提取工艺优化[4]、表面张力[5]及泡沫性能测试[6-7]等方面的工作.近年来一些研究表明,茶皂素具有优良的泡沫性能.黄文红等[6]比较α-烯烃磺酸钠、十二烷基硫酸钠、脂肪醇聚氧乙烯醚硫酸钠及茶皂素等表面活性剂的泡沫性能,发现茶皂素的起泡能力稍差,但其泡沫的半衰期最长,具有较好的稳定性.Jian等[7]研究了茶皂素与十二烷基硫酸钠(SDS)及溴代十六烷基三甲胺(CTAB)等相互作用的泡沫性能,结果表明茶皂素单独存在时起泡性稍差,而泡沫稳定性较高.茶皂素的良好泡沫性能为其在泡沫浮选、泡沫驱油及洗发香波等方面的应用奠定了物质基础,但目前关于茶皂素良好泡沫稳定性能的机理尚缺乏系统研究.
本文采用传统醇提法提取油茶饼粕中的茶皂素,采用表面张力仪测试了其表面张力,采用界面扩张流变仪测试了其表面扩张流变性质.扩张流变性质是流体界面的重要性质之一,其与泡沫及乳状液等的稳定性密切相关[8-9].通过对茶皂素表面扩张流变性质的研究,有助于揭示其泡沫性质的稳定机理.
1 实验部分
1.1 试剂与仪器
试剂:无水乙醇、石油醚(60~90℃)、氢氧化钠、香草醛、浓硫酸,均为分析纯,购于天津光复精细化学品有限公司.
仪器:索氏提取器、UV-2700型紫外可见分光光度计,日本岛津公司产品;FTIR-650红外光谱仪,天津港东科技发展股份有限公司产品;Bruker AutoflexTM型质谱仪,德国Bruker公司产品;JK99C全自动表面张力测量仪,上海中晨数字技术设备有限公司产品;TRACKER扩张流变仪,法国IT-CONCEPT公司产品.
1.2 茶皂素的提取
关于茶皂素的提取已经有大量文献报道,本文采用较为简便的乙醇提取法.首先在提取管中加入用滤纸包裹好的油茶饼粕粉末10 g,同时在提取瓶内加入约200 mL乙醇,然后安装好提取装置,并加热提取瓶,使热乙醇进入提取管浸提其中茶皂素.提取2 h后将乙醇溶液蒸发除去溶剂,所得固体粉末即为茶皂素.参照文献[10],采用香草醛-浓硫酸显色法测定茶皂素的提取率为14.3%.
1.3 表面张力的测量
将提取得到的茶皂素配制不同浓度的水溶液,采用JK99C型全自动表面张力仪(Wilhelmy吊片法)测试不同pH条件下不同浓度茶皂素溶液的表面张力,实验温度为(30±0.5)℃,表面张力均为3次平行测量的平均值.
1.4 表面扩张流变的测量
[11]中的方法:对悬挂的气泡进行周期性振荡,然后利用滴外形分析方法测定气-液表面扩张流变性质.实验温度为(30.0±0.1)℃,扩张形变为10%(ΔA/A).
2 结果与讨论
2.1 茶皂素结构表征
目前文献中关于茶皂素结构表征的报道还较为少见,本文采用红外光谱和质谱(MALDI-TOFMS)测试了所提取茶皂素的化学结构和分子质量.基质辅助激光解析电离(matrix assisted laser desorption ionization,MALDI)为软电离技术,由于其几乎不产生碎片离子,因此MALDI-TOFMS被广泛用于生物大分子和高聚物的研究中.
首先采用傅里叶红外光谱仪测试了茶皂素的红外光谱,结果如图1所示.
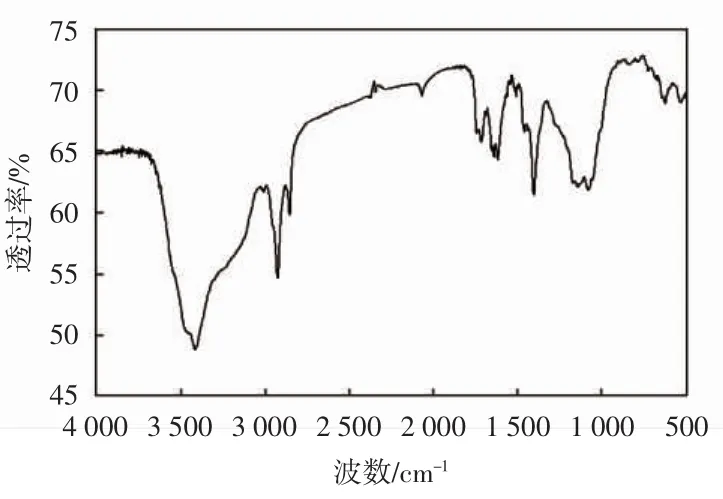
图1 茶皂素的红外谱图Fig.1 FTIR spectrum of tea saponin
由图1可见,3 414 cm-1附近的宽峰源于茶皂素分子中羟基的伸缩振动,2 928 cm-1、2 847 cm-1及1 400 cm-1处的吸收峰归属于甲基和亚甲基基团的伸缩振动,1 716 cm-1处的吸收峰为羰基基团的吸收峰,而1 617 cm-1处的吸收峰则为茶皂素苷元C=C键的伸缩振动,1 142 cm-1和1 070 cm-1处的吸收峰归属于饱和六元环醚的C—O—C的伸缩振动.该红外谱图与文献[7]报道的红外谱图基本一致.
为进一步验证茶皂素结构,采用MALDI-TOFMS测试了茶皂素的分子质量,结果如图2所示.
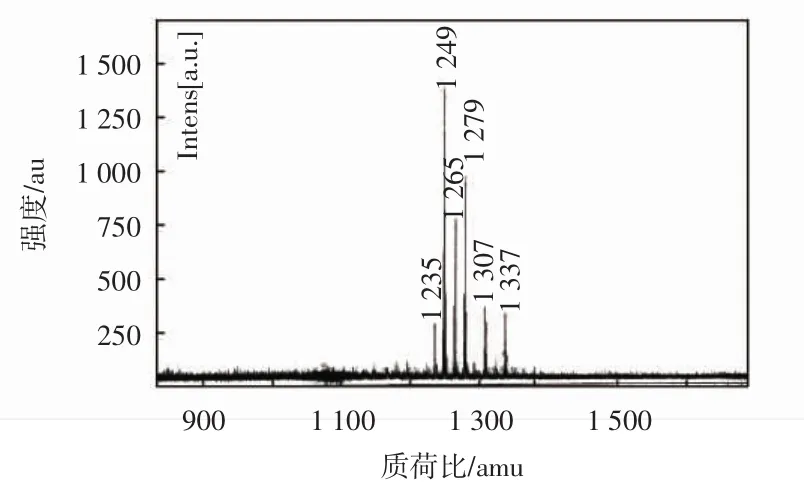
图2 茶皂素的MALDI-TOFMS质谱图Fig.2 MALDI-TOFMS spectrum of tea saponin
图2中丰度较高的离子峰的m/z主要为1 235、1 249、1 265、1 279、1 307及1 337,表明所提取的茶皂素主要为含6种不同配基的茶皂素的混合物,其结构式如图3所示.其中分子离子峰为1 249、1 265和1 279的茶皂素的含量较高,与文献[12]结果吻合.
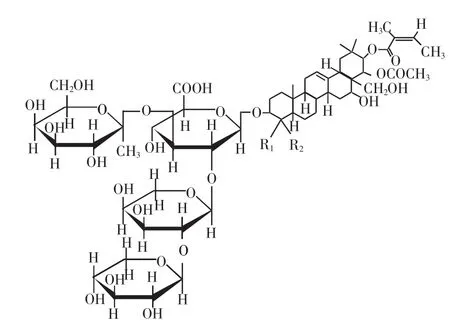
图3 茶皂素的结构式Fig.3 Structure of tea saponin
2.2 茶皂素表面张力
茶皂素的分子结构中含有亲水基团和疏水基团,因此具有表面活性.分子结构中除具有糖基和苷元外,还具有羧基和酯基等基团,其表面活性容易受到溶液pH环境的影响.因此考察溶液pH值对茶皂素表面张力的影响对其应用具有重要的意义.
2.2.1 pH对茶皂素表面张力的影响
图4示出了在不同pH条件下茶皂素溶液表面张力随浓度变化曲线.
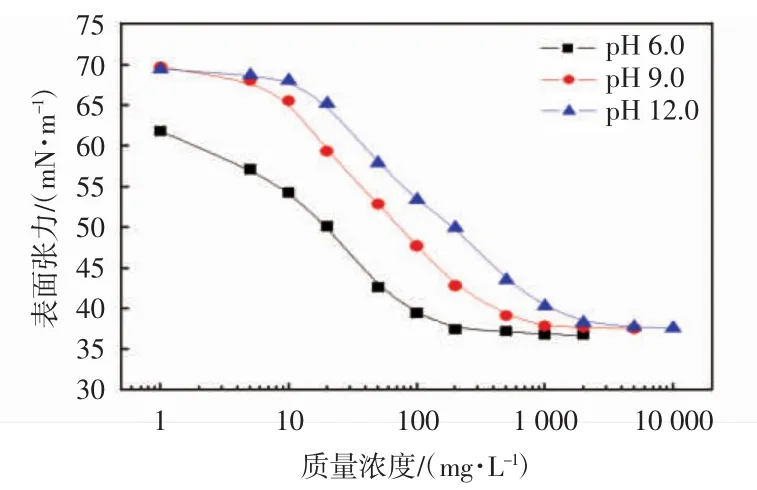
图4 pH值对茶皂素表面张力的影响Fig.4 Influence of pH on surface tension of tea saponin
从图4中可看出,在溶液pH为6.0时,茶皂素的表面活性较高,临界胶束浓度(CMC)为0.11×103mg/ L,临界胶束浓度所对应的表面张力为37.6 mN/m;当溶液pH值上升到9.0时,CMC为0.38×103mg/L,CMC所对应的表面张力为37.8 mN/m;继续升高溶液pH值至12.0时,CMC为1.14×103mg/L,CMC所对应的表面张力为38.4 mN/m.由此可见,随着溶液pH值上升,茶皂素的表面活性减弱,表现在临界胶束浓度和表面张力均升高.这是因为茶皂素的分子结构中含有羧基,加入碱(NaOH)后,NaOH与羧基反应生成的羧酸钠,使茶皂素的水溶性增强,因此茶皂素的表面张力及临界胶束浓度增加.由此可见,茶皂素在接近中性条件下(弱酸性)表面活性较高,在此条件下使用将有助于充分发挥其性能.
2.2.2 电解质对茶皂素表面张力的影响
电解质(NaCl)浓度对茶皂素表面张力的影响如图5所示.
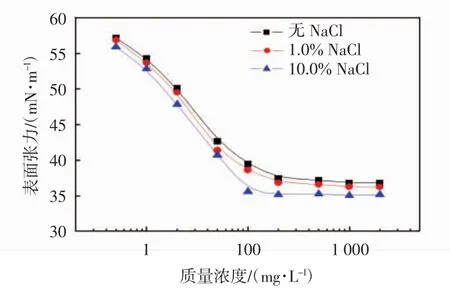
图5 NaCl浓度对茶皂素表面张力的影响Fig.5 Influence of NaCl concentration on surface tension of tea saponin
从图5中可看出,随着NaCl的加入,茶皂素的表面张力和临界胶束浓度均有所下降,且随着NaCl浓度升高,表面张力的下降幅度增大,但CMC变化不大.当NaCl质量分数为10.0%时,茶皂素溶液的表面张力为35.1 mN/m,而CMC为1.10×103mg/L,该CMC与未加NaCl时的CMC接近.由此可见,NaCl的加入对茶皂素表面活性影响不大,这可能是因为茶皂素的亲水基团主要为糖基,属于非离子类型,NaCl对该类型表面活性剂的胶束化行为没有显著影响.
2.3 茶皂素表面扩张流变性质
2.3.1 茶皂素浓度对表面扩张流变性质的影响
大量的研究表明,茶皂素作为天然的表面活性剂,具有十分优异的泡沫性质,尤其是稳泡性能最佳.但文献中对茶皂素的稳泡机理几乎没有报道.泡沫的产生伴随着气液界面的形成,泡沫的破坏过程则主要是液膜排液,由厚变薄,直至破裂的过程.因此泡沫的稳定性主要决定于液膜的强度.泡沫的液膜为气-液界面(表面),其强度可通过表面扩张流变手段来进行表征.
表面扩张流变方法通过扩张和收缩扰动液膜的界面面积,获得表面活性物质的界面动力学特性参数(如扩张模量、扩张相角、扩张弹性、扩张黏性等).其中界面扩张模量反映界面膜的强弱,分析界面扩张模量有助于人们了解分子在界面上的排布、分子间的相互作用以及超分子聚集体等信息[13-14].茶皂素在水溶液中形成的表面膜受到压缩或扩张形变时,局部表面积的变化将导致局部表面张力的变化,从而形成表面张力梯度来对抗所受到的形变.茶皂素的这种对抗形变的能力可以用表面扩张模量来描述.
图6所示为不同工作频率条件下茶皂素浓度对表面扩张模量的影响.
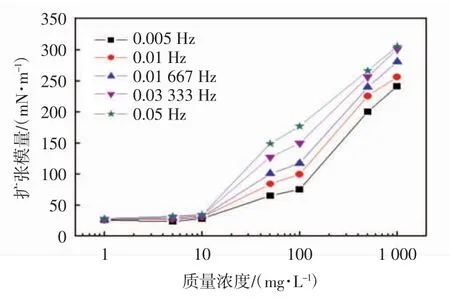
图6 茶皂素浓度对表面扩张模量的影响Fig.6 Influence of tea saponin concentration on dilational modulus
从图6中可看出,在各工作频率下,茶皂素的表面扩张模量在不同浓度区域内相差很大:当茶皂素质量浓度低于10 mg/L时,表面扩张模量随浓度增加变化不大,此时由于浓度低,表面上分子数少,分子间几乎没有相互作用.当质量浓度高于10 mg/L后,表面活性剂在溶液表面逐渐富集,随浓度升高,表面张力迅速下降(图4),表面扩张模量急剧上升(图6).这表明随着表面上表面活性剂分子的增加,分子间的相互作用逐渐增强,形成的表面膜强度增大.
此外,从图6中还可看出,茶皂素溶液的表面扩张模量最高可达300 mN/m,远高于常规表面活性剂的表面扩张模量(通常低于100 mN/m)[9,13].表面扩张模量较高说明茶皂素在气-液界面形成的界面膜强度较高,这种高强度的界面膜有利于克服泡沫排液造成的液膜变薄及强度降低的问题,因此有利于稳定泡沫,即所形成的泡沫的稳定性较高,与文献报道的泡沫稳定性结果吻合[7].
2.3.2 pH值对茶皂素表面扩张流变的影响
从2.3.1节的结果可知,茶皂素的表面活性受到溶液pH值的影响,这是因为当pH值不同时,茶皂素分子结构中羧基的存在形式不同,这种结构的变化必然会影响到表面活性剂的亲水亲油平衡能力,最终影响其分子在界面上的相互作用.pH值对茶皂素表面扩张流变的影响如图7所示.
由图7可以看出,随着茶皂素浓度升高扩张模量增大,而随着溶液pH值升高,茶皂素的表面扩张模量成下降趋势.这是因为茶皂素中含有-COOH,可与溶液中的碱发生反应,生成的-COONa.-COONa基团具有较强的水溶性,破坏了原来界面上表面活性剂分子存在的-COOH之间及其与-OH之间的氢键,致使表面活性剂在表面上的相互作用降低,削弱了表面膜的强度,从而导致扩张模量下降.
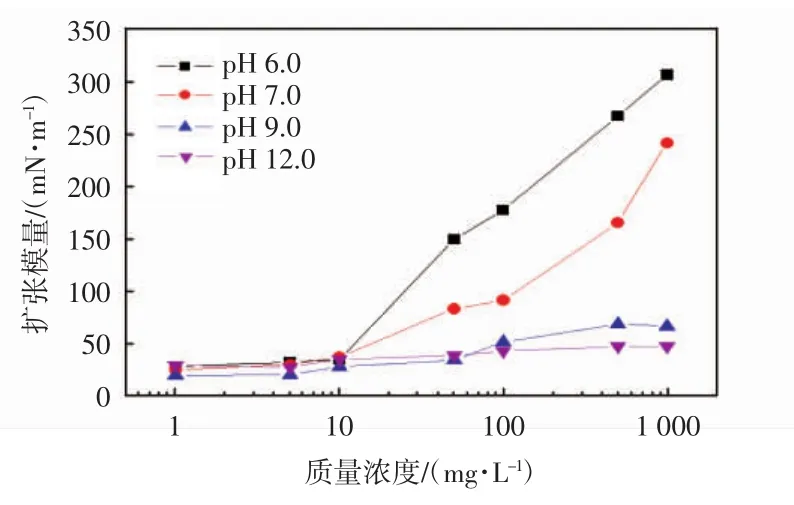
图7 pH值对茶皂素溶液的表面扩张模量的影响Fig.7 Influence of pH on dilational modulus of tea saponin
2.3.3 电解质对茶皂素表面扩张流变的影响
NaCl浓度对茶皂素溶液的表面扩张模量的影响如图8所示.
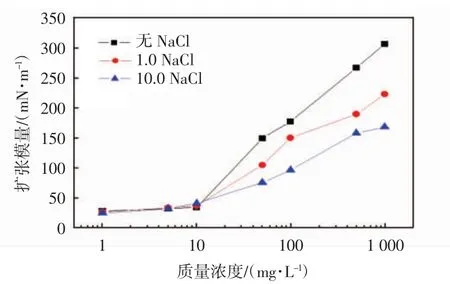
图8 NaCl浓度对茶皂素溶液的表面扩张模量的影响Fig.8 Influence of NaCl concentration on dilational modulus of tea saponin
从图8中可以看出,随着盐浓度的升高,茶皂素的表面扩张模量成下降趋势,即加入NaCl后溶液的表面扩张模量降低.这是由于在中性条件下,茶皂素主要表现为非离子表面活性剂,电解质的加入会对表面活性剂产生“盐析”作用[15],破坏表面活性剂分子之间的氢键,溶液表面分子之间的相互作用减弱,从而表面扩张模量下降,表面膜的弹性降低.随着电解质浓度升高,这种盐析作用增强,因此表面扩张模量随着电解质浓度的升高而下降.
3 结论
本文重点研究了溶液pH值和电解质浓度对茶皂素表面活性剂的表面张力和表面扩张模量的影响,得到结论如下:
(1)随着溶液pH值升高,茶皂素的表面活性降低,其临界胶束浓度显著增大,在中性条件下茶皂素的CMC为0.11×103mg/L,CMC所对应的表面张力为37.6 mN/m;
(2)由于茶皂素在中性条件下表现为非离子表面活性剂,氯化钠的加入对茶皂素的表面张力和临界胶束浓度影响不大,但氯化钠的加入会破坏表面上茶皂素分子之间的氢键作用,从而影响其表面扩张模量;
(3)随着溶液pH值升高,溶液表面茶皂素分子之间的氢键作用减弱,茶皂素的表面扩张模量显著下降;
(4)中性茶皂素溶液的表面扩张模量较高,最高能接近300 mN/m,高的扩张模量反映其高的界面弹性,有利于其形成泡沫的稳定,有望在泡沫领域应用.
参考文献:
[1]严峰,王莉,晁玉广,等.茶皂素提取及性能研究综合化学实验设计[J].天津工业大学学报,2012,31(S1):143-144. YAN F,WANG L,CHAO Y G,et al,Design of comprehensive chemistry experiment on extraction and properties study of tea saponin[J].Journal of Tianjin Polytechnic University,2012,31(S1):143-144(in Chinese).
[2]王廷吉,魏俊峰,李天顺.茶皂甙纯化及其初步鉴定[J].华东地质学院学报,1991,14(1):88-92. WANG T J,WEI J F,LI T S.Purpification of teasaponin and primany test on its purity[J].Journal of East China College of Geology,1991,14(1):88-92(in Chinese).
[3]LI X,MA J Z,XIA J,et al.A study on the extraction and purification technology of tea saponin[J].African Journal of Biotechnology,2010,9(18):2691-2696.
[4]REN H J,XIAO Q,ZHOU Z,et al.Study of tea saponin toothpaste[J].Tenside Surfactants Detergents,2015,52(4):329-332.
[5]FENG J,CHEN Y,LIU X,et al.Efficient improvement of surface activity of tea saponin through Gemini-like modification by straightforward esterification[J].Food Chemistry,2015,171:272-279.
[6]黄文红,皮晓龙,黄文新,等.茶皂素的泡沫性能研究[J].新疆石油天然气,2010,6(2):44-47. HUANG W H,PI X L,HUANG W X.The study on foam properties of natural tea saponin[J].Xinjiang Oil&Gas,2010,6(2):44-47(in Chinese).
[7]JIAN H L,LIAO X X,ZHU L W,et al.Synergism and foaming properties in binary mixtures of a biosurfactant derived from camellia oleifera Abel and synthetic surfactants[J].Journal of Colloid and Interface Science,2011,359:487-492.
[8]宋冰蕾,翟兆兰,赵剑曦,等.Gemini表面活性剂/C12En混合体系的界面吸附、扩张粘弹与泡沫稳定性[J].物理化学学报,2015,31(12),2324-2331. SONG B L,ZHAI Z L,ZHAO J X,et al.Interfacial adsorption,dilational visco-elasticity and foam stability in a mixed system of gemini surfactant/C12En[J].Acta Phvsico-Chimica Snica,2015,31(12):2324-2331(in Chinese).
[9]曹绪龙,崔晓红,李秀兰,等.扩张流变法研究表面活性剂在界面上的聚集行为[J].化学通报,2009,6:507-515. CAO X L,CUI X H,LI X L,et al.Study on the aggregation behavior of surfactant at interface by the dilatational rheological methods[J].Chemistry Bulletin,2009,6:507-515(in Chinese).
[10]杜志欣,张崇坚,万端极.超声波辅助乙醇法提取茶皂素工艺优化[J].化学与生物工程,2015,32(3):56-59. DU Z X,ZHANG C J,WAN D J.Optimization of extraction process of tea saponin by ultrasonic-assisted ethanol method[J]. Chemistry&Bioengineering,2015,32(3):56-59(in Chinese).
[11]王其伟.十六烷基聚氧乙烯醚羟丙基羧酸甜菜碱表面扩张流变研究[J].天津工业大学学报,2013,32(2):46-50. WANG Qi-wei.Study on surface dilational rheology of hexadecyl polyoxyethylene glycidyl ether glycine betaine[J].Journal of Tianjin Polytechnic University,2013,32(2):46-50(in Chinese).
[12]刘昕.基于茶皂素分子改性的表面活性剂的研究[D].济南:齐鲁工业大学,2013. LIU X.Studies on the surfactants based on tea saponins molecular modification[D].Jinan:Qilu University of Technology,2013(in Chinese).
[13]李振泉,张磊,严峰,等.不同结构芳香侧链酰基牛磺酸钠的表面扩张性质[J].物理化学学报,2009,25:1939-1944. LI Z Q,ZHANG L,YAN F,et al.Surface dilational properties of N-acyltaurate amphiphiles with aromatic side chains[J].Acta Phvsico-Chimica Snica,2009,25:1939-1944(in Chinese).
[14]YOU Y,ZHONG B X,ZHAO J X.Adsorption and micellization of alkanediyl-bis(dimethyldodecylammonium bromide)in isopropyl myristate/aqueous system[J].Colloid and Polymer Science,2010,288(14/15):1359-1367.
[15]赵国玺,朱瑶.表面活性剂作用原理[M].北京:中国轻工业出版社,2003:263-272. ZHAO G X,ZHU Y.Principles of Surfactant Action[M].Beijing:Chinese Light Industry Press,2003:263-272(in Chinese).
Extraction of tea saponin and surface performance of its solutions
MAO Lei-ting1,QI Ya-hui2,SUN Zhen-dong1,ZENG Qiang1,YAN Feng2
(1.Sinopec Energy and Environmental Engineering Co Ltd,Dongying 257026,Shandong Province,China;2.School of Environmental and Chemical Engineering,Tianjin Polytechnic University,Tianjin 300387,China)
The tea saponin was extracted from camellia cake by ethanol,and the influences of pH and electrolyte(NaCl)concentration on the surface performance of tea saponin solutions were investigated.It was shown that the critical micelle concentration(cmc)increased,while the surface dilational modulus decreased with increasing pH value of solution.NaCl has little effect on the surface tension and cmc,but it decreased the surface dilational modulus of tea saponin solution due to breaking the hydrogen bond between surfactant molecules on surface.The surface dilational modulus of tea saponin is more than 200 mN/m under neutral condition,which may be the main reason for it high foam stability.
tea saponin;surfactant;surface tension;critical micelle concentration;surface dilational modulus
TQ914.1;TQ423
A
1671-024X(2016)05-0032-05
10.3969/j.issn.1671-024x.2016.05.006
2016-07-13 基金项目:国家科技重大专项基金资助项目(2011ZX05011-004);天津市科技特派员项目(14JCTPJC00568)
毛雷霆(1984—),男,工程师,研究方向为油田化学品.E-mail:maoleiting@163.com
严 峰(1980—),男,副教授,主要研究方向为胶体界面化学及膜分离.E-mail:yanfeng@tjpu.edu.cn
