碱金属修饰g-C3N4的能带结构调控与载流子迁移过程
2016-11-22马新国徐国旺黄楚云
祝 林 马新国,* 刘 娜 徐国旺 黄楚云,*
(1湖北工业大学理学院,武汉430068;2湖北工业大学太阳能高效湖北省协同创新中心,武汉430068)
碱金属修饰g-C3N4的能带结构调控与载流子迁移过程
祝林1,2马新国1,2,*刘娜1徐国旺1,2黄楚云1,2,*
(1湖北工业大学理学院,武汉430068;2湖北工业大学太阳能高效湖北省协同创新中心,武汉430068)
采用平面波超软赝势方法研究了Li、Na、K三种碱金属离子修饰对g-C3N4能带结构和载流子迁移过程的影响。对建立的六种吸附构型分别采用广义梯度近似和局域密度近似进行计算,发现三种碱金属离子均更趋向于吸附在g-C3N4片层内的大空洞中央位置(F位置)。对于碱金属与g-C3N4形成的n型Schottky结,通过能带结构和功函数的计算,发现界面电荷的平衡使g-C3N4的能带电位分别整体下移1.52 V(Li)、1.07 V (Na)、0.86 V(K)。其中K离子的引入一方面将g-C3N4的价带和导带调整到更合适的氧化还原电位,另一方面增大了g-C3N4的最高占据轨道(HOMO)和最低未占据轨道(LOMO)的分布,有利于提高载流子的迁移率,同时出现的HOMO和LOMO轨道非共面特性有利于电子和空穴的分离。
光催化;g-C3N4;能带结构;载流子迁移
1 引言
寻找具有可以直接光催化裂解水和降解污染物的高活性半导体光催化剂是当前光催化领域研究的热点之一。发生光催化反应的先决条件是具有强的可见光吸收和合适的氧化还原电位1,2,即要求光催化材料在电子特性上具有特殊的半导体特征。TiO2被认为是最有潜力的半导体光催化材料,但是过宽的带隙以及量子产率不高等不易克服的缺点限制了其广泛应用。多元金属氧化物光催化材料一度也是光催化研究领域的热点,如InMO4(M=Nb,Ta)3、BiVO44,5、Bi2WO66、Ga1-xZnxN1-xOx7、以及我们前期研究的BiPO48和Ag3PO49,但要实现其应用目标还很远。最近发现部分层状聚合物半导体是光催化候选材料,如类石墨层状聚合物C3N4的带隙为2.7 eV,其价带顶和导带底具有较合适的氧化还原电位,表现出一定的光催化性能10,11。同时,它还具有制备简单、环境友好、适合规模化生产等优点12,13。
尽管如此,进一步提高g-C3N4的可见光吸收及载流子迁移率,以改善光电转换效率仍然面临着挑战14。由于g-C3N4是一种类石墨的六方晶系层状结构,且层内存在较大空洞,因此具有很高的比表面积和分散性,进行化学掺杂是一种有效调控g-C3N4电子结构和表面性能的有效手段。在过去的实验研究中发现,共轭聚合物半导体在异质元素的修饰下,有可能窄化带隙和降低HOMO轨道15,以及我们报道的S和P非金属掺杂不仅可以提高可见光吸收,而且为载流子的输运通道由原本的C―N―C改变为C―N―P―N―C16,克服了桥位N原子对载流子迁移限制作用,从而提高其迁移率。此外,还有报道I修饰g-C3N4增大了可见光吸收至600 nm,且增大了表面17;S修饰g-C3N4降低了过电位,提高了阳极光催化活性18;通过控制g-C3N4形变,提高了可见光吸收,且增强了载流子迁移19。
与过去的质子化掺杂和非金属的共价掺杂不同,具有非局域化特性的金属修饰g-C3N4,一定程度上可以活化g-C3N4表面,因此金属修饰方法成为g-C3N4改性的新研究热点。最近发现Fe离子修饰g-C3N4有更好的光催化活性,其作用机理为引入的Fe离子与N形成配位键,从而改变了g-C3N4的电子结构,降低了带隙,提高了可见光吸收20,碱金属K21和Na22修饰g-C3N4同样也获得较好的光催化活性,碱金属的引入使能带整体下移,提高了价带的氧化能力,此外还促进了载流子的分离。然而碱金属与周围N原子的作用以及对能带结构的调控机理仍缺乏研究,载流子的迁移过程仍需探讨。因此,本文从g-C3N4的基本结构出发,采用平面波超软赝势方法计算了碱金属在层状聚合物g-C3N4内六种吸附构型的吸附能;并通过能带结构和功函数计算,确定出碱金属吸附对g-C3N4能带结构及载流子迁移过程的影响。这些结果的获得将为新型高效光催化体系的设计提供理论依据和新思路。
2 物理模型和计算方法
层状聚合物g-C3N4是一种空间群为cmc21(No. 36)的六方晶体,由氮原子连接三均三嗪(C6N7)组成ABAB层叠结构,一个晶胞包含56个原子,其中N原子为32个,C原子为24个。所有的C原子与周围的3个N原子形成三配位,桥位和中心位置的N原子与周围的3个C原子形成三配位,而边缘N原子与周围的2个C原子形成二配位。由于碱金属原子,尤其是K、Na原子的半径较大(DLi=0.15 nm,DNa=0.19 nm,DK=0.23 nm),而C3N4环的直径仅为0.22 nm,因此,若掺入的碱金属在g-C3N4片层内,则仅有可能在N围成的大空洞中。若掺入的碱金属在片层内,最有代表性的位置是在原子的正上方。因此,我们选取了位于A、B、C、D、E原子的正上方的5种吸附构型;以及位于片层内N围成的大空洞中心的构型,共确定了6种可能的吸附构型,所有的吸附位置如图1所示。
采用基于密度泛函理论的平面波超软赝势方法研究结构的稳定性及电学性质23。交换关联能采用广义梯度近似(GGA)24。为了能正确描述层间的范德华力,选用一种杂化的半经验方法(OBS)处理衰减原子对的离散修正量C6R-6,该修正方案可以较好平衡在处理该离散项上计算时间的花费与改善非成键作用之间的需要25。原子-电子间的相互作用采用了Vanderbilt方案的超软赝势26。在描述原子实与价电子之间的相互作用时,选取的价电子组态分别为C:2s22p2,N:2s22p3,Li:1s22s1,Na:2s22p63s1,K:3s23p64s1,其他轨道电子视为芯电子进行计算。平面波截断能设置为340 eV,第一布里渊区采用Monkhorst的5×5×4。结构优化选用的自恰收敛精度设置为1×10-6eV·atom-1,原子受力不超过0.01 eV,最大原子位移不超过5× 10-5nm。

图1 碱金属吸附于g-C3N4的六种掺杂构型俯视图Fig.1 Top views of the six doped configurations of alkali metal adsorbed on g-C3N4The lettersA-F represent the absorption positions of alkali metal atom,respectively.
3 结果和讨论
3.1结构的稳定性
运用LDA和GGA方法优化后,结果显示g-C3N4具有稳定的平面层状结构,这与单层g-C3N4容易形成弓形的几何结构完全不同27,23。与实验结果相比较,众所周知采用LDA方法往往会低估晶体结构常数,高估体系的结合能,而GGA方法刚好相反。前者与文献28,29中的理论结果比较一致。Gracia和Kroll29采用分子动力学方法优化的结果显示在面内相临的三均三嗪中心N原子之间的距离为0.677 nm,这个结果与Wang等10采用XRD方法获得结果(0.681 nm)比较一致。这两个结果与Bojdys等12的实验结果(0.730 nm)有很大出入。认为实际体相的g-C3N4中,晶体结构参数应该在LDA和GGA两种方法计算的结果之间,因此可以估算面内相临的三均三嗪中心N原子之间的距离和层间距离分别为0.714和0.319 nm。
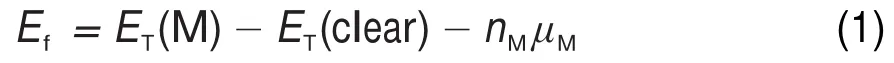
为获得结构合理且稳定的吸附构型,对建立的6种掺杂构型进行了吸附能的计算。碱金属在g-C3N4表面上的吸附能定义为其中ET(M)为M原子吸附在化学计量比结构内的体系总能量,ET(clear)为清洁化学计量比结构的体系总能量,nM为吸附的碱金属原子数,μM为吸附的碱金属原子的绝对化学势。当吸附能为负数时,表示该吸附为放热过程,且数值越大表明吸附作用越强,吸附结构越稳定。
根据(1)式,计算出了Li、Na、K三种碱金属6种不同掺杂构型的吸附能,列于表1中。可以看出,对于Li、Na、K离子掺杂所选取的A-F共6种不同掺杂构型中,构型F的吸附能比其他的AE吸附构型分别要高1.8(Li)、3.6(Na)和5.3 eV(K)以上。吸附构型F的吸附能均为负数,且绝对值最大,即最大的吸附能分别为Ef(Li)=-4.477 eV,Ef(Na)=-4.144 eV,Ef(K)=-3.603 eV。这些结果均说明了吸附构型F的结构最为稳定,并且掺杂易于实现。为了更精确地确定吸附构型F中碱金属原子所处的位置,将结构优化后的碱金属原子M到周围最邻近6个N原子的距离列于表2中。结果显示,M到周围N原子的距离表现出高度的对称性,即M―N1和M―N2距离相等,M―N3和M―N6距离相等,M―N4和M―N5距离相等,这说明碱金属M完全处于N六边形的空洞中心,而且位于平面内。这个结果与Hu等30基于实验的推测是一致的。
3.2Schottky结能级调制
为了探讨掺杂构型F会对g-C3N4的能带结构带来的影响,分别采用LDA和GGA方法计算了纯g-C3N4的能带结构和掺杂后的能带结构,所得带隙值记录在表3中。从结果上看,采用LDA和GGA方法所得的带隙值均比实验值要小,而与Xiong31和Aspera32等的理论结果比较一致,这是由于DFT在计算带隙值时普遍存在不可避免的误差。碱金属的引入对能带的形状影响不大,碱金属掺入前后,能带结构的骨架基本未变,而带隙有明显减小,这说明吸收谱的范围会有一定的红移,这与Hu等30的实验结果和Xiong等31的理论结果相符;同时可以发现,随着碱金属原子半径的增大,对带隙的窄化能力逐步减弱。此外,这种窄化应该是与掺入碱金属的浓度有关的,在Hu等30的实验结果中,K掺杂g-C3N4的带隙值随着K浓度的变化而在2.52-2.65 eV间变化。
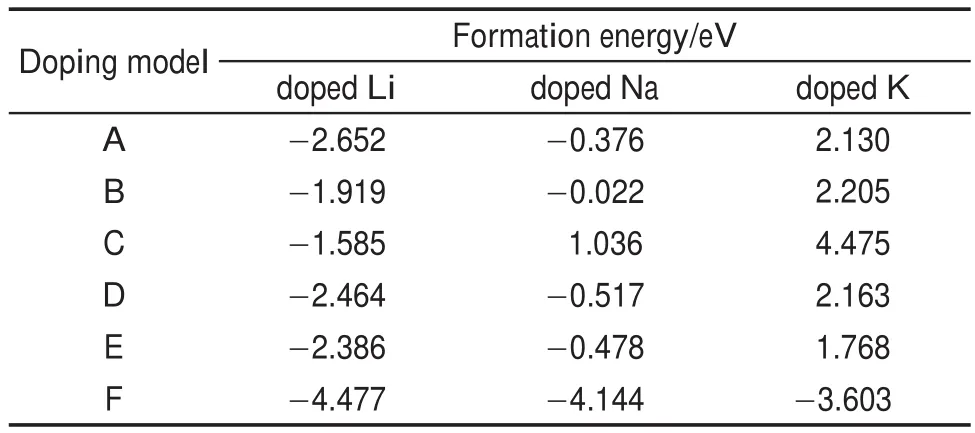
表1 三种碱金属分别掺杂g-C3N4时,6种不同吸附构型(A-F)的吸附能Table 1 Adsorption energies of six different adsorption configurations(A-F)for doped g-C3N4with three alkali metals
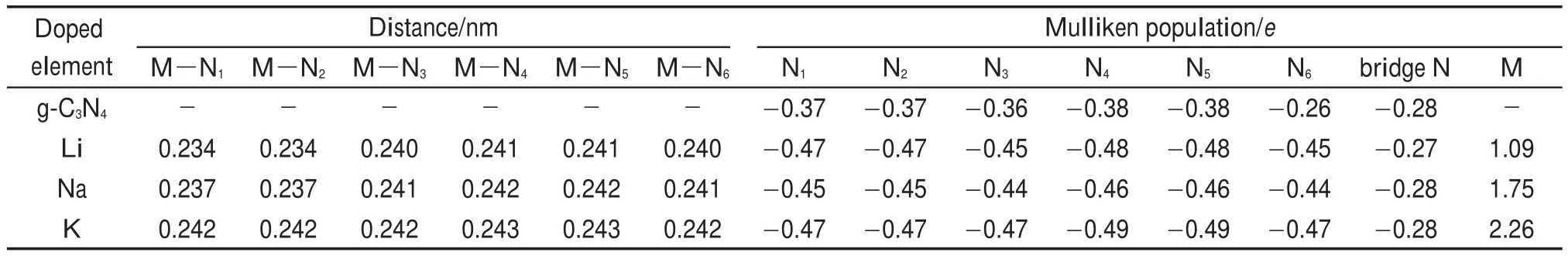
表2 吸附构型F中碱金属离子M与周围6个N原子的距离及碱金属M和6个N原子的Milliken布居数Table 2 Distances between the alkali metal ion M and its neighboring six N atoms and the Milliken population of alkali metal ion M and its neighboring six N atoms for adsorption configuration F
空洞周围N原子的2p轨道对价带顶和导带底都有贡献。因此,碱金属引入导致这些N原子的电荷分布发生改变,势必对g-C3N4原有费米能级的位置产生一定的影响。一般而言,金属和半导体表面接触形成Schottky结,在界面上形成表面势垒。由于半导体的费米能级较高,半导体的费米能级随着整个能带结构移动到与金属的费米能级相平。为了定量分析Schottky结的能级调制,计算了纯g-C3N4以及碱金属掺杂后g-C3N4的功函数。其物理意义是把一个电子从固体内部移到此物体表面所需的最少的能量,其值也等于费米能级对绝对真空能级(AVS)的电位,在这里用于确定掺杂前后g-C3N4费米能级的位置。
针对前面的物理模型,建立(001)晶面的Slab结构(真空为1.5 nm),获得的纯g-C3N4功函数为4.42 eV,Li、Na、K掺杂g-C3N4的功函数为5.94、5.57和5.32 eV,其结果如图2所示。由于氢还原能级(NHE)与绝对真空能级(AVS)间的相对因子为4.5 eV,换算后费米能级的电位分别为-0.08、1.44、1.07和0.82 V(vs NHE)。可以看出掺杂后,g-C3N4费米能级在向正向移动。同时,随着碱金属原子半径的增大,费米能级下降的幅度逐次减小。
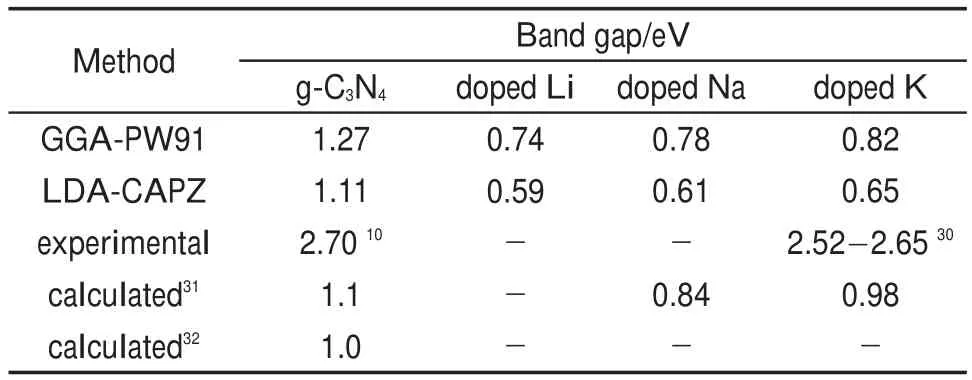
表3 掺杂前后g-C3N4的带隙值Table 3 Band gap of g-C3N4before and after doping
导带边电位采用电化学方法测量是一件比较困难的事情。为了直接从理论上获得导带边和价带边的电位(真空电位),运用原子平均电负性方法以及实验带隙值通过下列式子进行估算33,34
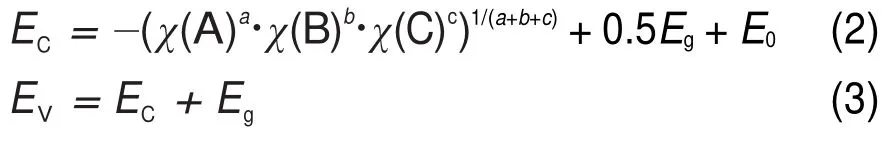
这里χ(A)、χ(B)和χ(C)分别为原子A、B和C的绝对电负性,EC、EV和Eg分别为导带底电位、价带顶电位和带隙值,这里真空电位与氢还原电位差E0为4.44 V。一般而言,在温度T=298 K,气压为1.013×105Pa时,许多半导体(如Ta3N5,GaN等)在溶剂中与H+或者OH-离子反应,结果界面上的带边将随溶剂的pH值按照大约60 mV·pH-1的线性关系而变化33,35,这主要是由于表面吸附的H+或者OH-
离子的驱动作用。在pH=pHZPC,计算获得纯g-C3N4的导带边和价带边电位(相对氢还原)分别为-1.05和1.65 V。
当向g-C3N4中掺入碱金属以后,g-C3N4的费米能级将下移,碱金属的费米能级将上移,直至两者费米能级拉平,由于Schottky结作用,g-C3N4的能带整体下移,即价带顶电位向正向移动,其光生空穴的氧化性将增加,同时导带底电位也向正向移动,其光生电子的还原能力有所减弱。其中Li、Na的掺杂使g-C3N4的导带电位降低到0 V以下,过大的能级调制使其还原能力有所不足,而K掺杂对g-C3N4导带底的电位降低至-0.09 V,而价带顶的电位调整为2.41 V,可以满足光催化反应过程中光生电子和空穴的电位要求1,2。事实上,这种电位的调制应该与掺入碱金属离子的浓度有相当大的关系,Hu等30通过控制K离子的浓度使g-C3N4的导带和价带电位在-1.09-1.56 V和-0.31-2.21 V间变化。为了清楚地了解在同一浓度下,三种碱金属引入所引起的能级变化,将纯g-C3N4和碱金属掺杂后g-C3N4的价带和导带电位总结于图3中。

图2 沿着垂直g-C3N4(001)晶面方向的功函数Fig.2 Work functions in the vertical direction of g-C3N4(001)plane (a)pure g-C3N4;(b)Li doped g-C3N4;(c)Na doped g-C3N4;(d)K doped g-C3N4
3.3载流子迁移过程
碱金属掺杂对g-C3N4的能带结构显示出一定的调制作用,这必然对光生载流子的迁移过程的产生重要影响。首先分析了纯g-C3N4和碱金属掺杂g-C3N4的分波态密度(PDOS),如图4所示。可以看出,纯g-C3N4和碱金属掺杂g-C3N4的导带底附近均是由N 2p和C 2p轨道杂化构成,而价带顶附近均来自N 2p态的贡献,少量来自C的贡献。尤其值得注意的是,碱金属的杂质能级位置很深,在价带顶和导带底附近均无态密度分布,因此可以预见碱金属离子并不直接参加光生载流子的产生、分离和转移过程。那么,碱金属的引入对g-C3N4电子结构的影响应该来自于碱金属对周围邻近N原子的电荷重新分布。为了证明这种观点,对邻近N原子的Mulliken原子布居定量地进行了分析,如表2所示。可以看出,随着由Li到K碱金属原子的金属性增强,Mulliken布居数依次增大,且数值都大于1,这说明碱金属不仅失去了外层电子,次外层电子也失去了一部分;而且这些失去的电子大部分转移给了周围的N原子。显然,碱金属的引入对周围N原子的电荷分布有重要影响。
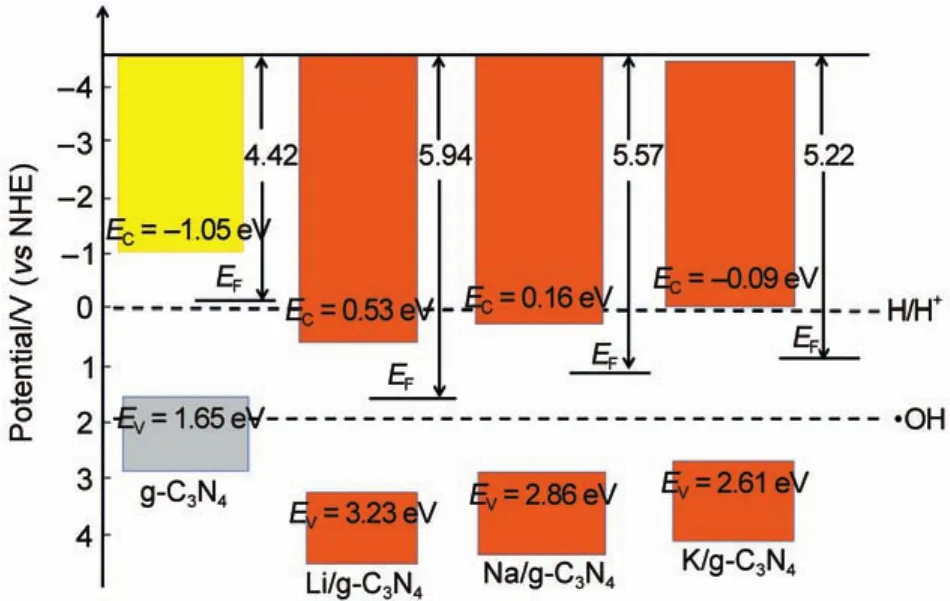
图3 纯g-C3N4和碱金属掺杂后g-C3N4的导带和价带电位Fig.3 Valence band and conduction band potentials for pure g-C3N4and alkali metal doped g-C3N4

图4 纯g-C3N4和碱金属掺杂后g-C3N4的分波态密度图Fig.4 Partial density of states(PDOS)for pure g-C3N4and alkali metal doped g-C3N4
为了进一步分析复杂的活性位置,提供了价带顶和导带底附近的HOMO和LOMO信息,如图5所示。从分布图来看,掺杂前后的HOMO均主要由低配位N原子在面内的2p轨道构成,而LOMO均主要由C原子在Z方向的2p轨道构成。因此,在可见光激发下空穴仅仅出现在低配位N原子周围,在面内表现出氧化活性,而电子出现在C原子周围,在Z方向上表现出还原性。对于纯g-C3N4,一方面,HOMO在低配位N原子以及LOMO在C原子Z方向的局域性都较强;另一方面,桥位N原子连接了三个三均三嗪(C6N7)结构单元,它的2p占据态位于费米能级下方0.60 eV位置,未占据态位于导带底上方1.35 V位置,表明桥位N原子的轨道分布对价带顶和导带底没有任何贡献,而且局域性很强。也就是说载流子不能通过桥位N原子从一个大三角形的三均三嗪(C6N7)结构单元到其他的结构单元,载流子的迁移受到桥位N原子的限制。
这里以K掺杂为例说明载流子的迁移过程。由于碱金属的杂质能级位置很深,掺杂后碱金属离子并不直接参加光生载流子的产生、分离和转移过程。比较图5(a)和(b)可以发现,K掺杂后,一方面使桥位N原子附近LUMO的非局域性有所增强,可见光激发下光生电子可以通过桥位的N原子在相邻的三均三嗪(C6N7)结构单元间自由迁移,这将克服桥位N原子对载流子迁移限制作用,从而提高其迁移率。同时还发现K掺杂使LUMO集中到掺杂层,而HOMO主要集中到非掺杂层。因此,当可见光激发下的光生电子从HOMO跃迁至LUMO,电子和空穴分别在掺杂层和非掺杂层内迁移,大大降低载流子的复合几率,延长了载流子的寿命。也就是说,增大的HOMO和LOMO分布有利于提高载流子的迁移率,而HOMO和LOMO的非共面特性有利于电子和空穴的分离16,36。
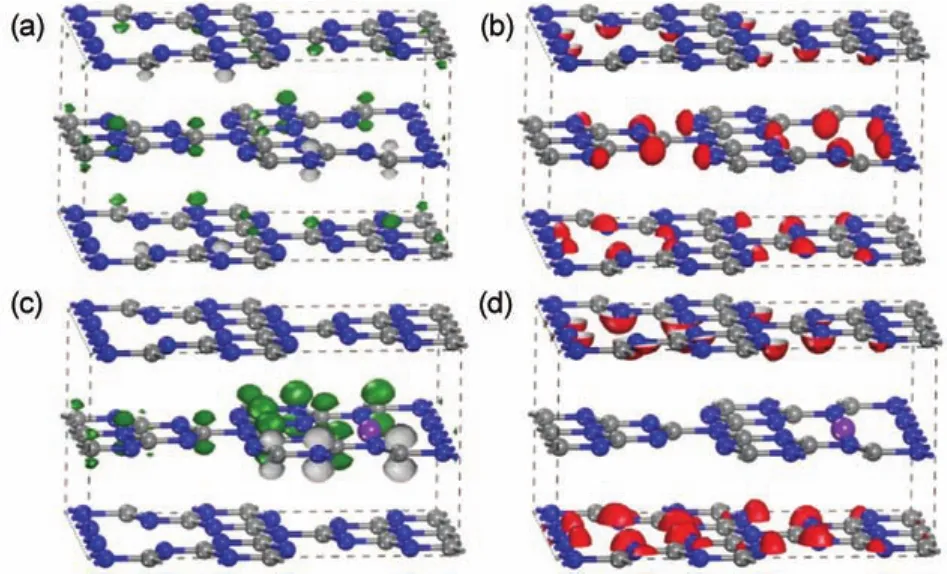
图5 LUMO和HOMO分布图Fig.5 Distribution of LUMO and HOMO
4 结论
采用第一性原理方法研究了三种碱金属离子修饰对g-C3N4能带结构和载流子迁移过程的影响。对建立的六种吸附构型进行吸附能计算,均发现三种碱金属原子吸附于g-C3N4片层内的大空洞中央位置(F位置)时,显示出最大的吸附能且为负数,说明了该吸附构型较易于实现。功函数计算的结果显示碱金属与g-C3N4形成的异质结界面的电荷平衡会使g-C3N4的能带位置整体下移,尤其值得注意的是K离子的引入使g-C3N4的价带和导带的电位分别调整为2.51和-0.19 eV,具有比未掺杂的g-C3N4更合适的氧化还原电位。由于碱金属的杂质能级位置很深,掺杂的碱金属离子并不直接参加光生载流子的产生、分离和转移过程,但是影响周围邻近其他原子的电荷分布,即表现出HOMO和LOMO非共面特性以及增大的HOMO和LOMO分布,这有利于电子和空穴的分离和迁移。
References
(1) Chen,X.B.;Shen,S.H.;Guo,L.J.;Mao,S.S.Chem.Rev. 2010,110,6503.doi:10.1021/cr1001645
(2) Kudo,A.;Mesiki,Y.Chem.Soc.Rev.2009,38,253. doi:10.1039/B800489G
(3)Zou,Z.G.;Ye,J.H.;Sayama,K.;Arakawa,H.Nature 2001, 414,625.doi:10.1038/414625a
(4) Kudo,A.;Ueda,K.;Kato,H.;Mikami,I.Catal.Lett.1998,53, 229.doi:10.1023/A:1019034728816
(5) Kohtani,S.;Tomohiro,M.;Tokumura,K.;Nakagaki,R.Appl. Catal.B-Environ.2005,58,265.doi:10.1016/j. apcatb.2004.12.007
(6) Fu,H.B.;Zhang,S.C.;Xu,T.G.;Zhu,Y.F.;Chen,J.M.Environ.Sci.Technol.2008,42,2085.doi:10.1021/es702495w
(8) Pan,C.S.;Zhu,Y.F.Environ.Sci.Technol.2010,44,5570. doi:10.1021/es101223n
(9) Ma,X.G.;Lu,B.;Li,D.;Shi,S.;Pan,C.S.;Zhu,Y.F.J.Phys. Chem.C 2011,115,4680.doi:10.1021/jp111167u
(10)Wang,X.C.;Maeda,K.;Thomas,A.;Takanabe,K.;Xin,G.; Carlsson,G.M.;Domen,K.;Antonietti,M.Nat.Mater.2009,8, 76.doi:10.1038/nmat2317
(11) Yan,S.C.;Li,Z.S.;Zou,Z.G.Langmuir 2009,25,10397. doi:10.1021/la900923z
(12) Bojdys,M.J.;Müller,J.;Antonietti,M.Chem.Eur.J.2008,14, 8177.doi:10.1002/chem.200800190
(13) Kroke,E.;Schwarz,M.Coord.Chem.Rev.2004,248,493. doi:10.1016/j.ccr.2004.02.001
(14) Zhang,J.S.;Chen,X.F.;Takanabe,K.Angew.Chem.Int.Ed. 2010,49,441.doi:10.1002/anie.200903886
(15) Liu,G.;Niu,P.;Sun,C.H.J.Am.Chem.Soc.2010,132, 11642.doi:10.1021/ja103798k
(16) Ma,X.G.;Lv,Y.H.;Xu,J.J.Phys.Chem.C 2012,116,23485. doi:10.1021/jp308334x
(17) Zhang,G.G.;Zhang,M.W.;Ye,X.X.;Qiu,X.Q.;Lin,S.; Wang,X.C.Adv.Mater.2014,26,805.doi:10.1002/ adma.201303611
(18) Lin,S.;Ye,X.X.;Gao X.M.;Huang,J.J.Mol.Catal.A:Chem. 2015,406,137.doi:10.1016/j.molcata.2015.05.018
(19) Chen,Y.;Wang,B.;Lin,S.;Zhang,Y.F.;Wang,X.C.J.Phys. Chem.C 2014,118,29981.doi:10.1021/jp510187c
(20) Jin,R.R.;You,J.G.;Zhang,Q.;Liu,D.;Hu,S.Z.;Gui,J.Z. Acta Phys.-Chim.Sin.2014,30,1706.[金瑞瑞,游继光,张倩,刘丹,胡绍争,桂建舟.物理化学学报,2014,30,1706.] doi:10.3866/PKU.WHXB201406272
(21) Gao,H.L.;Yan,S.C.;Wang,J.J.Appl.Catal.B-Environ.2014, 158,321.doi:10.1016/j.apcatb.2014.04.036
(22) Zhang,M.;Bai,X.J.;Liu,D.;Wang,J.;Zhu,Y.F.Appl.Catal. B-Environ.2015,164,77.doi:10.1016/j.apcatb.2014.09.020
(23) Segall,M.D.;Lindan,P.L.D.;Probert,M.J.J.Phys.Condens. Matter 2002,14,2717.doi:10.1088/0953-8984/14/11/301
(24) Kohn,W.;Sham,L.J.Phys.Rev.1965,140,A1133. doi:10.1103/PhysRev.140.A1133
(25) Ortmann,F.;Bechstedt,F.;Schmidt,W.G.Phys.Rev.B 2006, 73,205101.doi:10.1103/PhysRevB.73.205101
(27) Deifallah,M.;McMillan,P.F.;Cora,F.J.Phys.Chem.C 2008, 112,5447.doi:10.1021/jp711483t
(28) Pan,H.;Zhang,Y.W.;Shenoy,V.B.;Gao,H.J.ACS Catal. 2011,1,99.doi:10.1021/cs100045u
(29) Gracia,J.;Kroll,P.J.Mater.Chem.2009,19,3013. doi:10.1039/B821568E
(30) Hu,S.Z.;Li,F.Y.;Fan,Z.P.;Wang,F.;Zhao,Y.F.;lv,Z.B. Dalton Trans.2015,44,1084.doi:10.1039/C4DT02658F
(31) Xiong,T.;Cen,W.L.;Zhang,Y.X.;Dong,F.ACS Catal.2016, http://pubs.acs.org on March 7,2016.
(32)Aspera,S.M.;David,M.;Kasai,H.Jap.J.Appl.Phys.2010, 49,115703.doi:10.1143/JJAP.49.115703
(33) Xu,Y.;Schoonen,M.A.A.Am.Mineral.2000,85,543.
(35) Chun,W.J.;Ishikawa,A.;Fujisawa,H.;Takata,T.;Kondo,J. N.;Hara,M.;Kawai,M.;Matsumoto,Y.;Domen,K.J.Phys. Chem.B 2003,107,1798.doi:10.1021/jp027593f
(36) Fukuzumi,S.;Kotani,H.;Ohkubo,K.;Ogo,S.;Tkachenko,N. V.;Lemmetyinen,H.J.Am.Chem.Soc.2004,126,1600. doi:10.1021/ja038656q
Band Structure Modulation and Carrier Transport Process of g-C3N4Doped with Alkali Metals
ZHU Lin1MAXin-Guo1,2,*LIU Na1XU Guo-Wang1,2HUANG Chu-Yun1,2,*
(1School of Science,Hubei University of Technology,Wuhan 430068,P.R.China;2Hubei Collaborative Innovation Center for High-efficiency Utilization of Solar Energy,Hubei University of Technology,Wuhan 430068,P.R.China)
The effects of Li,Na,and K alkali metal ions on the band structures and carrier transfer of graphitic carbon nitride(g-C3N4)are investigated using the plane-wave ultrasoft pseudopotential method.The generalized gradient approximation and local density approximation are used to calculate total energies of six adsorption configurations.The three alkali ions all tend to adsorb on the large central cavity(F position)in g-C3N4layers. The calculated band structures and work function values indicate that the interface charge balance of the n-type Schottky junctions formed between the alkali metal ions and g-C3N4induces the total band edge potential of g-C3N4to shift down by 1.52 V(Li),1.07 V(Na),and 0.86 V(K).The incorporation of K ion adjusts the valence and conduction bands to more appropriate redox potentials than those of pure g-C3N4,and increases the distribution of the HOMO and LOMO of g-C3N4,which helps to improve the mobility of carriers.Meanwhile,the non-coplanar HOMO and LOMO favor the separation of electrons and holes.
Photocatalysis;g-C3N4;Band structure;Carrier transport
March 18,2016;Revised:June 21,2016;Published online:June 22,2016.
s.MAXin-Guo,Email:maxg2013@sohu.com.HUANG Chu-Yun,Email:chuyunh@163.com.
O649
10.3866/PKU.WHXB201606222
The project was supported by the National Natural Science Foundation of China(51102150,51472081),Foundation of Hubei University of
Technology for High-level Talents,China(GCRC13014),Development Founds of Hubei Collaborative Innovation Center,China
(HBSKFZD2014003,HBSKFZD2014011,HBSKFZD2015004),and Students Research Fund of Hubei Collaborative Innovation Center,China (HBSDY201511).
国家自然科学基金(51102150,51472081),湖北工业大学高层次人才启动基金(GCRC13014),湖北省协同创新中心开放基金项目
(HBSKFZD2014003,HBSKFZD2014011,HBSKFZD2015004)和湖北省协同创新中心大学生科技创新基金(HBSDY201511)资助©Editorial office ofActa Physico-Chimica Sinica
(7)Maeda,K.;Domen,K.Chem.Mater.2010,22,612. 10.1021/cm901917a
(26) Vanderbilt,D.Phys.Rev.B 1990,41,7892.10.1103/ PhysRevB.41.7892
(34) Pearson,R.G.Inorg.Chem.1988,27,734.10.1021/ ic00277a030
