耐甲氧西林金黄色葡萄球菌诱导牛乳腺上皮细胞炎症反应的分子标志物研究
2016-11-08宋敏艳韦艺媛MuhammadZahoorKhan
宋敏艳,韦艺媛,2,Muhammad Zahoor Khan,王 新,俞 英*
(1.中国农业大学动物科技学院,农业部动物遗传育种与繁殖重点实验室&畜禽育种国家工程实验室,北京 100193;2.重庆市畜牧技术推广总站,重庆 401121; 3.西北农林科技大学食品学院,杨凌 712100)
耐甲氧西林金黄色葡萄球菌诱导牛乳腺上皮细胞炎症反应的分子标志物研究
宋敏艳1,韦艺媛1,2,Muhammad Zahoor Khan1,王新3,俞英1*
(1.中国农业大学动物科技学院,农业部动物遗传育种与繁殖重点实验室&畜禽育种国家工程实验室,北京 100193;2.重庆市畜牧技术推广总站,重庆 401121; 3.西北农林科技大学食品学院,杨凌 712100)
旨在获得耐甲氧西林金黄色葡萄球菌(MRSA)诱导牛乳腺上皮细胞炎症反应的关键分子标志物。本研究以牛乳腺上皮细胞系Mac-T为试验材料,利用MRSA进行体外感染,通过与普通金葡菌感染组及未感染组进行比较,检测隐性乳房炎候选基因TRAPPC9、JAK2及炎症指示因子IL-6基因在MRSA感染不同时间点的基因表达量。结果显示,与未感染的对照组相比,MRSA 菌株体外感染Mac-T细胞6 h时,TRAPPC9基因表达量显著降低(P<0.05);感染8 h时,JAK2基因表达量显著降低(P<0.05);金葡菌菌株感染Mac-T细胞6 h时,TRAPPC9与JAK2基因表达量均显著降低(P<0.05)。与普通金葡菌相比,经MRSA处理6和10 h时,Mac-T细胞的TRAPPC9、JAK2及IL-6基因表达量均较高,且感染6 h时,MRSA处理组TRAPPC9基因表达量显著高于金葡菌处理组(P<0.05)。结果表明,MRSA及金葡菌感染Mac-T细胞后,3个基因表达变化规律基本相似,MRSA菌株感染更不易引起宿主细胞JAK2基因表达量的变化,而TRAPPC9基因则可作为MRSA金葡菌及普通金葡菌感染的首选分子标志物。
耐甲氧西林金黄色葡萄球菌;奶牛隐性乳房炎;乳腺上皮细胞;TRAPPC9;JAK2
耐甲氧西林金黄色葡萄球菌(Methicillin-resistantStaphylococcusaureus,MRSA)亦称“超级细菌”,于1961年首次报道,是一种重要的医院及社区感染病原菌,也是家畜临床病例经常分离到的致病菌。由于其具有多重耐药性和极易造成暴发流行病等特征,已成为目前人类临床抗感染治疗的一大难题,也是危害最严重的一类人畜共患菌[1-3]。
奶牛乳房炎是奶牛乳腺在受到蚊虫叮咬、物理刺激、病原微生物等环境刺激时,产生的一系列不同程度的炎症反应[4]。根据临床症状明显与否,将其分为临床乳房炎和隐性乳房炎,其中隐性乳房炎发病率最高(约占牛群的25%~68%),造成奶牛场经济损失极为严重[5]。金黄色葡萄球菌(Staphylococcusaureus,简称金葡菌)是引起奶牛隐性乳房炎最主要的病原微生物之一,它不仅能逃逸宿主牛的天然防御系统,还能摧毁宿主的免疫系统[3,5-6]。由金葡菌尤其是MRSA金葡菌引起的奶牛乳房炎具有极强耐药性,难以诊治,一旦发现只能淘汰[3]。
奶牛群生产管理常用乳汁体细胞数(Somatic cell count,SCC)作为判断隐性乳房炎的间接指标,每毫升乳汁SCC小于10万为乳房健康牛,大于50万为乳房炎阳性牛,20万~50万为隐性乳房炎牛[7]。本课题组X.Wang[8],董易春[9]和T.Usman[10]等利用全基因组关联分析及候选基因分析等方法发现,转运蛋白颗粒复合体9基因(Trafficking protein particle complex 9,TRAPPC9)和JAK-STAT(Janus kinase and signal transducer and activator of transcription)信号通路上的酪氨酸蛋白激酶2基因(Janus Kinase 2,JAK2)的单核苷酸突变(Single nucleotide polymorphisms,SNPs)与中国荷斯坦牛的乳汁SCC及血清细胞因子显著关联,提示两个基因可作为抗奶牛隐性乳房炎的关键候选基因。TRAPPC9基因位于奶牛14号染色体上,编码转运蛋白NIBP(NIK and IKKβ-binding protein),对炎症信号通路NF-κB(Nuclear factor kappa-light-chain-enhancer of activated B cells)的激活具有调控作用[11-12]。JAK2基因编码胞内酪氨酸蛋白激酶,通过激活JAK-STAT信号传导途径提高机体对细胞因子的敏感度,在炎性疾病治疗中具有重要作用[13]。此外,白介素6(Interleukin-6,IL-6)在免疫细胞的成熟、活化、增殖和免疫调节等一系列过程中发挥重要作用,并参与机体的多种生理及病理反应,与许多慢性炎症性疾病密切相关。研究表明,IL-6浓度与炎症反应程度呈正相关,可作为判断炎症反应的灵敏指标[14-15]。
为确定MRSA体外感染牛乳腺上皮细胞的最佳感染时间及关键分子标志物,本研究利用从新鲜牛奶中分离纯化的MRSA菌株体外感染牛乳腺上皮细胞系(Mac-T细胞),并与普通金葡菌感染及无感染的Mac-T细胞进行对比,检测并比较了隐性乳房炎关键候选基因TRAPPC9、JAK2及促炎因子基因IL-6在Mac-T细胞不同处理组及不同作用时间点的表达变化规律,进一步为奶牛MRSA金葡菌乳房炎的及早诊断及分子抗病育种提供基础数据。
1 材料与方法
1.1细胞系与菌株
所用细胞为牛乳腺上皮细胞系(Mac-T),由浙江大学奶业科学研究所惠赠。该细胞系是一种具有正常乳腺上皮细胞形态与特征的永生化细胞系,可稳定传代、无外源微生物污染、贴壁生长。
所用菌株为本课题组前期从荷斯坦牛新鲜乳汁中分离、纯化所得。其中一株为耐甲氧西林金黄色葡萄球菌(MRSA),含特异性耐药基因MecA;另一株为普通金葡菌,含金葡菌特异基因Nuc。
1.2Mac-T细胞培养
复苏冻存的Mac-T细胞,于37 ℃,5% CO2条件下用完全培养液(DMEM+10% FBS+1%双抗)培养。待细胞生长至80%汇合时,吸弃培养液,用无菌PBS清洗细胞两次;加入0.25% Trypsin-EDTA消化液,37 ℃,5% CO2条件下消化3~5 min,普通光学倒置显微镜下观察,待细胞变圆脱落时加入培养液终止消化,收集的细胞于1 000 r·min-1离心5 min,弃上清,加入PBS进行清洗,反复吹打混匀细胞,1 000 r·min-1离心5 min,弃上清,加入完全培养液混匀细胞,将收集的细胞按1∶2的比例接种于新培养皿中,于37 ℃,5% CO2培养箱中培养。每隔1 d换液1次,待细胞长至80%汇集时传代培养。
1.3菌株鉴定
使用细菌基因组DNA纯化试剂盒(Promega,Cat.A1120)提取菌株DNA,作为PCR反应模板。分别根据MRSA及金葡菌的特异基因MecA、Nuc序列进行特异性PCR扩增(引物信息见表1),PCR扩增产物用2.0%琼脂糖凝胶电泳显示扩增条带,进而用PCR产物直接测序法鉴定菌株类型。
细菌特异性PCR反应体系:模板3 μL,Premix 12.5 μL,正向引物(10 μmol)1 μL,反向引物(10 μmol)1 μL,ddH2O 7.5 μL,采用热盖反应进行PCR反应,具体条件:MRSA特异基因MecA:94 ℃预变性10 min;94 ℃变性40 s,58 ℃退火40 s,72 ℃延伸50 s;72 ℃延伸7 mim;4 ℃保存,变性到第一次延伸循环35次。金葡菌特异基因Nuc:94 ℃预变性10 min;94 ℃变性30 s,59 ℃退火30 s,72 ℃延伸30 s;72 ℃延伸7 mim;4 ℃保存,变性到第一次延伸循环35次。
1.4细菌悬液制备
将冻存的菌株从-80 ℃冰柜取出,室温溶解,接种到TSB液体培养基中,37 ℃,200 r·min-1震荡培养18~24 h。使用稀释平板计数法,取100 μL稀释后的菌液均匀涂布于新鲜的PCA固体培养基中,倒置于恒温培养箱中,37 ℃培养24 h,然后计数平板上的菌落。将收集到的细菌沉淀重悬于DMEM基础培养液中,调整菌株浓度为1×108cfu·mL-1,4 ℃短暂保存备用。
1.5菌株感染试验
传代培养3代的Mac-T细胞于37 ℃,5% CO2条件下细胞生长到80%汇合时,弃掉培养液,用无菌PBS洗2遍,添加DMEM基础培养液,于37 ℃,5% CO2培养箱内培养2 h,然后用浓度为1×108cfu·mL-1的MRSA菌株和金葡菌菌株悬液,以MOI=10∶1的比例分别侵染细胞3、6、8、10 h;阴性对照组细胞用无菌DMEM基础培养液培养;每组3个重复。感染之后的细胞用无菌PBS洗3遍,加入1 mL Trizol将细胞从瓶壁上裂解下来,保存于-80 ℃备用。
1.6细胞总RNA提取及基因表达量检测
使用Trizol法抽提处理后细胞的总RNA,利用NANODROP2000紫外分光光度计与凝胶电泳检测总RNA浓度及提取质量,用TaKaRa反转录试剂盒获得cDNA,再通过荧光定量RT-PCR检测菌株不同处理时间后TRAPPC9、JAK2及IL6基因的mRNA表达量,各基因引物见表1。以内参基因GAPDH对目的基因表达量进行标准化,并利用2-ΔΔCt法计算基因相对表达量,用t-检验比较感染组与对照组间的基因表达差异。
2 结 果
2.1普通金葡菌菌株与MRSA菌株特异性分子鉴定
Nuc基因与MecA基因分别是金葡菌菌株和MRSA菌株的特异性基因。特异性PCR鉴定结果显示,从荷斯坦牛乳汁中分离纯化的菌株,分别扩增到特定片段大小的单一目的条带(Nuc及MecA基因扩增片段分别为279和310 bp,图1)。PCR产物测序结果也表明,两条扩增产物分别为Nuc与MecA基因,确定了本研究使用的两株菌株分别为金葡菌菌株(图1A)及MRSA菌株(图1B)。2.2Mac-T细胞培养状态
复苏后培养的牛乳腺上皮细胞(Mac-T)呈典型的上皮细胞形态:培养至24 h,可见许多分散生长的鹅卵石样的单个细胞(图2A);培养至36 h时,这些鹅卵石样细胞开始聚集生长(图2B);继续培养至48 h时,细胞在瓶底已达80%汇集,细胞呈均匀的多角形和鹅卵石样混合生长(图2C);此时的Mac-T细胞再培养两代即可用于后续感染试验。
表1PCR扩增基因引物信息
Table 1The information of gene primer by PCR

基因Gene序列(5'-3')Sequence产物长度/bpProduct退火温度/℃Tm文献ReferenceNucF:GCGATTGATGGTGATACGGTTR:AGCCAAGCCTTGACGAACTAAAGC27959[16]MecAF:GTAGAAATGACTGAACGTCCGATAAR:CCAATTCCACATTGTTTCGGTCTAA31058[16]TRAPPC9F:CTGCTCCGCTCGGTGAATGACR:GCTTTACCGCCAGTTCCACCA10460[9]JAK2F:TGAAGACCGAGACCCTACACR:CTGCAAGGATTTAAGGATTTC21260[10]IL-6F:GAACGAGTATGAGGGAAATCR:TCTCAAGGTTTCTCAGGATG13860GAPDHF:GGCGTGAACCACGAGAAGTATAAR:CCCTCCACGATGCCAAAGT11960[10]
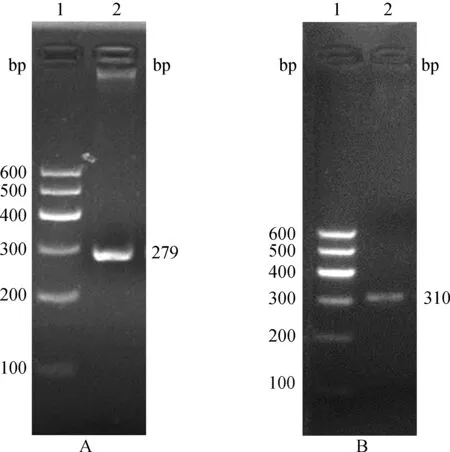
A:1.DNA相对分子质量标准;2.Nuc基因特异PCR产物;B:1.DNA相对分子质量标准;2.MecA基因特异PCR产物A:1.DL600 DNA marker;2.The specific PCR product of Nuc gene;B:1.DL600 DNA marker;2.The specific PCR product of MecA gene图1 特异性PCR鉴定Nuc与MecA基因Fig.1 The identification of Nuc and MecA genes by specific PCR
2.3菌株感染不同时间点牛TRAPPC9、JAK2及IL-6基因表达变化规律
为确定MRSA感染牛乳腺上皮细胞Mac-T后候选基因的表达变化规律,针对感染时间为3、6、8 以及10 h的MRSA处理组和金葡菌处理组Mac-T细胞,与无感染的对照组细胞进行对比,进行隐性乳房炎抗性候选基因TRAPPC9、JAK2及促炎因子基因IL-6的实时荧光定量RT-PCR(图3)。
针对TRAPPC9基因,比较MRSA菌株感染组与阴性对照组发现,其表达量在感染组细胞中随感染时间的延长呈下降趋势。统计学分析结果表明,与对照组相比,MRSA感染6 与10 h时TRAPPC9表达量显著下降(P<0.05,图3A)。对于JAK2基因,也发现其表达量随MRSA感染时间而下降,其中感染8与10 h时基因表达量显著低于对照组(P<0.05,图3B)。
金葡菌菌株感染与MRSA菌株感染结果相似,感染组Mac-T细胞的TRAPPC9、JAK2基因表达量均低于对照组,且当感染6、8 和10 h时,TRAP-PC9基因表达量极显著低于对照组(P<0.01,图3A);当感染6 和10 h时,JAK2基因表达量显著低于对照组(P<0.05,图3B)。与对照组相比,无论MRSA菌株感染组还是金葡菌菌株感染组,IL-6基因表达量均差异不显著,但可看出感染6 h时表达量较大(图3C)。
结果表明,MRSA菌株感染Mac-T细胞后,TRAPPC9与JAK2基因表达量均低于对照组,仅发现IL-6基因表达量略高于对照组,但差异不显著。金葡菌菌株感染后基因表达变化规律与MRSA相似。
2.4MRSA与普通金葡菌菌株感染Mac-T细胞的基因表达差异
为进一步确定MRSA菌株与金葡菌菌株感染细胞后的差异,将MRSA菌株与金葡菌菌株在6、8和10 h 3个具有显著性差异时间点的基因表达量进行比较(图4)。从图中可以看出,除了8 h时JAK2基因表达量在金葡菌处理组高于MRSA处理组,其余情况下3个基因的表达量均是MRSA处理组高于金葡菌处理组,且感染6 h时TRAPPC9基因表达量在两组间存在显著差异(P<0.05,图4A)。结合基因表达变化规律,即两株菌感染后TRAPPC9与JAK2基因表达量均低于未感染的对照组,提示MRSA感染后可能更不易被宿主细胞发现。
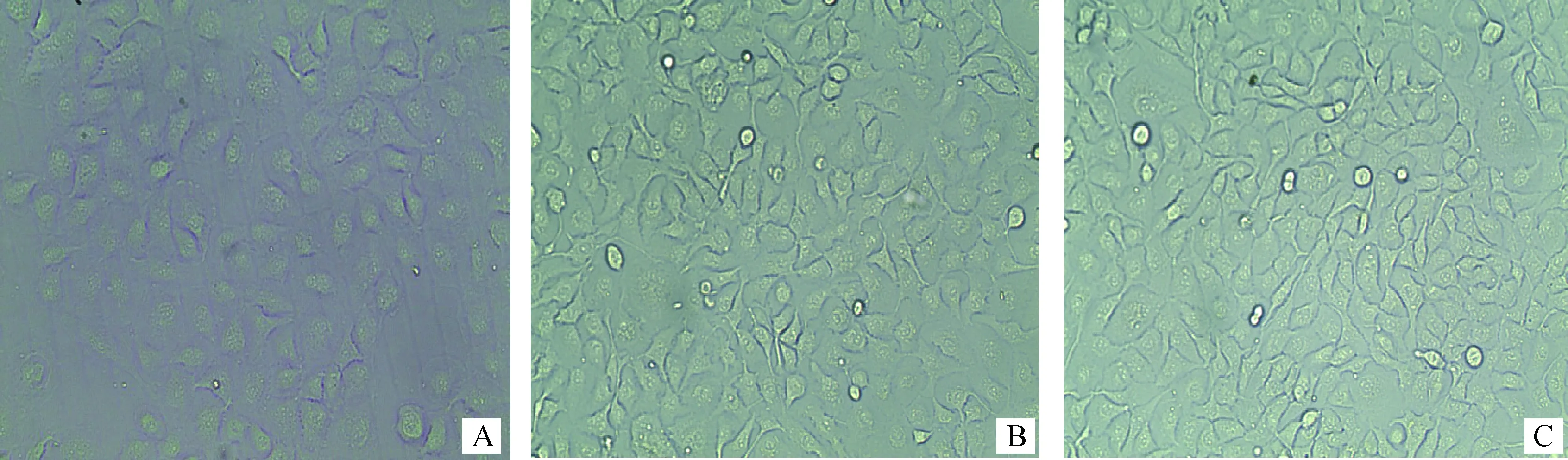
A.分散生长的鹅卵石状Mac-T细胞;B.聚集生长的鹅卵石状Mac-T细胞;C.多角形和鹅卵石状混合生长的Mac-T细胞A.The scattering growth of paving stone like Mac-T cells;B.The congregating growth of paving stone like Mac-T cells;C.The mixing growth of paving stone like and polygonous Mac-T cells图2 牛乳腺上皮细胞系Mac-T细胞形态 100×Fig.2 The morphology of bovine mammary epithelial cell lines (Mac-T cell) 100×
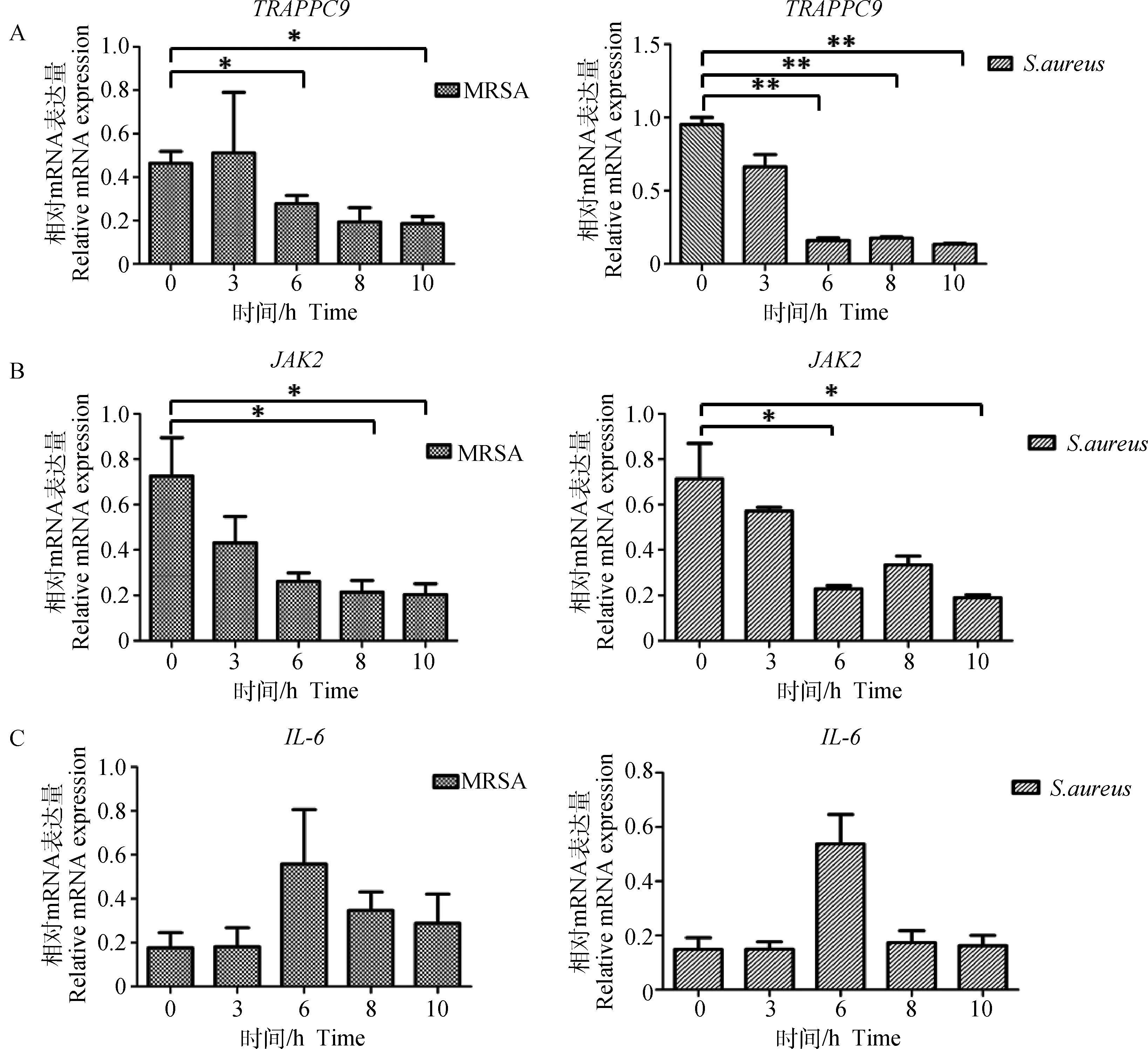
*.P<0.05;**.P<0.01图3 TRAPPC9、JAK2及IL-6基因在MRSA感染与金葡菌Mac-T细胞不同时间点的表达量Fig.3 The expression levels of TRAPPC9,JAK2 and IL-6 genes at different time points in Mac-T cells post-infected by MRSA and S.aureus

*.P<0.05图4 TRAPPC9、JAK2及IL-6基因在MRSA与金葡菌感染Mac-T细胞6(A)、8(B)和10 h(C)的表达量Fig.4 The expressions of TRAPPC9,JAK2 and IL-6 genes at 6 (A),8 (B) and 10 h(C) in Mac-T cells post-infected by MRSA and S.aureus
3 讨 论
奶牛乳腺上皮细胞既是泌乳细胞,又是重要的免疫调节和免疫效应细胞,在乳腺防御病原微生物感染中发挥重要作用[17]。本研究针对“超级菌”耐甲氧西林金黄色葡萄球菌(MRSA)感染引起的奶牛乳腺上皮细胞(Mac-T)炎症反应,通过与普通金葡菌感染的Mac-T细胞进行平行对比,检测并分析了课题组前期在中国荷斯坦牛群发现的奶牛隐性乳房炎抗性候选基因TRAPPC9[8]、JAK2[10]以及炎症指示因子IL-6[13]基因的表达情况,获得了MRSA菌株体外感染牛乳腺上皮细胞的关键分子标志物。
MRSA及普通金葡菌引起的奶牛乳房炎通常为不易发现、不易诊治的隐性乳房炎,尤其是MRSA菌因其较强耐药性,即使在人类医学中也难以攻克其引起的院内及社区感染[18]。据人们对中国北方地区6个省市9个奶牛场1 000余头中国荷斯坦牛乳汁中的细菌分离、纯化及分子鉴定发现,MRSA菌在其中一个牛场乳房炎牛中的检出率达7.2%[19],必须严加重视以防止其成为人畜交叉传染源。本研究利用其中一株MRSA 菌株体外感染Mac-T细胞,当感染6 h时,隐性乳房炎候选基因TRAPPC9表达量显著降低(P<0.05);感染8 h时,JAK2基因表达量显著降低(P<0.05),说明MRSA感染Mac-T细胞所引起的基因表达差异存在感染时间点的不同。此外,本研究用一株普通金葡菌感染Mac-T细胞,与MRSA感染不同的是,感染6 h时即引起JAK2表达量显著降低(P<0.05),提示MRSA菌感染更不易引起宿主细胞JAK2基因表达量的变化。
值得注意的是,TRAPPC9基因表达量在MRSA及金葡菌菌株感染6 h均呈现显著降低(P<0.05),提示该基因针对两种菌株感染的反应均较为及时且明显。TRAPPC9基因位于奶牛14号染色体上,编码转运蛋白颗粒复合体9蛋白(NIBP),即NIK及IKKβ结合蛋白,NIBP对NF-κB信号通路的激活具有调控作用[20]。NF-κB信号通路最早于1986年提出,其在乳房炎的发生发展中发挥重要调控作用[21]。本课题组研究发现,TRAPPC9基因不仅是荷斯坦牛隐性乳房炎的重要候选基因[8],且在金葡菌阳性牛外周血中的表达量也显著低于健康牛[22]。中国北方地区荷斯坦牛金葡菌感染率较高,所检测牛群金葡菌感染率达11.7%,其中临床乳房炎牛为10.8%,生产群泌乳牛更高为12.4%,须严加防范[19]。本研究检测到的TRAPPC9基因无论在奶牛乳腺上皮细胞,还是外周血中均呈现显著的基因表达量变化[22],可作为MRSA及金葡菌感染奶牛的关键分子标志物加以推广应用。
MRSA金葡菌及普通金葡菌具有免疫抑制及逃逸宿主免疫的特性,即抑制宿主免疫相关基因的表达或逃逸免疫细胞的识别,使宿主不能及时应对和抵抗菌体的感染[6,23]。研究发现,约40%的金葡菌感染隐性乳房炎奶牛其乳汁体细胞数低于20 万·mL-1[24],而小于20万·mL-1的体细胞数是目前广泛采用的健康牛标准[7]。本研究结果显示,MRSA菌株与普通金葡菌菌株感染Mac-T细胞6、8 及10 h后,TRAPPC9与JAK2基因表达量均明显低于对照组,提示TRAPPC9和JAK2可能与两株菌诱导的奶牛乳腺上皮细胞的炎症反应有关。但牛乳腺上皮细胞炎性反应受到MRSA菌株与普通金葡菌感染抑制的分子机理,除本研究的TRAPPC9、JAK2、IL-6基因外,还需对更多炎症相关基因的表达变化规律进行研究。
IL-6在免疫细胞的成熟、活化、增殖和免疫调节等一系列过程中均发挥重要作用,其中血液中IL-6浓度与患者炎症反应的程度呈正相关,可作为判断病情严重程度的灵敏指标[14-15]。然而在本研究中,未发现IL-6基因表达量与金葡菌感染有直接联系(图3C)。尽管当MRSA及普通金葡菌感染Mac-T细胞6 h时,IL-6基因表达量呈现升高趋势(未达统计学显著,P>0.05),但当感染8 h后,其表达量降低并与未感染细胞相近。究其原因,可能是IL-6主要由活化的单核/巨噬细胞产生,奶牛乳腺上皮细胞中的IL-6针对MRSA及金葡菌感染反应不敏感,不宜作为两种菌感染奶牛乳腺上皮细胞的分子标志物。
综上,本研究利用体外MRSA型金葡菌与普通金葡菌感染的牛乳腺上皮细胞模型,通过比较不同感染时间,获得TRAPPC9、JAK2和IL-6基因的表达变化规律,并从基因表达水平确定了MRSA菌感染牛乳腺上皮细胞的首选分子标志物是TRAPPC9基因,其次是JAK2基因。有关奶牛乳腺上皮细胞及免疫细胞先天性抵抗MRSA菌感染的分子机制,还有待针对两个基因进行深入的功能验证。
[1]BARBER M.Methicillin-resistantStaphylococci[J].JClinPathol,1961,14:385-393.
[2]FRANCIS J S,DOHERTY M C,LOPATIN U,et al.Severe community-onset pneumonia in healthy adults caused by methicillin-resistantStaphylococcusaureuscarrying the Panton-Valentine leukocidin genes[J].ClinInfectDis,2005,40(1):100-107.
[3]FERNANDES DOS SANTOS F,MENDONCA L C,REIS D R,et al.Presence of mecA-positive multidrug-resistantStaphylococcusepidermidisin bovine milk samples in Brazil[J].JDairySci,2015,99(2):1374-1382.
[4]GUNAWARDANA S,THILAKARATHNE D,ABEGUNAWARDANA I S,et al.Risk factors for bovine mastitis in the Central Province of Sri Lanka[J].TropAnimHealthProd,2014,46(7):1105-1112.
[5]WANG X,WANG X,WANG Y,et al.Antimicrobial resistance and toxin gene profiles ofStaphylococcusaureusstrains from Holstein milk[J].LettApplMicrobiol,2014,58(6):527-534.
[6]VILASACK T,DOMINIQUE M,OLAF S.Staphylococcusaureusdegrades neutrophil extracellular traps to promote immune cell death[J].Science,2013,342(6160):863-866.
[7]马裴裴,俞英,张沅,等.中国荷斯坦牛SCC变化规律及其与产奶性状之间的关系[J].畜牧兽医学报,2010,41(12):1529-1535.
MA P P,YU Y,ZHANG Y,et al.The distribution of SCC and its correlation with milk production traits in Chinese Holsteins[J].ActaVeterinariaetZootechnicaSinica,2010,41(12):1529-1535.(in Chinese)
[8]WANG X,MA P P,LIU J F,et al.Genome-wide association study in Chinese Holstein cows reveal two candidate genes for somatic cell score as an indicator for mastitis susceptibility[J].BMCGenet,2015,16(111):1-9.
[9]董易春,刘超,王晓,等.基于GWAS后分析策略研究TRAPPC9基因对奶牛产奶性状的遗传效应[J].畜牧兽医学报,2015,46(1):60-68.
DONG Y C,LIU C,WANG X,et al.Confirmaing the genetic effects of bovineTRAPPC9 on milk production traits based on post-GWAS strategies[J].ActaVeterinariaetZootechnicaSinica,2015,46(1):60-68.(in Chinese)
[10]USMAN T,YU Y,LIU C,et al.Genetic effects of single nucleotide polymorphisms in JAK2 and STAT5A genes on susceptibility of Chinese Holsteins to mastitis[J].MolBiolRep,2014,41(12):8293-8301.
[11]HU W H,PENDERGAST J S,MO X M,et al.NIBP,a novel NIK and IKKβ-binding protein that enhances NF-κB activation[J].JGenVirol,2005,280(32):29233-29241.
[12]KARIN M,GRETEN F R.NF-kappaB:linking inflammation and immunity to cancer development and progression[J].NatRevImmunol,2005,5(10):749-759.
[13]JAMES C,UGO V,CASADEVALL N,et al.A JAK2 mutation in myeloproliferative disorders:Pathogenesis and therapeutic and scientific prospects[J].TrendsMolMed,2005,11(12):546-554.
[14]YUDKIN J S,KUMARI M,HUMPHFIES S E,et al.Inflammation,obesity,stress and coronary heart disease:is interleukin-6 the link?[J].Atherosclerosis,2000,148(2):209-214.
[15]ROBERTO P F,LINDHOLM B,AXELSSON J,et al.Update on interleukin 6 and its role in chronic renal failure[J].NephrolDialTransplant,2003,18(6):1042-1045.
[16]ZHANG K,SPARLING J,CHOW B L,et al.New quadriplex PCR assay for detection of methicillin and mupirocin resistance and simultaneous discrimination ofStaphylococcusaureusfrom coagulase-negative staphylococci[J].JClinMicrobiol,2004,42(11):4947-4955.
[17]FOURNIER B,PHILPOTT D J.Recognition ofStaphylococcusaureusby the innate immune system[J].ClinMicrobiolRev,2005,18(3):521-540.
[18]KATAYAMA Y,ITO T,HIRAMATSU K.A new class of genetic element,Staphylococcus cassette chromosome mec,encodes methicillin resistance inStaphylococcusaureus[J].AntimicrobAgentsChemother,2000,44(6):1549-1555.
[19]王晓,俞英.中国北方奶牛金葡菌乳房炎感染现状及耐药性和流行类型研究进展[J].畜牧兽医学报,2015,46(9):1477-1488.
WANG X,YU Y.Infectious status of mastitis in dairy cattle induced byStaphylococcusaureusand its advances on epidemiological patterns and antimicrobial resistance in Northern China[J].ActaVeterinariaetZootechnicaSinica,2015,46(9):1477-1488.(in Chinese)
[20]SACHER M,KIM Y G,LAVIE A,et al.The TRAPP complex:insights into its architecture and function[J].Traffic,2008,9(12):2032-2042.
[21]王晓铄,俞英.表观遗传对炎症的调控机制及其在奶牛乳房炎抗病育种中的应用前景[J].遗传,2010,32(7):663-669.
WANG X S,YU Y.Regulation mechanisms of epigenetics on inflammation and its perspective on breeding for mastitis resistance in dairy cattle[J].Hereditas(Beijing),2010,32(7):663-669.(in Chinese)
[22]冯文,董易春,王晓,等.TRAPPC9基因对奶牛金葡菌乳房炎抗性性状的遗传效应[J].畜牧兽医学报,2016,47(2):276-283.
FENG W,DONG Y C,WANG X,et al.The genetic effect ofTRAPPC9 on mastitis resistance toS.aureusin Dairy cows[J].ActaVeterinariaetZootechnicaSinica,2016,47(2):276-283.(in Chinese)
[23]ROGHMANN M,TAYLOR K L,GUPTE A,et al.Epidemiology of capsular and surface polysaccharide in Staphylococcus aureus infections complicated by bacteraemia[J].JHospInfect,2005,59(1):27-32.
[24]JONES G M,PEARSON R E,CLABAUGH G A,et al.Relationships between somatic cell counts and milk production[J].JDairySci, 1984,67(8):1823-1831.
(编辑郭云雁)
Molecular Marker Study of Inflammatory Reaction in Bovine Mammary Epithelium Cell Line Induced by Methicillin-ResistantStaphylococcusaureus
SONG Min-yan1,WEI Yi-yuan1,2,Muhammad Zahoor Khan1,WANG Xin3,YU Ying1*
(1.KeyLaboratoryofAnimalGenetics,BreedingandReproduction,MinistryofAgriculture&NationalEngineeringLaboratoryforAnimalBreeding,CollegeofAnimalScienceandTechnology,ChinaAgriculturalUniversity,Beijing100193,China;2.ChongqingAnimalHusbandryTechniquesExtensionCenter,Chongqing401121,China;3.CollegeofFoodScienceandEngineering,NorthwestA&FUniversity,Yangling712100,China)
The aim of this study was to acquire key molecular marker related to inflammatory reaction of bovine mammary epithelium cells induced by Methicillin-resistantStaphylococcusaureus(MRSA).In this study,bovine mammary epithelium cell line (Mac-T) was infected with MRSAinvitroby compared with the cells treated byS.aureusas well the untreated cells.The expression levels of two candidate genes associated with subclinical mastitis ((trafficking protein particle complex 9(TRAPPC9),Janus Kinase 2(JAK2)) and one pro-inflammatory gene (interleukin 6,IL-6) were detected and compared among infected groups and non-infected group at different time points.Comparing with the untreated cells,the results showed that the mRNA expression level ofTRAPPC9 significantly decreased (P<0.05) in the Mac-T cells at 6 h post stimulation by MRSA,while that ofJAK2 significantly decreased (P<0.05) at 8 h;And the expression levels ofTRAPPC9 andJAK2 in the cells significantly decreased (P<0.05) at 6 h post infection byS.aureus.Compared withS.aureusstimuli,the expression levels ofTRAPPC9,JAK2 andIL-6 in the Mac-T cells were moderately higher at 6 and 10 h post infection by MRSA.Especially,the expression level ofTRAPPC9 was significantly higher in MRSA treated cells (P<0.05) compared toS.aureustreated cells at 6 h post infection.These results suggest that the genes expression changes in the Mac-T cells were similar after the infection of MRSA andS.aureus,while the gene expression changes ofJAK2 in the cells was delayed from MRSA infection compared toS.aureus.TRAPPC9 can be used as the preferred molecular marker for detecting MRSA andS.aureusinfection in bovine mammary epithelium cells.
Methicillin-resistantStaphylococcusaureus;bovine subclinical mastitis;mammary epithelium cell lines;TRAPPC9;JAK2
10.11843/j.issn.0366-6964.2016.10.007
2016-01-07
国家自然科学基金(31272420);国家奶牛产业技术体系专项资金(CARS-37-04B);“十二五”国家科技支撑项目(2011BAD28B02);教育部基本科研项目(2011JS006;Z109021306);长江学者与创新团队发展计划(IRT1191)
宋敏艳(1986-),女,陕西咸阳人,博士生,主要从事奶牛表观遗传调控与抗病机理研究,E-mail:songminyanjiandan@163.com
俞英,博士生导师,主要从事动物健康性状改良及表观遗传调控机制研究,E-mail:yuying@cau.edu.cn
S823;S813.3
A
0366-6964(2016)10-1995-08
