唾液中滥用物质分析的研究进展
2016-08-23冯雪伊沈敏陈航
冯雪伊,沈敏,陈航
(1.司法部司法鉴定科学技术研究所上海法医学重点实验室上海市司法鉴定专业技术服务平台,上海200063;2.中国刑事警察学院法化学系,辽宁沈阳110854)
鉴定综述Review
唾液中滥用物质分析的研究进展
冯雪伊1,2,沈敏1,陈航1
(1.司法部司法鉴定科学技术研究所上海法医学重点实验室上海市司法鉴定专业技术服务平台,上海200063;2.中国刑事警察学院法化学系,辽宁沈阳110854)
唾液作为非侵入性生物样品具有取材方便无创、感染机会少、适宜大规模人群采样等优势,是近年来法医毒物分析、临床药物监测、鉴定科学等领域的重要研究对象。国际上唾液样品已广泛应用于毒品滥用检测和监管等,与血、尿相比,唾液基底较为洁净,能降低基质效应产生的干扰,但是唾液采集也存在样少量微等困难,需要高效的前处理方法以及准确灵敏的分析技术。以唾液分析的方法学角度,对近十年来唾液中滥用物质的前处理手段和分析技术进行综述,同时对唾液检材的局限性及国内外唾液分析所面临的难点、热点予以讨论。
唾液;滥用物质;司法鉴定
口腔分泌液由唾液(唾液腺分泌)、口腔黏膜渗出液和龈沟液组成,由于唾液分泌途径较多,所占体积最大,在许多文献中,唾液指代为口腔分泌液,作为分析、检测的常用检材。早在20世纪中期,药物通过血液进入唾液的机理已有相关报道[1-3],血液中游离的药物分子通过上皮细胞进入唾液腺中,因此唾液中的药物浓度实际上反映的是血液中未与蛋白结合的药物浓度。Martin等[4]基于亨德森-哈塞尔巴尔赫方程创建了药物分子的唾液/血液浓度比(S/P)公式模型,酸碱性物质的S/P方程分别为:
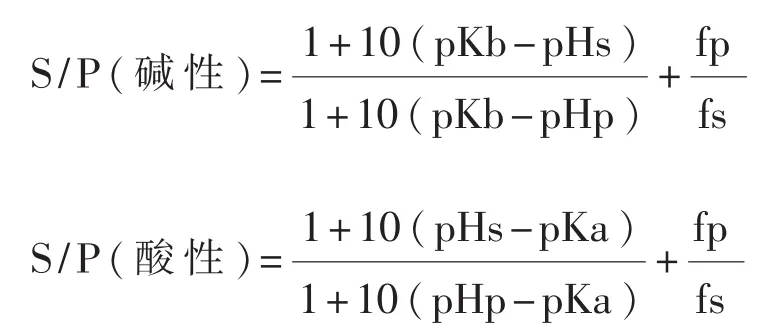
其中,S代表唾液中的药物浓度,P代表血液中的药物浓度,pKb为碱性物质的电离常数,pKa为酸性物质的电离常数,pHs和pHp分别为唾液和血液的pH值,fp和fs分别为血液和唾液中药物与蛋白的结合常数,唾液中的药物浓度与血液中的药物浓度有一定的相关性。国外文献报道了唾液分析在药后驾驶[5-7]、入职体检[8]等方面的应用优势,欧盟国家将唾液中的毒品检测结果作为毒驾的评价标准[9]。唾液检测窗口在12~24h内[10],能够真实反映当下机体的药物使用情况,在毒驾认定方面具有更高的参考价值。
此外,唾液样品还具有其他方面的优势,如采样方便无创,减少疾病感染机会,可通过现场监督防止掺假调换等[11],然而相比于血、尿样品,唾液往往样少量微,其所含药物及其代谢物的浓度相对较低,比尿液样品低约40倍[12],这些特点对唾液分析方法的灵敏度提出了更高的要求。同时,药物进入唾液腺前,必须通过三重屏障:毛细血管壁、基膜以及腺上皮细胞膜,唾液中药物含量的多少实际取决于其通过屏障的难易程度,由药物本身性质(如药物分子的pKa、药物的亲脂性、分子质量、空间构型、分子与蛋白结合度等)和个体差异性质(如膜厚、唾液流速、唾液pH、唾液结合蛋白以及唾液酶的含量等)决定[13]。这些变化参数均为唾液中的药物检测带来一定的困难和挑战。1992年,Schramm等[14]针对唾液作为滥用药物的分析检材的优势和缺陷进行了总结和讨论,所引文献较为早期;Bosker等[15]对2004—2009年之间唾液中滥用药物的分析文献进行了四方面的综述,包括样品收集方式、免疫筛选、仪器分析、相关研究与应用,阐述了唾液分析技术在五年间的快速发展;国内学者[16-17]对唾液中毒品检测的现状进行分析,并指出我国对毒驾的研究和管控方面缺乏重视。本文对近十年来的唾液分析的热点、难点进行综述,侧重于唾液中的滥用物质的检测手段、结果评估以及唾液检材的分析缺陷等方面,为更深入地研究唾液检材在法医毒物学、临床药学中的应用价值提供了参考。
1 唾液中滥用物质的研究现状
1.1苯丙胺类兴奋剂
唾液中苯丙胺类兴奋剂的分析方法有免疫法[18-19]、气相色谱-质谱(GC-MS)法[20-21]、液相色谱-荧光检测器[22](LC-FLD)、液相色谱-质谱[23]或串联质谱(LC-MS或LC-MS/MS)法等[24-25]。Laloup等[26]通过酶联免疫吸附法测定血液、唾液中的苯丙胺、MDMA 和MDA,Souza等[27]指出唾液的免疫分析法不适用于分析哌醋甲酯(利他能)、芬普雷司、安非拉酮这三种苯丙胺类结构的药物。
Pujadas等[28]建立了GC-MS方法同时分析唾液中包括苯丙胺类物质在内的30种精神活性药物,经固相萃取后,苯丙胺类物质用MSTFA乙酰化,检出限为2.9~6.9 ng/mL;另有用GC-MS法研究唾液样本中的7种苯丙胺类兴奋剂(苯丙胺AMP、甲基苯丙胺MAMP、亚甲二氧基甲基苯丙胺MDMA、亚甲基二氧基乙基苯丙胺MDEA、亚甲二氧基苯丙胺MDA、3-羟基-4-甲氧基甲基苯丙胺HMMA和3-羟基-4-甲氧基苯丙胺HMA)[29],第一次对MDMA的代谢物HMA进行分析,400μL唾液样品经固相萃取后,用HFFA衍生化,检出限在1.0~5.0 ng/mL范围内。
虽然GC-MS分析苯丙胺类物质的方法可靠、有效,然而为了降低样品高温损耗以及优化色谱行为,必须借助衍生化手段,前处理过程较为复杂。Liu等[30]建立了LC-MS/MS法分析唾液中的苯丙胺、甲基苯丙胺、吗啡、可待因、单乙酰吗啡和乙酰可待因,提取步骤主要为离心分离,检出限为1 ng/mL;Newmeyer等[31]使用一种Marfey衍生化试剂和LC-MS/MS分离分析血液和唾液中的L-和D-甲基苯丙胺以及其代谢物苯丙胺,手性分离可鉴别当事人摄入此类药物的途径是否合法,检出限为0.5 ng/mL,定量限低至1 ng/mL,低于GC-MS方法5~25倍。此外,Chen等[32]建立了一种微波辅助荧光标记-毛细管电泳法对6种苯丙胺类药物进行检测,唾液经液液萃取后,通过微波辅助加热大大缩短分析物荧光化时间;同时,荧光强度比传统衍生化过程有所增强,检出限最低可至0.05μg/mL,方法灵敏可靠。
1.2大麻类
大麻的主要活性成分是四氢大麻酚(THC),其代谢物四氢大麻酸(THC-COOH)在唾液中的浓度较低。Moore等[33]对被动吸入大麻烟的志愿者唾液进行THC、THC-COOH、大麻酚(CBN)、大麻二酚(CBD)检测分析,经酶联免疫法初筛后,THC、CBN 和CBD由GC-MS确证;THC-COOH由二维GC/ GC-MS测定。结果表明,所有唾液样品中的THC检测均为阳性,免疫法和GC-MS检出限分别为4ng/mL 和2 ng/mL,而THC-COOH均无法检出。在实际案件中,THC-COOH在唾液中的分析结果将成为区分主动吸食或者被动吸入大麻的关键性证据。Toennes等[5]对177例疑似毒驾者的血液和唾液样本进行GC-MS分析,研究血液及唾液的药物关联性,其中大麻阳性占结果的78%,THC及THC-COOH的血-唾液关联度分别为97%和92%。因此,在大麻检测方面唾液成为血液的替代检材具有极高的预估性和评判性。
Lendoiro等[34]首次运用分子印记固相萃取技术分析唾液和尿液中的THC和THC-COOH,500μL样品加入固相萃取柱,超声吸附30min,而后用丙酮:乙腈(v:v=3:1)洗脱,LC-MS/MS分析,唾液检出限和定量限分别为0.75 ng/mL和1 ng/mL,应用分子印记固相萃取处理实际唾液样品时,THC在20个样品中全部检出,THC-COOH均无法检出。Kneisel等[35]运用LC/ESI-MS/MS定量分析唾液中28种合成大麻素,检出限为0.02~0.04 ng/mL。不同时间段采集同一志愿者的唾液和血液样品进行对比分析,结果表明血液中合成大麻素转移进入唾液的速率极低,浓度极小,而许多案件中唾液呈大麻阳性的结果是由口服吸食造成的口腔污染所引起。Kneisel等还对合成大麻素类物质在唾液中的检测窗口时长进行分析,平均检测时长为6~28h,大部分物质在30min时间节点后的检测浓度下降至初期的30%,因此唾液中的合成大麻素类物质的分析可作为评判近期是否吸食的关键性证据。Fabritius等[36]比较了唾液样品的前处理方法,使用液液提取和固相萃取分别对唾液中的8种大麻类物质进行分析,液液提取检出限和定量限均低于固相萃取法。
1.3阿片类
唾液中阿片类物质的文献报道早期常侧重于与其他生物检材的比较分析,探讨了唾液在成为替代检材、判别摄毒及口服可食用阿片类植物的案件性质、短时服用证据等方面的价值性,2005年以后唾液中阿片类物质的研究重点趋向于色谱-质谱联用同时测定包括阿片类物质在内的十几种甚至几十种精神活性物质。Heiskanen等[37]对使用阿片类镇痛治疗的患癌病人的唾液及血液中的吗啡、羟考酮和芬太尼进行检测分析,考察唾液与血液的药物浓度比(S/P),定量限为0.5~1.0 ng/mL;结果表明,三种目标物在唾液中的浓度均大于血液,这是由于药物分子呈弱碱性而较容易进入偏弱酸性的唾液,实验证明了唾液能够替代血液检测其中的吗啡及芬太尼,其结果可为患癌病人接受阿片治疗监测提供分析依据。Cone等[38]对2004—2006年之间收集的8 679个呈滥用药物阳性的唾液样本进行确证分析,阿片类滥用者的唾液分析中,吗啡、可待因以及6-单乙酰吗啡为最常见分析物,其次是海洛因及6-乙酰可待因。基于大规模样本的药物分析能对现有社会上的流行滥用药物进行检测频率、原药及代谢物模式、浓度数据方面的总结、归纳,有助于实际案件的借鉴分析及快速认定,整体上把握社会上的滥用药物的流行化趋势。
Tuyay等[39]指出,服用羟考酮、氢可酮或可待因后,其在人体中的去甲代谢物(去甲羟考酮、去甲氢可酮和去甲可待因)在唾液中的浓度较高,而另外三种常见代谢物,即羟基吗啡酮、氢吗啡酮和吗啡在唾液中无法检出。因此,将去甲代谢物列为唾液鉴定的目标物有助于准确分析判断羟考酮、氢可酮或可待因的摄入与否。Enders等[40]使用直接稀释进样法,快速检测唾液中8种阿片类物质及其代谢物,包括可待因、吗啡、氢可酮、氢吗啡酮、去甲氢可酮、羟考酮、去甲羟考酮和羟基吗啡酮,样品仅需100μL,稀释10倍后直接进样,LC-MS分析,分析时长为5.1min,免去了前处理过程中繁琐的净化和浓缩步骤,大大提高了检测效率。
1.4可卡因类兴奋剂
可卡因是古柯叶的主要有效成分,由于吸食后能产生欢愉和兴奋感,因此常被人为滥用。可卡因在血液中会迅速代谢成苯甲酰爱康宁(BE)和爱康宁甲酯(EME)。Scheidweiler等[41]对皮下注射可卡因的志愿者进行唾液分析和药代动力学研究,首次给出单次摄入可卡因后唾液中的峰值时间。注射可卡因后,48 h内定时采集1mL唾液样本,固相萃取并衍生化后,进行GC-MS分析。结果表明,唾液中可卡因的最初检测窗口Tfirst为0.08~0.32 h,半衰期为1.1~3.8 h,峰值时间Tmax出现在0.2~2.1 h,而BE和EME的Tfirst为0.08~1.0 h,其半衰期和Tmax远大于可卡因,峰值浓度Cmax仅为可卡因的10%,唾液中的BE、EME和可卡因的比值随检测时间的增长而迅速增大,表明可卡因在人体内迅速代谢。此外,Scheidweiler等还指出,同一个体的唾液和血液中的三种目标物有相关性,但不排除个体差异性的因素而导致S/P值的不稳定性。
LC-MS/MS检测可卡因类兴奋剂具有高效、灵敏、专属性强等特点。Fritch等[42]建立了LC-MS/MS定性定量分析唾液中可卡因类、苯丙胺类、阿片类和苯环己哌啶的方法,400μL唾液样品稀释后进行固相萃取,提取回收率达91.2%,可卡因检出限为0.4ng/mL,定量限为0.8 ng/mL;Concheiro等[43]使用LC-MS/MS同时检测唾液中可卡因、阿片类、尼古丁及其代谢物,可卡因、BE、EME以及脱水芽子碱甲酯(AEME)的检出限为0.4~0.8 ng/mL,定量限为0.5~1 ng/mL,唾液量只需250μL,然而方法专属性中3-羟基-4-甲氧基苯丙胺对AEME有干扰。
一种新型的现场快速检测技术[44]——接触式喷雾质谱(Touch spraymass spectrometry,TS-MS)法已应用于唾液中可卡因类、阿片类、氯胺酮和苯丙胺类物质的定性和半定量分析。现场检测技术要求分析快速、准确度高,更侧重于方法的定性分析,TSMS法使用台式质谱仪,比免疫法具有更高的选择性、专属性和灵敏度。报道使用医用棉签吸取口腔唾液,此法同时作为采样工具和离子化底物,简化了样品前处理步骤。因此,这种一步式的筛选、确证分析技术对于现场快速检测的需求具有潜在的应用价值。
1.5安眠镇静类
1.5.1巴比妥类
巴比妥类药物在临床上用于抗癫痫以及麻醉诱导等,长期使用会形成生理和心理依赖;由于人体的耐受性,治疗剂量和致死剂量间的差距逐渐缩小,此类药物的滥用会对人体造成极大伤害。Dean等[45]人分析单次摄入巴比妥类物质后,不同时间段内唾液、血液和尿液中的药物分布情况。口服异丁巴比妥、苯巴比妥以及司可巴比妥钠后,分别于-1(服药前1 h)~36 h和48~52 h采集唾液及血、尿,唾液进行LC-MS/MS分析,定量限为8 ng/mL;血、尿进行GCMS分析,定量限为100 ng/mL。结果表明,唾液和血液中的三种目标物Tfirst大于尿液;48~52 h内,异丁巴比妥、苯巴比妥在所有样品中均可检出,司可巴比妥均无法检出。1~48h内,异戊巴比妥和苯巴比妥的S/P值保持稳定状态,证明了在分析巴比妥类药物方面,唾液作为血液和尿液替代检材的潜在优势。
1.5.2苯二氮卓类
苯二氮卓类物质是目前世界上应用最为广泛的安眠镇静药,临床上用于治疗抗焦虑、抗痉挛、抗失眠以及抗精神失常等,也常用作及肌肉松弛剂,具有较好的疗效。然而长期使用该药物可出现耐受性和依赖性,过量使用易引起中毒乃至死亡。由于苯二氮卓类药物容易得到,使用剂量小,体内代谢快,往往成为不法分子违法犯罪的主要辅助药物。国内外报道此类药物的滥用多涉及药后驾驶、自杀、麻醉抢劫、强奸等[46-49],血液、尿液为此类案件的常规检材。尿液检测多以代谢物为主,检测时限长,唾液检测主要为药物原体,通过分析唾液中的药物可以监测个体近期是否有药物服用情况。
苯二氮卓类物质众多,当涉及分析范围宽、化学异质性范围广、痕量检测时,LC-MS(/MS)具有明显的优势。George等[50]建立LC-MS/MS法同时测定唾液中14种苯二氮卓类物质,使用固相萃取,检出限为0.02~0.5 ng/mL,定量限为0.1~1 ng/mL,方法灵敏可靠,成功应用于41例唾液免疫筛选检测苯二氮卓类物质阳性的确证分析。类似地,Moore等[51]使用固相萃取LC-MS/MS分析唾液中14种苯二氮卓类物质,乙酸乙酯和2%氨水洗脱,定量限为0.5~1ng/mL,方法回收率均大于82.82%,结果表明唾液中的药物原体浓度远大于代谢物浓度。Melanson等[52]指出,7-氨基氯硝西泮比原体氯硝西泮更适合作为唾液中此类药物监测分析的目标物。对100份氯硝西泮及其代谢物7-氨基氯硝西泮阳性患者的唾液进行LC-MS/MS分析,其中91%检出7-氨基氯硝西泮,而44%检出氯硝西泮,代谢物的唾液浓度为原体的2~4倍。由于氯硝西泮分子为弱酸性,7位上的硝基还原成氨基后使得7-氨基氯硝西泮的碱性大于原体,而更易于进入弱酸性的唾液中,因此分析唾液中苯二氮卓类物质的代谢物有助于实际检测中排查原体的假阴性结果。
1.6其他
一些其他药物(如抗精神药物、其他安眠镇静药等)的唾液分析,有助于替代血液、尿液分析应用于大规模人群以及儿童、残障人士、创伤愈合障碍等人群的采样分析。DiCorcia等[53]使用UPLC-MS/MS快速分析唾液中44种道路现场检测中的常见药物(阿米替林、卡马西平、唑吡坦、氯胺酮、美沙酮、奥氮平、喹硫平、曲马多、文拉法辛、芬太尼及其代谢物等),前处理步骤简单快速,沉淀蛋白后离心,上清液直接进样分析。检出限范围为0.02~2.98ng/mL,定量限为1~10 ng/mL,方法高效灵敏,满足实际唾液样品的检测需求。Fisher等[54]比较分析了血浆、血清、全血以及唾液中的抗精神失常药物(氨磺必利、阿立哌唑、脱氢阿立哌唑、氯氮平、去甲氯氮平、奥氮平、喹硫平、利培酮、9-羟基利培酮以及舒必利),乙酸丁酯:丁醇(v:v=9:1)提取后进行LC-MS/MS分析。结果显示,回收率范围为16%~107%,同一目标物在不同基质中的浓度呈相关变化,仅有脱氢阿立哌唑、去甲氯氮平以及奥氮平的唾液浓度与血液浓度无相关性。与血液分析相比,唾液分析对此类药物中的个别目标物还具有一定的局限性。
2 唾液分析中存在的干扰因素
2.1唾液采集方式对唾液分析产生的影响
健康成年人每天能够产生约500~1 500mL唾液量,但在很多情况下,受年龄、生理状况、遗传因素、口腔疾病等影响,通过个人自然流出唾液的非刺激方式(吐口水)获得的唾液采集量往往不足(<1mL),且容易携带食物残渣、口腔黏膜等杂质。此外,长期抽烟或有药物摄入者容易产生口腔干燥症,这是由于药物引起交感神经活跃从而降低了唾液分泌率,需要通过刺激方式使唾液腺分泌量增加,短时间内获得更多样品。刺激方式主要有味觉刺激,如口含柠檬酸盐、酸性糖果,或者通过咀嚼石蜡、橡皮等的机械式刺激。不同的刺激方式会影响唾液的粘蛋白含量以及pH值,从而影响血液中的药物进入唾液的难易程度。由于健康人体的唾液pH比血液pH低,呈弱酸性(pH 6.2~7.4),因此脂溶性的碱性药物比酸性药物更容易从血液扩散进入唾液。碱性药物如苯丙胺类以及阿片类在唾液中的浓度高于血液,而酸性药物如巴比妥类的唾液浓度低于血液。酸性味觉刺激会使唾液的pH值更趋向于中性,降低弱碱性药物在唾液中的电离程度,阻碍其梯度扩散[55]。
Eric等[56]比较了刺激性和非刺激性的两种采集方式下,美沙酮的S/P差异。14位接受美沙酮治疗患者的唾液两份,分别通过非刺激性的收集装置以及口含柠檬酸自然流出的方式收集;同时收集血液样品,使用UPLC分析。结果显示,非刺激性方式表现出更高的唾液-血液的药物浓度关联性,其S/P值(0.9)高于利用酸刺激方式的S/P值(0.1~0.5)。酸刺激后会产生较多的碳酸氢盐,使唾液pH值升高从而降低弱碱性药物渗透唾液腺的几率。因此,唾液的pH值越接近药物的pKa值,血液中的游离药物进入唾液的几率则越小。此外,Eric等还研究了美沙酮的药物浓度随时间的变化规律,指出食物的摄入有利于增加美沙酮在唾液中的浓度。
另有文献报道,非刺激性方式产生的唾液中可待因浓度为刺激性方式的2~3倍[57],甲基苯丙胺为2~4倍[58],可卡因约为5倍[55]。
2.2唾液收集装置对唾液分析产生的影响
除了使唾液自然流出的收集方式之外,市面上有许多不同型号的唾液收集装置。由于收集装置的唾液吸收元件、装置缓冲液、装置防腐剂的种类各异,其对唾液中的药物浓度会造成一定影响。Lund等[59]发现Intercept装置较StatSure Saliva Sample装置受基质干扰较小,更适宜分析唾液中的32种滥用药物及其代谢物。另有文献[60]报道了两种收集装置Saliva Collection System(SCS)和Quantisal对12份唾液中的可待因检测产生的差异性影响。经GC-MS分析后发现,两种装置的唾液与血液的皮尔森相关系数(P=0.005)不同,SCS大于Quantisal,表明使用SCS装置收集时,可待因的唾液与血液关联度好,S/P值变化差异小。唾液收集装置的最大缺点是唾液收集体积的非固定性和不确定性,尤其影响药物在唾液装置上的回收率。Desrosiers等[61]对StatSure Saliva Sample和Oral-Eze两种装置对唾液中大麻类物质的分析影响进行了研究。通过GC/MS分析,表明Oral-Eze唾液样品中的THC-COOH和THC浓度高于StatSure样品。甚至通过非装置收集方式比装置收集方式得到的THC检测含量要高[62]。Gjerde等[63]指出Intercept装置的小体积唾液量比StatSure唾液量中的药物分析浓度高。类似还有文献[64]指出Salivette装置对于唾液中的THC具有较差的回收率,然而其适用于分析唾液中的可待因;Quantisal[65]和Oral-Eze[66]对唾液中的THC表现出良好的储存稳定性和较高的回收率。了解常用收集装置对唾液分析的影响有助于在实际交通安全检测及药物监测中分析特定目标物时选用适宜的收集装置。常见的唾液收集装置见表1。
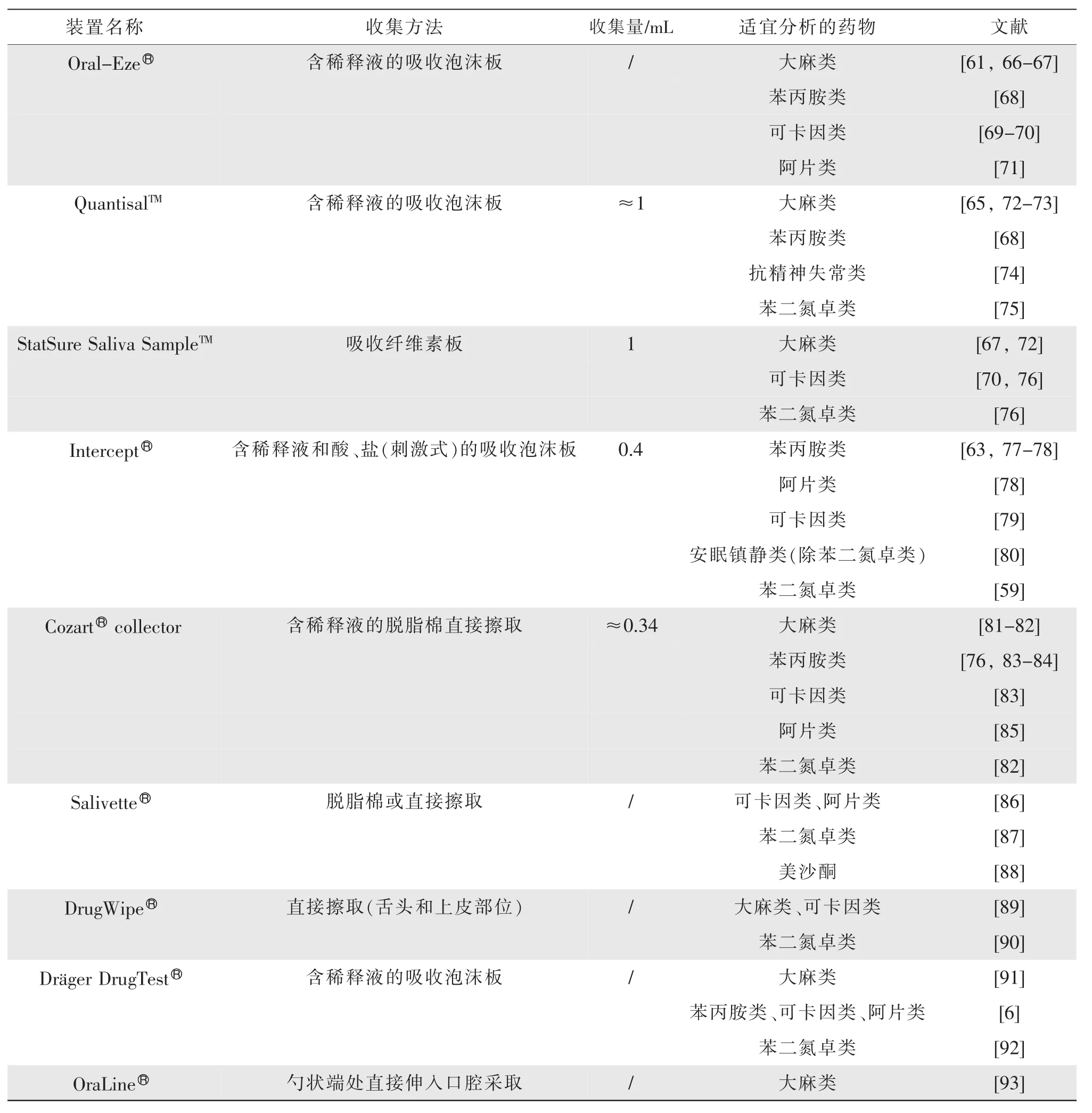
表1 常见不同型号的唾液收集装置及其收集方法
2.3进食对唾液分析产生的影响
食物和饮料的摄入会改变口腔环境,影响唾液的分泌状态,其在一定程度上会影响唾液中药物的分析结果。国外学者[94]分析进食后志愿者的唾液中所含苯丙胺类、美沙酮、阿片类和可卡因的情况,样品经两种唾液免疫检测法Concateno Certus和Orasure Intercept筛选呈阳性后进行GC-MS或LC-MS/ MS确证分析。结果表明,实验中可能的干扰性食物、饮料及外源性物质——咖啡、可乐、果汁、橙子、辣酱以及牙膏对两种免疫筛选方法的影响结果截然相反。Orasure法检出所有目标物,表明进食对唾液检测无干扰;而Concateno法对所有目标物均无法检出。此外,实验还证明了食醋的摄入会使免疫检测的分析窗口延长。因此在实际案件中,仅使用免疫法分析唾液中的滥用物质,无法排除进食对唾液分析的干扰,必须借助仪器分析方法进一步确证。
2.4其他干扰性因素
唾液能够成为血液分析的替代检材,最关键的前提是两者中的游离药物浓度具有关联性,只有在这种情况下,唾液的药物浓度值才能最真实地反映个体的受药影响程度。其中,药物摄入途径的差异是干扰唾液分析的首要因素之一,如吸烟、烫吸以及口服方式易造成药物在口腔黏膜中沉积,从而使得S/P值的测定偏高。Jenkins等[95]研究吸服和静脉注射两种不同的摄入途径对唾液及血液中的海洛因和可卡因的浓度分布影响。吸服和静脉注射海洛因的两种途径下唾液Tfirst均为2min,然而两种途径下的唾液Tmax和Cmax均不同,吸服方式较静脉注射延迟0~3min,前者浓度为后者的118~3430倍;吸服可卡因后的唾液Cmax为静脉注射的8~1 180倍左右,而吸服后的血液Cmax稍小于静脉注射方式。同时,研究表明吸服方式会延长海洛因唾液浓度的检测时间,而血液窗口不变;静脉注射方式下,唾液和血液的检测窗口没有明显差异性。实际案件分析中应更加注重检测对象的摄药情况,询问其摄入时间、剂量,尤其是摄入方式,合理地进行唾液分析结果的评价。
被动吸入是唾液分析的另一个研究热点。大麻是全球范围内滥用频率最高的毒品,吸食过程中常产生大麻烟雾,被动吸入大麻常易造成健康人体的唾液、尿液假阳性的情况。Niedbala等[96]提出健康人体唾液中的THC阳性可能是由于采集环境的污染(室内采集)造成,并通过实验进行证实。然而Moore等[33]在相对干净的环境里检测经大麻烟暴露后的健康人体唾液中的THC,结果仍能检出。Herrmann[97]探讨了大麻烟剂量和通风状况对被动吸入程度的影响,结果表明在一定程度上,大麻烟剂量越大,通风状况越差,THC的唾液、血液浓度相对较高,个体明显表现出眼睛和黏膜刺激感。
3 结语
综上所述,唾液作为生物检材在样品收集分析、处理和应用等方面具有一定的优势。目前对唾液检材的研究都集中在唾液和血液中药物浓度的关联性分析、唾液分析的影响因素等。但唾液的检测窗口短、收集体积量不足、弱酸性药物及代谢物含量低等缺陷也需要引起关注。唾液检材应用于毒驾分析已在许多发达国家普及并且检测技术日趋成熟。随着研究方法不断改进,检测技术不断提升,唾液分析将在我国药物监测、毒驾检测、吸毒认定等多个领域得以应用与普及。
[1]Borzelleca J F,Doyle C H.Excretion of Drugs in Saliva.Salicylate,Barbiturate,Sulfanilamide[J].Journal of Oral Therapeutics&Pharmacology,1966,3(2):104-111.
[2]Burgen A S.The Secretion of Non-Electrolytes in the Parotid Saliva[J].JCell Physiol,1956,48(1):113-138.
[3]Vining R,McGinley R A.Immunoassays of Steroids in Saliva:Transport of Steroids from Blood to Saliva[C].Cardiff:Alpha Omega Publishing Limited,1982.
[4]Matin S B,Wan S H,Karam JH.Pharmacokinetics of Tolbutamide:Prediction by Concentration in Saliva[J].Clin Pharmacol Ther,1974,16(6):1052-1058.
[5]Toennes SW,Steinmeyer S,Maurer H J,et al.Screening for Drugs of Abuse in Oral Fluid--Correlation of Analysis Results with Serum in Forensic Cases[J].JAnal Toxicol,2005,29(1):22-27.
[6]Toennes SW,Kauert G S,Moeller M R.Driving under the Influence of Drugs-Evaluation of Analytical Data of Drugs in Oral Fluid,Serum and Urine,and Correlation with Impairment Symptoms[J].Forensic Sci Int,2005,152 (2-3):149-155.
[7]Kintz P,Cirimele V,Ludes B.Detection of Cannabis in Oral Fluid(Saliva)and Forehead Wipes(Sweat)from Impaired Drivers[J].JAnal Toxicol,2000,24(7):557-561.
[8]George S.A Snapshot of Workplace Drug Testing in the UK[J].OccupationalMedicine,2005,55(1):69-71.
[9]Verstraete A.Rosita:Roadside Testing Assessment.ROSITA Contract No GGVII PL98-3032[K].Belgium:Ghent University,2000:1-397.
[10]Cone E J.Saliva Testing for Drugs of Abuse[J].Ann NY A-cad Sci,1993,694(6444):91-127.
[11]De Giovanni N,Fucci N.The State of the Art on the Use of Oral Fluid as Alternative Specimen in Forensic Toxicology[J].Curr Pharm Anal,2008,4(4):258-273.
[12]Vindenes V,Yttredal B,Oiestad E L,et al.Oral Fluid is a Viable Alternative for Monitoring Drug Abuse:Detection of Drugs in Oral Fluid by Liquid Chromatography-Tandem Mass Spectrometry and Comparison to the Results from Urine Samples from Patients Treated with Methadone or Buprenorphine[J].JAnal Toxicol,2011,35(1):32-39.
[13]Landon J,Mahmod S.Distribution of Drugs between Blood and Saliva[A]//Read G F,Riad-Fahmy D,Walker R F,Griffiths K.Immunoassaysof Steroids in Saliva:Proceedings of the Ninth TenovusWorkshop[C].Cardiff:Alpha Omega Publishing Limited,1982:47-55.
[14]Schramm W,Smith R H,Craig P A,et al.Drugs of Abuse in Saliva:A Review[J].JAnal Toxicol,1992,16 (1):1-9.
[15]BoskerW M,Huestis M A.Oral Fluid Testing for Drugs of Abuse[J].Clin Chem,2009,55(11):1910-1931.
[16]陈跃,于忠山,朱军,等.唾液检材在毒品检测中的应用[J].中国法医学杂志,2013,28(1):26-29.
[17]申文静,朱军,刘耀.人唾液中苯丙胺类药物检测方法进展[J].中国法医学杂志,2007,22(3):179-181.
[18]Cooper G,Wilson L,Reid C,et al.Validation of the Cozart?Amphetamine Microplate EIA for the Analysis of Amphetamines in Oral Fluid[J].Forensic Sci Int,2006,159(2):104-112.
[19]Crooks C R,Brown S.Roche DAT Immunoassay:Sensitivity and Specificity Testing for Amphetamines,Cocaine,and Opiates in Oral Fluid[J].JAnal Toxicol,2010,34(2):103-109.
[20]Peters F T,Samyn N,Kraemer T,et al.Negative-Ion Chemical Ionization Gas Chromatography-Mass Spectrometry Assay for Enantioselective Measurement of Amphetamines in Oral Fluid:Application to a Controlled Study with MDMA and Driving under the Influence Cases[J].Clin Chem,2007,53(4):702-710.
[21]Souza D Z,Boehl PO,Comiran E,et al.Determination of Amphetamine-Type Stimulants in Oral Fluid by Solid-Phase Microextraction and Gas Chromatography-Mass Spectrometry[J].Anal Chim Acta,2011,696(1):67-76.
[22]Concheiro M,De Castro A,Quintelaó,et al.Determination of MDMA,MDA,MDEA and MBDB in Oral Fluid Using High Performance Liquid Chromatography with Native Fluorescence Detection[J].Forensic Sci Int,2005,150 (2):221-226.
[23]Concheiro M,De Castro A,Quintelaó,etal.Confirmation by LC-MS of Drugs in Oral Fluid Obtained from Roadside Testing[J].Forensic Sci Int,2007,170(2):156-162.
[24]Van Eeckhaut A,Lanckmans K,Sarre S,et al.Validation of Bioanalytical LC-MS/MS Assays:Evaluation of Matrix Effects[J].JChromatogr B,2009,877(23):2198-2207.
[25]Liu H-C,Lee H-T,Hsu Y-C,et al.Direct Injection LCMS-MSAnalysis ofOpiates,Methamphetamine,Buprenorphine,Methadone and their Metabolites in Oral Fluid from Substitution Therapy Patients[J].JAnal Toxicol,2015,39 (6):472-480.
[26]Laloup M,Tilman G,Maes V,et al.Validation of an Elisa-Based Screening Assay for the Detection of Amphetamine,MADA and MDA in Blood and Oral Fluid[J].Forensic Sci Int,2005,153(1):29-37.
[27]Souza D Z,Boehl P O,Comiran E,et al.Which Amphetamine-Type Stimulants can be Detected by Oral Fluid Immunoassays?[J].Ther Drug Monit,2012,34(1):98-109.
[28]Pujadas M,Pichini S,Civit E,et al.A Simple and Reliable Procedure for the Determination of Psychoactive Drugs in Oral Fluid by Gas Chromatography-Mass Spectrometry[J].JPharm Biomed Anal,2007,44(2):594-601.
[29]Scheidweiler K B,Huestis M A.A Validated Gas Chromatographic-Electron Impact Ionization Mass Spectrometric Method for Methylenedioxymethamphetamine(MDMA),Methamphetamine and Metabolites in Oral Fluid[J].J Chromatogr B,2006,835(1-2):90-99.
[30]Liu H-C,Wang Y-S,Liu R-H,et al.The Quantitative Determination of Opiates and Amphetamines in Oral Fluid by Direct Injection Liquid Chromatography-Tandem Mass Spectrometry[J].Forensic Science Journal,2015,14(1):47-57.
[31]Newmeyer M N,Concheiro M,Huestis M A.Rapid Quantitative Chiral Amphetamines Liquid Chromatography-Tandem Mass Spectrometry:Method in Plasma and Oral Fluid with a Cost-Effective Chiral Derivatizing Reagent[J].J Chromatogr A,2014,(1358):68-74.
[32]Chen K-F,Lee H,Liu J-T,et al.A Microwave-Assisted Fluorescent Labeling Method for the Separation and Detection of Amphetamine-Like Designer Drugs by Capillary Electrophoresis[J].Forensic Sci Int,2013,228(1):95-99.
[33]Moore C,Coulter C,Uges D,et al.Cannabinoids in Oral Fluid Following Passive Exposure to Marijuana Smoke[J].Forensic Sci Int,2011,212(1-3):227-230.
[34]Lendoiro E,De Castro A,Fernández-Vega H,et al. Molecularly Imprinted Polymer for Selective Determination ofδ9-Tetrahydrocannabinol and 11-nor-δ9-Tetrahydrocannabinol Carboxylic Acid Using LC-MS/MS in Urine and Oral Fluid[J].Anal Bioanal Chem,2014,406(15):3589-3597.
[35]Kneisel S,Speck M,Moosmann B,et al.LC/ESI-MS/MS Method for Quantification of 28 Synthetic Cannabinoids in Neat Oral Fluid and its Application to Preliminary Studies on their Detection Windows[J].Anal Bioanal Chem,2013,405(14):4691-4706.
[36]Fabritius M,Staub C,Mangin P,et al.Analysis of Cannabinoids in Oral Fluid by Liquid Chromatography-Tandem Mass Spectrometry[J].Forensic Toxicol,2013,31 (1):151-163.
[37]Heiskanen T,Langel K,Gunnar T,et al.Opioid Concentrations in Oral Fluid and Plasma in Cancer Patients with Pain[J].JPain Symptom Manag,2015,50(4):524-532.
[38]Cone E J,Clarke J,Tsanaclis L.Prevalence and Disposition of Drugs of Abuse and Opioid Treatment Drugs in Oral Fluid[J].JAnal Toxicol,2007,31(8):424-433.
[39]Tuyay J,Coulter C,Rodrigues W,et al.Disposition of Opioids in Oral Fluid:Importance of Chromatography and Mass Spectral Transitions in LC-MS/MS[J].Drug Test Anal,2012,4(6):395-401.
[40]Enders JR,McIntire G L.A Dilute-and-Shoot LC-MS Method for Quantitating Opioids in Oral Fluid[J].J Anal Toxicol,2015,39(8):662-667.
[41]Scheidweiler K B,Spargo E A K,Kelly T L,et al.Pharmacokinetics of Cocaine and Metabolites in Human Oral Fluid and Correlation with Plasma Concentrations Following Controlled Administration[J].Ther Drug Monit,2010,32 (5):628-637.
[42]Fritch D,Blum K S.Identification and Quantitation of Amphetamines,Cocaine,Opiates,and Phencyclidine in Oral Fluid by Liquid Chromatography-Tandem Mass Spectrometry[J].JAnal Toxicol,2009,33(9):569-577.
[43]Concheiro M,Shakleya D M,Huestis M A.High-Throughput Simultaneous Analysis of Buprenorphine,Methadone,Cocaine,Opiates,Nicotine,and Metabolites in Oral Fluid by Liquid Chromatography Tandem Mass Spectrometry[J].Anal Bioanal Chem,2010,398(2):915-924.
[44]Pirro V,Jarmusch A K,Vincenti M,et al.Direct Drug Analysis from Oral Fluid Using Medical Swab Touch Spray Mass Spectrometry[J].AnalChim Acta,2015,(861):47-54.[45]Dean F,Kristen B,Sheena N,et al.Barbiturate Detection in Oral Fluid,Plasma,and Urine[J].ChemPhysChem,2009,10(18):3239-3248.
[46]Drummer O H,Gerostamoulos J,Batziris H,et al.The Involvement of Drugs in Drivers of Motor Vehicles Killed in Australian Road Traffic Crashes[J].Accid Anal Prev,2004,36(2):239-248.
[47]Steentoft A,Linnet K.Blood Concentrations of Clonazepam and 7-Aminoclonazepam in Forensic Cases in Denmark for the Period 2002-2007[J].Forensic Sci Int,2009,184(1):74-79.
[48]Lekka N P,Paschalis C,Beratis S.Suicide Attempts in High-Dose Benzodiazepine Users[J].Compr Psychiat,2002,43(6):438-442.
[49]石银涛,冯柏霖,王绘军,等.ASPE-LC-Q-TOF/MS检测血液中氯硝西泮和7-氨基氯硝西泮[J].药物分析杂志,2015,35(4):605-611.
[50]George N,Dean F,Kristen B,et al.Simultaneous Analysis of 14 Benzodiazepines in Oral Fluid by Solid-Phase Extraction and LC-MS-MS[J].JAnal Toxicol,2007,31 (7):369-376.
[51]Moore C,Coulter C,Crompton K,et al.Determination of Benzodiazepines in Oral Fluid Using LC-MS-MS[J].JAnal Toxicol,2007,31(9):596-600.
[52]Melanson S E,Griggs D,Bixho I,et al.7-Aminoclonazepam is Superior to Clonazepam for Detection of Clonazepam Use in OralFluid by LC-MS/MS[J].Clin Chim Acta,2016,(455):128-133.
[53]Di Corcia D,Lisi S,Pirro V,et al.Determination of Pharmaceutical and Illicit Drugs in Oral Fluid by Ultra-High Performance Liquid Chromatography-Tandem Mass Spectrometry[J].JChromatogr B,2013,(927):133-141.
[54]Fisher D S,Partridge S J,Handley SA,et al.LC-MS/MS of Some Atypical Antipsychotics in Human Plasma,Serum,Oral Fluid and Haemolysed Whole Blood[J].Forensic Sci Int,2013,229(1):145-150.
[55]Kato K,Hillsgrove M,Weinhold L,et al.Cocaine and Metabolite Excretion in Saliva under Stimulated and Nonstimulated Conditions[J].JAnal Toxicol,1993,17(6):338-341.
[56]Eric M D,Pilar M,Marta V,et al.Correlation of Methadone Concentrations in Plasma and Saliva Collected with and without Stimulation in Pain Management Patients[J].Clin Chem Lab Med,2015,53(4):109-112.
[57]O'Neal C,Crouch D,Rollins D,et al.The Effects of Collection Methods on Oral Fluid Codeine Concentrations[J].J Anal Toxicol,2000,24(7):536-542.
[58]Schepers R JF,Oyler JM,Joseph R E,et al.Methamphetamine and Amphetamine Pharmacokinetics in OralFluid and Plasma after Controlled Oral Methamphetamine Administration to Human Volunteers[J].Clin Chem,2003,49(1):121-132.
[59]Lund H M E,øiestad E L,Gjerde H,et al.Drugs of Abuse in Oral Fluid Collected by Two Different Sample Kits-Stability Testing and Validation Using Ultra Performance Tandem Mass Spectrometry Analysis[J].J Chromatogr B Anal Technol Biomed Life Sci,2011,879(30):3367-3377.
[60]Coucke L D,Smet L D,Verstraete A G.Influence of Sampling Procedure on Codeine Concentrations in Oral Fluid[J].JAnal Toxicol,2016,40(2):148-152.
[61]Desrosiers N A,Milman G,Mendu D R,et al.Cannabinoids in Oral Fluid by On-Site Immunoassay and by GCMSUsing Two Different Oral Fluid Collection Devices[J].Analytical&Bioanalytical Chemistry,2014,406(17):4117-4128.
[62]Houwing S,Smink B E.Repeatability of Oral Fluid Collection Methods for THCMeasurement[J].Forensic Sci Int,2012,223(1-3):266-72.
[63]Gjerde H,Normann P T,Christophersen A S.The Prevalence of Alcohol and Drugs in Sampled Oral Fluid is Related to Sample Volume[J].JAnal Toxicol,2010,34(7):416-419.
[64]Teixeira H,Proença P,Verstraete A,et al.Analysis ofδ 9-Tetrahydrocannabinol in Oral Fluid Samples Using Solid-Phase Extraction and High-Performance Liquid Chromatography-Electrospray Ionization Mass Spectrometry[J].Forensic Sci Int,2005,150(2-3):205-211.
[65]Moore C,Vincent M,Rana S,et al.Stability ofδ9-Tetrahydrocannabinol(THC)in Oral Fluid Using the QuantisalTMCollection Device[J].Forensic Sci Int,2006,164 (2):126-130.
[66]Samano L K,Anne L,Johnson T,et al.Recovery and Stability ofδ9-Tetrahydrocannabinol Using the Oral-EzeR○Oral Fluid Collection System and InterceptR○Oral Specimen Collection Device[J].JAnal Toxicol,2015,39(8):648-654.
[67]Sébastien A,BergamaschiM M,Barnes A J,et al.Impact of Oral Fluid Collection Device on Cannabinoid Stability Following Smoked Cannabis[J].Drug Test Anal,2015,7 (2):114-120.
[68]Newmeyer M N,Concheiro M,Costa J L D,et al.Oral Fluid with Three Modes of Collection and Plasma Methamphetamine and Amphetamine Enantiomer Concentrations after Controlled Intranasal l-Methamphetamine Administration[J].Drug Test Anal,2015,7(10):877-883.
[69]Ellefsen K N,Concheiro M,Pirard S,et al.Cocaine and Benzoylecgonine Oral Fluid On-Site Screening and Confirmation[J].Drug Test Anal,2016,8(3-4):296-303.
[70]Ellefsen K N,Concheiro M,Pirard S,et al.Oral Fluid Cocaine and Benzoylecgonine Concentrations Following Controlled Intravenous Cocaine Administration[J].Forensic Sci Int,2016,(260):95-101.
[71]Samano K L,Clouette R E,Rowland B J,et al.Concentrations of Morphine and Codeine in Paired Oral Fluid and Urine Specimens Following Ingestion of a Poppy Seed Roll and Raw Poppy Seeds[J].J Anal Toxicol,2015,39(8):655-661.
[72]Wille SM R,Fazio V D,Toennes SW,et al.Evaluation ofδ9-TetrahydrocannabinolDetection Using Drugwipe5sR○Screening and Oral Fluid Quantification after QuantisalTMCollection for Roadside Drug Detection Via a Controlled Study with Chronic Cannabis Users[J].Drug Test Anal,2014,7(3):178-186.
[73]Milman G,Barnes A J,Lowe R H,et al.Simultaneous Quantification of Cannabinoids and Metabolites in Oral Fluid by Two-DimensionalGas Chromatography Mass Spectrometry[J].JChromatogrA,2010,1217(1217):1513-1521.
[74]Patteet L,Maudens K E,Morrens M,et al.Determination of Common Antipsychotics in Quantisaltm-Collected Oral Fluid by UPLC-MS/MS:Method Validation and Applicability for Therapeutic Drug Monitoring[J].Ther Drug Monit,2016,38(1):87-97.
[75]Jang M,Chang H,YangW,et al.Development of an LCMS/MS Method for the Simultaneous Determination of 25 Benzodiazepines and Zolpidem in Oral Fluid and its Application to Authentic Samples from Regular Drug Users[J].JPharmaceut Biomed,2013,(74):213-222.
[76]Langel K,Engblom C A,Gunnar T,et al.Drug Testing in Oral Fluid-Evaluation of Sample Collection Devices[J].J Anal Toxicol,2008,32(6):393-401.
[77]Andås H T,Enger A,ØiestadÅ,et al.Extended Detection of Amphetamine and Methamphetamine in Oral Fluid[J].Ther Drug Monit,2016,38(1):114-119.
[78]Hallvard G,Jon M,Christophersen A R S,et al.Comparison of Drug Concentrations in Blood and Oral Fluid Collected with the Intercept Sampling Device[J].JAnal Toxicol,2010,34(4):204-209.
[79]Montse V,Simona P,Rosa V,et al.Stability of Drugs of Abuse in Oral Fluid Collection Devices with Purpose of External Quality Assessment Schemes[J].Ther Drug Monit,2009,31(2):277-280.
[80]Hallvard G,øiestad E L,øiestadÅM,et al.Comparison of Zopiclone Concentrations in Oral Fluid Sampled with InterceptR○Oral Specimen Collection Device and StatsureSaliva SamplerR○and Concentrations in Blood[J].J Anal Toxicol,2010,34(9):590-593.
[81]Pascal K,Bertrand B,Jean-FranOis M,et al.Evaluation of the Cozart DDSV Test for Cannabis in Oral Fluid[J].Ther Drug Monit,2009,31(1):131-134.
[82]Dickson S,Park A,Nolan S,et al.The Recovery of Illicit Drugs from Oral Fluid Sampling Devices[J].Forensic Sci Int,2007,165(1):78-84.
[83]Speedy T,Baldwin D,Jowett G,et al.Development and Validation of the CozartR○DDSOral Fluid Collection Device[J].Journal for Specialists in Group Work,2007,170 (2-3):117-120.
[84]Cooper G,Wilson L,Reid C.Validation of the Cozart Amphetamine Microplate EIA for the Analysis of Amphetamines in Oral Fluid[J].Forensic Sci Int,2006,159 (2-3):104-112.
[85]Cooper G,Reid C,Wilson L,et al.Validation of the CozartR○Microplate EIA for Analysis of Opiates in Oral Fluid[J].Forensic Sci Int,2005,154(2-3):240-246.
[86]Dams R,Choo R E,LambertW E,et al.Oral Fluid as an Alternative Matrix to Monitor Opiate and Cocaine Use in Substance-Abuse Treatment Patients[J].Drug Alcohol Depen,2007,87(2-3):258-267.
[87]Jiang F,Rao Y,Wang R,et al.Sensitive,Automatic Method for the Determination of Diazepam and its Five Metabolites in Human Oral Fluid by Online Solid-Phase Extraction and Liquid Chromatography with Tandem Mass Spectrometry[J].JSep Sci,2016,39(10):1873-1883.
[88]Rosas M E R,Preston K L,Epstein D H,et al.Quantitative Determination of the Enantiomers of Methadone and its Metabolite(EDDP)in Human Saliva by Enantioselective Liquid Chromatography with Mass Spectrometric Detection[J].JChromatogr B,2003,796(2):355-370.
[89]JMichaelW,Ron F,Crouch D J,et al.An Evaluation of Rapid Point-of-Collection Oral Fluid Drug-Testing Devices[J].JAnal Toxicol,2003,29(4):244-248.
[90]Tom B,Kari V,Pirjo L.Benzodiazepine Whole Blood Concentrations in Cases with Positive Oral Fluid On-Site Screening Test Results Using the DrugwipeR○Single for Benzodiazepines[J].JAnalToxicol,2011,35(6):349-356.
[91]Logan B K,Mohr A L A,Talpins S K.Detection and Prevalence of Drug Use in Arrested Drivers Using the Drager Drug Test 5000 and Affiniton Drugwipe Oral Fluid Drug Screening Devices[J].JAnal Toxicol,2014,38(7):444-450.
[92]Kempf J,Wuske T,Schubert R,et al.Pre-analytical Stability of Selected Benzodiazepines on a Polymeric Oral Fluid Sampling Device[J].Forensic Sci Int,2009,186(1-3):81-85.
[93]Cirimele V,Villain M,Mura P,et al.Oral Fluid Testing for Cannabis:On-Site OralineR○IV S.A.T.Device Versus GC/MS-Forensic Science International[J].Forensic Sci Int,2006,161(2-3):180-184.
[94]Reichardt E M,Dene B,M David O.Effects of Oral Fluid Contamination on Two Oral Fluid Testing Systems[J].J Anal Toxicol,2013,37(4):246-249.
[95]Jenkins A J,Oyler JM,Cone E J.Comparison of Heroin and Cocaine Concentrations in Saliva with Concentrations in Blood and Plasma[J].JAnalToxicol,1995,19(6):359-374.
[96]Niedbala R S,Kardos K W,Fritch D F,et al.Passive Cannabis Smoke Exposure and Oral Fluid Testing.II.Two Studies of Extreme Cannabis Smoke Exposure in a Motor Vehicle[J].JAnal Toxicol,2005,29(7):607-615.
[97]Herrmann E S.Nonsmoker Exposure to Secondhand Cannabis Smoke.III.Oral Fluid and Blood Drug Concentrations and Corresponding Subjective Effects[J].J Anal Toxicol,2015,39(7):497-509.
(本文编辑:施妍)
Advances in Forensic Analysis of Drugs of Abuse and Psychoactive Drugs in Saliva
FENG Xue-yi1,2,SHEN Min1,CHEN Hang1
(1.Shanghai Key Laboratory of Forensic Medicine,Shanghai Forensic Service Platform,Institute of Forensic Science,Ministry of Justice,Shanghai200063,China;2.Department of Forensic Chemistry,National Police University of China,Shenyang 110854,China)
In recent years,there has been substantial interest in the use of saliva for drug testing in the fields of forensic toxicology and clinical drugmonitoring.As one type of non-invasive biological specimen,saliva has the advantages of easy collection,low risk of disease infection,and the potential of large-scale sampling.Saliva samples have been widely applied in developed countries for drug abuse test.Besides,the matrix of saliva is clearer than blood and urine,thus lessmatrix effect is observed.However,due to the disadvantage of inadequate volume and trace drug concentration,saliva analysis demands highly efficient sample preparation and more sensitive analytical techniques.In this paper,the research progress in saliva analysis for drugs of abuse and psychoactive drugs in the last ten years was introduced,focusing on sample preparation and analytical techniques.The limitation of saliva sample,the analytical difficulties and the research hotspots were also summarized.
saliva;drug of abuse;forensic identification
DF795.4
A
10.3969/j.issn.1671-2072.2016.04.010
1671-2072-(2016)04-0057-11
2016-05-12
国家级科研院所公益项目(GY2016Z-1);国家自然科学基金面上项目(81273340);上海市法医学重点实验室项目(14DZ2270800);上海市司法鉴定专业技术服务平台资助项目(16DZ2290900)
冯雪伊(1991—),女,硕士研究生,主要从事分析化学研究。E-mail:milk_juice@sina.com。
沈敏(1955—),女,研究员,博士研究生导师,主要从事法医毒物鉴定研究和司法鉴定管理工作。
E-mail:shenm@ssfjd.cn。
