氯吡格雷联合西洛他唑治疗急性心肌梗死经皮冠状动脉介入治疗术后合并消化道出血患者1例
2016-08-18顾崇怀赵昕韩雅玲
顾崇怀 赵昕 韩雅玲
·病例报告·
氯吡格雷联合西洛他唑治疗急性心肌梗死经皮冠状动脉介入治疗术后合并消化道出血患者1例
顾崇怀赵昕韩雅玲
急性心肌梗死;经皮冠状动脉介入治疗;冠状动脉综合征
1 临床资料
患者男,73岁,于2013年3月18日15:00突发心前区闷痛,向后背及左上肢放散,伴出汗,无明显胸闷、气短,每间隔15 min含服速效救心丸(10粒/次),共3次,持续1 h后缓解,未就诊。次日4:10再次出现上述症状加重,再次含服速效救心丸持续数分钟未见明显缓解,无恶心、呕吐、黑矇及晕厥症状,并于2013年3月20日9:30入沈阳军区总医院心内科重症监护病房(CCU)。既往高血压病史6个月,最高180/100 mmHg(1 mmHg=0.133 kPa),未系统监测及控制血压;慢性支气管炎史20余年,否认糖尿病及消化道系统疾病史,无吸烟、饮酒史,否认冠心病家族史。入院查体:体温36.7℃,心率92次/min,呼吸19次/min,血压147/80 mmHg,双肺未闻及干、湿啰音。入院心电图示:窦性心律,Ⅱ、Ⅲ、aVF导联ST段上抬0.2 mV,Ⅰ、aVL、V1~V6导联ST段下移0.1~0.2 mV。超声心动图示:左心房前后径28 mm,左心室舒张末期内径45 mm,左心室射血分数(left ventricular ejection fraction,LVEF)71%。实验室检查:红细胞计数(RBC)3.72×109/L,白细胞计数(WBC)9.2×109/L,中性粒细胞分数(NF)69.2%,血红蛋白(HGB)113 g/L,红细胞平均体积(MCV)97.9 fL,红细胞平均血红蛋白量(MCH)33.0 pg,红细胞平均血红蛋白浓度(MCHC)35.1%,血肌酸酐105 μmol/L,血钾4.6 mmol/L。入院时心肌酶谱:高敏肌钙蛋白T(high troponin T,hs-cTNT)0.324 ng/ml(参考值:0~0.05 ng/ml);肌酸激酶同工酶(creatine kinase-MB,CK-MB)47 U/L(参考值:0~25 U/L),每日连续监测心肌酶谱呈下降趋势。立即给予负荷剂量抗血小板药物(阿司匹林300 mg+氯吡格雷300 mg),24 h后采用光学比浊法测定血小板聚集率,花生四烯酸(AA)诱导的血小板聚集率70.2%,腺苷二磷酸(ADP)诱导的血小板聚集率33.2%。入院时GRACE评分102分,CRUSADE评分35分。入院第2天查便潜血阴性,第6天化验HGB 121 g/L,MCV 95.1 fL,MCH 36.2 pg,MCHC 38.5%。
入院诊断:急性下壁心肌梗死,Killip分级Ⅰ级,高血压病3级(极高危),慢性支气管炎。常规行吸氧、心电监护,抗血小板(阿司匹林负荷剂量300 mg,100 mg,每日1次维持;氯比格雷负荷剂量300 mg,75 mg,每日1次维持),抗凝(依诺肝素40 mg,每日2次维持),稳定血压,抑制心肌重构(咪达普利5 mg,每日1次维持),降低心率(琥珀酸美托洛尔12.5 mg,每日2次),调脂(瑞舒伐他汀10 mg,每晚1次),消化道黏膜保护(泮托拉唑 80 mg, 每日1次静脉滴注)等治疗后血流动力学稳定,心前区疼痛症状明显缓解。考虑患者急性心肌梗死发病超过24 h,择期PCI策略。
手术情况:患者于2013年3月26日(入院第6天)行择期冠状动脉造影检查及冠状动脉支架置入术。穿刺右侧桡动脉成功后,给予肝素5000 U,冠状动脉造影示左主干(LM)正常,左前降支(LAD)近段70%~80%狭窄,LAD中段60%~70%狭窄,第一对角支(D1)粗大,近段70%~80%狭窄,血流TIMI Ⅲ级;左回旋支(LCX)细小, 20%~40%狭窄,血流TIMI Ⅲ级;右冠状动脉(RCA)口部40%狭窄,远段99%次全闭,血流TIMI 0~Ⅰ级(图1~2)。根据患者临床表现、心肌酶谱及心电图结果拟采取RCA远段支架置入术。追加肝素2000 U,顺利于RCA远段置入2.75 mm×29 mm药物洗脱球囊支架1枚(Partner,乐普,图3)。
术后给予常规双联抗血小板治疗(阿司匹林100 mg,每日1次+氯吡格雷75 mg,每日1次)、抗凝(依诺肝素40 mg,每日2次)治疗。术后第2天患者开始出现上腹部不适及黑便,化验便潜血阳性。血常规:RBC降至2.88×109/L, HGB降至90 g/L,出血6 h后减少至67 g/L。紧急行床旁胃镜检查示:十二指肠球部可见大小约0.5 cm×0.6 cm溃疡,内膜表面糜烂,周围黏膜充血水肿,可见明显出血点,胃镜下予出血部位止血夹2枚,局部喷止血药。停用所有抗凝及抗血小板药物,待消化道出血停止(生命体征平稳及HGB、RBC计数不再下降),逐渐增加抗栓药物。术后第3天,患者血流动力学稳定,继续停用阿司匹林,给予氯吡格雷75 mg,每日1次及磺达肝癸钠2.5 mg,每日1次。同时给予补液2000~3000 ml、止血(云南白药0.5 g,每日3次)、强化消化道黏膜保护(泮托拉唑80 mg,每日2次静脉滴注及瑞巴派特100 mg,每日3次)治疗。术后第5天,未见消化道出血加重,给予西洛他唑50 mg,每日2次及氯吡格雷75 mg,每日1次,双联抗血小板。更改为上述治疗方案后,患者消化道出血得到控制且无胸痛发作,HGB维持在80 g/L,术后10 d病情平稳出院。出院前复查AA诱导的血小板聚集率71.4%,ADP诱导的血小板聚集率67.5%。
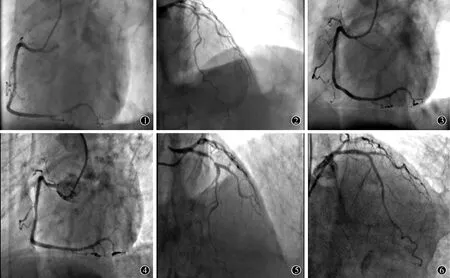
图1 2013年3月26日右冠状动脉造影;图2 2013年3月26日左前降支造影;图3 2013年3月26日右冠状动脉支架置入术后影像;图4 2015年9月1日右冠状动脉复查造影;图5 2015年9月1日左前降支复查造影;图6 2015年9月1日左前降支支架置入后造影
2013年9至11月,患者因横结肠癌行横结肠根治术,停用氯吡格雷53 d(期间坚持口服西洛他唑)。此后28个月内一直口服双联抗血小板、稳定血压、抑制心肌重构、降低心率、调脂及消化道黏膜保护药物,并定期进行门诊随访,无胸痛及其他不适症状再发,未复查胃镜。
2015年8月开始无诱因出现左侧心前区不适,2015年8月27日再次以心绞痛诊断收入本科住院治疗。术前继续给予氯吡格雷75 mg,每日1次及西洛他唑50 mg,每日2次双联抗血小板。实验室结果示:AA诱导的血小板聚集率80.5%,ADP诱导的血小板聚集率84.9%。2015年9月1日行冠状动脉造影示:LM大致正常,LCX细小,远段80%~90%狭窄,LAD近中段长病变,最重70%~80%狭窄,RCA原支架内无再狭窄(图4~5)。结合患者存在心绞痛症状。于LAD近中段置入2.75 mm×29 mm及2.75 mm×24 mm药物洗脱球囊支架2枚(Partner,乐普),两两相连。并于LAD及D1行对吻扩张(图6)。入院5 d后出院,继续口服氯吡格雷75 mg,每日1次及西洛他唑50 mg,每日2次及保护胃黏膜药物。术后1年(2016年9月)若无心绞痛症状,复查冠状动脉增强CT后支架良好,可酌情停用西洛他唑,长期口服氯吡格雷。
2 讨论
抗血小板治疗是经皮冠状动脉介入治疗(PCI)围术期的必要手段。对于急性冠状动脉综合征(ACS)尤其是急性心肌梗死(AMI)患者,抗血小板治疗更是影响临床预后的关键因素。但ACS合并消化道出血的发生却是临床上经常面临的棘手难题。恢复急性心肌梗死患者梗死相关冠状动脉血供是挽救心肌实现再灌注治疗的基本策略和原则,尽快实施PCI可减少心肌损害、降低急性心功能衰竭等相关并发症发生率[1]。同时,心肌梗死患者的成功救治也必须遵循有效的抗血小板治疗,以限制支架内血栓的发生[2]。然而,由抗血小板药物带来的包括消化道出血在内的一系列出血风险的增加,也成为临床关注的焦点。ACUITY研究[3]显示,由抗血小板治疗带来的消化道出血显著增加冠心病患者30 d(HR4.87)、1年(HR3.97)全因死亡率,并且增加心源性死亡率(HR5.35)。Yeomans等[4]指出,阿司匹林可使消化道损伤风险增加2~4倍。《抗血小板药物消化道损伤的预防和治疗中国专家共识(2012更新版)》中指出[5],即使小剂量阿司匹林也可能增加消化道损伤危险,氯吡格雷可加重消化道损伤,阿司匹林与氯吡格雷联合应用时危险性更高[6-7]。
2014年欧洲心脏病学会(ESC)心肌血运重建指南[1]建议,对于ACS、裸金属支架置入1个月内、药物涂层支架置入6个月内患者,应尽量避免停用抗血小板药物。接受双联抗血小板治疗的冠心病患者发生出血时,应先停用阿司匹林。严重消化道出血威胁生命时,需停用所有抗血小板药物,3~5 d后,如情况稳定,可重新开始使用阿司匹林或氯吡格雷。
西洛他唑通过选择性抑制磷酸二酯酶Ⅲ(PDE-Ⅲ)的活性,减少腺苷酸环化酶(AC)的降解、转化,增加血小板内环腺苷酸(cAMP)浓度,抑制抗血小板聚集,同时增加血管平滑肌内cAMP浓度,产生扩张血管的作用[8]。已有多项大型临床研究和Meta分析显示,西洛他唑联合经典双联抗血小板治疗方案(三联抗血小板治疗)可以获得更好的血小板抑制效果、降低主要不良心血管事件(major adverse cardiac events, MACE)发生率、减少支架内再狭窄及支架内血栓形成风险,且不增加出血事件(包括消化道出血事件)发生率[9-11]。
阿司匹林不仅会对消化道黏膜产生直接刺激并影响前列腺素(prostaglandin,PG)对黏膜的保护作用。既往有研究显示,对伴有消化道溃疡病史的患者,长期服用低剂量阿司匹林(<325 mg/d)增加的消化道出血风险可能高于其保护心血管所带来的获益[12]。但是否可以停用阿司匹林并使用西洛他唑进行替代治疗,尚无大规模临床试验证实。
本例患者为急性心肌梗死老年男性,围术期出现持续性活动性消化道出血,PCI术后血流动力学稳定时,胃镜检查是安全的。AMI合并有严重的、大量的及持续性消化道出血患者血流动力学稳定,应该在24 h之内接受诊断性或治疗性胃镜检查,且胃镜明确存在十二指肠球部溃疡,必要时行内镜下止血治疗。是否改变抗血小板和抗凝治疗方案,需权衡正在进行的大出血风险大还是患者发生冠状动脉缺血事件的风险大(特别是支架内血栓形成)。本中心对该患者采取立即停用阿司匹林,同时,因该患者存在氯吡格雷抵抗问题,故给予氯吡格雷联合西洛他唑行双联抗血小板治疗。经该抗血小板治疗方案随访2年结果显示,无MACE发生,靶血管通畅,无再狭窄或支架内血栓形成。笔者所在中心临床实际工作中遇见ACS合并消化道出血的患者并不在少数,在处理抗血小板和消化道出血的治疗上,所采取的这一治疗措施或许能给临床治疗带来更多的选择。
总之,对于临床并不罕见的冠心病合并消化道出血患者,抗栓方法也因患者的特点而不同,主要依据出血的时间(早期/晚期)、出血的严重程度和内镜治疗后发生再出血的风险来判断。此外还应考虑冠状动脉因素,比如支架因素(部位、长度、大小及数量等)、梗死面积大小和其他在冠状动脉介入治疗中的发现(如慢复流/无复流、钙化、迂曲等)。其治疗不能以偏概全,应采用个体化治疗,而本病例所阐述的西洛他唑联合氯吡格雷的抗血小板治疗或许在将来可以成为此类患者进行治疗的一种选择。当然这一方法的疗效还需多中心大型研究进行证实。
[1] Windecker S,Kolh P,Alfonso F,et al.2014 ESC/EACTS Guidelines on myocardial revascularization: The Task Force on Myocardial Revascularization of the European Society of Cardiology (ESC) and the European Association for Cardio-Thoracic Surgery (EACTS)Developed with the special contribution of the European Association of Percutaneous Cardiovascular Interventions (EAPCI). Eur Heart J, 2014,35(37):2541-2619.
[2] Antithrombotic Trialists′ Collaboration. Collaborative meta-analysis of randomized trials of antiplatelet therapy for prevention of death, myocardial infarction, and stroke in high risk patients. BMJ, 2002,324(7329):71-86.
[3] Nikolsky E,Stone GW,Kirtane AJ,et al. Gastrointestinal bleeding in patients with acute coronary syndromes:incidence, predictors, and clinical implications analysis from the ACUITY (Acute Catheterization and Urgent Intervention Triage Strategy) trial. J Am Coll Cardiol,2009,54(14):1293-1302.
[4] Yeomans ND, Lanas AI,Talley NJ, et al. Prevalence and incidence of gastroduodenal ulcers during treatment with vascular protective doses of aspirin. Aliment Pharmacol Ther, 2005, 22(9):795-801.
[5] 抗血小板药物消化道损伤的预防和治疗中国专家共识组.抗血小板药物消化道损伤的预防和治疗中国专家共识(2012更新版).中华内科杂志,2013,52(3):264-270.
[6] Aronow WS. Drug treatment of peripheral arterial disease in the elderly. Drugs Aging, 2006, 23(1):1-12.
[7] 吴思婧,刘宇扬.抗血小板治疗相关消化道出血浅析.中国介入心脏病学杂志,2015,23(1):30-33.
[8] Biondi-Zoccai GG,Lotrionte M,Anselmino M, et al. Systematic review and meta-analysis of randomized clinical trials appraising the impact of cilostazol after percutaneous coronary intervention. Am Heart J, 2008, 155(6): 1081-1089.
[9] Tamhane U, Meier P, Chetcuti S, et al. Efficacy of cilostazol in reducing restenosis in 28 patients undergoing contemporary stent based PCI: a meta-analysis of randomised controlled trials. EuroIntervention, 2009,5(3):289-91.
[10] Wang P, Zhou S, Zhou R, et al. The effectiveness and safety of triple-antiplatelet treatment based on cilostazol for patients receiving percutaneous coronary intervention: a meta-analysis.Clin Cardiol, 2012, 35(10):598-604.
[11] Ding XL, Xie C, Jiang B, et al. Efficacy and safety of adjunctive cilostazol to dual antiplatelet therapy after stent implantation: an updated meta-analysis of randomized controlled trials. J Cardiovasc Pharmacol Ther, 2013,18(3):222-228.
[12] Lanas A, Polo-Tomás M, Casado-Arroyo R. The aspirin cardiovascular/gastrointestinal risk calculator-a tool to aid clinicians in practice.Aliment Pharmacol Ther, 2013, 37(7): 738-748.
10.3969/j.issn.1004-8812.2016.03.009
中国医师协会探索心血管研究基金项目(DFCMDA201417)
110016辽宁沈阳,沈阳军区总医院心血管内科(顾崇怀、赵昕、韩雅玲);辽宁医学院(顾崇怀)
赵昕,Email:zhaoxin81830@sina.com;韩雅玲,Email:hanyaling@126.net
R542.22
2015-11-04)
