补肾化浊汤联合盐酸环丙沙星治疗慢性前列腺炎疗效及对炎症因子的影响
2016-08-10张阳光孟凡钦
张阳光,孟凡钦
(1. 四川省广元市第三人民医院,四川 广元 628000;2. 陕西省西安市第四人民医院,陕西 西安 710004)
补肾化浊汤联合盐酸环丙沙星治疗慢性前列腺炎疗效及对炎症因子的影响
张阳光1,孟凡钦2
(1. 四川省广元市第三人民医院,四川 广元 628000;2. 陕西省西安市第四人民医院,陕西 西安 710004)
[摘要]目的观察补肾化浊汤联合盐酸环丙沙星治疗慢性前列腺炎患者的临床疗效及对炎症因子IFN-γ、TNF-α、IL-10水平的影响。方法将116例慢性前列腺炎患者随机分为观察组58例和对照组58例,对照组采用口服盐酸环丙沙星治疗,观察组在此基础上给予补肾化浊汤治疗,2组均连续治疗4周,观察2组临床疗效及治疗前后炎症因子水平。结果观察组总有效率明显高于对照组(�2=4.54,P<0.05)。治疗后2组患者NIH-CPSI评分、前列腺液WBC计数及IFN-γ、TNF-α、IL-10水平均较治疗前明显减少或降低(P均<0.05),且观察组上述指标改善情况均明显优于对照组(P均<0.05)。结论补肾化浊汤联合盐酸环丙沙星治疗慢性前列腺炎疗效显著,其可能是通过调节炎症细胞因子IFN-γ、TNF-α、IL-10水平来达到治疗目的。
[关键词]补肾化浊汤;盐酸环丙沙星;慢性前列腺炎;炎症因子
慢性前列腺炎是较常见的泌尿生殖系统炎症性疾病,属于男科难治病之一。虽然本病不会对患者生命造成威胁,但却严重影响患者的生活质量。临床治疗慢性前列腺炎的方法众多,但是还没有哪一种方法或药物可以特别有效的适用所有前列腺炎患者[1]。西医主要采用抗生素治疗,但前列腺组织中血-前列腺屏障的存在,使抗生素对大部分慢性前列腺炎无效或疗效差[2],而中药治疗本病重在整体调节,在改善患者自觉症状和疗效的持久性方面有一定的优势。笔者根据临床经验,结合古代医家及现代研究对本病认识,认为湿热下注、肾虚、血瘀是导致本病的关键,故采用补肾化浊汤治疗慢性前列腺炎,取得较好疗效,现报道如下。
1临床资料
1.1一般资料选择广元市第三人民医院2013年12月—2015年9月门诊或住院明确诊断为慢性前列腺炎患者116例,均符合《前列腺炎诊断治疗指南》[3]和《中药新药临床研究指导原则》[4]中前列腺炎的诊断标准;年龄20~50岁;病程≥3个月;2周内未服用治疗慢性前列腺炎的其他药物或治疗方法。排除急性前列腺炎者;活动性溃疡及出血倾向者;合并心、脑、肾、肝病者;合并精囊炎、慢性附睾炎、尿道狭窄等疾病者;对多种药物过敏者;合并精神疾病者。患者均签署知情同意书。采用随机数字表法将患者分为2组:对照组58例,年龄26~48(38.92±6.03)岁;病程3~18(10.36±3.05)月。观察组58例,年龄24~49(39.03±5.81)岁;病程4~17(9.89±2.98)月。2组年龄、病程比较差异无统计学意义,具有可比性。
1.2治疗方法对照组给予盐酸环丙沙星片(哈药集团制药总厂,国药准字H23021557)口服,0.25 g/次,2次/d。观察组在对照组基础上给予补肾化浊汤口服,方药组成:熟地黄、茯苓各20 g,车前子、牛膝、白术、败酱草、丹参各15 g,延胡索、黄柏、莲子心、石菖蒲、补骨脂、川萆薢各10 g,由本院制剂室煎煮提供,1剂/d,早晚各1次。2组均连续治疗4周。
1.3观察指标①治疗前后慢性前列腺炎症状评分(NIH-CPSI):包括疼痛或不适、排尿、症状的影响和生活质量三项,总分0~43分,分值越高,症状越严重。②前列腺液WBC计数及IFN-γ、TNF-α、IL-10水平:于治疗前后留取患者前列腺按摩液(EPS)至少0.1 mL于专用容器内,-70 ℃保存待检。将带有EPS的载玻片置显微镜下,高倍镜(×400)下观察5个视野,计算每个视野下的平均数即为WBC计数。采用ELISE法检测IFN-γ、TNF-α、IL-10水平,所有操作按照试剂盒说明进行。
1.4疗效评定标准参照《慢性前列腺炎中西医结合诊疗指南》相关标准评定疗效[5]。痊愈:临床症状完全消失,EPS检查连续2次以上正常;显效:NIH-CPSI评分较治疗前降低10分以上,EPS检查连续2次以上WBC计数较治疗前减少≥60%;有效:NIH-CPSI评分较治疗前降低5分以上,EPS检查连续2次以上WBC计数较治疗前减少≥30%;无效:NIH-CPSI评分较治疗前降低少于5分,EPS检查连续2次以上WBC计数较治疗前减少<30%或无明显变化。
1.5统计学方法使用统计学软件SPSS 13.0进行数据处理。计数资料以率表示,组间比较采用2检验;计量资料以±s表示,组内及组间比较采用t检验。以P<0.05为差异有统计学意义。
2结果
2.12组临床疗效比较观察组总有效率明显高于对照组(P<0.05)。见表1。
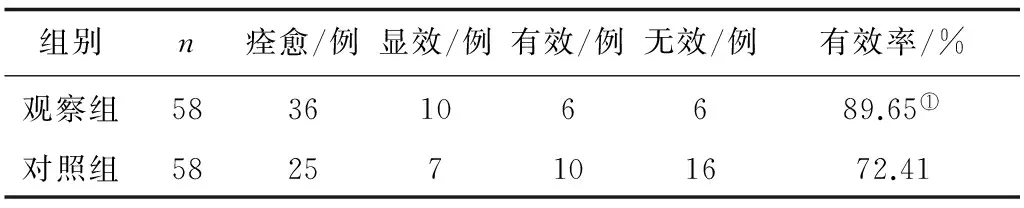
表1 2组临床疗效比较
注:①与对照组比较,2=4.54,P<0.05。
2.22组治疗前后NIH-CPSI积分及WBC计数比较2组治疗后WBC计数及NIH-CPSI评分均较治疗前明显减少或降低(P均<0.05),且观察组较对照组下降更显著(P<0.05)。见表2。
表2 2组治疗前后NIH-CPSI积分及WBC计数比较
注:①与治疗前比较,P<0.05;②与对照组比较,P<0.05。
2.32组治疗前后IFN-γ、TNF-α、IL-10水平比较2组治疗后IFN-γ、TNF-α及IL-10水平均较治疗前明显下降(P均<0.05),且观察组较对照组改善更为显著(P<0.05)。见表3。
表3 2组治疗前后IFN-γ、TNF-α、IL-10水平比较
注:①与治疗前比较,P<0.05;②与对照组比较,P<0.05。
3讨论
慢性前列腺炎是发生在前列腺的由多种病因引起、多种病理交织的慢性多发病,临床以发病较缓慢、反复发作、缠绵难愈、症状多样为特点,严重影响患者的生活质量。本病的病因、发病机制及病理生理过程至今不甚明确,但随着免疫学和分子生物学的发展,考虑本病是多种致病因素诱发而由免疫炎症细胞及细胞因子参与的炎症反应。细胞因子主要由免疫细胞分泌,参与炎症的发生,可通过多种细胞的产生和释放构成复杂的细胞因子网络,在损伤、炎症和感染局部起重要的免疫调节作用,并在组织损伤与修复过程中起关键作用,决定着炎症反应的类型和持续时间[6-7]。TNF-α和IFN-γ是促炎性因子,IL-10为抗炎性细胞因子。大量研究证实,慢性前列腺炎患者精浆中TNF-α和IFN-γ水平升高,TNF-α和IFN-γ可能在慢性前列腺炎的进展中起重要作用,通过增加某些黏附分子的表达促进炎症细胞的黏附、浸润,释放炎症介质等促进炎症反应[8]。IL-10作用于不同细胞上可以出现免疫抑制、免疫刺激和抗炎效应。在慢性前列腺炎患者中IL-10水平明显升高,而IL-10的水平与疼痛程度呈正相关[9]。
祖国医学并无慢性前列腺炎病名,根据其临床表现,归属于“精浊”范畴。本病以湿热为主,多为精室受湿热毒邪所侵,壅滞于内,疏泄失常;或因三焦气化不利,湿阻化热,湿热互结,则精气时有外溢,出现尿浊的症状。病久不愈,则致肾虚,常常虚实夹杂,湿热瘀阻经脉,导致秽浊难排,败精阻血,可致瘀血阻滞,贯穿本病始终。因此,本病的病因可概括为相伴而生、相互影响的湿热、肾虚、血瘀三方面,肾虚为发病之本,湿热为致病之标,血瘀为疾病发展的病理产物。治宜益气补肾、除湿化浊、活血化瘀。补肾化浊汤方中熟地黄补血滋阴,填精益髓;牛膝补益肝肾,补骨脂温肾助阳,白术健脾益气,黄柏清热燥湿,泻火解毒;川萆薢利湿去浊,祛风陈痹;茯苓利水渗湿;车前子清利下焦湿热,利尿通淋;石菖蒲芳香化湿,开窍导浊;败酱草清热解毒,散结排脓,活血止痛;丹参活血化瘀,延胡索和莲子心均能镇静安神。上述方药合用,共奏益气补肾、利湿化浊、活血止痛等功效。现代药理学研究表明,石菖蒲对金黄葡萄球菌、肺炎双球菌、大肠杆菌有抑制作用[10];牛膝对金黄色葡萄球菌、溶血性链球菌敏感,且牛膝有效成分牛膝总皂苷有抗炎、镇痛、活血作用[11];车前子可增加尿素、尿酸及氯化钠的排泄,对抗金黄色葡萄球菌,车前子多糖能降低蛋清诱导的大鼠滑膜细胞产生的TNF-α,减轻炎性因子的渗出[12];败酱草含三萜皂苷类、黄酮类等化学物质,可增强白细胞的吞噬能力,促进抗体形成,起到抗菌消炎的作用,对金黄色葡萄球菌有抑制作用;茯苓的有效成分茯苓多糖可下调IFN-γ、IL-10水平,提高机体的免疫功能,且可活化T细胞、增强巨噬细胞的吞噬功能,从而发挥抑制炎症的作用[13];白术煎剂对金黄色葡萄球菌、枯草杆菌、溶血性链球菌均有抑制作用,且有效成分β-桉叶油醇、苍术醇均有明显镇痛作用[14];丹参、萆薢也对金黄色葡萄球菌有明显抑制作用;黄柏善治下焦湿热,对多种泌尿生殖系统炎症有较好的疗效,其可下调DNFB诱导的小鼠血清IFN-γ水平,抑制TNF-α表达,从而减轻炎症损伤[15];延胡索的有效成分延胡素甲素、乙素、丑素均有镇痛作用,且延胡索乙素可阻断蛋白激酶磷酸化,从而抑制IL-8分泌[16]。
本研究结果显示,观察组总有效率明显高于对照组;2组治疗后WBC计数、NIH-CPSI评分及IFN-γ、TNF-α、IL-10水平均较治疗前明显减少或降低,且观察组上述指标改善情况均优于对照组。说明补肾化浊汤能够改善患者临床症状、体征,降低白细胞计数,下调IFN-γ、TNF-α、IL-10水平,使促炎性细胞因子和抗炎细胞因子之间保持平衡。
综上所述,补肾化浊汤治疗慢性前列腺炎疗效显著,考虑其可能机制是通过调节炎症细胞因子IFN-γ、TNF-α、IL-10水平来达到治疗目的。但是由于时间和条件限制,本研究观察样本较少,且观察时间仅为1个月,可能影响某些结果的判定,尚需进一步探讨其可能机制。
[参考文献]
[1]张兆宏,刘春雨. 慢性前列腺炎诊断与治疗进展[J]. 医学综述,2009,15(16):2463-2465
[2]Shokes DA,Manickam K. Herbal and complementary medicine in chronic prostatitis[J]. World J Urol,2003,21(2):109-113
[3]张凯,白文俊,邓春华. 前列腺炎诊断治疗指南 (试行版)[J]. 中华现代外科学杂志,2006,3(21):1766-1776
[4]李海松,韩富强,李曰庆. 918例慢性前列腺炎中医证型分布研究[J]. 北京中医药,2008,27(6):416-418
[5]中国中西医结合学会男科专业委员会. 慢性前列腺炎中西医结合诊疗指南[J]. 中国中西医结合杂志,2007,27(11):1052-1056
[6]胡小朋,白文俊,朱积川,等. 慢性前列腺炎细菌及免疫学研究[J]. 中华泌尿外科杂志,2002,23(1):29-31
[7]周晓辉,韩蕾,周智恒,等. 免疫性慢性非细菌性前列腺炎大鼠模型的形态学与分子生物学特性[J]. 中华男科学,2005,11(4):290-295
[8]黄鸿源. 前列舒通胶囊对慢性前列腺炎大鼠前列腺组织中IL-10及TNF-α表达的影响[J]. 亚太传统医药,2012,8(9):55-57
[9]钟景琦,屈平保,钱海宁,等. Ⅲ型前列腺炎治疗前后前列腺液中B7-H3,IFN-γ,IL-10的表达及临床意义[J]. 中国男科学杂志,2014,20(4):56-58
[10] 王争,王曙东,侯中华.石菖蒲成分及药理作用的研究概况[J]. 中国药业,2012,21(11):1-3
[11] 潘晓波. 牛膝的药理作用研究[J]. 长春中医药大学学报,2009,25(6):969
[12] 冯娜,刘芳,郭会彩,等. 车前子多糖抗炎作用机制的实验研究[J]. 天津医药,2012,40(6):598-601
[13] 侯安继,彭施萍,项荣. 茯苓多糖抗炎作用研究[J]. 中药药理与临床,2003,19(3):15-16
[14] 杨娥,钟艳梅,冯毅凡. 白术化学成分和药理作用的研究进展[J]. 广东药学院学报,2012,28(2):218-221
[15] 杨周平,武志军. 中药黄柏的药理作用和临床应用研究[J]. 甘肃医药,2010,29(3):329-331
[16] 张先洪,陆兔林,毛春芹. 延胡索不同炮制品镇痛抗炎作用研究[J]. 时珍国医国药,2009,20(2):449-450
doi:10.3969/j.issn.1008-8849.2016.21.037
[中图分类号]R697.33
[文献标识码]B
[文章编号]1008-8849(2016)21-2377-03
[收稿日期]2015-12-20
