局部进展期直肠癌新辅助治疗的策略:分而治之
2016-07-12丁培荣
丁培荣
•专家论坛•
局部进展期直肠癌新辅助治疗的策略:分而治之
丁培荣

丁培荣 主任医师、硕士生导师。2002年毕业于中山大学临床医学系,2009年6月~2010年6月赴美国斯隆凯特琳纪念癌症中心从事访问学者工作。第一届美中抗癌协会(USCACA)-美国国家癌症研究基金会(NFCR)杰出青年学者奖获者。临床主攻直肠癌低位保肛、肝转移多学科协作综合治疗以及遗传性肠癌的筛查和遗传咨询。中华消化外科主办的第二届“功夫剧场”腹腔镜结直肠手术大赛全国总冠军。中国抗癌协会临床肿瘤学协作专业委员会(CSCO)青年专家委员会委员、广东省抗癌协会大肠癌专业委员会青委会副主任委员、中国抗癌协会大肠癌专业委员会遗传学组委员、广东省抗癌协会大肠癌专业委员会委员、广东省医学会胃肠外科学分会中青年委员、以及 《中华结直肠疾病电子杂志》通讯编委。
【摘要】尽管术前放疗显著降低了局部进展期直肠癌的复发风险,但这种治疗模式不仅未能显著改善患者的总生存,而且还带来严重的远期毒性,使患者生存质量受到严重影响。本文将介绍该领域近年来的研究进展及对临床实践的影响。
【关键词】直肠肿瘤; 磁共振成像; 新辅助; 个体化
尽管全直肠系膜切除术(total mesorectal excision, TME)手术显著降低了直肠癌总体的局部复发风险,但局部进展期患者的处理仍然十分棘手。因为其治疗策略不仅要考虑如何通过手术达到根治性的目的,而且要考虑同时如何保护括约肌和性功能;更加重要的是要考虑如何对不同的患者恰当的使用不同的新辅助策略以达到最佳的根治性、最小的毒性和最理想的远期生存质量。
目前术前放疗(加或不加化疗)是局部进展期直肠癌的标准治疗,通过这种策略大约可以在TME手术基础上进一步降低6%~9%的局部复发率[1-3]。但是,遗憾的是术前放疗不仅不能改善总生存率,而且还带来严重的远期毒性,使患者生存质量受到严重影响。从表1中可以看到接受放射治疗的患者出现严重影响生存质量的问题[1,4-5],如控便功能受损、性功能障碍和第二原发肿瘤发生率等至少是单纯手术患者的2~3倍,而且这些问题随时间而加重。本中心在国内较早开展术前放化疗,积累了很多经验,虽然我们看到了很多患者因为放疗使肿瘤退缩而获益,但是也观察到一定比例的患者因为放疗的远期毒性而痛苦不堪。这些棘手的问题促使研究者不停思考是不是所有局部进展期直肠癌患者都需要术前放疗;能否筛选一些复发风险较低的患者使之免受放疗的近期和远期的毒性。经过近10年的探索,目前对局部进展期直肠癌的新辅助治疗模式逐渐由原来的简单的“一刀切”演进为“分而治之”,即基于复发风险进行分层治疗的模式。
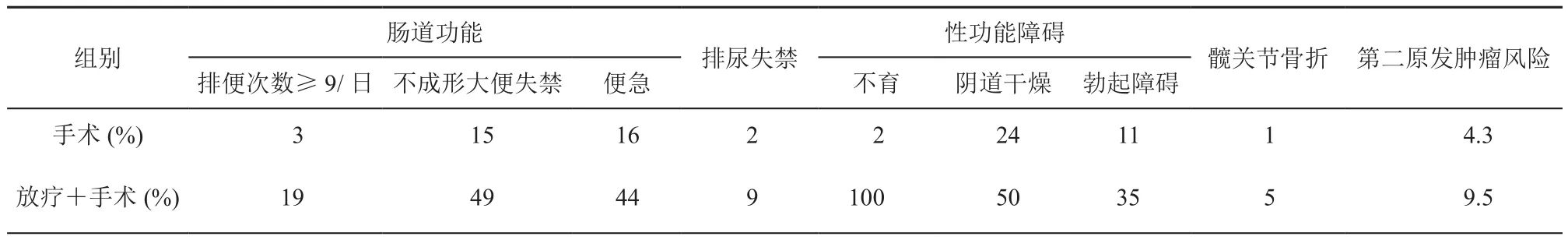
表1 放射治疗对远期生存质量的影响表
一、传统“局部进展期直肠癌”定义的局限性
不管是确立直肠癌新辅助放化疗地位的AIO-94研究[3],还是美国的NCCN指南,“局部进展期直肠癌”的定义都是非常粗糙的,凡是T3以上或淋巴结阳性都被归为“局部进展”并接受新辅助放疗。但临床试验的数据、解剖学和病理学的基础都显示这个群体异质性非常强,例如肿瘤的位置、肿瘤突破肌层的深度、环周切缘的状态等多种因素都与局部复发风险密切相关;特别是部分高位的T3N0患者,当不伴有其他高危因素(如环周切缘受侵),其局部复发风险不足5%,如果按照指南给予新辅助放疗势必对患者造成不必要的毒性并严重影响其远期的功能[6]。
二、对“局部进展期直肠癌”风险分层的可行性
对直肠癌进行分层治疗的关键是能够对患者的复发风险进行分层。既往采用超声内镜的分期方法难以进一步对复发风险进行分层,因此已逐渐被磁共振所替代。盆腔的磁共振(特别是高分辨率磁共振),除了常规的T和N分期之外,在T3的亚分期、环周切缘受累情况、腔外脉管侵犯(EMVI)、以及盆腔淋巴结转移具有非常明显的优势。MERCURY研究显示[7],壁外浸润深度(T3亚分期)是局部进展期直肠癌独立的预后预测因子,肌层外浸润深度5 mm以下者(T2, T3a/b)与浸润深度超过5 mm者(≥T3c)的5年无复发生存率分别为85%和54%;前者局部复发率仅为3%,提示给予新辅助治疗的获益可能性不大。研究同时证实高分辨率MRI判断浸润深度的准确性与组织病理的差异只有±0.5 mm(95%CI:-0.49~0.40 mm),提示MRI作为精准分期手段的可靠性。
三、风险分层与新辅助治疗策略
ESMO直肠癌新辅助治疗模式是直肠癌分层治疗策略的典范[8]。该策略以临床参数(治疗位置)和高分辨率磁共振参数(T分期、N分期、CRM/ MRF、EMVI和侧方淋巴结)作为风险分层指标,将直肠癌分为低危、中危和高危三组。低危患者推荐直接接受手术,手术后根据病理是否存在不良预后因素(如CRM +,N2)决定是否给予放化疗;中危患者推荐给予短程放疗;高危患者则推荐长程放化疗;对年老或身体状态无法耐受长程同期放化疗者亦可采用短程放疗并延长等待手术时间的策略。(表2)
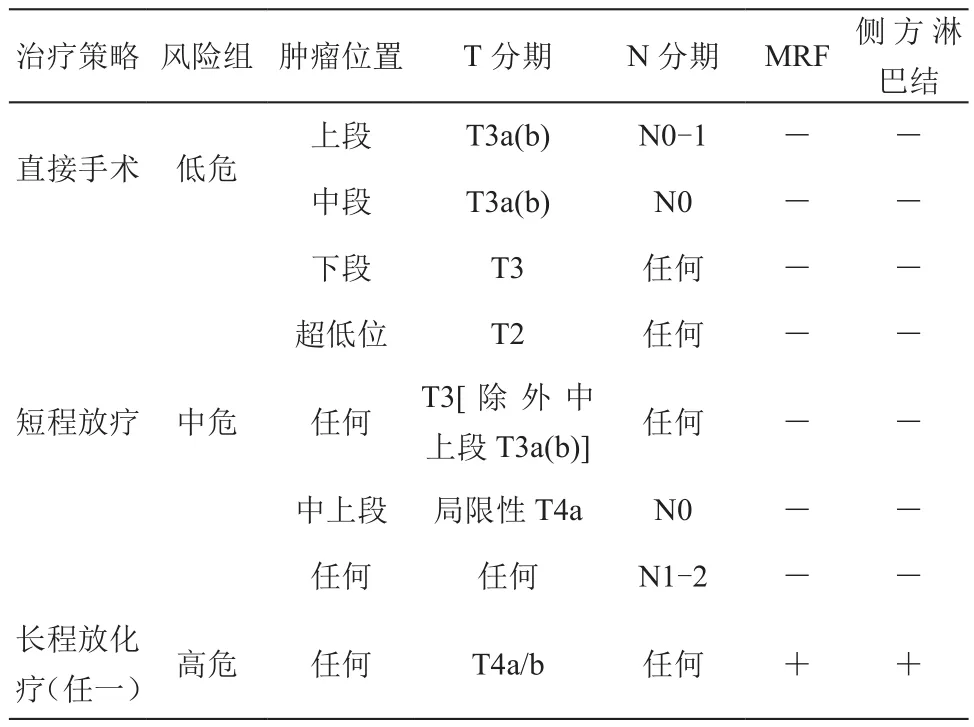
表2 风险分层及对应治疗策略表
这种策略的优点在于使部分患者避免了放疗的毒性,从而避免对远期生存质量的影响。与NCCN指南相比在直肠癌的个体治疗方面又迈进了一步(表3)。但是,ESMO策略的的缺点在于仍然过于依赖放射治疗,除了少数低位的患者避免放疗之外,其他大多数的局部进展期直肠癌仍然被推荐接受放射治疗;另一方面是对治疗团队要求较高,实施较复杂。目前我们国家的实际情况是多数医院甚至连术前放疗都没有开展,而即使是开展了术前放疗的中心多数都仅采用一种模式(长程或者短程)。这势必造成了患者的治疗过度或者不足,即在开展短程放疗的中心,指南中推荐长程放疗的患者(高危组)多数仅接受了短程放疗(治疗不足);而在开展长程放疗的中心,指南中推荐短程放疗的患者(中危组)接受了长程放疗(治疗过度)。
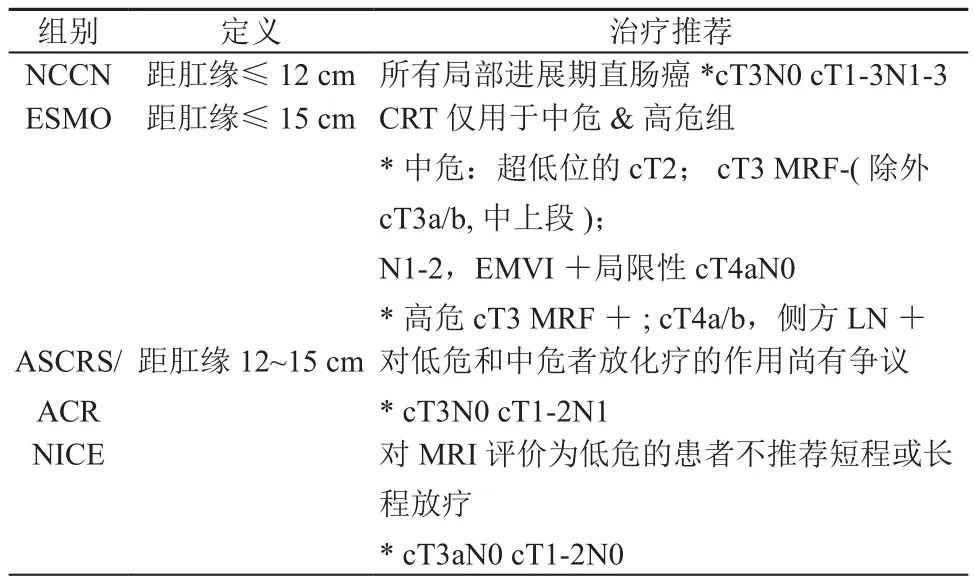
表3 不同指南对直肠癌的治疗推荐表
四、避免放射治疗毒性的新辅助治疗策略
直肠癌新辅助化疗是近年提出并逐渐被接受的新的治疗模式。最初,研究者发现转移性结直肠癌有效的化疗不仅能使转移灶退缩,原发灶也常同时出现退缩。理论上,新辅助化疗具有明显的优势,因为它比新辅助放疗或放化疗具有更强的全身控制效果,能够更有效的杀灭微转移从而降低远处转移的风险;另一方面,新辅助化疗后原发灶退缩理论上也可降低局部复发的风险。第一个提出新辅助化疗并前瞻性验证其有效性的研究来自美国纪念斯隆凯特琳癌症中心[9]。研究纳入32例“中低危”的局部进展期直肠癌,接受FOLFOX(6程)+ / -贝伐珠单抗(4程)的治疗,结果25%患者病理完全缓解;经过4年随访无一例发生局部复发,4年无病生存率为84%,4年总生存率为91%。单纯新辅助化疗的疗效完全可以与传统的放化疗媲美。研究结果让令医学界十分振奋,也开启了一系列的局部进展期直肠癌新辅助化疗的随机对照研究。2015年,我国学者汪建平教授率先在美国ASCO年会上报告了局部进展期直肠癌新辅助化疗对比传统放化疗的随机对照研究[10],结果单纯新辅助化疗组病理完全缓解率为6.1%,肿瘤退缩0~1级比例达到32.5%,再次证实单纯新辅助化疗对一部分患者具有显著的效果。考虑到该研究纳入了所有局部进展期的患者(包括高危组甚至T4b的患者),笔者推测如果将入组人群限制为中低危组,获得病理完全缓解或理想退缩的比例可能更高。目前的难点在于我们没有确切的手段预测能从单纯化疗中获益的人群,因此仍然要回归到ESMO的风险分层方法。从目前有限的数据及多数专家的意见来看,中危组可能是接受新辅助化疗的理想人群;高危组如果选择化疗作为初始治疗,在完成诱导化疗后仍然建议给予放疗。
五、加强全身控制和(或)改善肿瘤退缩的新辅助治疗策略
新辅助放疗备受诟病的原因之一在于其对全身微转移的控制不力,表现为未能改善总生存率。为此,研究者尝试将全身化疗前移到手术前。代表性的策略包括放疗之前的诱导化疗和放疗之后的巩固化疗。
尽管诱导化疗理论上能早期给予全身化疗,加强微转移的控制,而且肿瘤退缩后能改善局部血供从而改善放射治疗的效果。但是Ⅱ期随机对照研究[9]的结果显示,不管是局部肿瘤退缩还是远期生存,诱导化疗都不优于传统放化疗。
巩固化疗是在放疗结束后到手术之间的等候期给予的化疗,其主要目的也是加强全身控制和改善局部肿瘤退缩。2015年Lancet Oncol上发表了一项研究[11],比较放化疗结束后给予0~6程的mFOLFOX6方案的巩固治疗对肿瘤退缩的影响,随着巩固治疗时间的延长,病理完全缓解率相应改善;给予6程巩固治疗组的病理完全缓解率显著高达38%,而传统放化疗病理完全缓解率仅有18% (P=0.0036),优势十分明显。这种策略能否改善远期生存尚有待长期的随访结果。对于需要肿瘤退缩程度更明显者(例如治疗前局部侵犯严重的患者)或者选择watch & wait策略的患者,巩固化疗不失为合理的选择。
巩固化疗的另一种巧妙地策略是在短程放疗结束后不马上进行手术,而是将全身化疗提前到手术之前。这种策略具有传统短程放疗所不具备的局部肿瘤退缩的优势,而且全身化疗提前理论上能够更有效的杀灭潜在的微转移,可谓“一石二鸟”。2016年ASCO GI报告了一项来自波兰Ⅲ期随机对照研究[12],比较短程放疗序贯化疗与传统的放化疗,515例局部晚期直肠癌患者(cT3或cT4期)随机分配到试验组:5×5 Gy放疗,休息1周后行3周期FOLFOX4方案[5-氟尿嘧啶(5-FU)+四氢叶酸+奥沙利铂]化疗,或对照组:50.4 Gy (28 f),同时行5-FU +四氢叶酸+奥沙利铂化疗(对照组)。经过中位时间为35个月的随访,两组的R0切除率、病理完全缓解率、无疾病生存率、局部复发率、远处转移率均无显著差异率;试验组3年总生存率优于对照组(73% vs 65%,P=0.046)。该研究的现实意义在于这种策略在疗效上不劣于(甚至优于)传统治疗模式,而毒性反应更低、治疗更加方便,而且花费更少。因此在资源有限的情况下,这种治疗方法具有非常高的实用价值。
综上所述,局部进展期直肠癌的新辅助治疗十分复杂。只有兼顾根治性和远期功能的保存才是理想的策略。在进行决策时需要包括影像科医生、放疗、化疗及外科在内的多学科团队参与,根据精确的术前分期、治疗目标及依从性选择合适的新辅助治疗策略。
参 考 文 献
[ 1 ] van Gijn, W., Marijnen, C. A., Nagtegaal, I. D., et al.Preoperative radiotherapy combined with total mesorectal excision for resectable rectal cancer: 12-year follow-up of the multicentre, randomised controlled TME trial [J]. Lancet Oncol, 2011, 12(6): 575-582.
[ 2 ] Kapiteijn, E., Marijnen, C. A., Nagtegaal, I. D., et al. Preoperative radiotherapy combined with total mesorectal excision for resectable rectal cancer [J]. N Engl J Med, 2001, 345(9): 638-646.
[ 3 ] Sauer, R., Becker, H., Hohenberger, W., et al. Preoperative versus postoperative chemoradiotherapy for rectal cancer [J]. N Engl J Med, 2004, 351(17): 1731-1740.
[ 4 ] Wibe, A., Law, W. L., Fazio, V., et al. Tailored rectal cancer treatment--a time for implementing contemporary prognostic factors [J]? Colorectal Dis, 2013, 15(11): 1333-1342.
[ 5 ] Bruheim, K., Guren, M. G., Dahl, A. A., et al. Sexual function in males after radiotherapy for rectal cancer [J]. Int J Radiat Oncol Biol Phys, 2010, 76(4): 1012-1017.
[ 6 ] Wang, Q. X., Li, S. H., Zhang, X., et al. Identification of locally advanced rectal cancer with low risk of local recurrence [J]. PLoS One, 2015, 10(1): e0117141.
[ 7 ] Taylor, F. G., Quirke, P., Heald, R. J., et al. Preoperative high-resolution magnetic resonance imaging can identify good prognosis stage I, II, and III rectal cancer best managed by surgery alone: a prospective, multicenter, European study [J]. Ann Surg,2011, 253(4): 711-719.
[ 8 ] Glimelius, B., Tiret, E., Cervantes, A., et al. Rectal cancer: ESMO Clinical Practice Guidelines for diagnosis, treatment and follow-up [J]. Ann Oncol, 2013, 24 Suppl 6: vi81-88.
[ 9 ] Fernandez-Martos, C., Pericay, C., Aparicio, J., et al. Phase II,randomized study of concomitant chemoradiotherapy followed by surgery and adjuvant capecitabine plus oxaliplatin (CAPOX) compared with induction CAPOX followed by concomitant chemoradiotherapy and surgery in magnetic resonance imaging-defined,locally advanced rectal cancer: Grupo cancer de recto 3 study [J]. J Clin Oncol, 2010, 28(5): 859-865.
[ 10 ] YH, Deng, P, et al. A multi-center randomized controlled trial of mFOLFOX6 with or without radiation in neoadjuvant treatment of local advanced rectal cancer (FOWARC study): Preliminary results [J]. in asco. 2015, Chicago.
[ 11 ] Garcia-Aguilar J, Chow OS, Smith DD,et al.Effect of adding mFOLFOX6 after neoadjuvant chemoradiation in locally advanced rectal cancer: a multicentre, phase 2 trial [J]. Lancet Oncol, 2015,16(8): 957-966.
[ 12 ] Bujko, Krzysztof. Neoadjuvant chemoradiation for fixed cT3 or cT4 rectal cancer: Results of a Polish II multicentre phase III study [J]. ASCO GI, 2016, San Francisco.
(本文编辑:关旭)
丁培荣. 局部进展期直肠癌新辅助治疗的策略:分而治之[J/CD].中华结直肠疾病电子杂志, 2016, 5(3): 210-213.
Tailored neoadjuvant therapy for locally advanced rectal cancer
Ding Peirong. Department of Colorectal Surgery, Sun Yat-Sen University Cancer Center, Guangzhou 510060, China
Corresponding author: Ding Peirong, Email: dingpr@sysucc.org.cn
【Abstract】Neoadjuvant chemoradiotherapy has been proved to be effective in reducing the risk of local recurrence and became part of the standard therapy for locally advanced rectal cancer. However, the strategy does not improve overall survival.Moreover, the functional outcome and quality of life is significantly worse than surgery alone. This article will introduces the advances of neoadjuvant chemoradiotherapy and its effect on clinical practice.
【Key words】Rectal neoplasms; Magnetic resonance imaging; Neoadjuvant; Individualize
DOI:10.3877/cma.j.issn.2095-3224.2016.03.003
作者单位:510060 广州,中山大学附属肿瘤医院结直肠外科
通讯作者:丁培荣,Email:dingpr@sysucc.org.cn
收稿日期:(2016-04-21)
