PEI@SiO2材料的合成及其对CO2的吸附性能
2016-06-28周琳,刘苗,毕蓉,刘超
周 琳,刘 苗,毕 蓉,刘 超
1.桐城师范高等专科学校,安徽桐城,231400;2.宿州学院化学化工学院,安徽宿州,234000
PEI@SiO2材料的合成及其对CO2的吸附性能
周琳1,刘苗2,毕蓉2,刘超2
1.桐城师范高等专科学校,安徽桐城,231400;2.宿州学院化学化工学院,安徽宿州,234000
摘要:为了解决工业上常用胺溶液吸收CO2腐蚀性强和能耗高等问题,用聚乙烯亚胺 (PEI)修饰硅藻土制备成新材料PEI@SiO2复合材料。经化学表征,PEI@SiO2复合材料中PEI被成功地复合到硅藻土中,且新材料孔隙具有良好的孔隙结构,比表面积大,有利于气体流通,对CO2可有效地吸附,最大吸附量达到:0.96 mmol/g。
关键词:硅藻土;PEI;CO2;吸附性能
近年来,随着化石燃料的大量使用,二氧化碳气体的排放量与日俱增,随之而来的温室效应也越来越引起人们的关注。越来越多的人开始相信温室效应的出现是由于二氧化碳这一类温室气体的排放所造成的[1],这也使得人们开始重点关注如何有效减少二氧化碳的排放与已有二氧化碳的捕捉[2]。
对于捕捉CO2来说,使用固体吸附剂是一个很好的选择,通过反应过程将二氧化碳转化为固体形式,便于存储、使用和运输。现今国内外用于吸收CO2的各种材料有金属氧化物类、陶瓷材料及纤维类等,但总体上存在以下问题:吸附量偏低的材料易合成、原料来源广、技术成熟,吸附量偏高的材料费用高、能耗大、合成条件苛刻且反应过程不易控制。 因此,寻找吸附量高、污染低、成本低且可以大规模应用于工业生产的二氧化碳固体吸附剂,成为学界研究的热点之一。为寻找此类吸附剂,学界进行大量的探索,其中一些天然矿物材料具有大比表面积、成本低廉、吸附性优良、无二次污染等优点,已引起学界的广泛关注,尤其这些天然矿物质经改性后,吸附性能更加优越,有的已被广泛应用于治理水体污染。聚乙烯亚胺(PEI)是一种富含氨基的碱性聚合物,由于其带有大量的正电荷、良好的水溶性以及疏水碳链,PEI已经被证明在环境污染物的吸附结合上有优良的性能[3],被广泛使用于二氧化碳和酚类污染物的吸附材料制备中。因此,本文采用共沉淀技术实现PEI与硅藻土的有效复合,形成有机无机复合材料,并研究该复合材料对大气二氧化碳的吸附能力和性能。
1实验步骤
1.1PEI@SiO2复合材料合成
20g硅藻土被分散在1000mL2mol/L盐酸水溶液中,加热到363K在500rpm转速下磁力搅拌24h。之后,离心去残渣,制备成为17.66g/L硅源溶液,再加入0.21MPEI充分混合后,用1MHCl调节pH至10,陈化24h,所得沉淀即为PEI@SiO2有机无机复合材料。材料经多次水洗,离心去除残留的PEI,形成悬浮液用于吸附CO2。
1.2PEI@SiO2复合材料的表征
1.2.1红外分析
取PEI@SiO2和硅藻土粉末、PEI分别和KBr粉末一起研磨,混合均匀,压片后在红外光谱仪上测定样品的红外光谱。
1.2.2热重分析
分别将PEI@SiO2和SiO2干粉充分研磨后,于烘箱中110 ℃ 条件下烘干1h,取5~10mg粉末用于热重分析,以N2载气,流速100mL/min,50℃开始以10℃/min速度升温至1000℃。
1.2.3BET比表面积
取500mgPEI@SiO2粉末研磨,N2环境下,150℃在BET比表面积分析仪上测定其表面积和BJH孔及其分布。
1.3PEI@SiO2复合材料对二氧化碳的吸附
采用热重分析仪测定材料吸附二氧化碳量。分别选取10mgPEI@SiO2材料粉末,放入热重分析仪吸附测定。首先在150℃下通入N230min去除材料自身在空气中吸附的二氧化碳,记录样品重量为W0。待温度降为25℃后,以30mL/min的气流速度通入二氧化碳气体,30min后停止,计算样品重量增加值为Wt,则二氧化碳吸附量为 (Wt-W0)/W0。
2结果分析
2.1材料表征2.1.1FT-IR分析
与PEI红外谱图比较(图1),PEI@SiO2出现了PEI特征峰,如位于2917cm-1的C-H伸缩振动峰,2819cm-1的C-H伸缩振动峰,1756cm-1的-NH2和-NH-折叠振动峰,1472cm-1的-NH2和-NH-折叠振动峰,1290cm-1的-NH2和-NH-折叠振动峰,这些特征峰均表明PEI被成功复合到了硅藻土材料中。

图1 PEI(1)和PEI@SiO2(2)的红外图谱
2.1.2综合热分析
从综合热分析结果发现(图2、图3),PEI@SiO2材料的热分解分为三步:第一步发生于40℃~200℃,可能是材料在空气中吸附的水分和材料结晶水的去除造成的结果[4]。第二步发生于200℃~400℃,可能是Al2O3材料的分解以及PEI中支链分解造成的。第三步发生于400℃~500℃之间,可能是PEI直链分解造成的。这与已有无定形硅材料的热分析结果类似[5],PEI@SiO2材料失重达到25.3%,这与元素分析结果相似。硅藻土材料的热分解分为两步:第一步发生于40℃~200℃,可能是材料在空气中吸附的水分和材料结晶水的去除造成的结果[6]。第二步发生于200℃~500℃之间,可能是Al2O3材料的分解。硅藻土与PEI@SiO2材料的热分析结果存在差异,是由于PEI复合进入材料造成的。

图2 PEI@SiO2的热分析图

图3 硅藻土的热分析图
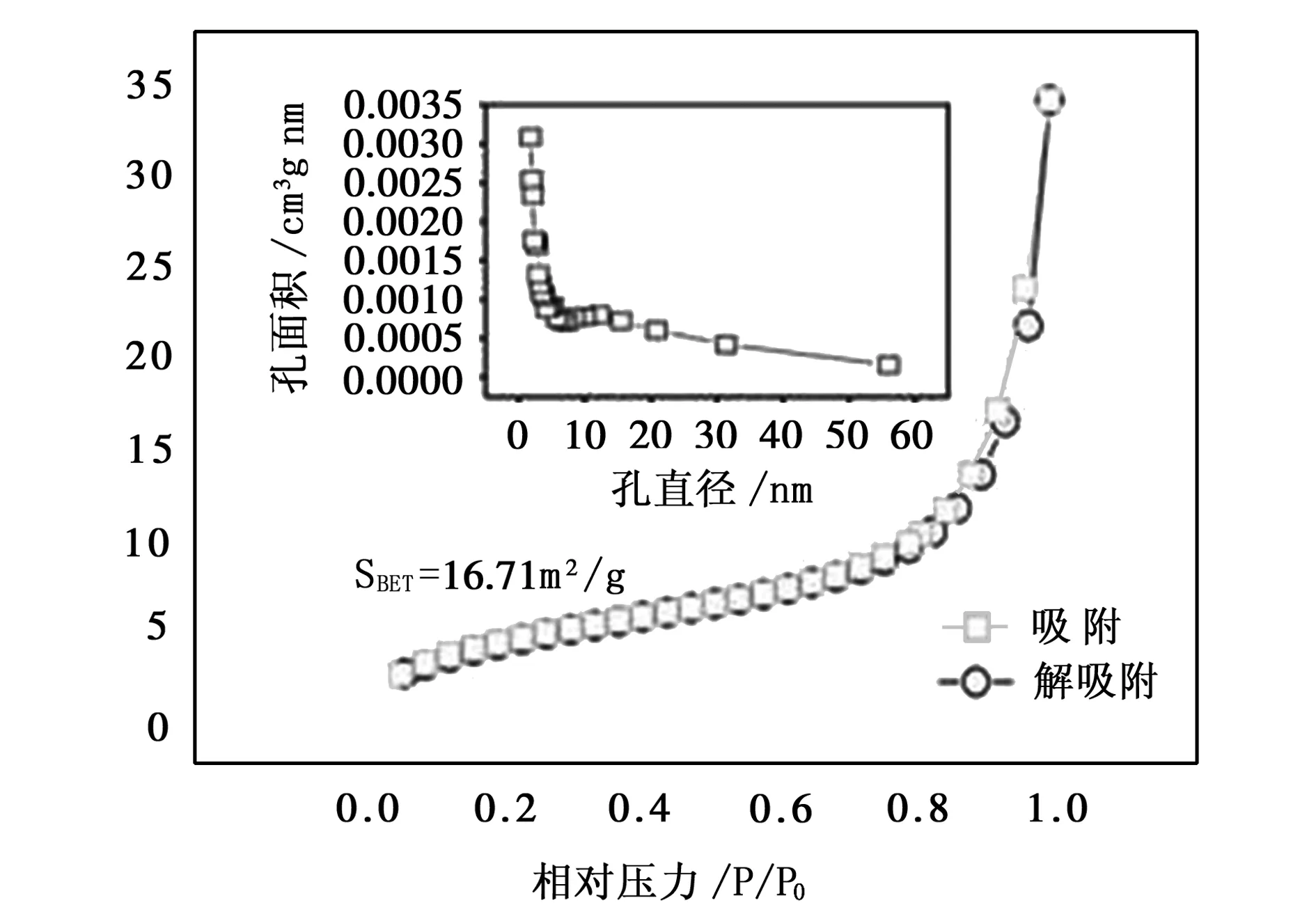
图4 PEI@SiO2材料的BET分析和孔径分布分析
2.1.3BET比表面积分析
由图4发现,PEI@SiO2材料的迟滞回线是Ⅳ型,这说明PEI@SiO2材料表现出介孔材料的性状。并且迟滞回线具有两个迟滞环,且属于不同类型:第一个迟滞环是位于相对压力0.8~0.9之间,为H1型,这说明在材料的内部具有圆柱形微孔结构[7]。第二个迟滞环位于相对压力0.9~1.0之间,为H3型,说明在材料内部具有裂隙孔[7]。孔径分布图可以发现,PEI@SiO2材料的孔径分布没有显著的峰,这暗示材料中存在的孔径为不规则尺寸。PEI@SiO2的比表面积为16.71m2/g。
2.1.4电镜扫描图谱分析
图5所示为硅藻土与PEI@SiO2的扫描电镜图。其中,图(A)显示的是未经PEI修饰的硅藻土,从图中可以明显地看出SiO2颗粒的表面极其粗糙且凹凸不平;图(B)经过PEI修饰后的PEI@SiO2,从图中不难看出,硅藻土经由PEI修饰之后表面明显变得更为光滑。综上所述,PEI确实起到了很好地修饰硅藻土的作用。

图5 硅藻土(A)与PEI@SiO2(B)的扫描电镜图谱
2.2二氧化碳吸附性能
由于PEI上具有大量的伯胺(RNH3)和仲胺 (R2NH),很容易与二氧化碳气体发生反应,对二氧化碳有很好的吸附作用,因此,PEI@SiO2材料对二氧化碳气体具有较强的吸附能力。具体吸附原理见公式(1)。
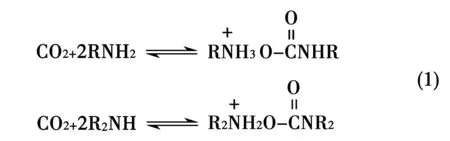
已有研究表明,CO2可以与氨基通过较弱的化学键结合生成氨基甲酸酯的离子[8]。本实验中,硅藻土材料对于CO2的吸附量达到0.69mmol/g,远大于已有报道的无机吸附材料[9]。这主要是因为硅藻土材料具有良好的孔隙结构,有利于通过物理吸附作用吸附二氧化碳气体。当PEI成功复合进入硅藻土材料中后,PEI@SiO2材料对二氧化碳吸附达到0.75mmol/g。一方面是因为PEI的复合增大了材料的比表面积,吸附二氧化碳的空间更大;另一方面由于PEI自身与二氧化碳具有化学反应能力,增加了材料的化学吸附性能。
最近的研究发现,PEI的加载能够提高材料吸附气体的能力,但是会阻碍气体在材料孔隙内部的流通。Double-exponential(DEM)模型被用来拟合PEI@SiO2材料对二氧化碳的吸附,具体模型见公式(2)。
qt=qe-D1exp(-K1t)-D2exp(-K2t)
(2)
D1(mg/g)和K1(min-1)分别表示快速吸附量和快速吸附时的弥散系数,D2和K2表示慢速吸附量和慢速吸附时的弥散系数。该模型适用于吸附剂同时具有两种吸附类型的吸附,即快和慢两个吸附步骤,其中化学吸附属于快速吸附,而物理吸附属于慢速吸附[10]。如图5和表1所示,在25、50、75和100℃下PEI@SiO2材料对二氧化碳的吸附行为符合DEM模型,其R2均大于0.9。吸附量随着温度的升高呈现为先增加后下降的趋势,在50℃时达到了最大吸附量0.96mmol/g。

图6 在25℃(1)、50 ℃(2)、75 ℃(3)和100 ℃(4)下PEI@SiO2对二氧化碳吸附拟合
在75℃和100℃下,PEI@SiO2材料对二氧化碳的吸附在5min内达到平衡,而随着温度的降低材料对二氧化碳的吸附速率降低,在25℃和50℃下材料对二氧化碳的吸附在15min之后达到平衡。通过弥散系数K1和K2发现,这主要是因为温度降低减缓了二氧化碳气体在材料内流通速率,这与已有的研究结果相一致[10]。并且通过图6可以看出,PEI@SiO2对二氧化碳的吸附平衡时间为18min,而硅藻土对二氧化碳的吸附平衡时间达到35min,表明PEI的存在提高了材料的吸附速率。
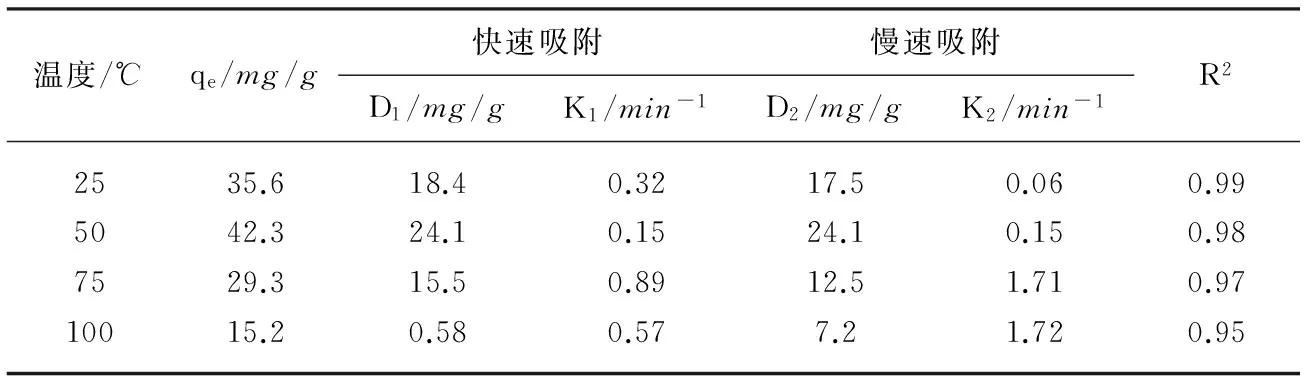
表1 通过DEM模型拟合的二氧化碳吸附相关系数
3结 论
本实验将PEI嵌入硅藻土中,制备了一种新型复合材料PEI@SiO2,该材料对二氧化碳具有良好的吸附能力。将原硅藻土单纯的物理吸附转变为物理吸附和化学吸附共同作用的吸附方式,赋予更多的性能,适用于工业化生产流程。由于PEI所带有的多氨基基团,使得PEI@SiO2对二氧化碳气体具有良好的吸附能力,50℃下吸附量达到0.94mmol/g。PEI@SiO2材料对二氧化碳的吸附在30min之内可以完成。由此可见,在未来的很长一段时间内, 开发物理及化学性能稳定且具有最佳吸附结构的复合吸附材料,将是该领域的研究热点和主要方向。
参考文献:
[1]YueMB,CHUNYuan,CAOYi,etal.CO2capturebyAs-preparedSBA-15withanoccludedorganictemplate[J].AdvancedFunctionalMaterials,2006,16(13):1717-1722
[2]OjuvaA,AkhtarF,TomsiaAP,etal.LaminatedadsorbentswithveryrapidCO2uptakebyfreeze-castingofzeolites[J].ACSAppliedMaterials&Interfaces,2013,5(7):2669-2676
[3]GhoulM,BacquetM,MorcelletM.UptakeofheavymetalsfromsyntheticaqueoussolutionsusingmodifiedPEI-silicagels[J].WaterResearch,2003,37(4):729-734
[4]ZhuravlevLT.Thesurfacechemistryofamorphoussilica.Zhuravlevmodel[J].ColloidsandSurfacesA-PhysicochemicalandEngineeringAspects,2000,173(1/3):1-38
[5]CHENK-t,LUC-s,CHANGT-h,etal.ComparisonofphotodegradativeefficienciesandmechanismsofVictoriaBlueRassistedbyNafion-coatedandfluorinatedTiO2photocatalysts[J].JournalofHazardousMaterials,2010,174(1/3):598-609
[6]张婷,李望良,唐煌,等.生物再生—吸附剂再生新方法[J].化工学报,2009,60(9):2145-2152
[7]WickramaratneNP,JaroniecM.ImportanceofsmallmicroporesinCO2capturebyphenolicresin-basedactivatedCarbonspheres[J].JournalofMaterialsChemistrya,2013,1(1):112-116
[8]GuiMM,YapYX,ChaiSP,etal.Multi-walledCarbonnanotubesmodifiedwith(3-aminopropyl)triethoxysilaneforeffectiveCarbondioxideadsorption[J].InternationalJournalofGreenhouseGasControl,2013,14(1/3):65-73
[9]QiangWang,HuiHuangTay,ZiyiZhong,etal.Synthesisofhigh-temperatureCO2adsorbentsfromorgano-layereddoublehydroxideswithmarkedlyimprovedCO2capturecapacity,Energy&EnvironmentalScience,2012,5(6):7526-7530
[10]CHENZhenhe,DENGShubo,WEIHaoran,etal.Polyethylenimine-impregnatedresinforhighCO2adsorption:anefficientadsorbentforCO2capturefromsimulatedfluegasandambientair[J].ACSAppliedMaterials&Interfaces,2013,5(15):6937-6945
(责任编辑:汪材印)
doi:10.3969/j.issn.1673-2006.2016.05.033
收稿日期:2016-01-25
基金项目:安徽省自然科学基金项目“极性功能基多孔配位聚合物的设计、合成及二氧化碳吸附分离性能的研究”(1508085QB36);国家级大学生创新创业训练计划项目“新型亚胺类钴金属配合物催化性能研究及催化技术推广”(201510379006);宿州学院产学研基金项目“含N杂环亚胺配体过渡金属配合物催化烯烃聚合技术研究”(2015hx014);桐城师专教科研项目“环境污染对湖泊水质的影响及其治理策略——以桐城市为例”(tcszky005)。
作者简介:周琳(1980-),安徽桐城人,硕士,讲师,主要研究方向:材料化学。
中图分类号:O643.36
文献标识码:A
文章编号:1673-2006(2016)05-0123-04
