159例氟喹诺酮类抗菌药物不良反应调查
2016-06-03吕长淮
吕长淮
(宿州市食品药品检验所化学室,安徽 宿州 234000)
159例氟喹诺酮类抗菌药物不良反应调查
吕长淮*
(宿州市食品药品检验所化学室,安徽 宿州234000)
DOI10.14009/j.issn.1672-2124.2016.04.045
摘要目的:了解氟喹诺酮类抗菌药物引发的药品不良反应(adverse drug reaction,ADR)情况,为临床合理用药提供参考。方法:对宿州市市立医院2014年2月—2015年2月159例氟喹诺酮类抗菌药物引发的ADR情况进行回顾性分析。结果:由左氧氟沙星引发的ADR例次最多(58例,36.48%),其次是环丙沙星(43例,27.04%);静脉滴注引发的ADR高于口服和静脉注射;>60岁患者引发的ADR占62.26%,≤60岁的患者占37.74%,说明年龄越大越易引发ADR。ADR涉及的头疼、失眠等症状较多(39.62%),皮疹、皮肤过敏等症状次之,占22.64%,明显高于其他系统。结论:氟喹诺酮类抗菌药物所引发的ADR,必须引起医务人员高度重视,切实降低其ADR发生率,确保临床用药安全。
关键词氟喹诺酮类抗菌药物; 不良反应; 调查分析
氟喹诺酮类抗菌药物是一类较新的化学合成广谱抗菌药物,目前被广泛应用于呼吸系统、消化系统、泌尿系统及皮肤软组织等感染性疾病的治疗[1]。但随着该类药被广泛应用于呼吸系统、消化系统、泌尿系统及皮肤软组织等感染的治疗[1],有关其药品不良反应(adverse drug reaction,ADR)的发生也越来越多。本调查分析了宿州市立医院氟喹诺酮类抗菌药物引发的ADR情况,旨在为临床合理用药提供参考。
1资料与方法
1.1资料来源
资料来源于宿州市立医院2014年2月—2015年2月的159例氟喹诺酮类抗菌药物ADR报告。其中,男性83例,占52.00%;女性76例,占48.00%;年龄在18~78岁之间,≤60岁的有60例,>60岁的有99例;上呼吸道和肺部感染46例,急、慢性泌尿生殖道炎症41例,细菌性腹泻41例,皮肤软组织疖肿31例。159例患者入院前均未使用过其他药物,剔除合并用药病例,入院后所使用的氟喹诺酮类抗菌药物为左氧氟沙星、环丙沙星、氟罗沙星、培氟沙星、洛美沙星及诺氟沙星6种。
1.2方法
采用回顾性方法对研究对象的临床资料进行整理,逐份阅读记录,针对患者的年龄、感染类型、给药方式、ADR出现时间、ADR所涉及的药物种类、ADR累及器官和(或)系统及临床表现等进行回顾性分析。
2结果
2.1ADR患者的年龄分布情况
本调查中,≤60岁的老年人中发生ADR的病例数为60例(占37.74%),>60岁者99例(占62.26%),>60岁者发生率明显多于≤60岁者,说明60岁以上老年人易发生ADR。
2.2ADR与给药方式
159例ADR中,口服给药方式所致ADR为28例(占17.61%),静脉给药方式所致ADR为131例(占82.39%),说明静脉给药方式比口服给药ADR的发生率高。
2.3ADR与用药时间
由于口服给药引发的ADR例数较少,故仅探讨131例静脉给药引发ADR的情况。其中,ADR出现时间≤1 d者79例(占60.31%),2~5 d者39例(占29.77%),≥6 d者13例(占9.92%)静脉给药引发的ADR大多出现在1 d内,且随着时间延长发生病例数减少。
2.4引发ADR的具体药品
左氧氟沙星引发的ADR病例数最多,其次是环丙沙星,氟罗沙星、培氟沙星、洛美沙星及诺氟沙星,见表1。
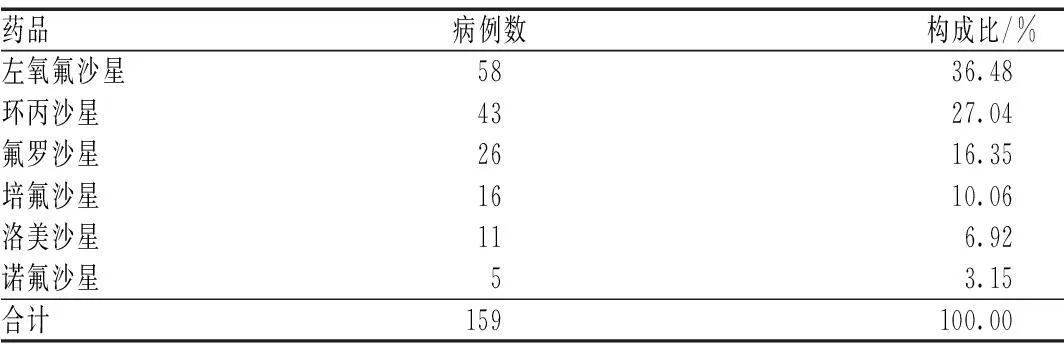
表1 引发ADR的具体药品
2.5ADR累及器官和(或)系统及临床表现
ADR累涉及的失眠、头痛、情绪异常等中枢神经系统症状为最多,占39.62%,其次为过敏、红斑、皮疹等皮肤及其附件(黏膜)的症状,占22.64%,明显高于其他系统,见表2。
3讨论
3.1氟喹诺酮类抗菌药物的结构与作用
氟喹诺酮类抗菌药物系第3代化学合成药,抗菌活性较强,对革兰阳性球菌、革兰阴性杆菌、衣原体、支原体、结核分枝杆菌均非常有效,特别是对肺炎双球菌、溶血性链球菌、军团菌、支原体、衣原体抗菌活性较强[2]。从化学结构上讲,主要是由于其6位引入了氟原子,7位增加了哌嗪环,能够高选择性地抑制细菌生长,抑制其脱氧核糖核酸(DNA)回旋酶及拓扑异构酶的活性,使细菌的DNA合成障碍,对处于活跃期、静止期阶段的细菌都有较强的杀灭作用[3-4]。鉴于其生物利用度高、抗菌谱广、血浆半衰期长,并具有口服片剂、静脉注射使用两种制剂,且不需做皮肤试验,所以广泛应用于临床[5]。近年来,随着氟喹诺酮类抗菌药物的应用广泛,其引发的ADR已受到临床医师的普遍关注。
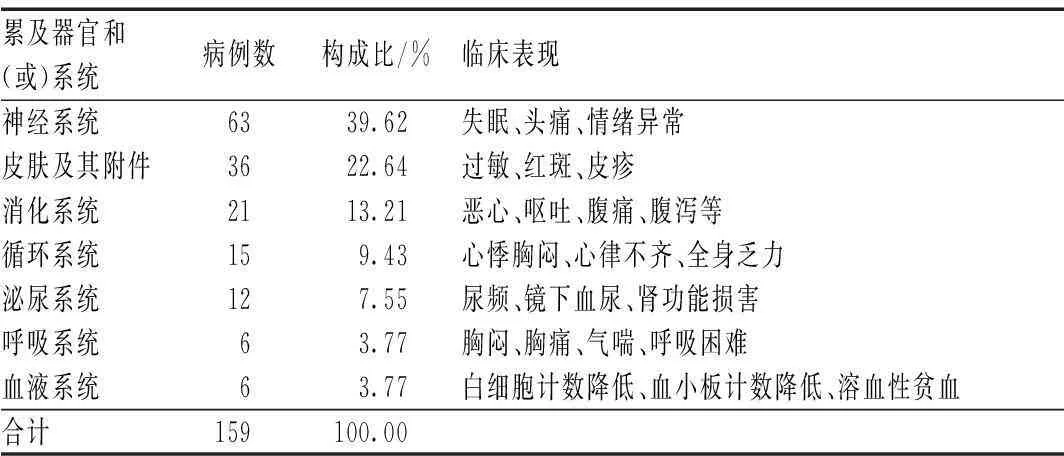
表2 ADR累及器官和(或)系统及临床表现
3.2ADR发生的年龄、给药方式、时间和种类
从表2中可以看出,左氧氟沙星引发的ADR病例数列首位,其次是环丙沙星。左氧氟沙星抗菌谱广、价格相对便宜,由于临床应用广泛,ADR随之升高,因此要严格其适应证。静脉滴注引发的ADR病例数明显高于口服给药,提示氟喹诺酮类药静脉滴注要注意滴速、输液前不宜空腹、输液过程中要注意观察。≥60岁的患者,ADR明显高于<60岁的患者,这是由于老年患者肝合成白蛋白功能下降,肝药酶作用下降,药物首关作用下降,肝功能衰退所致[6]。肾脏肾小球滤过功能下降,肾小管分泌功能下降,致肾功能逐渐衰退,极易引起体药物浓度增加和蓄积。所以,对于肝肾功能不全者,临床上应予以高度重视,要密切结合老年人的药物代谢特征,详细询问患者的病史,做到用药方案个性化,给药时应注意观察并适当减量,以最大限度地降低ADR的发生[7]。氟喹诺酮类抗菌药物引发的ADR出现时间≤1 d,ADR随着用药时间的增加而减少,提示用药后24 h内ADR的发生率较高,须密切注意观察。本调查结果与文献报道一致[8-10]。
3.3ADR累及器官和(或)系统及临床表现
本调查中,氟喹诺酮类抗菌药物引发的ADR涉及的失眠、头痛、情绪异常等中枢神经系统症状最多,占39.62%,过敏、红斑、皮疹等皮肤黏膜症状次之,占22.64%。提示必须注意该类药对中枢神经系统和皮肤黏膜方面的ADR。氟喹诺酮类抗菌药物及代谢产物特异性竞争性γ-氨基丁酸(GABA)受体,与GABA受体结合,使GABA受体活性受到抑制,导致中枢神经系统兴奋性增加,出现头痛、眩晕、睡眠障碍、情绪不稳、精神恍惚、视觉异常等方面的一系列症状[11];氟原子是能够通过血脑屏障进入脑细胞的原子,肝肾功能不全者还会引起大脑神经胶质细胞水肿,产生中枢神经系统症状[12-13]。有关皮肤的迟发变态反应,主要是涉及此类药的光过敏和光毒性,最易产生皮肤迟发变态反应的紫外线波长为315~400 nm,药物吸收紫外线后,会以半抗原形式与皮肤中的蛋白相结合,引起迟发变态反应,致使皮肤损伤[14]。有报道指出,该类药8位母核上有卤原子,且光毒性强(如克林沙星),如8位母核上无卤原子或连接了甲氧基则光毒性低(如莫西沙星)[15]。
通过对宿州市立医院2014年2月—2015年2月159例氟喹诺酮类抗菌药物ADR报告的分析,可知该类药引发的ADR必须引起医务工作者高度重视,原则是必须严格掌握用药指征,严格掌握药物的浓度和滴速,注意药物配伍,强化用药前后的护理和药物监测,以切实降低该类药ADR的发生率,确保临床用药安全。
参考文献
[1]肖永红,王进,朱燕,等.Mohnarin 2008年度全国细菌耐药监测[J].中华医院感染学杂志,2010,20(16):2377-2383.
[2]李振国,于文玫.氟喹诺酮类药品不良反应调查及临床合理用药的分析[J].中国医药指南,2014,12(17):25-26.
[3]庄秀怡.氟喹诺酮类药品不良反应的机制与化学结构关系的分析[J].抗感染药学,2014,11(2):162-164.
[4]张艳萍.氟喹诺酮类药品不良反应的机制与化学结构的关系[J].中外医疗,2014,4(7):130-132.
[5]李福长,曾明辉.氟喹诺酮类抗菌药物致药品不良反应205例调查分析[J].临床合理用药杂志,2012,3(5):40-41.
[6]宋伟杰.氟喹诺酮类药品不良反应的临床分析[J].中国现代药物应用,2015,9(15):158.
[7]徐辉.氟喹诺酮类药物临床常见不良反应分析[J].北方医学,2015,12(3):149-150.
[8]徐华涛.氟喹诺酮类药物临床不良反应及其合理用药分析[J].现代医药卫生,2014,30(24):3765-3766.
[9]苏坤华.我院氟喹诺酮类抗生素不良反应87例分析[J].临床合理用药杂志,2014,7(6):19-20.
[10]凌海鹰.我院氟喹诺酮类抗菌药物的不良反应及合理用药[J].海峡药学,2014,26(8):157-158.
[11]张波.氟喹诺酮类药物的临床应用与不良反应情况[J].中国现代继续医学教育,2015,7(25):179-180.
[12]步建设,袁德莲.氟喹诺酮类药品不良反应及其合理应用研究[J].中国现代药物应用,2013,7(2):122-123.
[13]王德华.氟喹诺酮类药物临床常见不良反应115例分析[J].内蒙古中医药,2013,32(22):79-81.
[14]俞春红,潘任桃,孙志良.氟喹诺酮类药物致神经系统和软骨毒性的机制研究进展[J].中国抗生素杂志,2013,38(11):810-813.
[15]陈园.氟喹诺酮类药品不良反应的机制与化学结构的关系[J].内蒙古中医药,2014,33(5):55-56.
Survey on 159 Cases of Adverse Drug Reaction Reports Induced by Fluoroquinolone Drugs in Suzhou Municipal Hospital
LÜ Changhuai
(Dept.Chemical Room, Anhui Suzhou Food and Drug Inspection, Anhui Suzhou 234000, China)
ABSTRACTOBJECTIVE:To investigate the status of adverse drug reaction(ADR) induced by fluoroquinolone drugs, and to provide reference for the rational drug use in clinic. METHODS: 159 cases of ADR induced by fluoroquinolone drugs in Suzhou Municipal Hospital from Feb. 2014 to Feb. 2015 were retrospectively analyzed. RESULTS: ADR induced by levofloxacin took the lead(58 cases, 36.48%), followed by ciprofloxacin(43 cases, 27.04%). Cases of ADR induced by intravenous drip were higher than that of oral and intravenous injection. Patients with ADR>60 years old was 62.26%, and ≤60 years old was 37.74%, which indicated that elderly patients had a high risk of ADR. The clinical manifestations of ADR were mainly headache and insomnia(39.62%), followed by skin rash, skin hypersensitivity(22.64%), significantly higher than other systems.CONCLUSIONS: Great attention should be given to ADR induced by fluoroquinolone drugs, so as to reduce the incidence of ADR and ensure the medication safety in clinic.
KEYWORDSFluoroquinolone drugs; Adverse drug reactions; Investigation and analysis
(收稿日期:2015-09-28)
中图分类号R969.3
文献标志码A
文章编号1672-2124(2016)04-0551-03
*主任药师。研究方向:药物分析。E-mail:lvchanghuai@126.com
