铈掺杂Bi2O3的制备及光催化性
2016-05-07姚威龙蒋琪英邓洪权刘学梅
王 松 姚威龙 蒋琪英,2 邓洪权 刘学梅 沈 娟
(1.西南科技大学材料科学与工程学院;2.西南科技大学生物质材料教育部工程研究中心)
铈掺杂Bi2O3的制备及光催化性
王松1姚威龙1蒋琪英1,2邓洪权1刘学梅1沈娟1
(1.西南科技大学材料科学与工程学院;2.西南科技大学生物质材料教育部工程研究中心)
摘要:通过微波水热辅助制备不同铈掺杂的氧化铋光催化剂。利用荧光光谱(PL)、X-射线粉末衍射(XRD)、傅里叶变换红外光谱(FT-IR)、紫外-可见漫发射光谱(Uv-vis DRS)等对催化剂物相和光谱特性进行了表征。结果表明,适量的铈掺杂能有效抑制Bi2O3由四方β相向单斜α相转变,并且能使Bi2O3光吸收范围拓展到更宽的可见区。甲基橙的光催化降解实验表明,铈掺杂后的Bi2O3具有更好的可见光催化性能,其中铈掺杂质量分数为2%的样品对甲基橙(20 mg/L)的催化效果最好,当添加量为1 g/L,中性环境中光照4 h后甲基橙的降解率可达85%。
关键词:Bi2O3铈微波水热法光催化
Bi2O3属于半导体氧化物,其价带由 Bi6s和O2p 轨道杂化而成, 这样价带很分散,有利于光生空穴的移动。通常存在4种主要晶相和2种非化学计量相,即单斜α-Bi2O3、四方体β-Bi2O3、立方γ-Bi2O3和面心立方δ-Bi2O3,禁带宽度分布范围较广(2~3.96 eV),在可见光范围内有良好的吸收[1]。其中,仅α-Bi2O3在室温能稳定存在,β相尽管具有最小的带隙,且催化活性最高,对可见光具有强吸收但在室温不能稳定存在。Bi2O3单独作为光催化剂对废水处理时存在两大缺陷:光生电子和空穴容易复合,光量子效率低;同时在反应过程中不稳定,先由β相变成α相,进而转变成碳酸氧铋(Bi2O2)CO3[2]。稀土掺杂是一种有效稳定Bi2O3晶相结构且能不同程度提高光催化效果的方式[3-5]。稀土离子具有特殊f 电子层结构,易产生多电子组态,其氧化物具有多晶型和电子型导电性的特点,可提供半导体表面光生电子的捕获陷阱,促进载流子转移和电荷有效分离,提高量子化效率;同时被捕获的电子易释放,可参加光催化反应,能有效提高光催化活性[6]。与其他稀土元素相比铈具有独特的4f13d14s2电子构型,可形成Ce3+/Ce4+氧化-还原偶对,促进氧空穴的形成及体相氧循环,提高催化剂的光催化活性,因此,铈成为了半导体氧化物的理想掺杂剂来提高电子的转移[7-8]。
催化反应是一个复杂过程,催化效果不仅与催化剂对光的吸收范围和强度有关,还与催化剂颗粒大小、比表面以及晶体缺陷等有关,而制备方法对催化剂结构和性能影响很大。水热法具有在低温高压作用下使粒径分布窄、形态均一、晶形完整等特点而广泛应用于制备各种氧化物。微波辐射作为一种新型的加热方式,使反应体系快速升温,加快反应速率,缩短反应时间,提高反应选择性,使受热体系均匀,同时可获得性能优异的新颖结构等,因而广泛应用于材料加工与合成等诸多方面[9-10]。本文将简单的水热法和快速的微波辐射结合形成的微波水热合成法用于对铈掺杂铋的前驱体进行处理,研究了不同掺杂量对Bi2O3的结构和性质的影响。
1实验
1.1试剂与仪器
Niconet 6700型傅里叶变换红外光谱仪(KBr 压片,4 000~400 cm-1), TA Q500热分析仪,Rigaku D/max-RB X射线衍射仪(靶材: 铜, Kα射线; 工作电压: 35 kV; 工作电流: 60 mA;3°~80°,4°/min),Hitachi Uv-3900紫外-可见光谱仪带积分球(200~800 nm, BaSO4为参比),Hitachi Uv-4500荧光光谱仪(200~800 nm),Cary50型分光光度计,SX2-4-10箱式电阻炉,TDL-80-2B低速离心机,自制列管式光催化反应器(365 nm光源,100 W),XH-800S-10型微波水热合成仪,马尔文MS2000激光粒度仪,Hitachi TM1000扫描电镜。
Bi(NO3)3·5H2O(AR),HNO3(AR),Ce(NO3)6·6H2O(AR),氨水(AR),甲基橙。
1.2铈掺杂氧化物的制备
称取一定量的硝酸铋溶于稀硝酸中,形成溶液A。按照Ce/Bi质量之比为0%,1%,2%,3%,4%的比例,分别称取一定量的硝酸铈铵溶于水中,形成溶液B。在室温下搅拌将上述溶液B加入溶液A中,用稀氨水调节溶液pH值为6~7,将得到的悬浊液置于压力容器中,填充度60%,然后置于微波水热合成仪中,于170 ℃保温1 h,待自然冷却后过滤,用蒸馏水洗涤沉淀,最后于100 ℃烘箱中将所得沉淀烘干得到铈掺杂的前驱体Bi(OH)3。将烘干的前驱体在一定温度下进行灼烧,即得不同铈量掺杂的Bi2O3催化剂粉末。
1.3光催化实验
将不同铈掺杂比例的Bi2O3光催化剂0.1 g加入100 mL浓度为20 mg/L的甲基橙水溶液中,此时溶液处于中性环境(pH值为6.5左右)。先避光曝气1 h使催化剂和甲基橙充分接触达到吸附平衡,然后用功率为100 W的卤素灯(中心波长365 nm)作为光源照射溶液,使其进行光降解反应,反应过程中持续曝气使整个溶液处于流化状态。每间隔1 h取大概5 mL左右溶液并高速离心分离,然后取上层清液测定样品的吸光度(465 nm)。根据溶液吸光度值,按如下公式计算甲基橙的降解率:
褪色率R(%)=(c0-ct)/c0×100%
=(A0-At)/A0×100%
(1)
式中c0,A0为光照前溶液的浓度(mg/L)和吸光度,ct,At光照时间t后溶液浓度(mg/L)和吸光度。
2结果与讨论
2.1前驱体的热稳定性
图1为不同量铈掺杂前驱体在氮气气氛下从室温到600 ℃范围以10 ℃/min的升温速率所得的TG曲线。从图1可以看出,当没有铈掺杂时,前驱体的起始热分解温度为360 ℃左右,最后在590 ℃分解结束,当铈掺杂后所得前驱体的热分解起始温度和结束温度都下降,但热分解趋势则基本相似,掺铈4%的前驱体最后稳定温度在535 ℃。由此可以说明,铈的掺杂可以降低前驱体的热稳定性。为考察掺杂量对Bi2O3的影响,同时考虑灼烧时前驱体用量比测TG时用量多,因此灼烧温度选在600 ℃进行,灼烧时间为1 h,灼烧所得粉末颜色随铈掺杂量增加由浅黄色到橘红色。
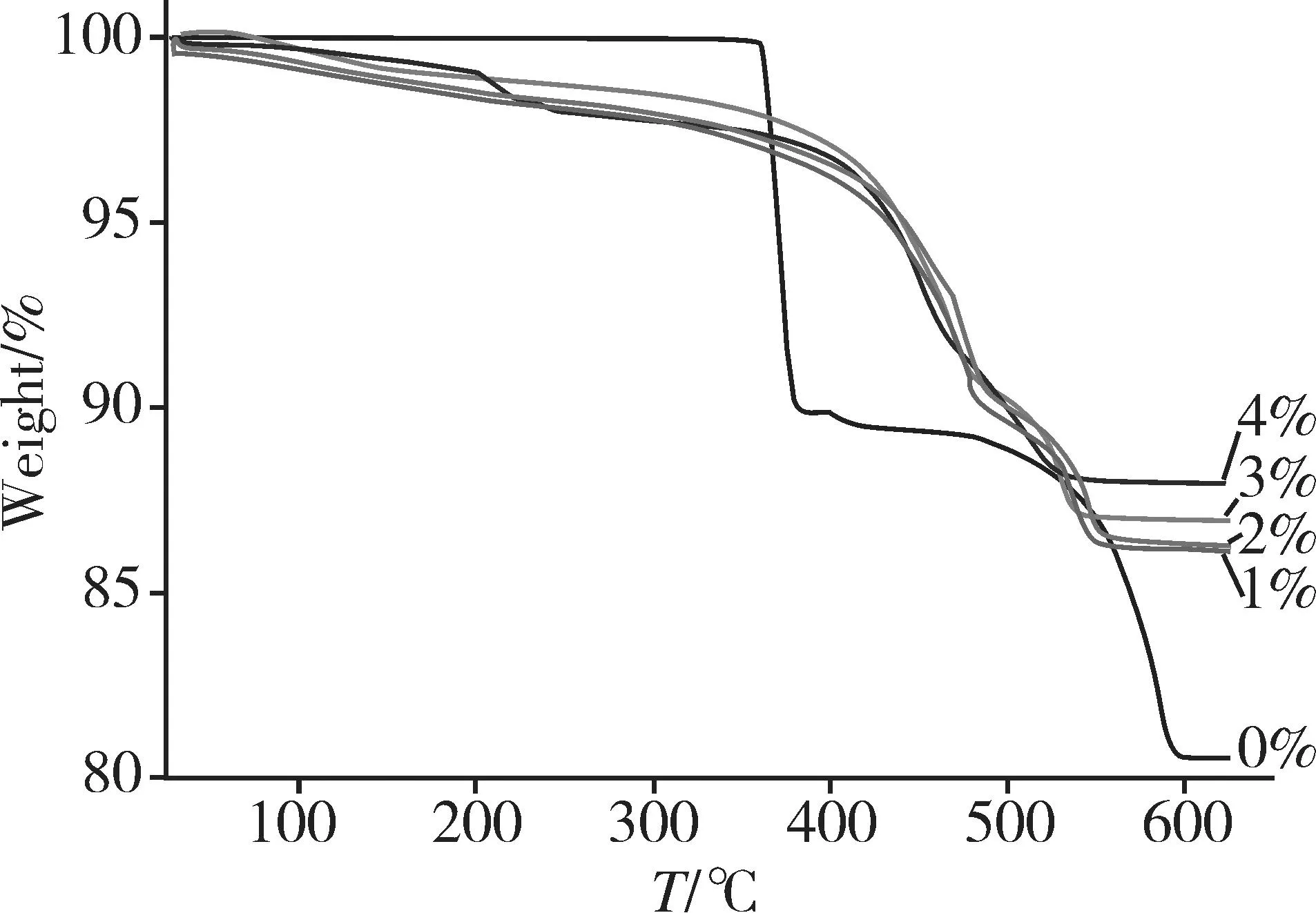
图1 前驱体的TG曲线
2.2铈掺杂对Bi2O3物相的影响
图2是灼烧1 h所得Bi2O3粉末的X粉末衍射图,其中内插图为所有Bi2O3粉末的红外光谱图。红外光谱图中,3 500 cm-1左右以及1 640 cm-1左右存在的弱吸收峰为样品吸附的游离水的O-H伸缩振动峰和H-O-H 的弯曲振动峰。在800~400 cm-1范围内存在红外吸收峰,其中0%,1%和2%3个样品的红外图谱一致,仅在550~400 cm-1区间出现归属于BiO6八面体中Bi-O键的红外吸收峰,而3%和4%两个样品的红外图谱中除与前3个样品相同的峰外,同时在600~750 cm-1间出现了归属于Ce-O的红外吸收峰[11-12]。从X粉末衍射图看,除2%掺杂量所得样品的衍射峰强度相对较弱外,其余各样品的特征衍射峰都很尖锐,说明前期通过微波水热方式处理后所制备的样品具有较高的结晶度。对比衍射峰位置发现,在所有粉末样品中并没有出现Ce及其氧化物的特征衍射峰,可能掺杂量太少或Ce4+在Bi2O3晶格中处于高度分散而没有检测出。该结果与Ce掺杂对ZnO催化剂物相的影响类似[11]。另外,从图2发现铈的掺杂对Bi2O3晶
相稳定性产生影响。前3个样品的XRD衍射峰与单斜α- Bi2O3的特征衍射峰(PDF No.76-1730)一致,而3%和4%铈掺杂所得粉末的X衍射峰数目和位置与前面3个相比发生了明显改变,其衍射峰27.977°,32.690°,46.226°,46.895°,55.484°,55.618°与四方β-Bi2O3的特征衍射峰(PDF No.27-0050)基本一致。由此说明,铈的掺杂引起了Bi2O3结晶度的改变并抑制β-Bi2O3随温度降低转变成α-Bi2O3。同时所有样品的衍射峰没有其他杂质的衍射峰,由此说明所制备的催化剂为单一氧化物。
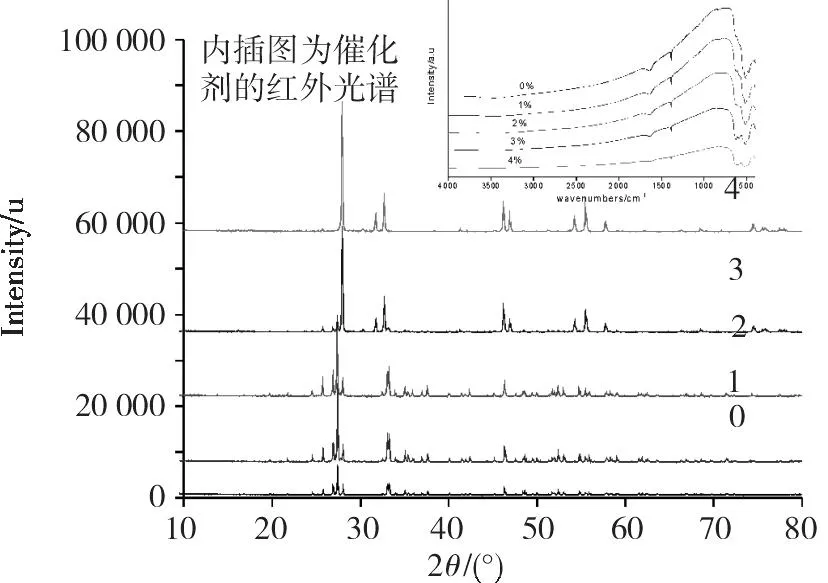
图2 催化剂的XRD图谱
2.3掺杂对催化剂粒度分布的影响
表1和图3为掺杂量对Bi2O3粒径及粒度分布的影响。从表中可以看出所制备的催化剂颗粒粒度较大,为几十微米。同时从表中发现Ce的掺杂对催化剂比表面积、颗粒均一性以及粒度分布存在影响。当Ce掺杂从0%增加到2%时,颗粒粒径减小,颗粒比表面积增大,随着Ce掺杂量继续增加,颗粒粒径反而增加,颗粒的增大使催化剂比表面积降低,降低催化剂的活性位,从而影响催化活性。
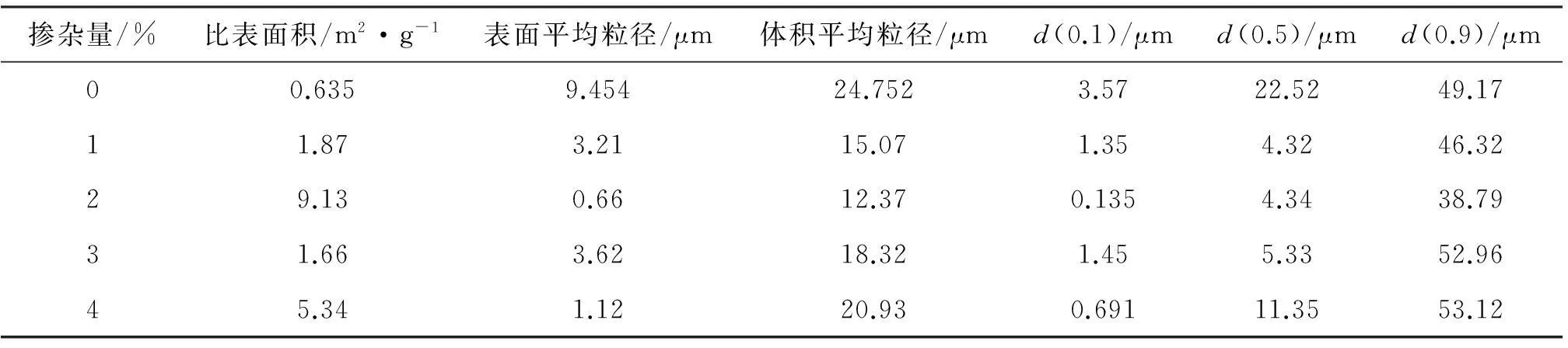
表1 掺杂对氧化铋催化剂粒度分布的影响
从表1和图3发现,掺杂量为1%的样品粒径10 μm内的颗粒超过70%,而掺杂量为4%的样品粒径分布较宽,且各范围的比例接近,而掺杂量为2%的样品粒径分布较窄,集中在40 μm以下,不过所有样品90%的颗粒粒径都小于60 μm。窄的粒径分布与采用的水热法有关。水热法在制备粉末样品时,制备的颗粒具有较好的均匀性和粒度分布窄的特点。
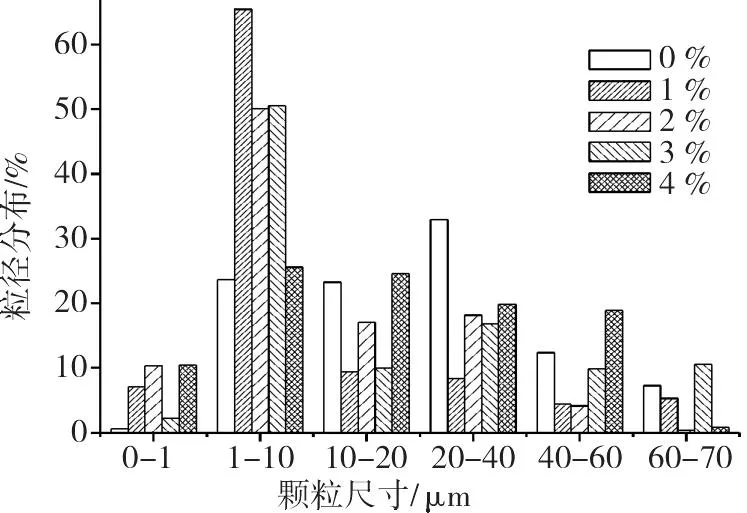
图3 催化剂颗粒粒度分布图
2.4SEM 分析
图4为样品的SEM图片。从图4可以看出,样品存在团聚现象呈不规则形状且颗粒较大。另外,铈的掺杂对催化剂的形貌存在影响。没有掺杂时,催化剂结块最大,而掺杂2%后所形成的催化剂颗粒分布均匀,颗粒粒径小,这可以提高催化剂的比表面积。SEM结果与粒度分布以及XRD一致。
2.5铈掺杂对Bi2O3紫外可见漫反射光谱的影响
由于对光的吸收是光催化反应发生的必要条
件,因此这项表征技术对光催化材料是十分重要的。图5是所制催化剂在200~800 nm区间的紫外可见漫反射吸收光谱。 从图5可以看出,铈掺杂量从0%增加到2%,样品的漫反射吸收曲线类似, 对400 nm前的紫外光具有强吸收,同时吸收边随掺杂量增大从458 nm左右增加到475 nm左右。当Ce掺杂含量继续增加到4%时,对光的强吸范围从紫外区(a:400 nm)扩展到可见区(b: 460 nm),其吸收边扩展到近600 nm。吸收边的红移意味着催化剂可以吸收更多的光子,这有利于提高催化效果[9]。各催化剂的带隙可由Eg(eV)=1240/λg(nm)估算,结果见表2。
从表2可以看出,由于铈的掺杂引起催化剂带隙均比室温下单独的Bi2O3(2.8 eV) 和CeO2(2.94 eV)小[12],由此只需较低能量的光即可激发价带上的电子跃迁到导带,有利于电子跃迁,这有利于对太阳光的利用。

表2 铈掺杂量对催化剂吸收光的影响

图4 催化剂粉末的SEM图片
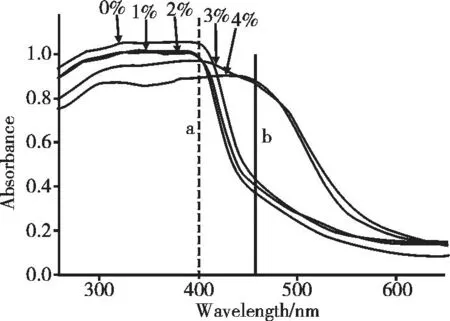
图5 催化剂的紫外吸收漫反射光谱
2.4掺杂量对Bi2O3荧光光谱的影响
催化剂能够吸收可见光,这为催化剂在可见光下的光催化过程提供了前提,但并不是在可见光范围内有光吸收性,催化剂就能受光子激发产生光生电子-空穴对,因此需要用表征手段来分析在光照射条件下光生电子-空穴的分离情况。在光催化过程中,光生载流子的复合会影响到催化剂的量子效率。而研究表明,就半导体材料而言,光生电子和空穴复合时会以荧光方式发出,当光照在半导体上,发射强度低的荧光意味着光生电子-空穴对复合几率低,因此可以通过荧光光谱来了解半导体催化剂的载流子俘获效率,评估其光催化性能[13]。图6为不同铈掺杂量的Bi2O3在365 nm激发波长下的发射光谱。从图6可以看出,所有样品的发射光谱都很弱,并且发射光谱强度随铈掺杂量的增加而降低,前3个样品的发射光谱相似,发射光谱强度随掺杂量的增加而轻微下降,当掺杂量达3%和4%时催化剂的发射谱线发生明显改变,且强度急剧降低,前3个样品PL光谱中450 nm范围可归属于Bi3+离子的3P1→1S0的发射峰消失,而在550 nm范围出现了可归属于铈的荧光发射光谱[14]。发射光谱强度的
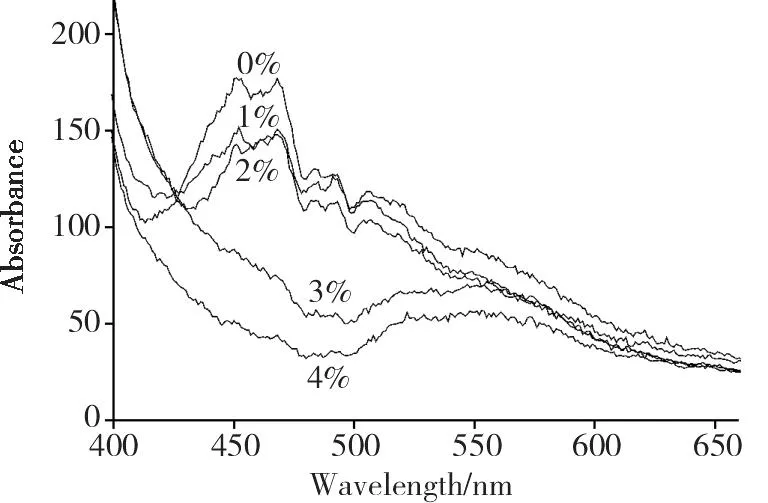
图6 催化剂的荧光光谱图
降低说明Ce4+的掺杂对电子对发生了争夺转变成Ce3+,减少了半导体表面光生电子与空穴复合几率,使得Bi2O3中电子和空穴得到有效分离,从而有利于提高Bi2O3的催化效果。
2.5光催化分析
甲基橙属于偶氮染料,抗直接光分解和氧化,为较难降解的有机物,其浓度采用分光光度法测定,方法简便,因此常被用做光催化反应的模型反应物来评价催化剂的性能。光催化反应是气固液三相反应,反应场所在催化剂的活性位上进行,因此催化剂对反应物的吸附多少对底物降解结果影响很大。表3反映了曝气1 h后甲基橙溶液吸光度的变化情况。从表2 可以看出,添加2%铈所得催化剂对甲基橙的吸附能力最强,而1%的样品最低,其他样品吸附能力接近,这可能与样品颗粒大小和比表面积有关。XRD和粒度分布以及SEM测试结果表明2%掺杂所形成的样品,粒度最小,比表面积最大,这样活性位多,有利于对物质的吸附,从而可以吸附更多的物质,有利于加速甲基橙的降解。
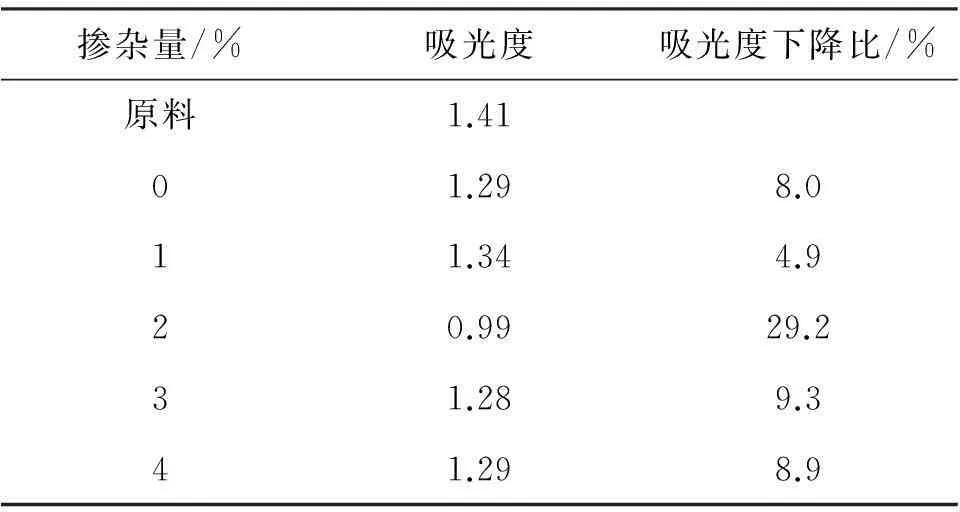
表3 掺杂量对甲基橙的吸附影响
图7为添加催化剂后甲基橙溶液随光照时间的降解曲线。图8为光照4 h后甲基橙溶液的吸收光谱图。
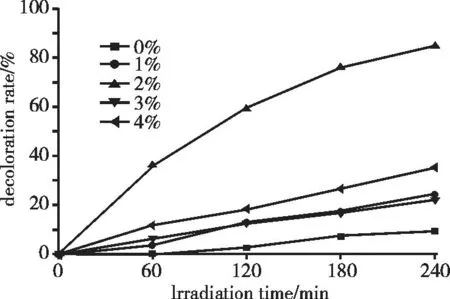
图7 甲基橙随光照时间的降解曲线
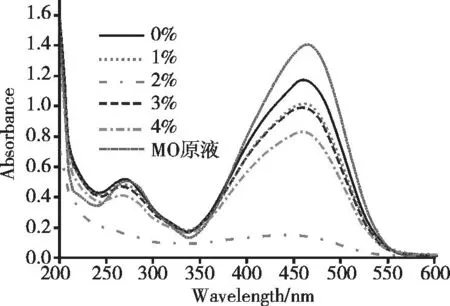
图8 甲基橙光照4 h后的吸收光谱
从图7可以看出,相比于纯Bi2O3而言,甲基橙的褪色率随铈的掺杂而增加,但甲基橙的褪色率并不完全随铈掺杂量增加而增加,其中添加2%铈催化剂的甲基橙溶液褪色率最高,经过4 h光降解,褪色率达85.87%。从图8可以看出,当加入铈掺杂量为2%的催化剂后MO溶液中归属于MO分子中偶氮基团(465 nm)以及苯环的π→π*(275 nm)的吸收峰已经消失,同时近紫外区中(220 nm左右)归属于C-H以及C-C键等的σ电子跃迁峰强度也急剧降低,说明这些基团被破坏并矿化,生成一些小分子物质。尽管3%和4%掺杂样品对光的强吸收扩展到可见区,同时PL发射光谱强度最弱,但催化效果却低,甲基橙退色率仅30%左右,这一方面可能与β-Bi2O3性质有关,β-Bi2O3的价带相对较负,这样价带光生空穴的氧化能力较弱[15]。同时,过多的铈离子掺杂,可能导致氧或铋缺陷的增加,也可能演变成为电子和空穴复合的中心,使得光生电子和空穴更易复合而导致Bi2O3光催化能力下降[16]。
3结论
通过微波辅助水热法以及灼烧方式制备对甲基橙光降解具有催化作用铈掺杂的Bi2O3催化剂。通过适量的铈掺入,得到了室温下稳定存在的四方β-Bi2O3,同时铈的掺杂使Bi2O3的光谱响应范围向可见光区拓展,红移至550 nm以上,提高了对可见光的吸收利用。适量的掺杂可提高Bi2O3光催化活性,在20 mg/L的甲基橙溶液中,2.0%掺杂的催化剂对甲基橙降解效果最好,光照4 h后褪色率达84.87%。
参考文献
[1]王伟华, 叶红齐, 覃涛,等. 含铋光催化材料的研究进展, 化工进展[J]. 2014, 33(4): 1475-1486.
[2]李二军, 陈浪, 章强, 等. 铋系半导体光催化材料, 化学进展[J]. 2010, 22(12): 2282-2289.
[3]ADHIKARI R, GYAWALI G, SUNG Hun Cho, et al. Er3+/Yb3+co-doped bismuth molybdate nanosheets upconversion photocatalyst with enhanced photocatalytic activity[J]. Journal of Solid State Chemistry, 2014, 2 (9): 74-81.
[4]刘卓婧, 宫喜君, 张凤君, 等. 掺杂铕氧化铋光催化剂的制备及其可见光的光催化性能[J]. 吉林大学学报, 2013, 51(3): 539-543.
[5]杨迎春, 卢远刚, 叶芝祥, 等. La掺杂Bi2O3的制备、表征与可见光催化活性[J]. 化学学报, 2012, 70(11): 1251-1255.
[6]ALEMI A A, KASHFI R, HABANI B S. Preparation and characterization of novel Ln (Gd3+, Ho3+and Yb3+)-doped Bi2MoO6with Aurivillius layered structures andphotocatalytic activities under visible light irradiation[J]. Journal of Molecular Catalysis A: Chemical 2014, (392): 290-298.
[8]肖国生, 刘佳露, 刘卓婧, 等. Ce掺杂Bi2O3光催化剂的制备、表征及其可见光催化性能[J]. 发光学报, 2014, 35(8): 956-961.
[9]HUANG Qian-qian , ZHANG Su-ning , CAI Chen-xin, et al.β- andα-Bi2O3nanoparticles synthesized via microwave -assisted method and their photocatalytic activity towards the degradation of rhodamine B[J]. Materials Letters, 2011, (65): 988-990.
[10] XIE H D, SHEN D Z, WANG X Q, et al. Microwave hydrothermal synthesis and visible-light photocatalytic activity of γ-Bi2MoO6nanoplates[J]. Materials chemistr and Physics, 2008, 110 (2-3): 332 -339.
[11] 余长林, 杨凯, 余济美, 等. 稀土Ce掺杂对ZnO结构和光催化性能的影响[J]. 物理化学学报, 2011, 27 (2): 505-512.
[12] 中本一雄. 无机和配位化合物的红外及拉曼光谱[M].北京: 化学工业出版社, 1986.
[14] GURUSHANTHA K , ANANTHARAJU K S, NAGABHUSHANA H , et al. Facile green fabrication of iron-doped cubic ZrO2nanoparticles by Phyllanthus acidus: Structural, photocatalytic and photoluminescent properties[J]. Journal of Molecular Catalysis A: Chemical, 2015, ( 397): 36-47.
[15] XIONG Y., WU MZ, YE J, et al. Synthesis and luminescence properties of hand-likeα-Bi2O3microcrystals[J]. Materials Letters, 2008, (62): 1165-1168.
[16] LI De-yi, Zhang Yong-gang , ZHANG Ya-lei, et al. Fabrication of bidirectionally dopedβ-Bi2O3-TiO2-NTs with enhanced photocatalysis under visible light irradiation[J]. Journal of Hazardous Materials, 2013, (258-259): 42-49.
Synthesis of Ce-doped Bi2O3and Its Photocatalytic Property
WANG Song1, YAO Wei-long2, JIANG Qi-ying1,2, DENG Hong-quan1,LIU Xue-mei1, SHEN Juan1
(1.SchoolofMaterialsScienceandEngineering,SouthwestUniversityofScienceandTechnology,Mianyang621010,Sichuan,China;2.EngineeringResearchCenterofBiomassMaterials,MinistryofEducation,SouthwestUniversityofScienceandTechnology,Mianyang621010,Sichuan,China)
Abstract:Ce-doped Bi2O3 photocatalysts with different molar ratio were prepared by the microwave-assisted hydrothermal method,and then calcined at 600 ℃ for 1 h. The phase and spectrum properties of prepared photocatalysts were characterized by X-ray diffraction (XRD) ,Fourier transform infrared spectroscopy (FT-IR), photoluminescence spectra(PL), and ultraviolet-visible diffuse reflectance spectroscopy(Uv-Vis DRS), respectively. The photocatalytic properties of Ce-Bi2O3 were evaluated by the photo degradation of Methyl orange under light irradiation. The results show that the doping of Ce can stabilize the crystalline phase of Bi2O3, decrease the band gap of Bi2O3 significantly,and improve the photocatalytic performance of Bi2O3. The decolorized rate of 20 mg/L MO solution is 85% under 4 h light irradiation in the present of photocatalyst(1 g/L) with the Ce dopant molar rate of 2%.
Key words:Bi2O3; Ce; Microwave- hydrothermal method; Photocatalytic property
中图分类号:X703
文献标志码:A
文章编号:1671-8755(2016)01-0014-06
作者简介:王松,男,本科生。通信作者: 邓洪权(1968—),男,副教授,研究方向为废水处理。 E-mail: denghongquan@swust.edu.cn
基金项目:国家自然基金青年基金项目(21201142);四川省教育厅项目(14ZA0101) 和国家级大学生创新创业训练计划项目(201410619008)。
收稿日期:2015-05-04
