槲皮素磁性分子印记聚合物的制备及其吸附性能
2016-04-26阮永欣马应霞王茹娟杜雪岩张文娟兰州理工大学材料科学与工程学院有色金属先进加工与再利用省部共建国家重点实验室兰州730050
阮永欣, 马应霞, 王茹娟, 邢 丹, 杜雪岩, 张文娟(兰州理工大学材料科学与工程学院,有色金属先进加工与再利用省部共建国家重点实验室,兰州730050)
槲皮素磁性分子印记聚合物的制备及其吸附性能
阮永欣,马应霞,王茹娟,邢丹,杜雪岩,张文娟
(兰州理工大学材料科学与工程学院,有色金属先进加工与再利用省部共建国家重点实验室,兰州730050)
摘 要:以槲皮素(Qu)为模板分子、N-乙烯基吡咯烷酮(NVP)和丙烯酸(AA)为功能单体、N,N'-亚甲基双丙烯酰胺(MBA)为交联剂、H2O2-Vc为引发剂、KH570修饰的Fe3O4纳米颗粒为磁性载体,借助表面分子印迹技术制备了能够对Qu进行特异性识别的槲皮素磁性分子印迹聚合物(Qu-MMIPs)。利用X射线衍射仪(XRD)、透射电子显微镜(TEM)、傅里叶变换红外光谱仪(FT-IR)、振动样品磁强计(VSM)和紫外-可见分光光度计(UV-Vis)对样品进行了结构和性能表征。结果表明:Fe3O4磁性载体表面已成功包覆了分子印迹聚合物。与化学组成相同的磁性非印迹聚合物(Qu-MNIPs)相比,Qu-MMIPs对Qu有较高的吸附选择性。静态吸附平衡实验和Scatchard分析结果表明,Qu-MMIPs中存在两类不同的结合位点,平衡解离常数分别为1.646× 10(-6)mol/L和6.387×10(-6)mol/L,最大吸附量分别为23.041 mg/g和29.923 mg/g。
关键词:槲皮素;磁性纳米颗粒;分子印迹聚合物;吸附
近年来,黄酮类化合物在抗病毒性、抗过敏性、抗炎性、抗肿瘤及抗氧化性等[1]方面表现出了独特的优势,从而引起了国内外研究者的广泛兴趣。在黄酮类化合物中,槲皮素(Qu,3,3',4',5,7-五羟基黄酮)具有清除人体氧自由基等多种生物活性[2-3],通常用于治疗慢性支气管炎,也可用于冠心病及高血压的辅助治疗[4]。Qu大多数以苷的形式存在于植物的花、叶及果实中,是许多中草药和天然产物如槐米、红枣、金银花、银杏叶、桑叶、三七的有效成分之一。由于在自然条件下槲皮素的浓度很低,并且其结构与其他黄酮类化合物类似,因此从复杂体系中分离、提纯Qu就显得尤为困难。而分子印迹聚合物(MIPs)因其对印迹分子特殊的高选择性和亲和力成为了近年来的研究热点,并在众多领域中有所应用。
目前,有关制备槲皮素分子印迹聚合物(Qu-MIPs)的相关报道也很多[4-8],并取得了一定的研究成果。范培民[7]等利用分子印迹技术,通过紫外光引发原位聚合的方法制备了槲皮素金属配位印迹聚合物,但是在其吸附后的分离过程中,往往要经过抽滤、离心等步骤,从而无法实现分离效率的有效提高。而磁性纳米颗粒由于其特殊的物理和化学性质,使得磁技术广泛应用在化学、生物医学等领域。尤其是以低毒、稳定、价廉易得的Fe3O4作为磁性材料的研究受到了人们的极大关注[9-10]。如果赋予MIPs磁响应性,不仅可以对分子产生特异性识别,而且能够实现MIPs在外加磁场作用下的快速定向移动,从而实现MIPs的大规模连续化生产。因此,制备以Fe3O4纳米颗粒(Fe3O4NPs)为载体的磁性分子印迹聚合物(MMIPs)用于Qu的分离和提纯具有潜在的应用价值。
本文以Qu为模板分子、N-乙烯基吡咯烷酮(NVP)和丙烯酸(AA)为功能单体、N,N'-亚甲基双丙烯酰胺(MBA)为交联剂、Fe3O4纳米颗粒为磁性载体,一步合成了对槲皮素具有特异识别性的槲皮素磁性分子印迹聚合物(Qu-MMIPs),并以Qu结构类似物染料木素(Ge)为竞争底物,研究了Qu-MMIPs的吸附特性。此外,对Qu-MMIPs的吸附特性和识别机理的研究将为类似分子识别的设计提供理论依据。
1 实验部分
1.1试剂与仪器
FeSO4·7 H2O、L-抗败血酸(Vc)、MBA:分析纯,天津市大茂化学试剂厂;正丁醇(NBA)、甲醇(MT)、冰乙酸(HAc)、无水乙醇(EA):分析纯,天津市富宇精细化工有限公司;双氧水、环己烷(CYH):分析纯,天津市恒兴化学试剂有限公司;NH3·H2O:分析纯,白银市化学试剂厂;FeCl3·6 H2O:分析纯,烟台市双双化工有限公司;KH570:分析纯,南京曙光化工集团有限公司;Qu:分析纯,陕西森佛生物技术有限公司;AA:分析纯,天津市光复精细化工研究所;NVP:分析纯,河南洛阳博爱新开源有限公司;Ge:分析纯,西安小草植物科技有限公司;乳化剂OP-10:化学纯,天津市北辰方正试剂厂。
采用上海一恒科学仪器有限公司HZQ-211C型落地恒温振荡器为样品提供吸附所需的恒温环境;采用日本电子公司JSM-2010型透射电子显微镜分析样品形貌;采用德国布鲁克公司D8/ADVANCE型X射线衍射仪和美国尼高力公司NEXUS-670型傅里叶变换红外光谱仪表征样品结构;采用美国Lakeshore公司7304型振动样品磁强计(VSM)测试样品的磁性能;采用上海精密科学仪器有限公司UV-752N型紫外可见分光光度计分析样品的吸附性能。
1.2槲皮素磁性分子印迹聚合物的制备
首先将16.000 g乳化剂OP-10、22 m L正丁醇和50 m L环己烷混合均匀后,加入到装有机械搅拌、球形冷凝管和N2导管的三口烧瓶中;然后将0.473 g FeCl3·6H2O和0.278 g FeSO4·7H2O溶于25 m L去离子水中,加入到上述三口烧瓶中;滴加3 m L浓氨水,20℃反应1 h。反应结束后,在该体系中加入0.96 m L KH570,50℃反应5 h。同时,将20 m L、10 mmol/L的Qu乙醇溶液、0.454 g AA和0.233 g NVP加入到50 m L烧杯中,室温下搅拌5 h后加入到上述经KH570改性后的体系中,搅拌10 min后,再加入5.265mmol MBA、0.08 mmol H2O2和0.16 mmol Vc,35℃反应28 h得到KH570改性的Fe3O4纳米颗粒(KH570-Fe3O4NPs)。产物利用外加磁场进行分离,先用甲醇-乙酸(甲醇与乙酸体积比为9/1)洗脱液清洗3次后,再放入盛有甲醇、乙酸洗脱液的索氏抽提器中洗脱模板分子,直到洗脱液的吸光度小于0.005。将产物在40℃真空干燥24 h,得到的样品标记为Qu-MMIPs。
用同样的方法,不加模板分子制备磁性非印迹聚合物,得到的样品标记为Qu-MNIPs。
1.3吸附性能测试
准确称取10 mg的磁性印迹聚合物于25 m L的锥形瓶中,分别加入5 m L不同质量浓度(0.1、0.5、1.0、1.5、2.0、2.5、3.0、3.5、4.0、4.5、5.0 g/L)的Qu乙醇溶液,封紧瓶口,室温下将其置于恒温振荡器中振荡吸附2 h,磁铁吸沉,取上清液用UV-752N在370 nm处测定残液的吸光度。根据公式(1)[11]计算Qu-MMIPs 对Qu的单位吸附量(Q,mg/g)。

式中:ρ0为Qu的初始质量浓度(g/L);ρ为Qu吸附残液的质量浓度(g/L);V为Qu乙醇溶液的体积(m L);
m为Qu-MMIPs的质量(g)。
1.4吸附选择性研究
选取与Qu结构类似的Ge为竞争底物,分别称取10 mg Qu-MMIPs和Qu-MNIPs置于25 m L的锥形瓶中,各加入5 m L Qu与Ge的混合溶液(每种底物的质量浓度均为0.1 g/L),恒温振荡吸附2 h,磁铁吸沉,取上清液用UV-752N分别在370 nm和262 nm的波长下测定残液中每种底物的吸光度。根据公式(2)计算Qu-MMIPs和Qu-MNIPs对每种底物的单位吸附量(Q,mg/g)。

式中:ρe为平衡时Qu吸附残液的质量浓度(g/L);V为Qu与Ge的混合溶液的体积(m L);m为Qu-MMIPs 或Qu-MNIPs的质量(g)。
1.5Qu-MMIPs重复利用率的研究
称取10 mg Qu-MMIPs于25 m L的锥形瓶中,加入5 m L质量浓度为0.1 g/L的Qu乙醇溶液,封紧瓶口,室温下静置吸附2 h,磁铁吸沉,取上清液用UV-752N在370 nm处测定残液的吸光度。然后用甲醇、乙酸洗脱液对吸附了Qu的Qu-MMIPs进行洗脱,除去印迹分子Qu,再次得到Qu-MMIPs。如此反复,测定每次吸附后残液的吸光度,根据公式(3)[12]计算Qu-MMIPs对Qu的吸附率(η,%)。

2 结果与讨论
2.1XRD分析
图1是Qu-MMIPs、KH570改性的Fe3O4NPs和Fe3O4NPs的XRD谱图。从图1可以清楚地看到:与JCPDS标准谱图进行比对,Fe3O4的6个特征峰30.38°、35.58°、43.14°、53.48°、57.08°、62.66°所对应的晶面指数分别为(220),(311),(400),(422),(511)和(440),说明制备的Fe3O4NPs具有反尖晶石的结构。由谢乐公式[13]计算得Fe3O4颗粒的平均粒径在6.7 nm。而经过KH570的表面修饰或印迹聚合反应后,Fe3O4的特征峰依然存在,只是强度依次减弱,说明Fe3O4NPs被成功修饰并且包覆了一层印迹聚合物。
2.2TEM分析
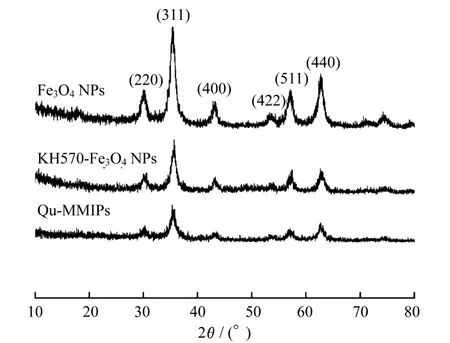
图1 样品的XRD谱图Fig.1 XRD spectra of samples
图2为Fe3O4NPs和Qu-MMIPs的TEM照片(图2 (a)、图2(b))、Qu-MMIPs和Fe3O4NPs的选区电子衍射谱图(图2(c)、图2(d))以及采用TEM统计的Qu-MMIPs粒径分布图(图2(e))。从图2(a)可见,Fe3O4纳米颗粒尺寸在7 nm左右,这与通过XRD计算得到的粒径大小基本一致,但团聚现象较为严重,这是因为颗粒尺寸较小时表面能较大,而团聚有利于降低表面能,从而达到稳定状态。图2(b)中纳米粒子的尺寸有所增大,约为10 nm,这归因于在磁性纳米颗粒表面包覆了一层印迹聚合物所致,使得Qu-MMIPs的分散性明显改善。对比Qu-MMIPs和Fe3O4NPs的选区电子衍射谱图可知,Fe3O4NPs的电子衍射环明显比Qu-MMIPs的清晰,这进一步说明在Fe3O4纳米颗粒的表面包覆了一层薄的印迹聚合物。根据TEM得到的粒径分布图,颗粒的粒径主要集中在9.0~10.5 nm,可见所制备的Qu-MMIPs颗粒拥有比较均一的粒径分布。

图2 Fe3O4NPs[10](a)和Qu-MMIPs(b)的TEM照片、Qu-MMIPs(c)和Fe3O4NPs(d)的选区电子衍射谱图以及采用TEM统计的粒径分布图(e)Fig.2 TEM images of Fe3O4NPs(a)and Qu-MMIPs(b),SAED patterns of Qu-MMIPs(c)and Fe3O4NPs(d)and particle size distribution collected by TEM(e)
2.3FT-IR分析
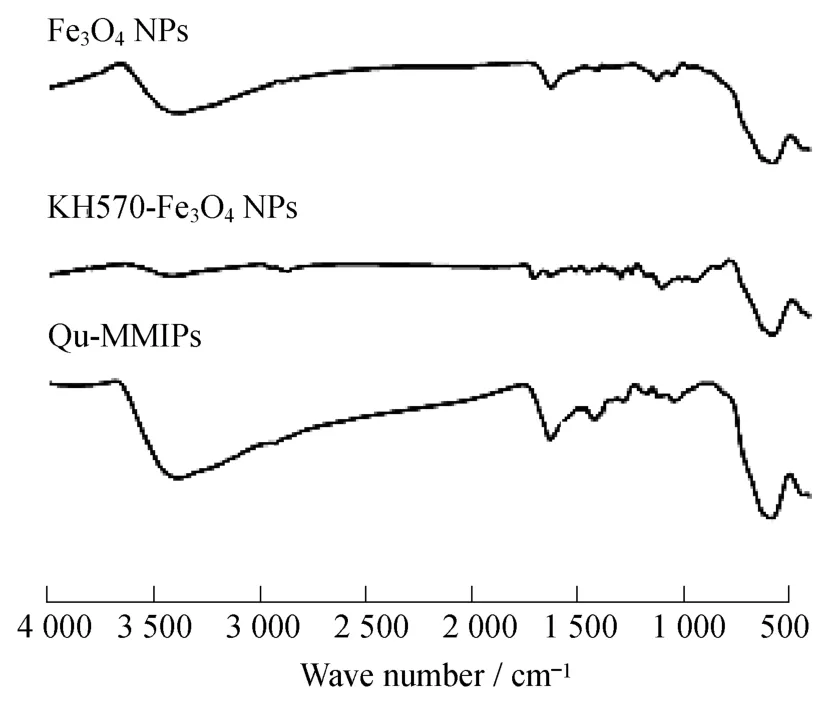
图3 样品的红外光谱图Fig.3 FT-IR spectra of samples
图3为Fe3O4NPs、KH570-Fe3O4纳米颗粒和Qu-MMIPs的红外光谱图。在Fe3O4NPs的红外光谱图中,587 cm-1处的强峰为Fe—O的伸缩振动峰[13],KH570-Fe3O4NPs和Qu-MMIPs的红外光谱图中也都出现了这个峰。KH570-Fe3O4的红外光谱图中,Si—O、CO和C—H的伸缩振动分别出现在1 100、1 713 cm-1和2 848 cm-1,所有这些变化都充分表明,KH570与纳米Fe3O4表面的羟基发生了化学反应,即达到了KH570改性纳米Fe3O4的目的。在Qu-MMIPs的红外光谱图中,1 181 cm-1以及1 416 cm-1处的峰分别是OC—O中C—O的不对称伸缩振动峰和O—H的变形振动吸收峰;NVP和AA中CO的伸缩振动峰在1 633 cm-1处;在2 929 cm-1处的峰是NVP和AA中甲基或亚甲基的伸缩振动峰;3 421 cm-1处的强宽峰为NVP中N—H和AA中O—H的伸缩振动峰,所有这些特征峰的出现都充分表明,AA和NVP与改性后的纳米Fe3O4表面的双键发生了聚合反应,从而形成了以Fe3O4为内核、聚合物为外壳包裹Fe3O4的核-壳结构。
2.4VSM分析
图4分别为Fe3O4NPs、KH570-Fe3O4NPs和Qu-MMIPs的磁滞回线。从图4可以看出,3种样品均没有磁滞现象,剩磁和矫顽力都近似为零,显示出超顺磁性。室温下,Fe3O4NPs、KH570-Fe3O4NPs和Qu-MMIPs的饱和磁化强度分别为63.7、58.4 emu/g和46.5 emu/g。与纯Fe3O4的饱和磁化强度相比,Qu-MMIPs的饱和磁化强度则有所下降,这可能是由于表面包覆了印迹聚合物层影响了其磁响应性所致。

图4 Fe3O4NPs和KH570-Fe3O4NPs(a)以及Qu-MMIPs(b)的磁滞回线Fig.4 Hysteresis loops of Fe3O4NPs,Fe3O4NPs modified with KH570(a)and Qu-MMIPs(b)
图5为Qu-MMIPs分散在水中和在外磁场作用下的磁分离数码照片。从图5可以看出,在没有外磁场存在时,Qu-MMIPs均匀地分散在水溶液中,呈黑色悬浮状。当施加外磁场时,黑色颗粒被快速吸引到有外加磁场的瓶壁一侧,溶液变得透明,这说明Qu-MMIPs具有良好的磁响应性,可作为磁性分离的载体。

图5 Qu-MMIPs分散在水中(a)和在外磁场作用下的磁分离(b)数码照片Fig.5 Digital photographs of Qu-MMIPs dispersed in the water(a)and external magnetic field(b)
2.5槲皮素磁性分子印迹聚合物Qu-MMIPs的吸附性能
2.5.1 吸附等温线 图6所示为Qu在0.01~2.5 g/L的吸附等温线和Qu-MMIPs对Qu的Scatchard分析曲线。当Qu的起始质量浓度低于1.0 g/L时,吸附量增加很快;当Qu的起始质量浓度高于1.0 g/L 时,吸附容量趋于平衡,这表明Qu-MMIPs上的活性结合位点达到吸附饱和。而Qu-MNIPs与Qu-MMIPs 对Qu的吸附变化趋势相同,吸附量也随模板分子浓度的增加而增加,随后也达到饱和。但与Qu-MMIPs相比,Qu-MNIPs的吸附容量却小很多。
为了进一步研究Qu-MMIPs的吸附特性,通过Scatchard模型对所得Qu-MMIPs的吸附热力学数据进行分析。Scatchard模型方程[14]为:

式中:Qe(mg/g)为不同质量浓度下的平衡吸附量;Qmax(mg/g)是Qu-MMIPs的最大吸附量;Kd(g/L)是Qu-MMIPs的平衡解离常数。
通过对Qe/ρe和Q关系图的两段线性部分进行拟合,可以分别得到高亲和力位点方程和低亲和力位点方程。根据上述两条线性曲线的斜率和截距便可计算出,高亲和位点的Kd和Qmax分别为0.497×10-3g/L 和23.041 mg/g,低亲和位点的Kd和Qmax分别为1.929×10-3g/L和29.923 mg/g。Qu-MMIPs会形成两种不同亲和能力的结合位点,这主要是因为功能单体与模板分子通过氢键相互作用,在印迹聚合物的合成过程中形成了一定数量的印迹孔穴,而没能与模板分子定向配位的功能单体在聚合物中是任意分布的,从而形成了特异性和非特异性两种不同的吸附。
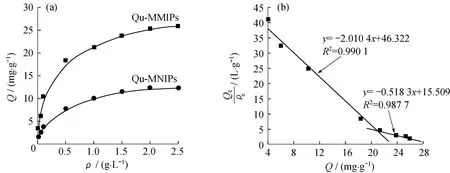
图6 Qu-MMIPs和Qu-MNIPs的结合吸附等温线(a),Qu-MMIPs对Qu的Scatchard分析曲线(b)Fig.6 Adsorption isotherms for Qu-MMIPs and Qu-MNIPs(a),Scatchard analysiscurve of Qu-MMIPs for Qu(b)
2.5.2 吸附选择性 图7为Qu-MMIPs和Qu-MNIPs分别对Qu和Ge的饱和吸附量。结果表明,Qu-MMIPs对模板Qu有较高的吸附量,但对Ge的吸附量则相对较低。这主要是由于在Qu-MMIPs中不存在Ge的特异性识别位点,从而使得Ge不能像Qu一样,可与特定的空间结合位点形成较强的作用力。Qu-MNIPs对两种底物的吸附量都较低,没有选择性,这也表明Qu-MMIPs对Qu的吸附是具有特异性的。
通常以印迹因子(α)来表示分子印迹聚合物的特异选择性(α=QQu-MMIPs/QQu-MNIPs,QQu-MMIPs和QQu-MNIPs分别为槲皮素磁性印迹和非印迹聚合物对Qu的吸附量),α值越大,特异性越强,印迹效果越好。经计算得到Qu和Ge的α分别为2.32和1.32。从这些数据可知,制备的磁性印迹聚合物具有一定的选择性,能够实现对Qu的选择性吸附。
2.5.3 重复利用性 图8为槲皮素磁性分子印迹聚合物的吸附量随洗脱次数变化的关系图。从图中可以看出,Qu-MMIPs呈现出良好的重复利用性,经过6次持续的吸附-洗脱循环之后,Qu-MMIPs对Qu的吸附率仅仅降低了9%。此结果表明,Qu-MMIPs在经过多次循环搅拌和抽提等机械外力的作用后,其空间结构并未损坏,仍保持着良好的结合位点,有较好的再生性能。

图7 Qu-MMIPs和Qu-MNIPs对Qu 及Ge的饱和吸附量Fig.7 Saturated adsorption amount of Qu-MMIPs and Qu-MNIPs for Qu and Ge
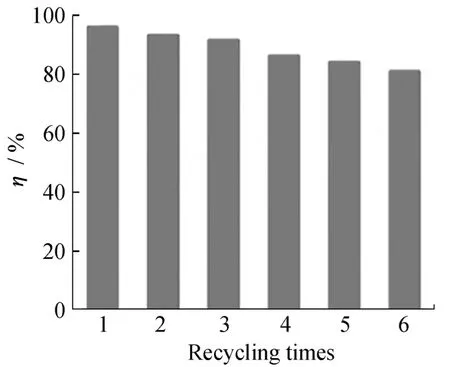
图8 Qu-MMIPs对Qu的吸附率与重复使用次数的关系Fig.8 Relationship between adsorption rate and recycling times of Qu-MMIPs for Qu
3 结 论
通过分子印迹技术,利用一步合成法成功制备了槲皮素磁性分子印迹聚合物,该聚合物具有良好的磁响应性,能够满足磁分离的要求,其对模板分子槲皮素具有特异的吸附能力,印迹因子为2.32。该方法将为多肽、蛋白质等生物大分子的有效分离提供一种新的途径。
参考文献:
[1]LIAN Wang,WANG Bao,LI Hao,et al.Quercetin,aflavonoid with anti-inflammatory activity,suppresses the development of abdominal aortic aneurysms in mice[J].European Journal of Pharmacology,2012,690(1-3):133-141.
[2]KANDASWAMI C,MIDDLETON E.Free Radical Scavenging and Antioxidant Activity of Plant Flavonoids[M].US:Springer,1994.
[3]SAPINO S,UGAZIO E,GASTALDI L,et al.Mesoporous silica as topical nanocarriers for quercetin:Characterization and in vitro studies[J].EuropeanJournal of Pharmaceutics& Biopharmaceutics,2015,89:116-125.
[4]常勇慧.壳聚糖分子印迹槲皮素识别材料的制备[J].江西化工,2011(2):98-101.
[5]颜流水,井晶,黄智敏,等.槲皮素分子印迹聚合物的制备及固相萃取性能研究[J].分析试验室,2006,25(5):97-100.
[6]何建峰,邓芹英.槲皮素分子烙印聚合物的单体优化、性能评价及其在薄层色谱分离中的应用[J].中药材,2007,30(5):588-591.
[7]范培民,王兵.槲皮素金属配位印迹聚合物膜的制备及性能研究[J].化学学报,2010,68(24):2543-2550.
[8]SONG Xingliang,LI Jinhua,WANG Jiangtao,et al.Quercetin molecularly imprinted polymers:Preparation,recognition characteristics and properties as sorbent for solid-phase extraction[J].Talanta,2009,80(2):694-702.
[9]杨卫海,吴瑶,张轶,等.磁性分子印迹聚合物核壳微球的制备及应用[J].化学进展,2010(9):1819-1825.
[10]王茹娟,马应霞,路翠萍,等.谷胱甘肽磁性分子印迹聚合物的制备及吸附性能研究[J].化学学报,2014,72(5):577-582.
[11]YURTSEVER M,SENGIL I A.Adsorption and desorption behavior of silver ions onto valonia tannin resin[J].Transactions of Nonferrous Metals Society of China,2012,22(11):2846-2854.
[12]WU Xueping,XU Yanqing,ZHANG Xianlong,et al.Adsorption of low-concentration methylene blue onto a palygorskite/ carbon composite[J].Carbon,2015,30(1):373.
[13]文潮,刘晓新,李迅,等.纳米石墨颗粒粒度的测量与表征[J].分析测试学报,2004,23(1):1-4.
[14]杜雪岩,马芬,李芳,等.Fe3O4@SiO2磁性纳米粒子的制备与表征[J].兰州理工大学学报,2011,37(2):22-25.
[15]LIU Qiuye,LI Wenyou,HE Xiwen.Study of recognition property of molecularly imprinted bovine hemoglobin on surfacemodified silica gel[J].Acta Chimica Sinica,2008,66(1):56-62.
欢迎订阅《功能高分子学报》
地址:上海市梅陇路130号华东理工大学436信箱 邮编:200237
联系电话:021-64253005 邮发代号:4-629
Preparation and Adsorption Property of Quercetin Magnetic Molecularly Imprinted Polymers
RUAN Yong-xin,MA Ying-xia,WANG Ru-juan,XING Dan,DU Xue-yan,ZHANG Wen-juan
(State Key Laboratory of Advanced Processing and Recycling of Non-ferrous Metals,School of Materials Science and Engineering,Lanzhou University of Technology,Lanzhou 730050,China)
Abstract:Quercetin(Qu)magnetic molecularly imprinted polymers(Qu-MMIPs)with the specific recognizing property for Qu,were prepared using Qu as template molecule,acrylamide(AA)and N-vinylpyrrolidone(NVP)as functional monomers,N,N'-methylene bisacrylamide(MBA)as crosslinker,H2O2-Vc as initiator and Fe3O4nanoparticles(NPs)modified withγ-methacryloxypropyltrimethoxysilane (KH570)as magnetic carrier.The as-synthesized polymers were characterized by X-Ray Diffraction(XRD),Transmission Electron Microscopy(TEM),Fourier Transform Infrared Spectroscopy(FT-IR),Vibrating Sample Magnetometer(VSM)and UV-Visible Spectrophotometer(UV-Vis).Results indicated that the modified Fe3O4magnetic carriers were coated with molecularly imprinted polymers.In comparison with magnetic molecularly non-imprinted polymers,Qu-MMIPs had better recognition performance for the Qu molecules.Static adsorption test and Scatchard analysis showed that two kinds of binding sites existed inbook=69,ebook=78Qu-MMIPs,and the corresponding dissociation constants were 1.646×10(-6)mol/L and 6.387×10(-6)mol/L.Furthermore,the maximum adsorption capacities of Qu onto Qu-MMIPs were 23.041 mg/g and 29.923 mg/g,respectively.
Key words:quercetin;magnetic nanoparticles;molecularly imprinted polymer;adsorption
作者简介:阮永欣(1988-),男,江苏徐州人,硕士生,主要从事磁性纳米功能材料的研究。E-mali:15214038152@163.com
基金项目:国家自然科学基金(51403091);甘肃省自然科学基金(1310RJZA081);省部共建有色金属先进加工与再利用国家重点实验室开放基金(SKL1315)
收稿日期:2015-11-16
文章编号:1008-9357(2016)01-0068-007
DOI:10.14133/j.cnki.1008-9357.2016.01.008
中图分类号:TB34
文献标志码:A
通信联系人:杜雪岩,E-mali:Duxy@lut.cn
