洛铂联合吉西他滨治疗晚期肺鳞癌疗效分析
2016-03-31孔天东沈志博
王 伟,孔天东,沈志博
(1.郑州大学第一附属医院肿瘤科,河南 郑州 450052;
2.郑州市第三人民医院、郑州市肿瘤医院,河南 郑州 450002;
3.郑州大学第一附属医院生物治疗中心,河南 郑州 450052)
洛铂联合吉西他滨治疗晚期肺鳞癌疗效分析
王伟1,2,孔天东2,沈志博3
(1.郑州大学第一附属医院肿瘤科,河南 郑州 450052;
2.郑州市第三人民医院、郑州市肿瘤医院,河南 郑州 450002;
3.郑州大学第一附属医院生物治疗中心,河南 郑州 450052)
[摘要]目的明确洛铂联合吉西他滨方案在晚期肺鳞癌中的疗效和安全性。方法入组66例晚期肺鳞癌患者分为2组,试验组30例患者接受洛铂联合吉西他滨化疗,对照组36例患者接受顺铂联合吉西他滨化疗,并比较观察2组的近期疗效和毒副反应。结果试验组有效率为36.7%,对照组为36.1%,差异无统计学意义(P>0.05);试验组Ⅲ、Ⅳ度血小板减少多于对照组,而Ⅲ、Ⅳ度恶心呕吐、乏力少于对照组,差异均有统计学意义(P均>0.05)。结论洛铂联合吉西他滨一线治疗晚期肺鳞癌近期疗效与顺铂联合吉西他滨方案相似,毒副反应方面存在差异,值得临床进一步研究。
[关键词]洛铂;吉西他滨;肺鳞癌
肺癌是目前全球发病率最高的恶性肿瘤[1],近年来发病率和死亡率逐年上升,其中非小细胞肺癌(non-smallcell lung cancer,NSCLC)占肺癌总数的80%~85%左右,鳞癌为NSCLC的一种,约占肺癌发病率的20%~30%[2-3]。最近10 a,肺腺癌的治疗发展迅速,各种新的有效的化疗药物及靶向药物层出不穷,总生存率有明显延长,但肺鳞癌治疗进展缓慢,靶向药物治疗进展缓慢,无特异性治疗靶点[4],对局部晚期或转移性肺鳞癌,化疗仍为主要治疗手段。化疗以紫杉类、吉西他滨、长春瑞滨联合顺铂或卡铂为主要治疗方案,但传统第1、2代铂类药物易产生耐药,洛铂为第3代铂类,具有低毒高效的优势,对顺铂、卡铂耐药患者无交叉耐药[5],目前在肺癌,尤其是肺鳞癌方面研究较少,本回顾性研究拟探讨洛铂联合吉西他滨一线治疗晚期肺鳞癌与顺铂联合吉西他滨在临床疗效及毒副反应方面的差异,为临床进一步研究提供借鉴。
1资料与方法
1.1入组标准组织学或细胞学明确诊断为肺鳞癌;有临床或影像学可明确测量病灶;经多学科会诊无法行手术切除;临床分期为Ⅲb~Ⅳ期;无脑转移病灶;无明显心脏或肝、肾功能损伤;无精神病史;既往未行抗肿瘤治疗;预期生存期>3个月;年龄18~75岁;ECOG评分0~1分;病历资料完整。
1.2排除标准合并肺纤维化或间质性肺炎;合并活动性感染(除外病毒性肝炎);有严重合并症不适合化疗;精神疾病。
1.3入组情况按照以上入组及排除标准,筛选我院从2010年6月至2014年6月资料完整患者,共纳入76例,其中试验组30例、对照组36例。
1.4治疗方案本回顾性研究共分2组,试验组患者接受洛铂联合吉西他滨化疗,具体方案:洛铂30 g·m-2,d1,静脉滴注;吉西他滨注射液1.0 g·m-2,d1,8,静脉滴注。对照组患者接受顺铂联合吉西他滨化疗,具体方案:顺铂70 g·m-2,d1,静脉滴注;吉西他滨注射液1.0 g·m-2,d1,8,静脉滴注。2组方案均21 d为2周期,至少完成1周期化疗后评价毒副反应,至少完成2周期化疗后评价近期疗效。
1.5评价标准近期疗效按实体瘤RECIST 1.0标准,分为完全缓解(CR)、部分缓解(PR)、稳定(SD)和进展(PD)[6],以CR+PR计算有效率。毒副反应按照NCI-CTC 4.0标准分为0~Ⅳ度[7]。
1.6统计学处理采用SPSS 17.0处理数据,计数资料比较采用χ2检验,检验水准α=0.05。
2结果
2.1一般资料2组患者的年龄、性别、临床分期、ECOG评分等一般资料比较差异无统计学意义(P>0.05),具有可比性。见表1。
表12组患者治疗前一般资料比较

项目试验组(n=30)对照组(n=36)χ2P年龄/岁 ≥6017151.4740.225 <601321性别 男21192.0330.154 女917临床分期 Ⅲb期11100.5960.440 Ⅳ期1926ECOG评分/分 010130.0560.814 12023
2.2近期疗效试验组有效率为36.7%,对照组为36.1%,差异无统计学意义(χ2=0.002,P=0.963)。见表2。
表22组近期疗效比较
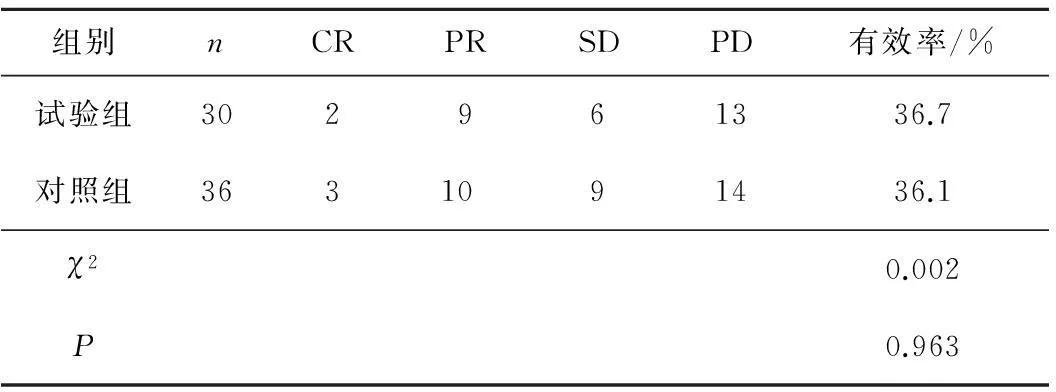
组别nCRPRSDPD有效率/%试验组302961336.7对照组3631091436.1χ20.002P0.963
2.3毒副反应试验组Ⅲ、Ⅳ度血小板减少多于对照组,而Ⅲ、Ⅳ度恶心呕吐、乏力少于对照组,差异均有统计学意义(P均>0.05)。见表3。
表32组毒副反应比较

毒副反应试验组(n=30)Ⅰ、Ⅱ度Ⅲ、Ⅳ度对照组(n=36)Ⅰ、Ⅱ度Ⅲ、Ⅳ度χ2P1)恶心呕吐7316125.0730.024乏力627138.0780.004白细胞下降1011763.4230.064贫血43520.0450.832血小板下降128733.9600.047神经毒性51740.5210.470肾毒性10320.4970.294耳毒性00511.0000.545皮肤黏膜炎52630.0001.000
注:1)Ⅲ、Ⅳ度毒副反应比较
3讨论
肺鳞癌的治疗方式近年来无明显变化,仍以手术、放疗、化疗为主,但许多患者在确诊时已属中晚期,失去手术机会,治疗以化疗为主[8]。临床上目前以传统第1、2代铂类联合长春瑞滨、吉西他滨及紫杉类为主要一线化疗方案。
吉西他滨是一种新型的抗代谢类化疗药物,该药主要作用于G2期及S期细胞,此外,吉西他滨活性产物二磷酸盐抑制核糖核酸还原酶,能够降低细胞分裂代谢所需的脱氧核苷酸量,从而使DNA链断裂,合成终止,进而使得细胞死亡[9]。有研究[10]提示对于NSCLC患者,尤其是鳞癌患者采用吉西他滨单药治疗有效率为15%~20%,其与铂类药物有协同作用,并且相互之间无交叉耐药性,吉西他滨联合铂类能够使鳞癌患者获得更好的疗效及生存期。
洛铂为第3代铂类,与其他铂类无交叉耐药,具有高效低毒、抗肿瘤作用强等特点[11],相比卡铂、顺铂等第1、2代铂类有独特的作用优势。洛铂最早由德国研发,2005年在我国批准上市。洛铂与第1、2代铂类空间结构相似,但洛铂中心铂离子右侧的离去集团由顺铂的氯离子变为环丁烷,肾毒性及耳毒性均明显降低;另外中心铂离子左侧的配基由顺铂的二氨基更改为乳酸,也减少了交叉耐药的发生[12]。在临床上洛铂几乎没有肾毒性、耳毒性及神经毒性,恶心呕吐反应轻,也不需水化,主要毒副反应可能是血小板减少,与剂量相关[13]。
洛铂很早就被用于NSCLC的治疗及研究。研究[12]表明,无论是体外还是体内研究,单药或联合,洛铂对NSCLC 都具有明确的抗肿瘤活性,并且联合化疗有更好的疗效,且对腺癌、鳞癌均有效。秦玲等[13]的一项Meta分析共纳入了12项洛铂对比顺铂治疗中晚期肺癌的RCT研究,6项为NSCLC,结果提示,在中国NSCLC患者中,洛铂及顺铂2组的客观疗效无明显差异,2组血小板减少也无明显差异,但洛铂组的Ⅲ、Ⅳ度胃肠道反应明显低于顺铂组。曾洪生等[14]的研究将洛铂、顺铂分别联合吉西他滨治疗NSCLC,其中有效率分别为36.0%、38.5%,1 a生存率分别为40.2%、43.5%,中位疾病进展时间分别为4.8、5.3个月,中位生存期分别为9.6、10.3个月,2组相似。洛铂组的Ⅲ、Ⅳ度血小板减少发生率明显高于顺铂组。在另一项有关洛铂及顺铂联合吉西他滨在老年晚期NSCLC的研究中,2组患者有效率、疾病控制率均相似,洛铂组血液学毒性明显高于顺铂组,白细胞减少、血小板减少及贫血发生率在洛铂组均较高,顺铂组恶心呕吐发生率较高[15]。我们的研究提示,洛铂联合吉西他滨和顺铂联合吉西他滨治疗肺鳞癌的有效率无明显差异,且前者的恶心呕吐、乏力明显少于后者,而血小板减少多于后者。
总之,洛铂联合吉西他滨在晚期鳞癌一线治疗中有临床可行性,适合体弱不能耐受顺铂的患者,但血液学毒性稍高,值得临床进一步研究。
参考文献:
[1]Siegel R, Ma J, Zou Z, et al.Cancer statistics, 2014 [J].CA Cancer J Clin, 2014,64(1):9-29.
[2]张宁宁,王阿曼.肺鳞癌的分子病理学研究进展[J].临床肿瘤学杂志, 2013,18 (10): 947-951.
[3]Piperdi B,Merla A,Perez-Soler R.Targeting angiogenesis in squamous non-small cell lung cancer[J].Drugs,2014,74(4):403-413.
[4]姜莹.肺鳞癌的分子靶向治疗研究现状及进展[J].山东医药, 2015, 55(44):104-107.
[5]黄勇,秦叔逵.洛铂治疗非小细胞肺癌的实验与临床研究现状及进展[J].临床肿瘤学杂志,2015, 20(10): 937-942.
[6]Khokher S, Qureshi MU, Chaudhry NA.Comparison of WHO and RECIST criteria for evaluation of clinical response to chemotherapy in patients with advanced breast cancer [J].Asian Pac J Cancer Prev, 2012,13(7):3213-3218.
[7]Liu YJ, Zhu GP, Guan XY.Comparison of the NCI-CTCAE version 4.0 and version 3.0 in assessing chemoradiation-induced oral mucositis for locally advanced nasopharyngeal carcinoma [J].Oral Oncol, 2012,48(6):554-559.
[8]杨静翔,罗虎,周向东.紫杉醇脂质体对比吉西他滨联合顺铂一线治疗中晚期肺鳞癌的疗效评价[J].第三军医大学学报, 2014,36(2): 140-143.
[9]Wickremsinhe ER, Lee LB, Schmalz CA, et al.High sensitive assay employing column switching chromatography to enable simultaneous quantification of an amide prodrug of gemcitabine (LY2334737), gemcitabine, and its metabolite dFdU in human plasma by LC-MS/MS[J].J Chromatogr B Analyt Technol Biomed Life Sci,2013,932:117-122.
[10]Wu YL, Lu S, Cheng Y, et al.Efficacy and safety of pemetrexed/cisplatin versus gemcitabine/cisplatin as first-line treatment in Chinese patients with advanced nonsquamous non-small cell lung cancer [J].Lung Cancer, 2014,85(3):401-407.
[11]杨柳青,秦叔逵.第3代铂类药物洛铂的研究新进展[J].临床肿瘤学杂志,2009,14(12): 1134-1139.
[12]黄勇,秦叔逵.洛铂治疗非小细胞肺癌的实验与临床研究现状及进展[J].临床肿瘤学杂志,2015,20(10):937-942.
[13]秦玲,吴巧萍,王天科.新一代铂类药物洛铂在中国肺癌患者治疗中效果的Meta分析[J].中国临床药理学与治疗学, 2015, 50(6):653-659.
[14]曾洪生,郭其森,傅玲.吉西他滨联合洛铂治疗晚期非小细胞肺癌疗效分析[J].山东医药, 2011, 51(19):29-31.
[15]全吉钟,冯燕,王冬旭, 等.吉西他滨联合洛铂或顺铂一线治疗老年晚期非小细胞肺癌患者的疗效 [J].中国老年学杂志, 2014,34(5):1181-1182.
Efficacy of Lobaplatin Combined with Gemcitabine in the Treatment of Patients with Advanced Lung Squamous Cell Carcinoma
Wang Wei1,2, Kong Tiandong2, Shen Zhibo3
(1.DepartmentofOncology,theFirstAffiliatedHospitalofZhengzhouUniversity,Zhengzhou450052,China;2.TheThirdPeople’sHospitalofZhengzhou,Zhengzhou450002,China;3.BiotherapyCenter,theFirstAffiliatedHospitalofZhengzhouUniversity,Zhengzhou450052,China)
[Abstract]ObjectiveTo investigate the efficacy and safety of lobaplatin combined with gemcitabine in the treatment of patients with advanced lung squamous cell carcinoma.MethodsSixty-six patients with advanced lung squamous cell carcinoma were divided into two groups, 30 patients of the experimental group received lobaplatin combined with gemcitabine, and 36 patients of the control group received cisplatin combined with gemcitabine, and the short-term efficacy and toxicities were compared.ResultsThe objective response rate in experimental group was 36.7%, and was 36.1% in the control group, there was no significant difference between the two groups (P>0.05).The incidence of Ⅲ and Ⅳ degree thrombocytopenia in the experimental group was higher than that in the control group, but the incidences of Ⅲ and Ⅳ degree nausea and vomiting, anergy were lower than those in the control group (P<0.05).ConclusionLobaplatin combined with gemcitabine in the first-line treatment of advanced lung squamous cell carcinoma has similar effectiveness with cisplatin combined with gemcitabine, but the toxicities is different, lobaplatin combined with gemcitabine is suitable for further clinical studies.
[Key words]lobaplatin; gemcitabine; lung squamous cell carcinoma
(收稿日期:2015-11-30)
[中图分类号]R734.2;R730.53
[文献标识码]A
[文章编号]1673-5412(2016)01-0026-04
DOI:10.3969/j.issn.1673-5412.2016.01.008
作者简介:王伟(1973-),女,副教授,副主任医师,硕士生导师,主要从事食管癌、肺癌、乳腺癌、肾癌等恶性肿瘤的临床和基础研究。E-mail:wangwei669@qq.com
基金项目:国家自然科学基金资助项目(编号:812111102、81171986、81271815);河南省科技攻关项目(编号:42102310330);河南省基础与前沿技术研究计划项目(编号:122300410102);河南省教育厅自然科学基础研究计划项目(编号:12A320053);郑州市普通科技攻关计划项目(编号:141PPTGG454);郑州市国际合作及交流项目(编号:141PGJHZ539);郑州大学第一附属医院青年基金项目
