洛铂联合吉西他滨治疗晚期非小细胞肺癌的临床研究
2017-06-20张健邵丽华
张健+邵丽华
【摘要】 目的 评价新一代铂类抗癌药物洛铂(LBP)联合吉西他滨(GEM)组成的GL方案治疗晚期非小细胞肺癌(NSCLC)的疗效及毒副反应。方法 72例经病理或细胞学确诊的NSCLC患者, 随机分为GL组及GP组, 各36例。GL组行GEM 1000 mg/m2, d1、8静脉滴注;LBP 30 mg/m2, d2静脉滴注。GP组行GEM 1000 mg/m2, d1、8静脉滴注;顺铂(DDP)30 mg/m2, d2~3静脉滴注。比较两组患者的疗效及毒副反应发生情况。结果 GL组完全缓解(CR)0例, 部分缓解(PR)13例, 稳定(SD)15例, 进展(PD)8例, 有效率(RR)为36.1%, 疾病控制率(DCR)为77.8%;GP组CR 0例, PR 12例, SD 17例, PD 7例, RR为33.3%(17/36), DCR为80.6%;两组RR、DCR比较差异无统计学意义(P>0.05)。GL组中位生存时间为9.8个月, GP组 为10.1个月, 两组比较差异无统计学意义 (P>0.05)。GL组粒细胞减少、血小板减少发生率稍高于GP组, 但差异无统计意义(P>0.05);GL组消化道反应如恶性呕吐、食欲不振发生率低于GP组, 差异具有统计学意义 (P<0.05), GL組患者未发现明显的肾毒性、听力下降等。结论 LBP联合GEM与DDP联合GEM治疗非小细胞肺癌疗效相当, 骨髓抑制相似, 但LBP联合GEM治疗患者消化道不良反应较轻, 耐受较好。
【关键词】 洛铂;吉西他滨;顺铂;晚期非小细胞肺癌
DOI:10.14163/j.cnki.11-5547/r.2016.36.006
【Abstract】 Objective To evaluate curative effect and toxic and side effects by lobaplatin (LBP), as a new anticancer platinum drug, combined with gemcitabine (GEM) as GL regimen in the treatment of advanced non-small cell lung cancer (NSCLC). Methods A total of 72 patients with pathologically or cytologically diagnosed NSCLC were randomly divided into GL group and GP group, with 36 cases in each group. GL group received 1000 mg/m2 GEM by intravenous drip in d 1 and 8, and 30 mg/m2 LBP by intravenous drip in d 2. GP group received 1000 mg/m2 GEM by intravenous drip in d 1 and 8, and 30 mg/m2 cisplatin (DDP) by intravenous drip in 2~3. Curative effects and toxic and side effects were compared between the two groups. Results GL group had 0 case with complete remission (CR), 13 cases with partial remission (PR), 15 cases with stable disease (SD) and 8 cases with progress disease (PD), with response rate (RR) as 36.1% and disease control rate (DCR) as 77.8%. GP group had 0 CR case, 12 PR cases, 17 SD cases and 7 PD cases, with RR as 33.3% (17/36) and DCR as 80.6%. There was no statistically significant difference of RR and DCR between the two groups (P>0.05). GL group had median survival time as 9.8 months, which was 10.1 months in GP group, and the difference between the two groups had no statistical significance (P>0.05). GL group had slightly higher incidences of granulocytopenia and thrombocytopenia than GP group, while their difference had no statistical significance (P>0.05). GL group had lower incidence of pernicious vomiting and anepithymia as gastrointestinal reactions than GP group, and their difference had statistical significance (P<0.05). There was no case with obvious renal toxicity or hearing loss in GL group. Conclusion Combination of LBP and GEM provides similar curative effect and myelosuppression in treating non-small cell lung cancer as DDP combined with GEM, while combination of LBP and GEM in treatment shows slighter adverse gastrointestinal reactions and better tolerance.
【Key words】 Lobaplatin; Gemcitabine; Cisplatin; Advanced non-small cell lung cancer
肺癌是我国发病率及死亡率均居首位的恶性肿瘤, 每年新发病例约70.5万, 死亡约为56.9万, 而NSCLC占肺癌80%~85%, 其中约2/3就诊时即为晚期, 对于晚期NSCLC铂类联合第3代细胞毒性药物是标准化疗方案[1-4]。DDP作为第1代铂类具有明显耳毒性及肾毒性, 且需要大量水化治疗, 而卡铂作为第二代铂类虽然肾毒性及耳毒性减轻, 但其骨髓抑制明显, 且疗效略逊于DDP。LBP作为第三代铂类药物疗效与DDP及卡铂具有相似抗癌活性, 且毒副反应较轻[5, 6]。本科于2014年6月~2015年6月对72例晚期NSCLC患者采用LBP或DDP联合GEM化疗, 观察LBP联合GEM方案的疗效和不良反应, 现报告如下。
1 资料与方法
1. 1 一般资料 选取2014年6月~2015年6月于本院就诊的72例晚期NSCLN患者, 均经病理组织学或细胞学确诊, 体力状况(PS)评分0~2分, 预计生存3个月以上, 具有可测量的原发灶和转移灶(脑转移除外), 能客观判断疗效, 治疗前肝肾功能及血常规均正常。将患者随机分为GL组和GP组, 各36例。GL组男28例, 女8例;年龄38~73岁, 中位年龄57岁;其中腺癌23例, 鳞癌10例, 鳞腺混合癌3例;ⅢB期24例, Ⅳ期12例。GP组男26例, 女10例;年龄38~70岁, 中位年龄55岁;其中腺癌24例, 鳞癌8例, 鳞腺混合癌4例。ⅢB期25例, Ⅳ期11例。两组患者性别、年龄等一般资料比较差异无统计学意义(P>0.05), 具有可比性。
1. 2 治疗方法 GL组予GEM(江苏恒瑞医药股份有限公司)1000 mg/m2, d1、8加入生理盐水100 ml中静脉滴注, LBP(海南海南长安国际制药)30 mg/m2, d2加入5%葡萄糖溶液500 ml中静脉滴注, 21 d为1个周期;GP组予GEM 1000 mg/m2, d1、8加入生理盐水100 ml中静脉滴注, DDP(江苏豪森药业股份有限公司)30 mg/m2, d2~3加入生理盐水500 ml中静脉滴注, 21 d为1个周期。两组化疗前均常规使用5-羟色胺3(5-HT3)受体拮抗剂止吐, GP组规范水化治疗, 监测血象和肝肾功能变化;给予重组人粒细胞集落刺激因子(G-CSF)、白细胞介素-11(IL-11)以及输血等对症处理以纠正骨髓抑制。
1. 3 观察指标及疗效评价标准 2个周期化疗结束后进行疗效评价, 有效病例于4周后进行疗效确认, 中位随访时间为12个月。肿瘤的客观疗效按照RECIST1.1标准分为CR、PR、SD和PD, RR(response rate)=(CR+PR)/总例数×100%, DCR(disease control rate)=(CR+PR+SD)/总例数×100%[7]。毒副反应根据NCI CTC 4.03标准进行评价[8]。
1. 4 统计学方法 采用SPSS19.0统计学软件对研究数据进行统计分析。计数资料以率(%)表示, 采用χ2检验;中位生存时间采用log-rank检验。P<0.05表示差异具有统计学意义。
2 结果
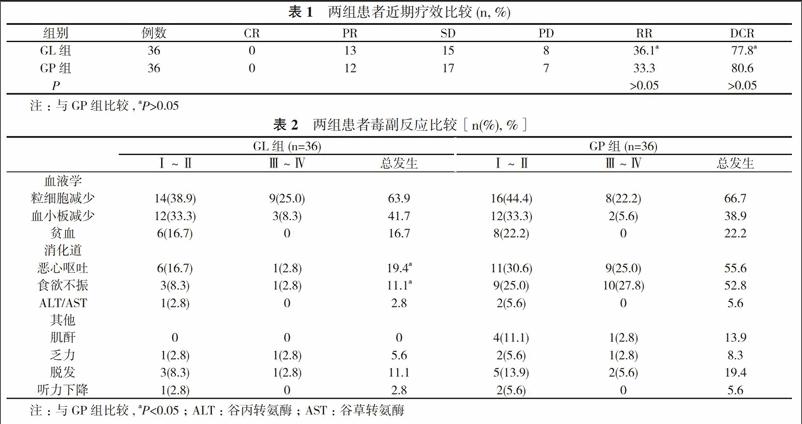
2. 1 临床疗效 近期疗效:GL组CR 0例, PR 13例, SD 15例, PD 8例, RR为36.1%, DCR为77.8%;GP组CR 0例, PR 12例, 将患者SD 17例, PD 7例, RR为33.3%, DCR为80.6%, 两组RR、DCR比较差异无统计学意义(P>0.05)。见表1。远期疗效:GL组中位生存时间为9.8个月, GP组 为10.1个月, 两组比较差异无统计学意义 (P>0.05)。
2. 2 毒副反应 骨髓抑制:GL组和GP组粒细胞减少发生率分别为63.9%、66.7%;血小板減少发生率分别为41.7%、38.9%, GL组粒细胞减少、血小板减少发生率稍高于GP组, 但差异无统计意义(P>0.05)。消化道反应:GL组和GP组恶心呕吐发生率分别为19.4%、55.6%, 食欲不振发生率分别为11.1%、52.8%, GL组恶心呕吐、食欲不振发生率均低于GP组, 差异有统计学意义(P<0.05);GL组未发现明显的肾毒性、听力下降等未见肾毒性及听力下降。见表2。以上不良反应经及时处理, 未影响化疗。
3 讨论
NSCLC起病隐匿, 发病时大部分患者为晚期, 对于晚期NSCLC患者化疗较最佳支持治疗能延长患者生存时间, 提高患者生活质量。以铂类联合第三代化疗药物方案有效率约17%~22%, 中位生存期7.4~8.1个月[9-12], 被认为晚期NSCLC标准的治疗方案。铂类也成为标准治疗基础用药。然而DDP肾毒性、耳毒性及严重的消化道毒性使其受到明显限制, 而寻求疗效相当毒副作用小的铂类而被国内外学者关注。
LBP是作为第三代新型铂类抗癌药, 沿用了前两代铂类顺式结构中心铂离子, 而离去基团采用更为稳定的环丁烷, 配基为乳酸, 而明显降低了耳、肾毒性, 减少交叉耐药, 同时LBP为两种非对异构体, 均可与DNA结合对多种肿瘤细胞株显示出抗癌活性[13, 14]。国外研究表明LBP与DDP的抗癌活性相似, 但肾毒性和胃肠道反应较轻, 且可能对部分DDP耐药的肿瘤有效[4]。目前SFDA批准LBP的适应证是小细胞肺癌、乳腺癌和慢性粒细胞性白血病, 而对于NSCLC国内学者正在积极探索之中。
本研究采用LBP或DDP联合GEM治疗晚期NSCLC, 结果提示GL组CR 0例, PR 13例, SD 15例, PD 8例, RR为36.1%, DCR为77.8%;GP组CR 0例, PR 12例, SD 17例, PD 7例, RR为33.3%, DCR为80.6%, 两组RR、DCR比较差异无统计学意义(P>0.05)。GL组中位生存时间为9.8个月, GP组 为10.1个月, 两组比较差异无统计学意义 (P>0.05)。与曾洪生等[15]分别应用LBP、PDD 联合GEM 治疗NSCLC报道(RR 36.0%VS38.5%, P>0.05)相一致。提示GL和GP方案两组疗效相似。毒副作用方面, GL组粒细胞减少、血小板减少稍高于GP组(63.9%VS66.7%, 41.7%VS38.9%), 但差异无统计学意义(P>0.05), 粒细胞减少应用G-CSF后可恢复;血小板减少短期内恢复正常, 无出血发生。GL组恶心呕吐、食欲不振发生率明显低于GP组(19.4%VS55.6%、11.1%VS52.8%, P<0.05)。与石沛[16]采用LBP或DDP联合GEM治疗晚期NSCLC研究骨髓抑制相似(白细胞、血小板减少60.5%VS55.2%、44.7%VS47.4%, P>0.05), 消化道反应(GL28.9%VSGP50.0%, P<0.05)相一致。同时在GL组未表现肾毒性、耳毒性, GL组脱发少于GP组, 提示GL与GP组骨髓抑制相似, 但消化道反应轻微, 无肾耳毒性, 依从性更好, 且不需水化, 给药方便。
综上所述, GL治疗晚期NSCLC疗效和GP方案相当, 但不良反应较GP方案低, 并可提高生活质量, 可作为晚期NSCLC治疗方案。
参考文献
[1] 陈万青, 郑荣寿, 张思维, 等. 2012年中国恶性肿瘤发病与死亡分析. 中国肿瘤, 2016, 1(24):1-8.
[2] Schiller JH, Harrington D, Belani CP, et a1. Comparison of four chemotherapy regimens for advanced non-small-cell lung cancer. N Engl J Med, 2002, 346(2):92-98.
[3] McKeage MJ. Lobaplatin:a new antitumour platinum drug. Expert Opin Investig Drugs, 2001, 10(1):119-128.
[4] Welink J, Boven E, Vermorken JB, et al. Pharmacokinetics and pharmacodynamics of lobaplatin (D-19466) in patients with advanced solid tumors, including patients with impaired renal or liver function. Clin Cancer Res, 1999, 9(5):2349-2358.
[5] 吴月明. 洛铂或顺铂联合吉西他滨治疗晚期非小细胞肺癌的疗效分析. 中国医师进修杂志, 2013, 36(17):66-67.
[6] 全吉钟, 冯燕, 王冬旭, 等. 吉西他滨联合洛铂或顺铂一线治疗老年晚期非小细胞肺癌患者的疗效. 中国老年学, 2014, 34(5):1181-1182.
[7] 阚庆生, 李红, 张长永, 等. 吉西他滨联合洛铂治疗老年晚期非小细胞肺癌疗效及安全性分析. 世界最新医学信息文摘:电子版, 2013(9):199-200.
[8] 劉淑, 郑玉龙, 王伟, 等. 吉西他滨联合奈达铂与吉西他滨联合顺铂治疗老年晚期非小细胞肺癌的临床研究. 现代肿瘤医学, 2010, 18(4):722-724.
[9] 李静静. 顺铂联合多西他赛或吉西他滨治疗晚期非小细胞肺癌的临床对照研究. 中国当代医药, 2011, 18(11):54-55.
[10] 黄岩, 刘云鹏, 周建英, 等. 培美曲塞联合顺铂对比吉西他滨联合顺铂一线治疗晚期非鳞非小细胞肺癌的随机、对照、多中心临床研究. 中国肺癌杂志, 2012, 15(10):576-582.
[11] 刘永玲, 王中民, 陆克亮, 等. 吉西他滨联合顺铂治疗晚期非小细胞肺癌临床观察. 中国基层医药, 2010, 17(4):445-446.
[12] 秦文文, 金普乐. 吉西他滨联合顺铂治疗晚期非小细胞肺癌临床观察. 河北医药, 2010, 32(22):3157-3158.
[13] 吴尉, 朱跃红, 袁志军, 等. 吉西他滨或培美曲塞联合顺铂治疗晚期非小细胞肺癌的临床比较研究. 临床和实验医学杂志, 2010, 9(8):576-577.
[14] 管薇. 洛铂和顺铂分别用于两药联合方案治疗晚期肺癌的对比研究. 吉林大学, 2013.
[15] 曾洪生, 郭其森, 傅玲. 吉西他滨联合洛铂治疗晚期非小细胞肺癌疗效分析. 山东医药, 2011, 51(19):29-31.
[16] 石沛. 顺铂和洛铂分别用于两药联合方案治疗晚期非小细胞肺癌的临床疗效观察. 中国地方病防治杂志, 2016, 31(2):198-200.
