血流感染病原菌分布及耐药性分析
2016-03-10李娟,赵英萍,郭淑丽等
血流感染病原菌分布及耐药性分析
李娟1*,赵英萍2,郭淑丽1,木克代斯1,韩雪1
(1.新疆维吾尔自治区人民医院,新疆 乌鲁木齐830001; 2.乌鲁木齐市明园石油医院 检验科)
血液细菌培养是对败血症和菌血症诊断和治疗的重要依据,随着近年来器官移植、抗生素、免疫抑制剂的大量使用及侵入性治疗措施的普遍开展,致使院内血流感染的发生率明显增加[1]。为临床患者的诊治提供更可靠的依据,快速了解患者血流感染病原菌分布和耐药性变迁情况就显得非常重要,本文回顾性分析本院2013年1月至2014年12月期间1430株血液细菌培养阳性结果。现报道如下。
1一般资料
1.1菌株来源选择本院2013年1月至2014年12月期间住院患者血液细菌培养结果为阳性的标本1430株,同一种菌同一患者多次培养的仅作一次统计。
1.2药敏纸片、E试验条和培养基美罗培南、头孢哌酮-舒巴坦、米诺环素、头孢西丁、苯唑西林﹑左氧氟沙星、头孢唑啉、阿米卡星、呋喃妥因、利福平和青霉素11种抗菌药物纸片及Optoching纸片均来自于英国OXOID公司。青霉素、美罗培南﹑万古霉素、亚胺培南E试验条、Mueller-Hinton(MH)培养基均来源于法国梅里埃公司。
1.3仪器与试剂血培养采用法国梅里埃公司生产的Bact/ALERT○R3D 全自动血培养仪及其配套的血培养瓶和北京伯盛泰科技有限公司生产的BST/MDS100全自动血培养仪及其配套的血培养瓶;菌种鉴定采用常规方法或法国梅里埃公司的VITEK 2 Compact鉴定系统及鉴定药敏试卡。诊断用金葡菌乳胶凝集试剂﹑肺炎链球菌特异单克隆乳胶试剂﹑β内酰胺酶试剂-Nitrocefin均来自于法国生物梅里埃公司。
1.4药物敏感试验药敏卡如无该抗生素即采用纸片扩散法。药敏试验结果的判断采用2013年CLSI推荐的标准执行[2]。质控菌株金黄色葡萄球菌ATCC25923、大肠埃希菌ATCC25922、肺炎克雷伯菌ATCC700603、铜绿假单胞菌ATCC27853、流感嗜血杆菌ATCC49247、肺炎链球菌ATCC49619均来自于上海汉尼生物技术有限公司。采用大肠埃希菌ATCC25922、铜绿假单胞菌ATCC27853、金黄色葡萄球菌ATCC25923标准菌株作每周的药敏质控。
1.5标本处理在患者寒颤或发烧时,无菌条件下采集静脉血,成人8-10 ml,儿童3-5 ml,婴幼儿1-2 ml,注入相应血培养瓶,置血培养仪中进行培养和监测,当仪器提示有细菌生长时,做涂片革兰染色,移种血平板、麦康凯平板、巧克力平板,置35℃培养18-24 h,镜检结果电话报告临床护士,发血培养一级报告。所有操作按照(全国临床检验操作规程)进行[3]
1.6数据统计分析采用WHONET5.6软件对鉴定及药敏结果进行统计学处理。
2结果
2.1菌种分布2013年1月-2014年12月由临床送检血培养标本11200份,共分离细菌1 430株,培养阳性率为12.8%,其中革兰阳性菌523株占36.6%,革兰阴性杆菌859株占60.1%,真菌48株占3.4%;排名前五位的细菌依次为大肠埃希菌25.5%、金黄色葡萄球菌15.9%、肺炎克雷伯菌属11.0%、凝固酶阴性葡萄球菌9.4%、马耳他布鲁菌7.7%。各种病原菌株的分布,见表1。

表1 1 430株血培养阳性菌种分布构成比
2.2革兰阳性菌对抗菌药物的耐药性分析
2.2.1葡萄球菌属523株阳性菌中葡萄球菌属363株(69.4%),检出耐笨唑西林葡萄球菌(MRSA)99株,阳性率为43.4%,耐笨唑西林凝固酶阴性葡萄球菌(MRCNS)119株,阳性率为88.1%,MRSA的耐药率远高于MSSA,MRCNS对大多数药物的耐药率都高于MRSA;为发现耐万古霉素、替考拉宁、利奈唑胺的菌株,见表2。

表2 葡萄球菌属对常用抗菌药物的耐药率(%)
2.2.2肠球菌属肠球菌属中检出屎肠球菌63株(67.7%),粪肠球菌30株(32.%3),屎肠球菌耐药率明显高于粪肠球菌,检出2株耐万古霉素、2株耐替考拉宁的屎肠球菌;4株耐万古霉素、3株耐替考拉宁的粪肠球菌,结果见表3。
2.2.3链球菌属共20株肺炎链球菌,其中成人分离株16株,儿童分离株4株。对苯唑西林抑菌圈直径不超过19 mm的有2株,经青霉素E试验确定2株为青霉素中介肺炎链球菌(PISP)10.0%,2株为高耐青霉素(PRSP)10.0%;检出无乳链球菌18株、化脓链球菌11株、草绿色链球菌18株。耐药率见表4。
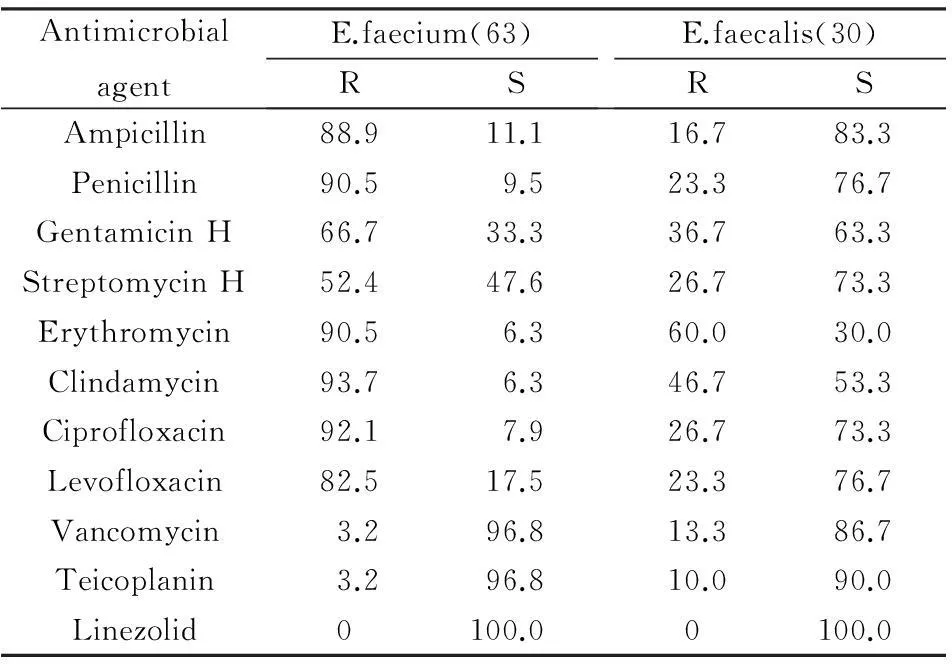
表3 肠球菌属对常用抗菌药物的耐药率(%)

表4 链球菌属细菌对抗菌药物的耐药率和敏感率(%)
2.4革兰阴性菌对抗菌药物的耐药性分析
2.4.1859株革兰阴性杆菌中大肠埃希菌365株(25.5%)、克雷伯菌属158株(11.0%)检出率最高,对哌拉西林、庆大霉素、妥布霉素、环丙沙星、左氧氟沙星、氨苄西林/舒巴坦及复方新诺明耐药率均在40%以上,发现对碳青霉烯类(亚胺培南和美罗培南)2株耐药、2株中介的肺炎克雷伯菌;未发现对大肠埃希菌的耐药株。马尔他布鲁氏菌110株(7.7%);鲍曼不动杆菌对多数抗菌药物耐药率均〉70%,对碳青霉烯类的耐药率已超过85%。沙门氏菌26株,除氨苄西林耐药率在65.4%,其他抗菌药物耐药率都较低在20%以下,见表5。

表5 主要革兰阴性杆菌对常用抗菌药物的耐药率(%)
3讨论
血流感染是临床严重的全身性感染,其发生率、病死率较高,及时准确将血培养结果通知临床医师,有助于早期诊断及治疗。我院2013年1月-2014年12月送检住院患者血液标本11200份,分离病原菌1430株,阳性率为12.8%,革兰阴性菌60.1%分离率明显高于革兰阳性球菌36.6%,接近国内文献报道[4-5]。往年病原菌的检出都是以凝固酶阴性葡萄球菌为主,近2年统计资料显示:大肠埃希菌占首位25.5%,并且阳性球菌中金黄色葡萄球菌15.9%的检出率高于凝固酶阴性葡萄球菌9.4%,可能与微生物实验室对临床医护人员正确及规范化血液采集有关。当然凝固酶阴性葡萄球菌的检出,在排除导致污染的因素外,其意义必须结合临床表现、是否双瓶采集及血培养报警时间判断。
葡萄球菌属中,耐笨唑西林金黄色葡萄球菌(MRSA)耐药率和耐笨唑西林凝固酶阴性葡萄球菌(MRCNS)耐药率分别为43.4%和88.1%;耐药率明显高于MSSA、MSCNS,虽然未发现耐药的万古霉素、替考拉宁、利奈唑胺的葡萄球菌,但屎肠球菌及粪肠球菌都发现对万古霉素、替考拉宁耐药、中介的菌株,值得关注,临床合理规范用药不容忽视,严格掌握万古霉素的使用,避免滥用造成耐药菌的增加。链球菌属近年来在血培养分离菌中有上升的趋势,由2013年23株迅速上升到2014年44株,与临床及时送检血液标本有密切关联;除红霉素、克林霉素、四环素、阿奇霉素外,其他抗生素耐药率都较低,未检出青霉素耐药的无乳链、化脓链和草绿色链球菌。
革兰阴性杆菌是以大肠埃希菌占首位,碳青霉烯类(亚胺培南和美罗培南)抗菌活性最强。未发现耐药菌株;克雷伯菌属检出率仅次于大肠埃希菌,对大多数的抗菌药物的耐药率都高于大埃希菌,并检出对碳青霉烯类(亚胺培南和美罗培南)2株耐药、2株中介的肺炎克雷伯菌;我院2011年经PCR检测多药耐药肺炎克雷伯菌发现均携带KPC-2基因和I类整合子,此次血培养耐药菌株是否携带此基因,还需进一步研究确认。检出沙门氏菌26株,除氨苄西林外,其他药物耐药率均较低。多耐药乃至泛耐药鲍曼不动杆菌在我院血培养标本中从2013年16株迅速上升到2014年78株,对大多数测试药物的耐药率均在70%以上,相对较低的米诺环素、头孢哌酮/舒巴坦耐药率分别为43.6%、44.7%。2年来共检出马耳他布鲁菌110株,检出率有逐年上升的趋势,此菌是生物危害极强的高致病性病原体,对培养及鉴定操作规程微生物实验室应严格按照生物安全要求执行,同时也要引起临床医师的高度重视。
参考文献:
[1]韩福禄,王文艳,庞莉.血培养常见病原菌分布及耐药性分析[J].中华医院感染学杂志,2012,22(3):630.
[2 ]Clinical and Laboratory Standards Institute.Performance standards for antimicrobial SusceptibilityTesting[S].M100-S23.CLSI,2013.
[3]叶应妩,王毓三.全国临床检验操作规程[M].第3版.南京:东南大学出版社,2010:500-514.
[4]洪亚明,范国萍,朱月霞,等. 血培养病原菌分布及耐药分析[J].中华医院感染杂志, 2012,22(24):5645。
[5]李光辉,朱德妹,汪复,等.2011年中国CHINET血培养临床分离率的分布及耐药性 [J].中国感染与化疗杂志,2013,13(4):241.
(收稿日期:2015-03-16)
文章编号:1007-4287(2016)02-0272-04
*通讯作者
