HGF/c—met传导通路在子宫内膜癌发生发展中的作用及意义
2015-12-28王江芬王月玲
王江芬 王月玲

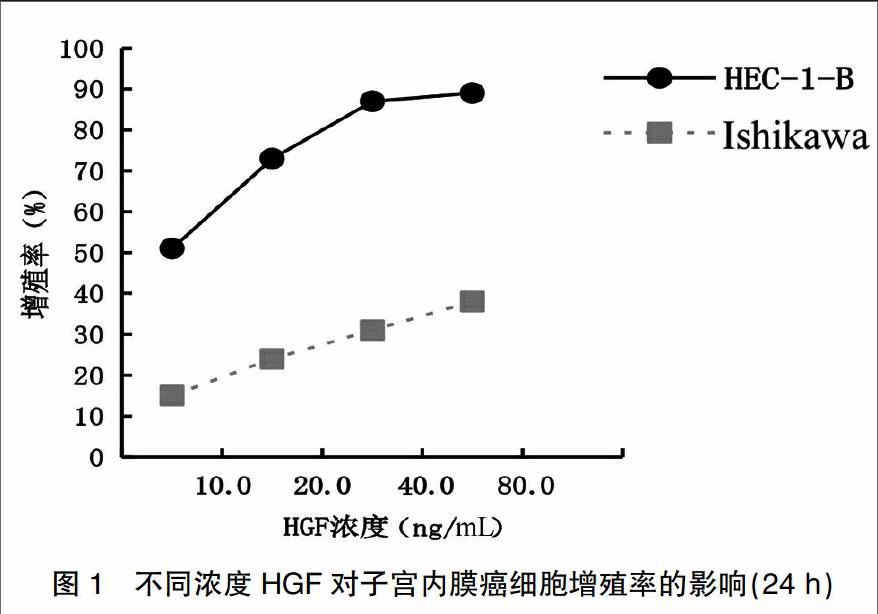

[摘要] 目的 检测HGF/c-met传导通路对Survivin、XIAP表达的影响,探讨HGF/c-met通路在子宫内膜癌发生发展中的作用机制。 方法 培养ER表达水平不同的子宫内膜癌细胞系HEC-1B(ER低表达)和Ishikawa(ER高表达),通过MTT法检测不同浓度HGF对两种细胞增殖率的影响;AnnexinV-FITC法检测不同浓度HGF对细胞凋亡率的影响。Western Blot检测Survivin及XIAP蛋白的表达水平。 结果 HGF可促进子宫内膜癌细胞的增殖,在80 ng/mL内具有剂量依赖性,在72 h内具有时间依赖性(P<0.05);当HGF浓度为40 ng/mL时,HEC-1B细胞24 h增值率达到(87.0±0.02)%,为最适诱导浓度。Survivin、XIAP mRNA及蛋白的表达随着HGF浓度的增高而上调,上调作用具有剂量效应关系。HGF在ER低表达的HEC-1B细胞中作用明显高于Ishikawa细胞,差异具有统计学意义(P<0.05)。 结论 HGF/c-met传导通路的激活可促进子宫内膜细胞增殖,抑制细胞凋亡,HGF/c-met可能是调控子宫内膜癌发生发展的分子靶点。
[关键词] 子宫内膜癌;HGF/c-met传导通路;Survivin;XIAP
[中图分类号] R737.33 [文献标识码] A [文章编号] 1673-9701(2015)32-0001-07
[Abstract] Objective To detect the influence of HGF/c-met pathway on expression of survivin and XIAP and to discuss the action mechanism of HGF/c-met pathway in occurrence and ddevelopment of endometrial cancer. Methods Cell lines of endometrial cancer with different ER expression level were cultivated: HEC-1B(ER low expression) and Ishikawa (ER high expression). The effects of HGF in various concentrations on cell proliferation rate of both cell lines were detected by MTT method, and effects on cell apoptosis rate were detected by AnnexinV-FITC method. The expression levels of survivin and XIAP were measured by western blot. Results HGF facilitated the proliferation of endometrial cells, which was dose-dependent within 80 ng/mL, and time-dependent within 72 h(P<0.05); When HCF=40 ng/mL, the 24 h proliferation rate of HEC-1B cells reached (87.0±0.02)%, and 40 ng/mL was the optimum inducing concentration. The mRNA and protein expressions of surviving and XIAP were up regulated by the rising HGF concentration, which had a dose-effect relationship. The effect of HGF on ER low expression HEC-1B cells was evidently higher than that on Ishikawa cells, the difference was statistically significant(P<0.05). Conclusion The activation of HGF/c-met pathway can facilitate the proliferation and inhibit the apoptosis of endometrial cells. HGF/c-met is probably the molecular target regulating the occurrence and development of endometrial cancer.
[Key words] Endometrial cancer; HGF/c-met pathway; Survivin; XIAP
子宫内膜癌是女性生殖系统三大恶性肿瘤之一。近年来,其发病率在世界范围内呈上升趋势[1]。子宫内膜癌发生发展的分子机制目前尚未完全明白。近年来,研究发现,肿瘤分子传导通路与肿瘤的发生发展密切相关[2,3]。c-met原癌基因编码肝细胞生长因子(hepatocyte growth factor,HGF)受体,HGF与c-met结合,激活c-met受体发生磷酸化,通过c-met信号通路发挥多种生物学效应[4]。文献报道,HGF/c-met传导通路在多种恶性肿瘤组织中过度激活,不仅c-met的表达水平上调,血清HGF浓度也增高,与肿瘤细胞的增殖,凋亡和侵袭能力有关[5]。本研究成员在前续实验中证实c-met在子宫内膜癌组织中表达上调,其上调程度与临床分期、组织学分级及淋巴转移相关[6]。
细胞增殖及凋亡受癌基因及抑癌基因调控,如Bcl-2家族,IAP家族等,IAP家族通过细胞色素c和细胞凋亡活化因子1抑制其下游因子caspase-9的活化,从而抑制细胞凋亡[7]。研究发现,HGF/c-met 传导通路通过AKT通路影响其下游因子Survivin、XIAP的表达进而影响大肠癌的增值和凋亡[8]。本实验通过体外HGF激活c-met传导通路,研究c-met在子宫内膜癌细胞系中的表达并进一步分析其下游因子Survivin、XIAP的表达,探讨其在子宫内膜癌发生发展中的作用,为进一步研究子宫内膜癌发生发展的分子机制提供理论基础。
1 资料与方法
1.1 细胞选择及来源
本实验所选择Ishikawa细胞为一种高分化的子宫内膜癌细胞,其雌激素受体表达为阳性。而低分化子宫内膜癌来源的HEC-1B细胞,其雌激素受体表达水平极低,国内学者大部分将其视为ER阴性的子宫内膜癌细胞[9]。本实验时间为2013~2015年。
1.2 主要试剂
RPMI1640培养基为GIBCO公司生产,胰酶为北京索莱宝科技有限公司生产(Solarbio),血清为兰州民海生物工程有限公司生产的优级新生牛血清。RNA提取试剂:RNAisoTMPlus宝生物工程有限公司,反转录试剂盒:PrimeScriptTMRT reagent Kit宝生物工程有限公司。HGF购自PeproTech公司,Survivin兔抗人多克隆抗体购自美国Sant Cruz 公司,XIAP兔抗人多克隆抗体购自bioworld公司,β-actin兔抗人多克隆抗体购自北京博奥森生物技术有限公司,羊抗兔二抗购自Pioneer Biotechnolgy。
1.3 实验方法
1.3.1 细胞培养 子宫内膜癌Ishikawa 和HEC-1B 细胞分别常规培养置于含10%胎牛血清(经56℃水浴30 min灭活)的RPMI 1640 培养基中,于37℃、5% CO2培养箱中培养,3~4 d传代一次。取对数生长期细胞为实验对象。
1.3.2 MTT法检测HGF对细胞增殖活性的影响 将生长良好的细胞接种于96孔板中,3×103个细胞/孔,分别加入不同浓度(0、10、20、40、80 ng/mL)HGF和PBS继续培养24 h后,加入MTT(5 mg/mL)20 μL/孔继续培养4 h,吸尽各孔中的培养液,加入DMSO 150 μL/孔,振荡10 min,使结晶物充分溶解后在酶联免疫检测仪上测定各孔在波长为490 nm处的吸光度(D)值。每组设5个复孔,实验重复3次。细胞增殖率=处理组吸光度值/对照组吸光度值-1。
1.3.3 AnnexinV-FITC法检测不同浓度HGF对细胞凋亡率的影响 不同浓度HGF(10、20、40 ng/mL)及PBS处理,细胞继续培养24 h后冰预冷PBS洗涤细胞两次,1000 rpm离心2 min,收集细胞,以106细胞/mL的浓度重悬于结合缓冲液中。取100 μL细胞悬液(105个细胞)加入离心管中,分别加入5 μL Annexin V-FITC和10 μL PI;轻轻震荡混匀,室温暗室孵育15 min。每管加入400 μL PBS,混匀,立即进行流式细胞仪分析。
1.3.4 RT-PCR半定量c-met、Survivin、XIAP mRNA 当细胞生长至80%融合时,分别加入不同浓度HGF(10、20、40 ng/mL)和PBS继续培养24 h,取细胞约106个,提取细胞总RNA,以0.5 μg总RNA为模板反转录合成第一链cDNA,反转录反应条件为85℃ 15 min、60℃ 5 s。所有引物均合成自华大基因公司,引物序列见表1。按照PCR反应试剂盒的说明设置反应条件如下,94℃热启动5 min,94℃变性30 s,退火30 s,72℃延伸30 s,扩增c-met、Survivin、XIAP、GAPDH片段,扩增反应的退火温度分别为55℃、58℃、55℃、55℃,反应循环均为30次。配置0.5×TBE buffer,制备2%琼脂糖凝胶,加样孔加样5 μL,50 V电压电泳30~40 min后凝胶成像分析,在适宜曝光速度下拍照,分析目标条带和内参照条带的荧光定量值。
1.3.5 Western blot检测细胞中Survivin、XIAP的蛋白表达 当细胞生长至80%融合时,分别加入不同浓度HGF(0、20、40 ng/mL)和PBS继续培养24 h,收获细胞后配置RIPA裂解液提取细胞总蛋白,并用BCA蛋白质定量试剂盒测定蛋白浓度。取50 μg总蛋白进行12% SDS-PAGE电泳,将电泳产物转移到NC膜上,在含5%脱脂奶粉的TBST中室温摇床封闭两小时,加入抗Survivin(1∶1000)、抗XIAP(1:500)单抗和抗β-actin单抗(1∶500 ),4°C孵育过夜。TBST洗膜3次,加入1∶5000稀释的辣根过氧化物酶标记的二抗,室温摇床培育1.5 h,按照ECL发光试剂盒说明书进行增强的化学发光显色。Bandscan凝胶图像分析软件进行光密度分析。
1.4 统计学分析
采用SPSS 13.0统计学软件进行分析。计量资料以均数±标准差(x±s)表示,以F检验检测数据方差齐性,采用方差分析并采用LSD-t检验进行组间比较。所有结果均以α=0.05做为检验水准,判定结果。
2 结果
2.1 MTT法检测HGF/c-met传导通路的激活对细胞增殖的影响
不同浓度HGF作用于子宫内膜癌细胞HEC-1B、Ishikawa 12、24、48 h后,各实验组增殖率较对照组均明显增高,且其增殖率呈HGF浓度及时间依赖性。在ER低表达的HEC-1B细胞中增殖作用明显高于ER高表达的Ishikawa细胞,差异具有统计学意义(P<0.05)。在HEC-1B细胞中,HGF浓度由40 ng/mL增高为80 ng/mL时,其增殖率差异无统计学意义,故40 ng/mL为最适诱导浓度;HGF(40 ng/mL)作用24 h增殖率为(87.0±0.02)%,差异具有统计学意义(P<0.05),故24 h为最适作用时间。见表2、图1、2。
2.2 Annexin V-FITC法检测HGF/c-met传导通路的激活对细胞凋亡的影响
不同浓度HGF作用子宫内膜癌细胞HEC-1B、Ishikawa 24 h后,早期凋亡细胞(右下象限)及中晚期凋亡细胞(右上象限)的百分比均减少。总凋亡率随着HGF浓度的增高而减少,具有剂量效应关系(表3、图4、5)。HGF对HEC-1B细胞的抗凋亡作用明显高于ishikawa细胞,差异具有统计学意义(图3)。
2.3 c-met在HEC-1B和Ishikawa细胞中的基础表达
通过RT-PCR半定量ER表达水平不同的两种子宫内膜癌细胞中c-met mRNA的相对水平,结果表明,ER高表达的Ishikawa细胞c-met表达水平较低,而ER低表达的HEC-1B细胞c-met明显高表达,对条带积光度进行分析,HEC-1B细胞中c-met mRNA表达量约为Ishikawa中的2.5倍(图6)。
2.4 HGF对c-met、Survivin、XIAP mRNA表达水平的影响
不同浓度HGF处理HEC-1B及Ishikawa细胞后,RT-PCR法半定量c-met、Survivin、XIAP mRNA,结果显示:HGF/c-met传导通路的激活可上调Survivin、XIAP mRNA的表达,且呈HGF剂量效应关系,在HEC-1B细胞中,该上调作用明显高于Ishikawa细胞,差异具有统计学意义(P<0.05),见图7、表4、5。
2.5 HGF对Survivin、XIAP 蛋白的表达
不同浓度HGF作用HEC-1B、Ishikawa细胞后,Survivin、XIAP蛋白表达升高,且其表达量呈HGF剂量效应关系。40 ng/mL HGF处理HEC-1B细胞后,Survivin表达水平较对照组上调2.1倍;XIAP较对照组上调2.2倍(图8、表6、7)。在HEC-1B细胞中,该上调作用明显高于Ishikawa细胞,差异具有统计学意义(P<0.05)。
3 讨论
目前,子宫内膜癌的发病机制仍不清楚,其发生发展涉及多个基因的异常,其中c-met的异常表达及其相关传导通路的调控近年备受关注。在子宫内膜癌组织中c-met高表达,对应血清HGF浓度也增高,二者构成异常自分泌环,促进肿瘤的发生发展[5]。
c-met是新近发现的一促癌因子,其是由原癌基因c-met编码的一种酪氨酸激酶受体, 与细胞增殖与存活、细胞迁移、诱导细胞极化、血管形成、损伤修复、组织重建等生物学效应相关[4]。研究表明,人类的许多肿瘤组织中均存在c-met的过表达,如胰腺癌、胃癌、结肠癌、肝细胞癌、肺癌、卵巢癌、乳腺癌和淋巴瘤等[10]。c-met在肿瘤中高表达,促进肿瘤细胞的增殖,侵袭及转移,并与肿瘤局部组织微血管形成有关,是恶性肿瘤靶向治疗的靶点之一[11]。但目前针对c-met基因在子宫内膜癌中的研究尚浅,大部分局限于表达异常,其下游因子及相关传导通路的研究尚少。本实验通过RT-PCR半定量ER表达水平不同的两种子宫内膜癌细胞中c-met mRNA的相对水平,结果表明,ER高表达的Ishikawa细胞c-met表达水平较低,而ER低表达的HEC-1B细胞c-met明显高表达,且HEC-1B细胞中c-met mRNA表达量约为Ishikawa中的2.5倍,与前续实验子宫内膜癌组织中c-met表达与ER呈负相关相一致[6]。这一结果从基因水平证实c-met在子宫内膜癌特别是ER低表达的子宫内膜癌发生发展中起重要作用,为我们下一步研究子宫内膜癌中c-met传导通路及下游分子奠定了基础。
研究表明,凋亡的抑制与肿瘤的发生密切相关。促进细胞增殖和抑制其凋亡的蛋白表达过多,使子宫内膜细胞逃逸生长调控,这可能是子宫内膜癌发病机制中的关键环节[12-14]。细胞的增殖、凋亡在正常情况下受许多信息的调控,肿瘤的形成与细胞增殖凋亡失衡密切相关。c-met作为癌基因,其表达产物促进细胞增殖,抑制细胞凋亡,在肿瘤形成过程中起着不可忽视的作用[5]。HGF作为c-met的配体,与c-met结合,激活c-met受体发生磷酸化,其酪氨酸激酶活性增强,通过c-met信号通路引起其下游多种底物蛋白磷酸化水平增高。c-met信号通路包括表面共存受体和相关下游通路(丝裂原活化蛋白激酶(mitogen-activated protein kinase,MAPK)、磷脂酰肌醇3-激酶(phosphoinositide 3-kinase,PI3K)和Stat3等[15,16]。本实验通过MTT法检测HGF/c-met传导通路的激活对子宫内膜癌细胞增殖的影响,AnnexinV-FITC法检测其对细胞凋亡的影响,结果表明HGF/c-met信号传导通路的激活可促进子宫内膜癌细胞增殖,抑制细胞凋亡,且呈明显的浓度依赖性。该生物学效应在ER低表达的HEC-1B细胞中较ER高表达的Ishikawa更明显,说明HGF/c-met传导通路的过度激活参与子宫内膜细胞异常增殖,凋亡受抑,从而导致子宫内膜癌的发生及恶性化,且其在ER低表达的子宫内膜癌发生发展中作用更为明显,这可能也是ER低表达的子宫内膜癌预后不良的一个可能因素。这一推论为我们提供了子宫内膜癌辅助治疗的新方法:阻断HGF/c-met传导通路,抑制c-met的激活可能成为子宫内膜癌特别是ER低表达或不表达子宫内膜癌的治疗及预防复发的新方法。
凋亡抑制蛋白(inhibitor of apoptosis protein,IAP)家族是一类广泛存在于酵母、昆虫及哺乳动物细胞中的进化上高度保守的细胞死亡抑制分子。迄今为止已确定的哺乳动物IAP家族成员有NIAP、c-IAPI、c-IAPZ、XIAP、appollon、Ts-XIAP、livin、Survivin、Bruce等[17-19]。本实验选取IAP家族中最具代表性的Survivin和XIAP作后续研究。Survivin表达的肿瘤特异性最强,因而受到了广大研究者的关注,然而Survivin与子宫内膜癌关系的研究目前仍局限于表达异常方面,其作用机制及相关通路调控研究尚少。X染色体连锁的凋亡抑制基因(X-linked inhibitor of apoptosis protein,XIAP)是凋亡抑制基因家族中重要的成员之一,其编码的蛋白XIAP通过选择性的抑制Caspase3、7和9,并参与其它途径来抑制细胞的凋亡,XIAP是该基因家族中唯一能够同时抑制起始和效应阶段的IAP[20]。子宫内膜癌中,c-met传导通路所引起的细胞增殖与凋亡抑制是否与IAP家族具有某种联系呢?国内外未见相关报道。本实验假定Survivin、XIAP为HGF/c-met传导通路的下游因子,通过HGF激活c-met传导通路,通过RT-PCR及western blot对Survivin、XIAP进行mRNA及蛋白的定量[21]。本实验研究结果显示,在子宫内膜癌HEC-1B和Ishikawa细胞中,HGF呈浓度依赖性诱导Survivin及XIAP的表达,在c-met高表达的HEC-1B中,该诱导作用更明显。在HEC-1B细胞中,HGF浓度为40 ng/mL作用24 h,Survivin 较对照组上调2倍,XIAP上调3倍。以上实验结果表明HGF/c-met传导通路的激活在转录及翻译水平上调Survivin、XIAP的表达,进而抑制子宫内膜癌细胞凋亡,促进细胞增殖,促进子宫内膜癌的发生发展。同时该结果提示Survivin、XIAP可能是HGF/c-met传导通路的下游因子,然而,该诱导作用是通过什么途径发挥的,尚需后续研究。
综上所述,HGF/c-met传导通路的激活可上调Survivin、XIAP的表达,促进子宫内膜细胞增殖,抑制细胞凋亡,且在ER低表达的子宫内膜癌中作用更显著,Survivin、XIAP可能是HGF/c-met传导通路的下游因子,该传导通路参与子宫内膜癌的发生发展,阻断该传导通路为我们提供了一条子宫内膜癌治疗及预防的新思路。子宫内膜癌的发病机制仍需要更为深入地研究。相信随着研究的不断深入,我们会更加深刻地了解HGF/c-met信号传导系统在子宫内膜癌中的功能,揭示其内在的分子机制以及潜在的临床应用价值。
[参考文献]
[1] Jonathan S,Berek N. 妇科学[M]. 北京:人民卫生出版社,2008.
[2] Mendes KN,Nicorici D,Cogdell D,et al. Analysis of signaling pathways in 90 cancer cell lines by protein lysate array[J]. Journal of Proteome Research,2007,6(7): 2753-2767.
[3] Su HY,Lai HC,Lin YW,et al. Epigenetic silencing of SFRP5 is related to malignant phenotype and chemoresistance of ovarian cancer through Wnt signaling pathway[J]. International Journal of Cancer,2010,127(3):555-567.
[4] Maulik G,Shrikhande A,Kijima T,et al. Role of the hepatocyte growth factor receptor,c-met,in oncogenesis and potential for therapeutic inhibition[J]. Cytokine & Growth Factor Reviews,2002,13(1):41-59.
[5] Kammula US,Kuntz EJ,Francone TD,et al. Molecular co-expression of the c-met oncogene and hepatocyte growth factor in primary colon cancer predicts tumor stage and clinical outcome[J]. Cancer Letters,2007,248(2):219-228.
[6] Yueling Wang,Weidong Dai,Jiangfen Wang,et al. Expression of estrogen receptor subtypes and c-met proto-oncogene in endometrial carcinoma and their correlation[J]. Academic Journal of Xian Jiaotong University,2010,22(1):54-58.
[7] Hunter AM,LaCasse EC,Korneluk RG. The inhibitors of apoptosis(IAPs)as cancer targets[J]. Apoptosis,2007,12(9):1543-1568.
[8] Takeuchi H,Kim J,Fujimoto A,et al. X-linked inhibitor of apoptosis protein expression level in colorectal cancer is regulated by hepatocyte growth Factor/C-met pathway via Akt signaling[J]. Clinical Cancer Research,2005,11(21):7621-7628.
[9] Guseva NV,Dessus-Babus SC,Whittimore JD,et al. Characterization of estrogen-responsive epithelial cell lines and their infectivity by genital Chlamydia trachomatis[J]. Microbes and Infection,2005,7(15):1469-1481.
[10] Ma PC,Maulik G,Christensen J,et al. c-met:Structure,functions and potential for therapeutic inhibition[J]. Cancer and Metastasis Reviews,2003,22(4):309-325.
[11] Abidoye Oyewale,Murukurthy Nadh,Salgia Ravi. Review of clinic trials:Agents targeting c-Met[J]. Rev Recent Clin Trials,2007,2(2):143-147.
[12] Ai ZH,Yin LH,Zhou XR,et al. Inhibition of survivin reduces cell proliferation and induces apoptosis in human endometrial cancer [J]. Cancer,2006,107(4):746-756.
[13] Nachmias B,Ashhab Y,Ben-Yehuda D. The inhibitor of apoptosis protein family(IAPs):An emerging therapeutic target in cancer[J]. Seminars in Cancer Biology,2004,14(4):231-243.
[14] Eckelman BP,Salvesen GS,Scott FL. Human inhibitor of apoptosis proteins:Why XIAP is the black sheep of the family[J]. Embo Reports,2006,7(10):988-994.
[15] Wang XF,Wu YH,Wang MS,et al. CEA,FP,CA125,CA153 and CA199 in malignant pleural effusions predict the cause[J]. Asian Pacific Journal of Cancer Prevention,2014,3(2):611-620.
[16] 高新萍,赵丽君. 子宫内膜癌患者血清及病理分子标志物与其病理特征关系的研究[J]. 中国妇产科临床杂志,2014,4(6):45-49.
[17] 赵玉斌. 子宫内膜癌EphB4、ERα和ERβ的表达及意义[J]. 中国妇幼保健,2014,6(28):33-36.
[18] Keam Bhumsuk,Im Seock-Ah,Lee Kyung-Hun,et al.Ki-67 can be used for further classification of triple negative breast cancer into two subtypes with different response and prognosis[J]. Breast cancer research:BCR,2013,21(2):71-82.
[19] Chen Yu-Li,Huang Chia-Yen,Chien Tsai-Yen,et al. Value of pre-operative serum CA125 level for prediction of prognosis in patients with endometrial cancer[J]. The Australian & New Zealand Journal of Obstetrics & Gynaecology,2014,11(3):61-70.
[20] A Ben Arie,O Lavie,M Gdalevich,et al. Temporal pattern of recurrence of stage I endometrial cancer in relation to histological risk factors[J]. European Journal of Surgical Oncology,2012,14(5):98-111.
[21] S Erkanli,F Kayaselcuk,E Kuscu,et al. Expression of survivin,PTEN and p27 in normal,hyperplastic,and carcinomatous endometrium[J]. International Journal of Gynecological Cancer,2012,3(6):11-23.
(收稿日期:2015-08-06)
