盐酸-磷酸络合浸出人造白钨矿试验研究
2015-12-16薛济来
刘 亮,薛济来
(北京科技大学 冶金与生态工程学院,北京 100083)
用盐酸浸出白钨矿为传统的钨工业生产方法,常温下其反应平衡常数约为104,从反应热力学数据看,反应能够快速完成,但实际生产中,由于浸出过程中产生的钨酸会致密包裹在未反应白钨矿表面,极大地阻碍反应的进行,反应速度较慢。已有学者对此进行了研究,通过降低矿物粒度[1]、加大盐酸用量、用盐酸-乙醇体系[2-3]等方法提高浸出速率,这些方法在一定程度上可以加速反应的进行,但也带来诸如增加生产成本、能耗、物耗,提高生产设备工艺要求(耐强酸反应设备),增大环境污染等问题。传统的钨矿分解,除了用盐酸浸出外,也有用苛性钠浸出、苏打高压浸出等方法[4],过程中会生成人造白钨矿,然后再通过酸分解、氨溶等处理并制备后续钨产品。
在钨分析技术中,有用盐酸-磷酸溶解白钨矿的研究报道[5-7],即在盐酸溶解过程中加入络合剂可获得可溶性钨杂多酸,但由于不同的白钨矿成分不同,试验结果也会有差异。根据白钨矿在盐酸-磷酸络合体系中可以生成水溶性磷钨杂多酸的特点,提出采用盐酸-磷酸络合体系浸出人造白钨矿获得磷钨杂多酸,主要化学反应为
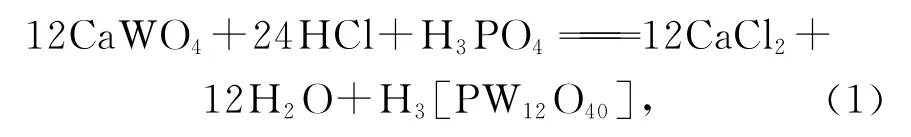
1 试验部分
1.1 试验原料
试验所用原料为人造白钨矿,采用分析纯二水合钨酸钠(w(Na2WO4·2H2O))≥99.5%)与氯化钙(w(CaCl2)≥96.0%)制备而成,其为球形颗粒,粒度大部分介于2~10μm之间,化学组成见表1,主要成分为钙、钨,也有极少量钠、硫等。主要矿物成分为钨酸钙。
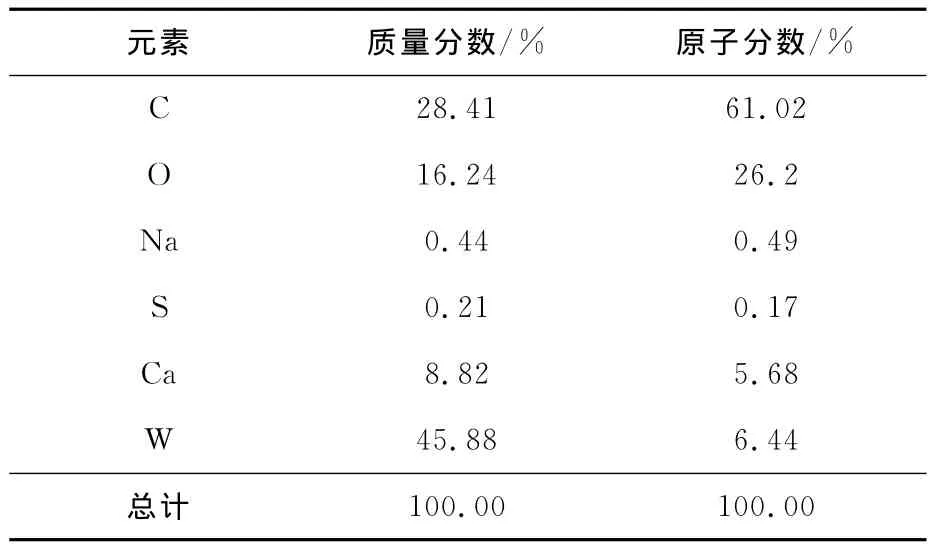
表1 试验所用人造白钨矿的化学组成
1.2 试验方法及过程
反应在三口平底烧瓶中进行,采用集热式磁力加热搅拌器(DF-1,荣华仪器)加热、搅拌并控温,用冷凝管对平底烧瓶进行冷凝。首先取一定量盐酸、磷酸及去离子水100mL于三口平底烧瓶中,低速搅拌升温至所需温度。随后称取白钨矿从取样口快速加入瓶中,同时开启搅拌并计时。反应以人造白钨矿全部溶解、溶液澄清为终点。到达设定时间后,用装有微孔滤膜的针管式过滤器定量抽取浸出液,同时补加同体积预配溶液。对浸出液采用可见分光光度法(UV-2000型,UNICO)测定钨质量浓度,计算钨出率。
2 试验结果与讨论
2.1 搅拌速度对钨浸出率的影响
搅拌速度对钨浸出率的影响试验结果见表2。反应温度50℃,盐酸初始浓度0.36mol/L,n(W)/n(P)=7/1(盐酸3mL,磷酸170μL,加去离子水至100mL)。反应5min及终点时,分别取样分析浸出液中钨质量浓度,计算钨浸出率。
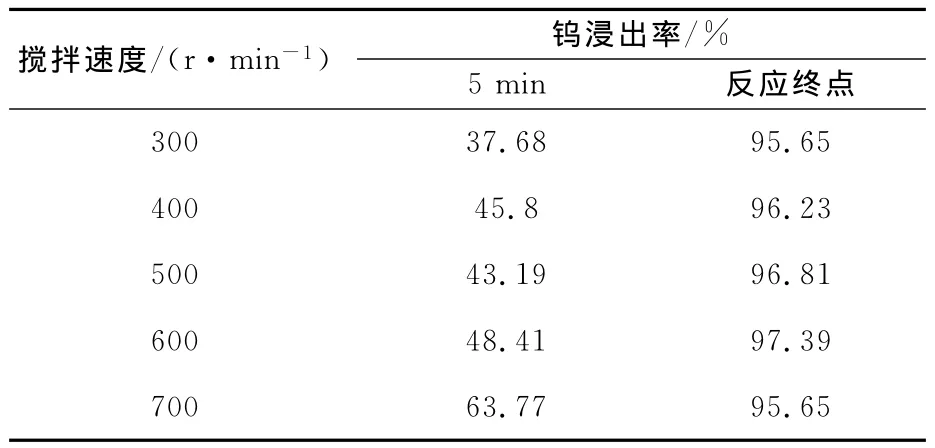
表2 搅拌速度对人造白钨矿浸出的影响
从表2看出:随搅拌强度加大,钨浸出率增大;但搅拌强度大于700r/min后,反应物被强烈搅动出现粘壁现象,致使钨浸出率有所下降。搅拌速度以300~700r/min为宜。反应5min时,不同搅拌速度下的钨浸出率在35%~65%之间。不同搅拌速度下,反应至终点所需时间不同:搅拌速度为300r/min时,反应至终点需要75min;而搅拌速度为700r/min时,反应至终点所需时间为50min。实际生产中,为了消除矿物原料反应时固液传质间的阻力,需要一定强度的搅拌[8],为保证固体颗粒充分悬浮,反应完全进行,而固体颗粒不至于出现粘壁现象,试验确定适宜的搅拌速度为600r/min。
2.2 n(W)/n(P)对钨浸出率的影响
加入磷元素可使反应产物由传统工艺的固体钨酸变为可溶性磷钨杂多酸。根据化学反应(1),磷酸根理论用量为钨酸钙物质的量的1/12。在温度50℃、盐酸初始浓度0.36mol/L、搅拌速度600r/min条件下,n(W)/n(P)对钨浸出率的影响试验结果如图1所示。
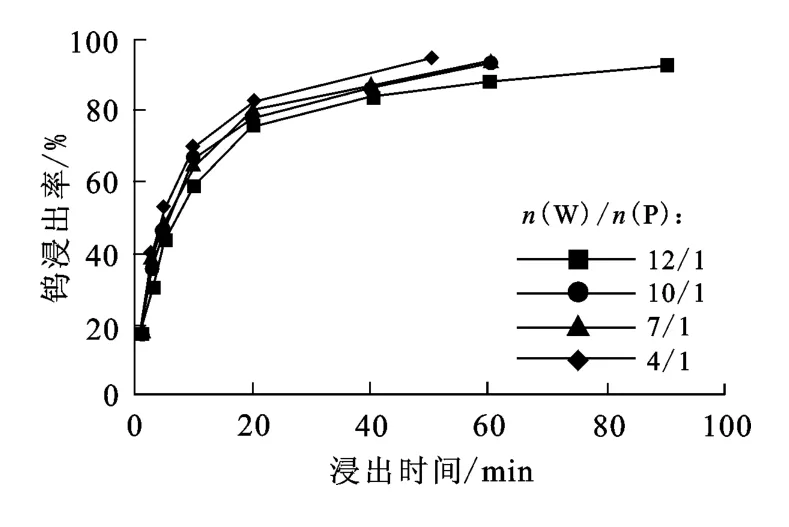
图1 n(W)/n(P)对钨浸出率的影响
从图1看出:不同n(W)/n(P)条件下的反应趋势基本相同,按生成12-磷钨杂多酸计算,n(W)/n(P)=12/1时,理论上正好反应完全。在此条件下,反应后期大部分磷酸已被消耗,盐酸浓度也有大幅降低,此时液相中剩余的反应物被溶剂阻隔,固液反应物分子间有效碰撞大大减少,反应速率明显下降,反应物全部溶解需90min。n(W)/n(P)为10/1、7/1条件下,反应于60min结束,钨浸出率略低;而n(W)/n(P)=4/1条件下,反应时间有所缩短,但磷酸用量过大,对后期的钨磷分离不利:所以,后期试验中n(W)/n(P)均采用7/1。
2.3 盐酸初始浓度对钨浸出率的影响
试验条件:温度50℃,n(W)/n(P)=7/1,搅拌速度600r/min。盐酸初始浓度对钨浸出率的影响试验结果如图2所示。
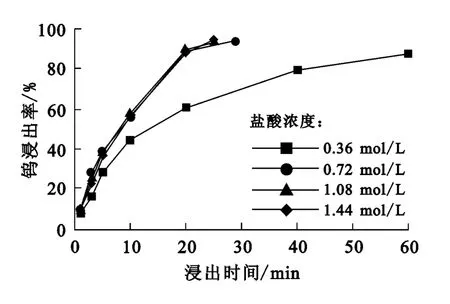
图2 盐酸初始浓度对钨浸出率的影响
从图2看出:盐酸浓度为0.36mol/L时,反应速率明显偏低,反应40min时钨浸出率仅为80%左右;相比之下,提高初始盐酸浓度至0.72mol/L,钨浸出率达95%所需时间仅为25min;但继续加大盐酸浓度,反应加速并不明显。综合考虑,后续试验中,盐酸初始浓度均确定为0.72mol/L。
设x为钨浸出率,不同盐酸浓度下的1-(1-x)1/3随反应时间的变化关系如图3所示。可以看出:在较高的盐酸浓度(0.72,1.08,1.44 mol/L)下,1-(1-x)1/3随时间的变化基本符合式(2)界面化学反应控速时液固多相反应动力学方程的直线关系,表明其反应过程为界面化学反应控制;而盐酸浓度为0.36mol/L时,反应初期(10min内)曲线基本呈直线,后期略偏离直线,这是因为盐酸逐步消耗而浓度下降,使得反应转为外扩散控制模式。
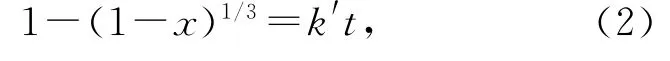
式中的k′为综合速率常数。
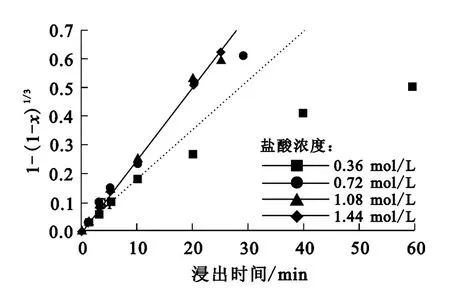
图3 不同盐酸初始浓度下,1-(1-x)1/3-t曲线
2.4 反应温度对钨浸出率的影响
试验条件:盐酸初 始浓度 0.72mol/L,n(W)/n(P)=7/1,搅拌速度600r/min。温度对钨浸出率的影响试验结果如图4所示。
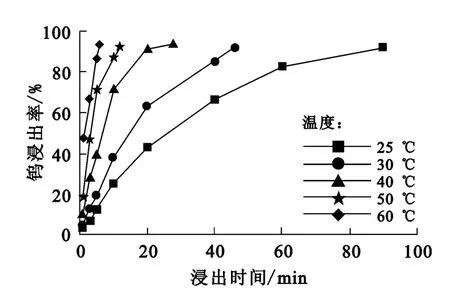
图4 反应温度对钨浸出率的影响
从图4看出:反应温度在25~60℃范围内,钨浸出率基本在95%以上(含取样损失);但反应速率随温度升高而加快,25℃时,反应至终点所需时间为90min,但升温至60℃时仅需6min。考虑到所用物料粒度较细,过高温度会引起回流损失,所以反应温度选择以50℃为宜。
对浸出率、浸出时间按1-(1-x)1/3-t作图,如图5所示。不同温度条件下,1-(1-x)1/3与时间基本呈直线关系,拟合后相关系数均大于0.99。由此表明,盐酸-磷酸络合浸出人造白钨矿的过程符合多相界面化学反应控速模型。反应速率常数见表3。
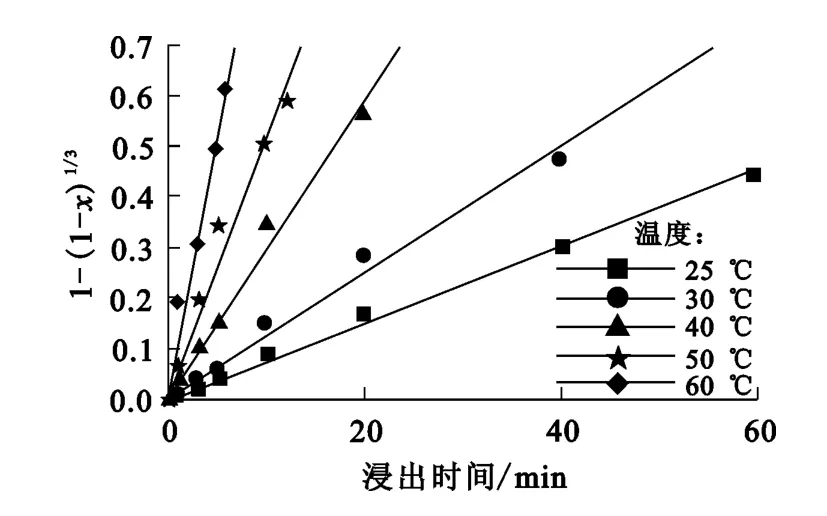
图5 不同温度下的1-(1-x)1/3-t曲线

表3 不同反应温度下的反应速率常数
2.5 反应的表观活化能
根据Arrhenius公式[9]

式中:k为温度为T时的反应速率常数;A为指前因子(频率因子);Ea为表观活化能;R为摩尔气体常数。对上式两边同时取对数,并以lnk对1/T作图,得直线斜率k′为

由此可求出表观活化能。计算过程及结果如图6所示,其中线性拟合相关系数为0.997 7,斜率为-7 295.197,代入式(4)求得浸出反应的表观活化能Ea=60.652kJ/mol。对于液固多相反应,界面化学反应控速时表观活化能一般在30~85 kJ/mol之间[10]。
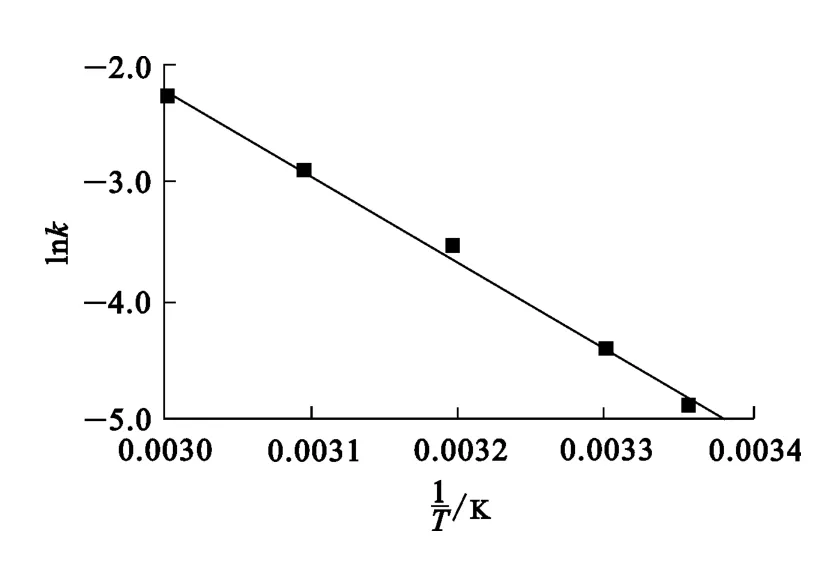
图6 白钨矿浸出过程中,不同温度条件下的lnk与1/T之间的关系
2.6 浸出液的红外光谱分析
盐酸-磷酸浸出人造白钨矿生成12-钨磷酸,n(W)/n(P)理论配比为12/1。由图1可知,反应速率随n(W)/n(P)增大而加快,但磷酸过量会造成浪费,同时也会增大后续钨、磷分离难度。天然白钨矿在n(W)/n(P)=12/1、90±0.5℃条件下反应20min,会有黄色的钨酸沉淀生成[5],研究者推断这是由于络合浸出反应生成了部分2∶18型磷钨杂多酸根离子:
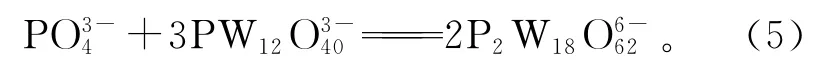
通常,该反应需要更多磷酸根参与。文献[11]表明:12-钨磷酸根离子[PW12O40]3-在水溶液中存在于pH≤2条件下,随溶液pH升高会发生碱性水解;而[P2W18O62]6-则在pH≤4条件下存在。本研究中,不同n(W)/n(P)条件下所得浸出液pH均在1.18~1.22之间,所以,2种杂多酸离子都可能存在。试验过程中,用磷酸作络合剂,人造白钨矿可以完全溶解但并未观察到黄色固态钨酸生成,这与文献描述不同。推测认为,相关文献中使用的是天然白钨矿,其中的脉石成分可能消耗了部分磷,导致生成了部分固态钨酸。为此,对钨磷物质的量比为12/1条件下络合浸出所得浸出液进行红外光谱测试,结果如图7所示。
根据文献[11],H3[PW12O40]·(6~7)H2O的红外光谱峰为1 080cm-1(P-O)、990cm-1(W=O),890cm-1(W-O-W),810cm-1(WO-W)。从图7看出:在600~1 100cm-1范围内有4条谱带,分别对应文献中的特征峰,表明浸出液主要成分为[PW12O40]3-;图谱中没有出现Dawson结构[P2W18O62]6-的特征峰,进一步证明络合浸出得到的是[PW12O40]3-。
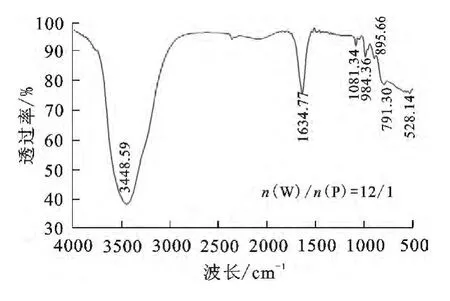
图7 浸出液红外光谱分析结果
3 最佳条件下的浸出试验
以盐酸-磷酸络合浸出人造白钨,同条件下进行两组试验。试验条件为:人造白钨矿质量5g,反应温度50 ℃,HCl初始浓度0.72mol/L,n(W)/n(P)=7/1,即盐酸体积6mL,磷酸170 μL,加水至100mL,搅拌强度600r/min。试验结果见表2。

表2 最佳条件下的人造白钨矿浸出试验结果
4 结论
用盐酸-磷酸体系络合浸出人造白钨矿是可行的,反应过程符合液固多相缩核反应模型,反应过程受界面化学反应控制,反应的表观活化能为60.652kJ/mol。试验条件下,盐酸-磷酸体系络合浸出人造白钨矿的最佳参数为:HCl初始浓度0.72mol/L,反应温度50℃,n(W)/n(P)=7/1,搅拌速度600r/min。最佳条件下,钨浸出率在98%以上,浸出产物为12-磷钨酸 H3[PW12O40]。
[1]李希明,陈家镛,Kammel R.细磨活化对白钨矿浸取行为的影响[J].金属学报,1991(6):83-87.
[2]Girgin I,Erkal F.Dissolution Characteristics of Scheelite in HCl-C2H5OH-H2O and HCl-C2H5OH Solutions[J].Hydrometallurgy,1993,34(2):221-230.
[3]Ozdemir S,Girgin I.Decomposition of Scheelite in Acid-alcohol Solutions[J].Minerals Engineering,1991,4(2):179-184.
[4]郭永忠,谢彦.我国钨湿法冶炼技术的研究进展[J].稀有金属与硬质合金,2009(3):39-42.
[5]Xuin G H,Yu D Y,Su Y F.Leaching of Scheelite by Hydrochloric Acid in the Presence of Phosphate[J].Hydrometallurgy,1986,16(1):27-40.
[6]Kalpakli A O.Dissolution Behavior of Calcium Tungstate in Oxalic Acid Solutions[J].Hydrometallurgy,2012,121/124:7-15.
[7]黄金,谢芳浩,肖海建,等.盐酸磷酸络合浸出白钨矿的试验研究[J].稀有金属,2014,38(4):703-710.
[8]荀国华,尢大钺,苏元复.盐酸-络合浸取白钨矿精矿的动力学研究[J].有色金属(冶炼部分),1984(6):45-48.
[9]华一新.冶金过程动力学导论[M].北京:冶金工业出版社,2004:28.
[10]李洪桂.冶金原理[M].北京:科学出版社,2005:298.
[11]伊万科热夫尼科夫,唐培堃.精细化学品的催化合成:多酸化合物及其催化[M].北京:化学工业出版社,2005:23,58.
