富G 寡核苷酸-N-甲基卟啉二丙酸荧光法测定铀
2015-07-13李名慧王永生
李名慧,王永生
(南华大学 公共卫生学院,湖南 衡阳 421001)
铀是一种无处不在的放射性元素。在工业废弃物中,铀主要呈阳离子复合物如氟化铀酰、碳酸铀酰、磷酸铀酰或硫酸铀酰等形式存在;在水溶液中,六价铀最为稳定[1]。随着经济社会发展,铀在军事和核能方面的应用日益增加,人们有更多的机会暴露于这种有害金属。因此,建立一种经济、快捷测铀的新方法也就势在必行。本文基于富G 寡核苷酸形成的G-四聚体能与NMM 作用导致荧光显著增强[2-4],而UO2+2与NMM 在酸性环境下作用导致荧光猝灭,并抑制NMM 与G-四聚体的作用,且荧光强度变化值与UO2+2浓度在一定范围内线性相关的原理,建立了富G 寡核苷酸-N-甲基卟啉二丙酸荧光法测定铀的新方法。
1 实验部分
1.1 试剂与仪器
醋酸双氧铀、NMM、HEPES、MES、Tris-HCl 等均为分析纯;DNA 制品:5’-AGGAAGATGGGAGGGAGGGAGGGTACTAT-3’;实验用水均为灭菌超纯水(电阻为18.26 MΩ);NMM 按照文献[4-5]配制。
UV-2550 紫外-可见分光光度计;F-4500 荧光分光光度计;AB204-S 电子分析天平;PB-21 型精密酸度计。
1.2 实验方法
取35 μL 2.16 ×10-6mol/L NMM 溶液,不同体积1.0 ×10-5mol/L UO2+2 标准溶液,40 μL pH 5.5的HEPES 缓冲溶液,40 μL 1. 0 mol/L KCl 溶液,40 μL 1.0 mol/L NaCl 溶液,依次加入2 mL EP 管中,用蒸馏水定容至450 μL,摇匀,常温下反应20 min,加入50 μL 1.0 ×10-6mol/L DNA,室温反应20 min,在荧光分光光度计进行560 ~700 nm 波长范围内扫描,设置λex= 399 nm,在λmax= 609 nm处记录空白组F0和实验组F,得ΔF=F0-F。
2 结果与讨论
2.1 荧光光谱特征
荧光光谱分析见图1。

图1 NMM--G-四聚体体系荧光光谱图Fig.1 Fluorescence spectra of the NMM--Gquadruplex system
NMM 本身具有微弱的荧光。NMM 能够特异性地识别G-四聚体[5],导致体系的荧光强度显著增强(图1,曲线1)。在酸性环境中,可与之发生反应猝灭荧光。应用不同浓度的在酸性环境下与一定量的NMM 作用后,再加入适量的G 四聚体,此时溶液中剩余的NMM 可与G 四聚体结合,使荧光增强。浓度越高,则剩余的NMM 量就越少,体系相应的荧光值也就越低,即浓度与体系的荧光值大小成反比(图1,曲线2 ~10)。由此说明,在实验条件下,NMM 可能与作用形成复合物。与游离的NMM 不同,可能形成的NMM-复合物不能通过π-π 堆积作用而结合到G-四聚体表面,导致体系的荧光猝灭,且与浓度线性相关。
2.2 实验条件的优化
2.2.1 缓冲溶液和pH 的选择 分别在pH 5.5 的MES、HEPES、Tris-HCl 3 种缓冲体系中进行实验,见图2。
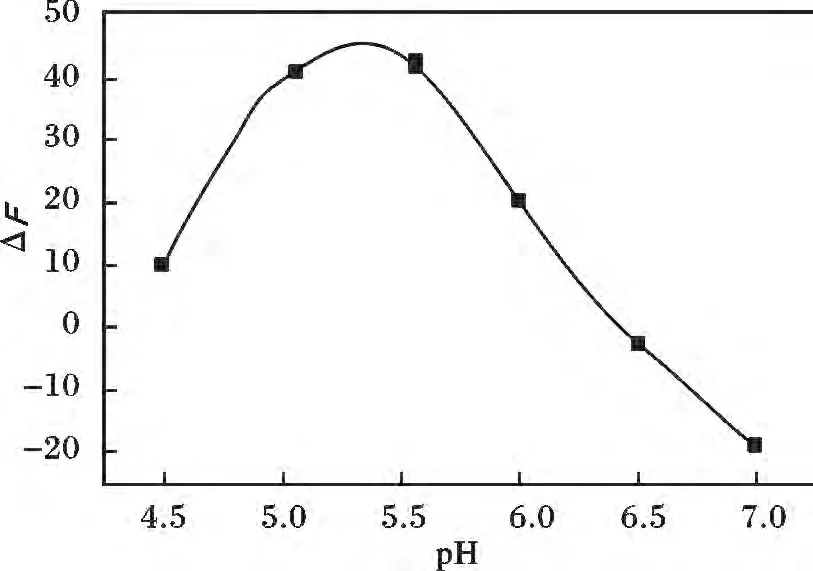
图2 pH 值对荧光值的影响Fig.2 Effect of pH value on the fluorescence cDNA =0.1 ×10 -6 mol/L;cNMM =0.15 ×10 -6 mol/L;cUO22+ =0.4 ×10 -6 mol/L
由图2 可知,该反应体系在HEPES 缓冲溶液中变化最明显。在HEPES 缓冲溶液中,在pH 5.5 处ΔF 值最大;当pH 接近中性时,反应趋于终止。故本实验选择pH 5.5 的HEPES 缓冲溶液控制体系的酸度。
2.2.2 KCl 和NaCl 浓度对反应体系的影响 研究了不同浓度KCl 和NaCl 对荧光值的影响,结果表明,当KCl 和NaCl 的浓度均为80 mmol/L 时,体系荧光值变化最明显。所以本实验采用80 mmol/L 作为KCl 和NaCl 的最优浓度。
2.2.3 反应温度对体系的影响 将反应体系分别在10,20,30,40,50,60,70,80,90 ℃的温度下进行反应。结果显示,反应在30 ℃时效果最好。温度过低,分子运动速度慢;温度过高时,形成的G-四聚体不稳定,NMM 无法与G-四聚体结合,从而影响实验结果。
2.3 干扰物质的影响
为了评价本实验对待测物的选择性,根据环境样品中其它金属离子可能共存的情况,进行了干扰实验。在相对标准偏差不超过10%的情况下,5 倍的Cu2+;10 倍的Ca2+;25 倍的Mg2+、Ni2+、Co2+、Pb2+;100 倍的Fe3+、Mn2+、Cr3+;200 倍的Hg2+、Cd2+均不会干扰实验测定。由此可看出,各金属离子对本方法的干扰较小,用本方法测选择性高。
2.4 标准曲线、检出限及精密度
依照实验方法,加入不同浓度的铀标准溶液进行实验,绘制标准曲线见图3。
由图3 可知,在1.29 ×10-7~7.0 ×10-6mol/L范围内,浓度与ΔF 呈线性关系,其回归方程为:ΔF=4.91 +3.91 c(×10-7mol/L),r=0.999 4。
根据CL= 3sb/k(sb为11 次空白值标准偏差,k为直线回归方程的斜率)公式计算检测限为3.86 ×10-8mol/L。平行配制11 管浓度分别为2. 0 ×10-7mol/L,1.6 ×10-6mol/L,5.0 ×10-6mol/L 的铀标准溶液进行精密度的测定,其相对标准偏差分别为2.7%,3.9%和2.3%。
2.5 样品分析
表1 样品中测定结果(n=6)Table 1 Determination results ofin the samples

表1 样品中测定结果(n=6)Table 1 Determination results ofin the samples
样品 测定方法 测定值/(mol·L -1) RSD/% 加标量/(mol·L -1) 测定总值/(mol·L -1) 回收率/% t 1 a 7.97 ×10 -7 0.70 5.0 ×10 -7 12.96 ×10 -7 99.8 1.06 b 7.93 ×10 -7 0.56 5.0 ×10 -7 12.75 ×10 -7 96.3 2 9.93 ×10 -7 2.15 5.0 ×10 -7 14.86 ×10 -7 98.5 2.07 b 10.16 ×10 -7 2.70 5.0 ×10 -7 15.01 ×10 -7 a 97.1
3 结论
[1] Solgy M,Taghizadeh M,Ghoddocynejad D. Adsorption of uranium(VI)from sulphate solutions using Amberlite IRA-402 resin:Equilibrium,kinetics and thermodynamics study[J].Annals of Nuclear Energy,2015,75:132-138.
[2] Hu D,Pu F,Huang Z,et al. A quadruplex-based,labelfree,and real-time fluorescence assay for RNase H activity and inhibition[J]. Chemistry,2010,16(8):2605-2610.
[3] Qin H,Ren J,Wang J,et al. G-quadruplex facilitated turn-off fluorescent chemosensor for selective detection of cupric ion[J]. Chem Commun(Camb),2010,46(39):7385-7387.
[4] Zhao C,Wu L,Ren J,et al.A label-free fluorescent turnon enzymatic amplification assay for DNA detection using ligand-responsive G-quadruplex formation[J]. Chem Commun (Camb),2011,47(19):5461-5463.
[5] Guo L,Nie D,Qiu C,et al. A G-quadruplex based labelfree fluorescent biosensor for lead ion[J].Biosens Bioelectron,2012,35(1):123-127.
