用于糖醇混合物氢解的Ni基催化剂
2015-06-28陈洁静孙兆林宋丽娟
陈洁静, 孙兆林, 宋丽娟, 姜 恒, 王 晓, 项 伟
(1. 中国石油大学 化学工程学院,山东 青岛 266580;2. 辽宁石油化工大学 辽宁省石油化工重点实验室,辽宁 抚顺 113001;3. 中国石油 抚顺石化公司,辽宁 抚顺 113001)
用于糖醇混合物氢解的Ni基催化剂
陈洁静1,3, 孙兆林1,2, 宋丽娟1,2, 姜 恒2, 王 晓3, 项 伟3
(1. 中国石油大学 化学工程学院,山东 青岛 266580;2. 辽宁石油化工大学 辽宁省石油化工重点实验室,辽宁 抚顺 113001;3. 中国石油 抚顺石化公司,辽宁 抚顺 113001)
制备了Ni-Ru/C催化剂,采用XRD、TEM和XPS手段进行了表征;以糖醇生产过程中富含糖醇的副产物---糖醇水溶液为原料,氢解制备乙二醇、丙二醇、丁二醇等低碳二元醇的反应评价其催化活性,并与Ni-Ru/Clay和Ni-Sn/C催化剂对比。结果表明,3种Ni基催化剂均具有较高的催化糖醇氢解反应的活性,Ni-Ru/C、Ni-Ru/Clay、Ni-Sn/C催化剂3次催化糖醇氢解的平均转化率分别达到92.10%、91.32%、94.90%;低碳二元醇的总收率和总选择性差别较大,Ni-Ru/Clay催化所得低碳二元醇总收率最高,Ni-Sn/C催化所得低碳二元醇总选择性最高。
糖醇;氢解;Ni基催化剂;对比
部分糖醇,如山梨醇和木糖醇,是重要的生物化学品。因其产自于生物质,且可通过生物或化学反应进一步转化为很多有价值的化学品或基本有机化工原料,已被确定为生物化工领域重要的基础原料[1-2]。近年来,山梨醇或木糖醇转化为乙二醇、丙二醇、丁二醇等低碳醇的工艺开发已成为一项前景良好、具有挑战性的课题[3],针对性的催化剂开发、反应条件优化相关研究不断增加[4-10]。
纯净木糖醇或山梨醇的生产流程长、工艺复杂,不但价格较高,且产量有限。因此尽管已有山梨醇氢解制低碳二元醇工业化装置建成[11],但出于经济性的考虑,该工艺工业化步伐仍然缓慢。寻求低廉糖醇原料和开发高效催化剂,是改进该工艺的关键。在某种糖醇生产过程中,产生一种富含糖醇的副产物——糖醇水溶液,其中含山梨醇、甘露醇、 木糖醇、阿糖醇等C5、C6糖醇。如能开发出适用的催化剂,将该糖醇水溶液用作低碳二元醇生产原料,将大幅度降低原料价格,具有较好的经济意义。
针对上述糖醇混合物水溶液转化为低碳二元醇,陈洁静等[12-13]开发了 Ni-Ru/黏土和 Ni-Sn/C催化剂。研究者们[8-9, 14-15]进一步开发了一种 Ni-Ru/C催化剂,同样取得了较高的转化率、选择性和收率,达到目前单质糖醇研究的最好水平。但是,糖醇氢解反应是典型的近临界水热反应,在此条件下使用的非均相催化剂,除了应具备化学活性之外,还面临原料稳定性的挑战[16-19]。传统有机化学和石油化工上应用的催化剂,提供了所需化学活性的材料,但大多数材料缺乏所需的稳定性。本课题组开发的3种催化剂均以石油化工所用加氢催化剂中最常用的金属Ni作为活性金属,以Ru、Sn作为第二金属,以黏土和活性炭作为载体,3种催化剂既有相同金属不同载体,也有相同载体不同金属。笔者对比了3种催化剂的制备方法、表面结构、产物分布,结合循环反应实验,考察了3种催化剂的稳定性,以探索对该催化剂进一步改进的方向。
1 实验部分
1.1 原料和试剂
催化剂制备所用原料Ni(NO3)2·6H2O由国药化学试剂公司提供,活性炭由福建鑫森炭业有限公司提供,NaOH、KOH试剂由国药集团提供,RuCl3·xH2O由沈阳金属研究所提供。糖醇混合物由长春和禾生物化工股份有限公司提供。
1.2 催化剂制备
称取322.1 g Ni(NO3)2·6 H2O,用2 L水溶解,搅拌下加热至90~95℃,然后加入100 g活性炭(椰壳炭,110℃下烘干12 h),搅拌1 h,加入88.69 g NaOH,成浆状液,老化、沉降、过滤和水洗后,120℃烘干,然后用100%H2,400℃ 下还原2 h,20℃下空气钝化,得到Ni/C催化剂。
称取6.86 g RuCl3·xH2O,加入200 mL水溶解。然后加入50 g Ni/C催化剂,滴加4.723 g KOH溶液(纯度89.5%),搅拌2 h。用去离子水洗涤,过滤至无Cl-,滤饼120℃烘干。按上述相同方式还原、钝化,得到Ni-Ru/C催化剂。
1.3 分析和表征
采用JEOL公司JEM 2100型透射电子显微镜观察催化剂颗粒的形状及大小(JEM-100CX,加速电压80 kV);采用Thermo Fisher公司Multilab 2000型X射线光电子能谱仪测定活性物质在载体上的分散状态(分析室真空≤5×10-8Pa,操作室真空≤1×10-5Pa);采用Micromeritics仪器公司A 2405型物理吸附仪测定试样的比表面积。采用气相色谱方法分析糖醇原料组成;采用Shimadzu LC 20 AT液相色谱仪测定产物组成;采用pH计测量反应物pH值。
1.4 糖醇混合物的氢解反应
实验所用原料糖醇混合物为植物芯秸水解装置残液,是含糖醇质量分数45%的水溶液。糖醇的主要成分为C5和 C6糖醇,其中,C5糖醇质量分数31%(木糖醇19%、阿拉伯糖醇12%),C6糖醇14%(山梨醇8%、甘露醇4%、卫矛醇2%)。
在2 L高压釜中,加入1200 g糖醇混合物水溶液(糖醇质量分数30.38%)、180 g Ni-Ru/C(或Ni-Ru/Clay、Ni-Sn/C)催化剂,加入NaOH调节pH值为11~13。通H2还原1 h,然后升压至12 MPa,逐渐升温至230~245℃,进行反应。随着反应的进行,压力逐渐降低,当压力下降至8 MPa时,补充H2至12 MPa。如此反复至压力基本稳定,继续反应20 min,反应完成,检测pH值。将反应物冷却、沉降、过滤,将反应产物与催化剂分离。反应产物蒸馏脱水,切除残液,得到馏分液,分析其组成。根据得到的馏分液质量和组成,计算低碳二元醇的转化率、收率和选择性。过滤后催化剂再重复使用2次。
二元醇收率(y)、糖醇转化率(x)和二元醇总选择性(s)分别由式(1)~(3)计算。
y=m(Di)/m(P)×100%
(1)
x=[m(C5+C6)-m′(C5+C6)]/m(C5+C6)×100%
(2)
s=m(D)/m(P)×100%
(3)
式(1)~(3)中,m(Di)为乙二醇、丙二醇或丁二醇中某一种二元醇质量,g;m(P)为蒸去水后的产物总质量,g;m(C5+C6)、m′(C5+C6)分别为原料中和产物中C5和C6多元醇的总质量,g;m(D)表示3种二元醇总质量,g。
2 结果与讨论
2.1 Ni-Ru/C、Ni-Ru/Clay和Ni-Sn/C的表征结果
2.1.1 N2吸附-脱附和XRD表征结果
3种催化剂组成和织构性质列于表1。表1中催化剂金属含量按制备原料投入量计算而得。Ni-Ru/Clay催化剂所用黏土的比表面积为132 m2/g、孔容0.41 cm3/g、平均孔径12.5 nm。活性炭载体比表面积为1729 m2/g、孔容1.13 cm3/g、平均孔径2.7 nm。与活性炭载体比较,Ni-Ru/C和Ni-Sn/C催化剂比表面积、孔容有大幅下降,但平均孔径基本未变,孔径分布主要在2.0~5.0 nm之间,平均仍在2.7 nm附近。
Ni-Ru/C、Ni-Ru/Clay和Ni-Sn/C催化剂的XRD谱示于图1。Ni-Ru/C的XRD谱显示,两侧馒头峰为无定型相的活性炭,2θ=31.74°处出现Ni2O3的特征衍射峰,未检测到Ru,可能是其高度分散于催化剂表面。Ni-Ru/Clay的XRD谱显示,在 2θ=20.42°处出现无定形态SiO2特征衍射峰,即黏土中SiO2有部分是以无定型形态存在的;2θ=26.66°处出现SiO2特征衍射峰,2θ为44.53°、51.93°出现Ni特征衍射峰,没有出现Ru的特征衍射峰,可能是Ru高度分散于催化剂表面的原因。Ni-Sn/C的XRD谱显示,2θ为44.78°、59.30°处出现Ni3Sn3特征衍射峰,2θ=43.00°处出现Ni17Sn3特征衍射峰,2θ=51.64°处出现Ni特征衍射峰,2θ为30.34°、63.31°处出现Ni3Sn2特征衍射峰,2θ=34.40°处出现Ni2SnO4特征衍射峰。

表1 Ni-Ru/C、Ni-Ru/Clay和Ni-Sn/C催化剂的金属含量和织构性质
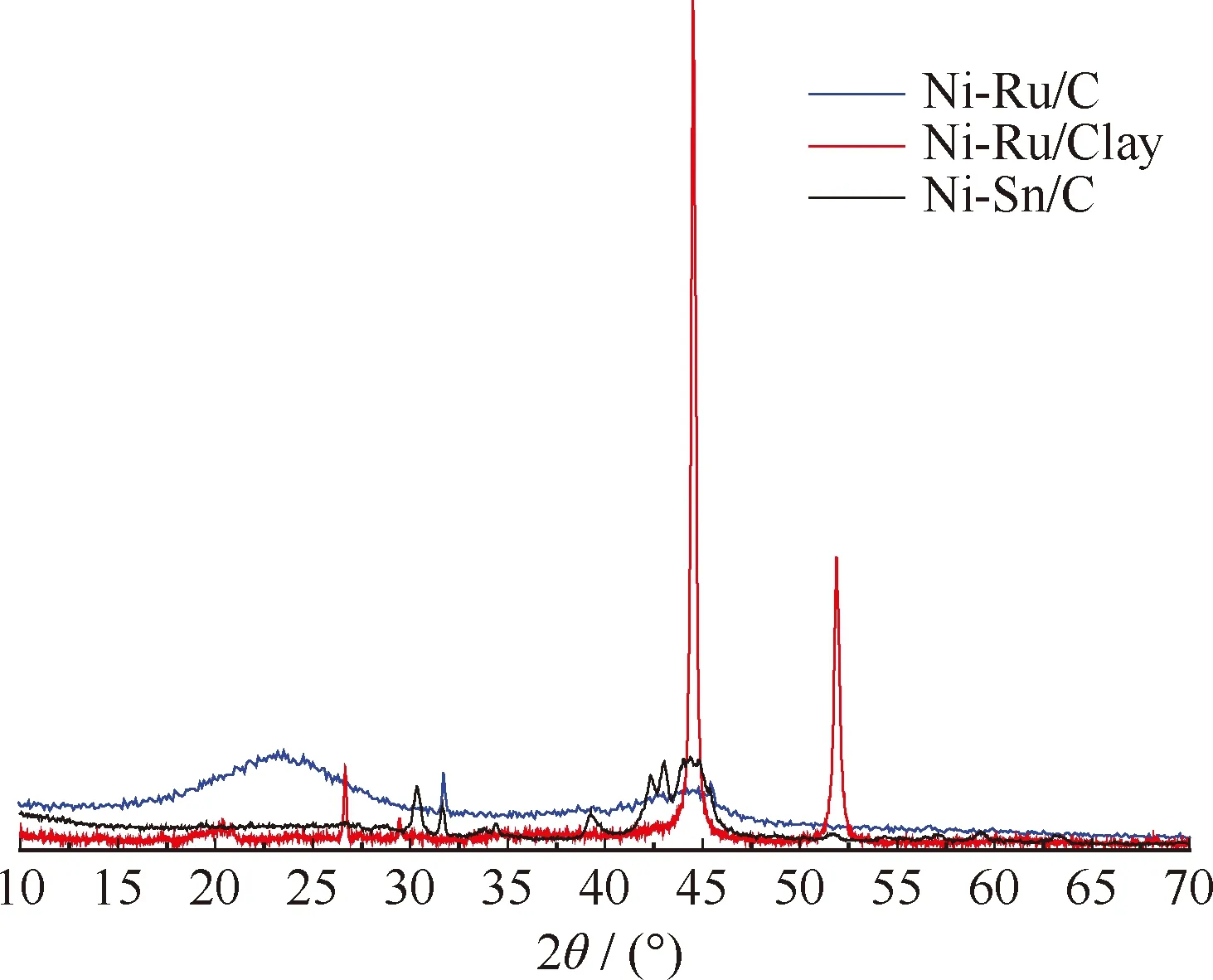
图1 Ni-Ru/C、Ni-Ru/Clay和Ni-Sn/C催化剂的XRD谱
2.1.2 TEM表征结果
图2为3种催化剂的TEM照片,用来检测载体上金属分布情况。 从图2(a)、(b)可以清晰地看到,Ni-Ru/C和Ni-Sn/C表现为典型的活性炭结构;Ni-Ru/C的颗粒分散均匀,约在1.7~1.9 nm,能谱分析显示既有Ni颗粒,也有Ru颗粒存在,C、Ni、Ru元素以79.5%、15.8%、4.7%(质量分数,下同)存在; Ni-Sn/C表面颗粒分散均匀,约3.0~5.0 nm,能谱分析显示,C、O、Sn、Ni元素以60.8%、9.1%、12.9%、17.2%存在,结合XRD表征,表面颗粒应为纯氢还原后形成的Ni、Sn粒子。从图2(c)可见,Ni-Ru/Clay表现为典型的棒状黏土形态,其表面颗粒约为1.0~1.2 nm,均匀分布在催化剂表面,能谱分析显示,催化剂中O、Mg、Al、Si、Ni、Ru元素以42.3%、6.9%、6.6%、30.5%、12.5%、1.2%存在,与Ni/Clay催化剂的TEM照片[12]相比,可确定这些颗粒应为Ru粒子。
2.1.3 XPS表征结果
图3为相同金属的Ni-Ru/C 和 Ni-Ru/Clay 2种催化剂的Ni2p、 Ru3d、 C1s、 Ru3p和 O1sXPS谱,用以检测催化剂表面上Ru、Ni 粒子的分布和化学价态。由图3可见,污染C和载体C的C1s谱峰重叠,并与已知C1s的XPS数据相符,因此XPS结果可信[20]。
Ni-Ru/Clay和 Ni-Ru/C 2种催化剂的Ru3d、Ru3pXPS谱明显不同。Ni-Ru/Clay在280.6 eV处出现Ru3d谱峰,应为单质Ru;Ni-Ru/C 的Ru3d、Ru3p谱峰同时出现,位于463.3 eV应为Ru2+(RuO),而276.1 eV处应为Ru3+化合物[21]。虽然XRD表征未出现Ru的特征峰,但TEM及XPS表征均证实有Ru的存在。
Ni-Ru/Clay和 Ni-Ru/C 2种催化剂的Ni2pXPS谱的形状虽有些相似,但2种催化剂载体完全不同,Ni的状态也不相同。在Ni-Ru/Clay催化剂制备过程中,其3个阶段Ni2pXPS谱基本相同[12],显示催化剂上Ni的状态相同,854.7 eV处应为NiO[22]。Ni-Ru/C催化剂是在Ni/C上进一步负载金属Ru,并再次还原和钝化后制备而成,其Ni2pXPS谱的856.1 eV处应为Ni2O3。图3 O1sXPS谱显示,2种催化剂表面主要是晶格氧,与Ni2pXPS的表征结果相一致。
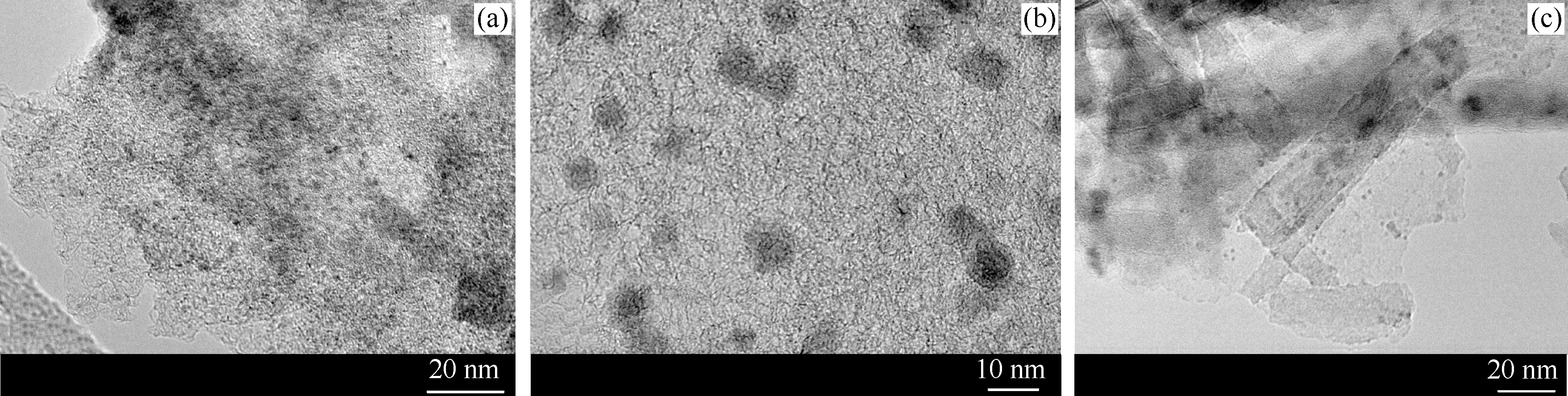
图2 Ni-Ru/C、Ni-Ru/Clay和Ni-Sn/C 3种催化剂的TEM照片

图3 Ni-Ru/C和Ni-Ru/Clay的Ni2p、Ru3d、C1s、Ru3p和O1s的XPS谱
2.2 Ni-Ru/C、Ni-Ru/Clay和Ni-Sn/C对糖醇氢解的催化活性和产物分布
2.2.1 催化活性
Ni-Ru/C、Ni-Ru/Clay和Ni-Sn/C对糖醇混合物氢解反应的催化活性和产物收率、选择性结果列于表2。其中,总收率指的是乙二醇、丙二醇、丁二醇和其他醇,即全部低碳醇总质量与原料中各种糖醇总质量之比,选择性指的是乙二醇、丙二醇、丁二醇3种低碳二元醇总质量占全部低碳醇总质量之比。
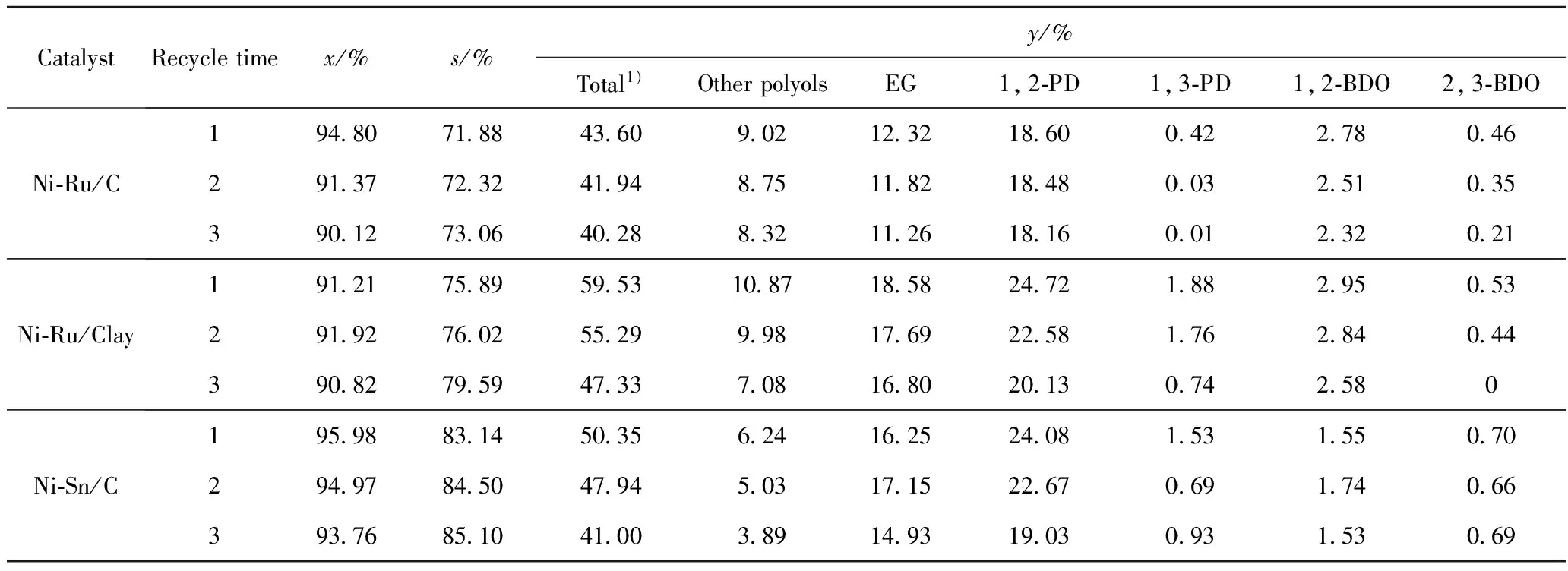
表2 3种Ni基催化剂催化糖醇混合物氢解反应的性能
1) Other polyols + EG + PD + BDO; EG—Ethylene glycol;PD—Propylene glycol;BDO—Butanediol
θ=235-245℃;p=11-12 MPa; pH value of 11.5; Mass fraction of sugar alcohol mixture of 30.38%
从表2可以看出,3种Ni基催化剂对糖醇氢解反应均具有较高的催化活性,但低碳醇总收率和总选择性差别较大。以Ni-Ru/Clay为催化剂时,低碳醇总收率最高,总选择性居中;以 Ni-Sn/C为催化剂时,低碳醇总选择性最高,总收率居中;Ni-Ru/C催化剂的性能较上述2种催化剂略差。
3种催化剂随重复使用次数增加,均出现转化率略有降低、低碳醇总收率明显下降、选择性逐渐增加的现象。从反应过程分析,反应系统不仅是水热反应,而且存在酸碱环境的变化,反应前系统是pH值为12~13的碱性水溶液,因反应过程中乳酸等有机酸的生成,pH值下降到3~5,为酸性水溶液。这种反应条件的变化无疑影响了催化剂稳定性。
催化剂的稳定性包括两方面,一方面是活性金属的稳定性,另一方面是载体的稳定性。选择活性炭作为催化剂载体,也是基于活性炭耐酸碱,化学性质稳定,具有发达的孔隙结构和巨大的比表面积[23-24]。选择黏土作为催化剂载体,主要是因其具有不可还原性,具有独特的分散、耐高温、抗盐碱等良好的胶体性质[25]。基于前期的相关基础及探索性实验[16-18],选择金属Ni作为活性金属,并引入Ru、Sn元素。本课题组曾在与本实验相同的反应条件下,采用6种含Ni的商品催化剂、1种Ru催化剂进行氢解反应实验,其中仅1种含Ni质量分数3%的Ni基催化剂和Ru催化剂所得转化率低于90%外,其余Ni质量分数在20%以上的5种Ni基催化剂催化糖醇氢解反应的转化率均能达到90%以上。
由表2还可见,以Ni-Ru/Clay为催化剂时,第一次催化糖醇氢解反应的低碳醇总收率达到59.53%,3种目的产物总选择性达到75.89%。催化剂较高的活性归功于Ni的作用,较高选择性归功于金属Ru的引入[12]。Ru结晶核首先形成小的Ru原子簇,当还原时,Ni原子沉积在Ru原子簇上,形成Ni-Ru双金属簇,提高了Ni的分散度[26-27],从而显著地提高了低碳二元醇的选择性。相比另2种催化剂而言,Ni-Ru/Clay催化剂制备时是采用湿混法将Ni与黏土混合,因此Ni在催化剂中的分散不够均匀,且催化剂的比表面积很小,但催化糖醇氢解的性能却很好,表明对糖醇氢解反应而言,催化剂的比表面积、Ni分布的均匀性不是关键,而金属种类、含量和修饰金属的分布才是根本的影响因素。随着Ni-Ru/Clay使用次数的增加,所得低碳醇总收率下降应是受pH值变化的影响。虽然黏土能够耐受高温和碱性环境,但在氢解反应后期,因有机酸的生成,溶液变为酸性,黏土中的MgO、CaO等碱性氧化物与体系中的酸性物质作用,导致本身结构发生变化[28],从而使催化剂氢解催化活性减弱,发生其他副反应。因此,尽管反应转化率不变,反应物中二元醇选择性增加,但总收率下降。
Ni-Sn/C第一次催化糖醇氢解反应的低碳醇总收率达50.35%,3种目的产物总选择性可达83.14%。选择性高的原因是Sn的引入[13]。实验证明,Ni-Sn/C催化剂制备方法不同,效果相差很大。采用Ni和Sn同时负载到活性炭载体上的制备方法时,Ni-Sn/C催化剂才会具有较高活性和选择性,如采用与Ni-Ru/C催化剂相同的制备方法,在Ni/C催化剂上第二步负载金属Sn,催化剂不具有反应活性[13]。上述现象主要归功于适量的Sn修饰促进了活性物种Ni的分散,Sn大部分与Ni紧密结合,形成Ni-Sn粒子,从而才能获得较高的催化活性和目的产物选择性[22, 29-30]。随着Ni-Sn/C催化剂使用次数的增加,收率明显下降,说明催化剂活性不够稳定。应是因金属Ni、Sn采用浸渍沉淀法负载在活性炭载体上,化学组成不够稳定,Ni、Sn易流失的结果。Shabaker等[22]在与本实验条件极其相似的含氧烃类物质水相重整制氢反应中也发现同样问题,负载的Ni基催化剂失活迅速,其根本原因是受水热反应的影响,金属聚集或流失到反应物中。
与Ni-Ru/Clay催化剂相比,Ni-Ru/C催化糖醇氢解反应的转化率基本相同,目的产物总选择性、收率偏低,其中Ru的引入作用相同,均为显著地提高了二元醇的选择性。与Ni-Sn/C催化剂相比,Ni-Ru/C催化糖醇氢解的转化率,目的产物总选择性、收率均偏低,并且从制备方法和金属价格上看,Ni-Sn/C催化剂均优于Ni-Ru/C催化剂。
综合而言,在下一步的相关研究中,可考虑仍采用Ni为活性金属的催化剂。催化剂中Ni质量分数宜控制在20%以上,且Ni以NiO状态存在活性更好。Ni基催化剂中的修饰金属既可用Sn,也可用Ru;Sn与Ni形成Ni-Sn粒子,更有利于提高催化剂活性,而Ru以单质或RuO状态存在的活性更高。载体选择方面,应规避在水热和酸碱环境中不稳定的物质,如黏土、氧化铝、氧化硅等,可尝试化学性质更加稳定的物质,如α-氧化铝、氧化锆等。制备方法方面,宜考虑采用湿混法[31]或其他化学组成更加稳定的方法。Ni-Ru催化剂制备时,可将Ni、Ru分步负载;Ni-Sn催化剂制备时,宜将Ni、Sn同时负载。
2.2.2 反应产物分布
3种Ni基催化剂催化糖醇氢解反应的产物基本相似,均主要是1,2-丙二醇和乙二醇(见表2),说明糖醇混合物中的C5糖醇、C6糖醇氢解遵循了同样的规律。在存在Ni基催化剂、碱性条件下,木糖醇等C5糖醇一般发生C(2)—C(3)键的断裂,产物主要是1,2-丙二醇和乙二醇;山梨醇氢解主要发生在C(3)—C(4)及相连的O原子上,产物主要是1,2-丙二醇。稍不同于Ni-Ru催化剂,Ni-Sn催化剂催化糖醇氢解反应物中丁二醇的收率较低,但其中2,3-丁二醇含量稍有增加。在木糖醇氢解为乙二醇、丙二醇过程中,关键控制步骤在于第一步的脱氢过程,最终产物分布由金属表面的加氢反应和碱催化反应竞争决定[9]。因此,Ni-Sn催化剂与Ni-Ru催化剂催化糖醇氢解产物分布的不同应是第二步的加氢反应的不同所致。
3 结 论
(1)制备的Ni-Ru/C催化剂,Ni质量分数为38.0%,Ru质量分数为5.08%,催化剂比表面积为1166.2 m2/g,孔容为0.78 cm3/g。其催化糖醇混合物氢解反应的平均转化率达92.10%,低碳二元醇总收率平均达41.94%,低碳二元醇总选择性平均达72.42%。
(2)Ni-Sn/C、Ni-Ru/C、Ni-Ru/Clay 3种催化剂3次催化糖醇混合物氢解反应的平均转化率依次降低,而低碳二元醇平均总收率由高到低的催化剂顺序为Ni-Ru/Clay、Ni-Sn/C、Ni-Ru/C,平均总选择性由高到低的催化剂顺序为Ni-Sn/C、Ni-Ru/Clay、Ni-Ru/C。
(3)用于糖醇混合物氢解反应的催化剂以Ni为活性金属为宜,修饰金属选用Sn或Ru,均可取得较好效果。
[1] WERPY T, PETERSEN G. Top value added chemicals form biomass 1 Results of screening for potential candidates form sugars and synthesis gas[R]. Washington D.C.:US DOE report, 2004.
[2] 闵恩泽. 利用可再生农林生物质资源的炼油厂——推动化学工业迈入“碳水化合物”新时代[J]. 化学进展, 2006, 18(2/3): 131-141.(MIN Enze. Developing biorefinery by utilizing agriculture and forestry biomass resource striding forward the "carbohydrate" era [J]. Progress in Chemistry,2006, 18(2/3): 131-141.)
[3] JI N, ZHANG T, ZHENG M Y, et al. Direct catalytic conversion of cellulose into ethylene glycol using nickel-promoted tungsten carbide catalyst[J]. Angew Chem Int Ed, 2008, 47(44): 8510-8513.
[4] WERPY T, FRYE J. Hydrogenolysis of 5-carbon sugars, sugar alcohols and compositions for reactions involving hydrogen: US, 6677385[P]. 2003.
[5] WERPY T, FRYE J. Hydrogenolysis of 5-carbon sugars, sugar alcohols, and other methods and compositions for reactions involving hydrogen: US, 6479713[P]. 2002.
[6] WERPY T, FRYE J. Hydrogenolysis of 6-carbon sugars and other organic compounds: US, 6841085[P]. 2003.
[7] GIUSEPPE G, BRUNO C. Ruthenium-based catalyst for producing lower polyhydric alcohols: US, 5403805[P]. 1995.
[8] WERPY T, FRYE J. Hydrogenolysis of 5-carbon sugars, sugar alcohols, and methods of making propylene glycol: US, 7038094[P]. 2004.
[9] SUN J, LIU H. Selective hydrgenolysis of biomass-derived xylitol to ethlene glycol and propylene glycol on supported Ru catalysts[J]. Green Chem, 2011, 13(1): 135-142.
[10] BANU M, SIVASANKER S, SANKARANARAYANAN T M, et al. Hydrogenolysis of sorbitol over Ni and Pt loaded on NaY [J]. Catalysis Communication, 2011, 12(7): 673-677.
[11] 尤新. 生物合成产业化最新领域—可再生资源代替石油原料生产化学品[J]. 精细与专用化学品, 2005, 13(3/4): 5-8.(YOU Xin. Novel field for biosynthesis industrialization: Renewable resource producing chemicals instead of petroleum materials [J]. Fine and Specialty Chemicals, 2005, 13(3/4): 5-8.)
[12] 陈洁静,孙兆林, 宋丽娟,等. NiRu/黏土催化糖醇混合物氢解制低碳二元醇[J]. 石油化工, 2012, 41(4): 401-404.(CHEN Jiejing, SUN Zhaolin, SONG Lijuan, et al. Hydrogenolysis of sugar alcohol mixture to low carbon dihydric alcohols over Ni-Ru/clay catalyst [J]. Petrochemical Technology, 2012, 41(4): 401-404.)
[13] 陈洁静,孙兆林, 宋丽娟,等. 用于糖醇混合物氢解制低碳二元醇的NiSn/炭催化剂[J]. 石油化工, 2014, 43(7): 816-820.(CHEN Jiejing, SUN Zhaolin, SONG Lijuan, et al. NiSn/C catalyst for hydrogenolysis of sugar alcohol mixture to lower diols [J]. Petrochemical Technology, 2014, 43(7): 816-820.)
[14] GUBITOSA G, BRUNO C. Method for producing lower polyhydric alcohols and a new ruthenium-catalyst used in this method: US, 5600028[P]. 1997.
[15] ZHAO L, ZHOU J H, SUI Z J, et al. Hydrogenolysis of sorbitol to glycols over carbon nanofiber supported ruthenium catalyst [J]. Chemical Engineering Science, 2009, 11(6): 1281-1284.
[16] DOUGLAS E. The use of catalysts in near-critical water processing [C]//Chapter T13-KN in Joint 20th AIRAPT - 43th EHPRG International Conference on High-Pressure Science and Technology.Forschungszentrum Karlsruhe, Karlsruhe, Germany, 2005.
[17] DOUGLAS E, KEITH P. Effects of trace contaminants on catalytic processing of biomass-derived feedstocks [J]. Applied Biochemistry and Biotechnology, 2004, 115(1): 807-825.
[18] DOUGLAS E, TODD H. Catalyst and method for aqueous phase reactions: US, 5977013[P]. 1999.
[19] DOUGLAS E, TODD H. Method for aqueous phase reactions: US, 6152975[P]. 2000.
[20] 辛勤. 固体催化剂研究方法[M].北京:科学出版社,2004: 497-558.
[21] ALEXANDER V N, ANNA K V, STEPHEN W G, et al. NIST X-ray Photoelectron Spectroscopy(XPS)Database[EB/OL]. http://srdata.nist.gov/xps/main_search_menu.aspx. 2012-09-15/2014-08-05.
[22] SHABAKER J W, SIMONETTI D A, CORTRIGHT R D, et al. Sn-modified Ni catalysts for aqueous-phase reforming: Characterization and deactivation studies[J]. Journal of Catalysis, 2005, 231(1): 67-76.
[23] HOFFER W, CREZEE E, MOOIJMAN M. Carbon supported Ru catalysts as promising alternative for Raney-type Ni in the selective hydrogenation of d-glucose[J]. Catalysis Today, 2003, 253(2): 35-41.
[24] AUER E, FREUND A, PIETSCH J, et al. Carbons as supports for industrial precious metal catalysts[J]. Applied Catalysis A, 1998, 173(2): 259-271.
[25] HETTINGER J, WILLLIAM P. Removal of coke and metals from carbo-metallic oils: US, 4915820[P]. 1990.
[26] CRISAFULLI C, SCIRÉ S, MINICS, et al. Ni-Ru bimetallic catalysts for the CO2reforming of methane[J]. Applied Catalysis A: General, 2002, 225(1-2): 1-9.
[27] BRAOS-GARCA P, GARCA-SANCHO C, INFANTES-MOLINA A, et al. Bimetallic Ru/Ni supported catalysts for the gas phase hydrogenation of acetonitrile[J]. Applied Catalysis A: General, 2010, 381(1-2): 132-144.
[28] 王庆根,屠迈, 王纬东,等. 凹凸棒黏土表面酸碱性质的研究[J]. 高等学校化学学报, 1997, 18(4): 625-627.(WANG Qinggen, TU Mai, WANG Weidong, et al. Studies of surface acidity and basicity of the attapulgite[J]. Chemical Journal of Chinese Universities, 1997, 18(4): 625-627.)
[29] 孔令鸟,马磊, 卢春山,等. Sn改性Raney Ni催化分解N,N-二甲基甲酰胺的研究[J]. 高校化学工程学报, 2010, 24(2): 214-217.(KONG Lingniao, MA Lei, LU Chunshan, et al. Catalytic decomposition ofN,N-dimethylformamide over raney Ni catalysts modified with Sn[J]. Journal of Chemical Engineering of Chinese Universities, 2010, 24(2): 214-217.)
[30] 邱爱玲, 邵丽丽. Sn修饰的Ni/γ-Al2O3催化乙二醇液相重整制氢[J]. 石油化工, 2013, 42(7): 724-729.(QIU Ailing, SHAO Lili. Aqueous-phase reforming of ethylene glycol to H2on Sn-modified Ni/γ-Al2O3catalyst[J]. Petrochemical Technology, 2013, 42(7): 724-729.)
[31] 袁胜华,郑进保, 谭亚南,等. 非负载Ni基催化剂的加氢性能[J]. 石油学报(石油加工), 2013,29(3): 482-485.(YUAN Shenghua, ZHENG Jinbao, TAN Ya’nan, et al. Hydrogenation performance of unsupported Ni-based catalyst [J]. Acta Petrolei Sinica(Petroleum Processing Section), 2013,29(3): 482-485.)
Ni-Based Catalysts for Hydrogenolysis of Sugar Alcohol Mixture
CHEN Jiejing1, 3, SUN Zhaolin1, 2, SONG Lijuan1,2, JIANG Heng2, WANG Xiao3, XIANG Wei3
(1.CollegeofChemicalEngineering,ChinaUniversityofPetroleum,Qingdao266580,China;2.KeyLaboratoryofPetrochemicalCatalysisScienceandTechnologyofLiaoningProvince,LiaoningShihuaUniversity,Fushun113001,China;3.FushunPetrochemicalCompany,CNPC,Fushun113001,China)
Ni-Ru/C catalyst was prepared and characterized by using XRD, TEM and XPS. The prepared Ni-Ru/C catalyst was used for sugar alcohol mixture hydrogenolysis to low carbon dihydric alcohols. The catalytic performance of the Ni-Ru/C was compared with that of Ni-Ru/Clay and Ni-Sn/C. The results showed that all the three catalysts possessed rather high catalytic activity in sugar alcohol mixture hydrogenolysis with the average conversion rates for three times hydrogenolysis reactions of 92.10%, 91.32% and 94.90%, respectively, however, the significant differences in total yield and selectivity of low carbon dihydric alcohols over the three catalysts were found, in which both the total yield over Ni-Ru/Clay catalyst and the total selectivity over Ni-Sn/C catalyst were the highest.
sugar alcohol; hydrogenolysis; Ni-based catalyst; comparison
2014-12-17
辽宁省教育厅重点实验室项目(2009S065)资助
陈洁静,女,高级工程师,博士研究生,从事催化剂制备研究;E-mail: fs-cjj@petrochina.com.cn
1001-8719(2015)03-0782-08
TQ 426.82
A
10.3969/j.issn.1001-8719.2015.03.025
