固相法合成梯度孔γ-Al2O3及其形成机制
2015-06-28胡小夫柳云骐李国良马跃龙刘晨光
胡小夫,柳云骐,李国良,3,马跃龙,刘晨光
(1. 中国华电集团科学技术研究总院, 北京 100077;2. 中国石油大学 重质油国家重点实验室, 山东 青岛 266555;3. 北京燃气绿源达清洁燃料有限公司,北京 100772)
固相法合成梯度孔γ-Al2O3及其形成机制
胡小夫1,2,柳云骐2,李国良2,3,马跃龙1,刘晨光2
(1. 中国华电集团科学技术研究总院, 北京 100077;2. 中国石油大学 重质油国家重点实验室, 山东 青岛 266555;3. 北京燃气绿源达清洁燃料有限公司,北京 100772)
以硝酸铝和碳酸氢铵为原料、PEG-400为形貌诱导剂,采用低温固相反应,在温和条件下制备出棒状碳酸铝铵(AACH),AACH焙烧后形貌和尺寸经拓扑转化,得到具有开放性孔道结构、高比表面积和大孔容的梯度孔γ-Al2O3。采用XRD、BET、SEM方法对AACH和梯度孔γ-Al2O3进行了表征。考察了棒状AACH在热转化过程中物相和形貌的改变以及形貌诱导剂PEG-400对梯度孔γ-Al2O3织构性能的影响,探讨了梯度孔γ-Al2O3的形成机制。结果表明,通过调节PEG-400的用量可调变AACH的形貌,从而可调控γ-Al2O3纳米粒子的形貌,最终得到比表面积高达422.1 m2/g、孔容为1.90 mL/g的梯度孔γ-Al2O3。梯度孔γ-Al2O3中,3~6 nm尺寸的孔由棒状AACH焙烧产生气体的扩孔作用形成, 10~35 nm尺寸的孔由棒状γ-Al2O3纳米颗粒堆积形成。
梯度孔;氧化铝;低温固相;合成
γ-Al2O3作为一种多孔性、高分散度的固体材料,因其具有较高的比表面积和发达的孔道结构、良好的化学稳定性和热稳定性而被广泛应用于催化剂载体、吸附材料、分离材料等方面。工业催化剂用的活性氧化铝粉一般为无定型细小颗粒的硬团聚体[1-2]。这种自然堆积的球形颗粒易形成“墨水瓶”型孔,其结构联通性差,造成大分子在其底部的吸附与结焦。而随着能源结构和化工原料结构逐渐向重碳、大分子方向发展,一般工业用的球形颗粒γ-Al2O3较难消除原料结构大分子化带来的影响,而具有开放性、连通性好,且呈梯度分布的孔结构、大比表面积和大孔容的梯度孔γ-Al2O3能解决上述问题[3]。
一般孔结构的连通性与γ-Al2O3颗粒的形貌直接相关,梯度分布的孔结构与γ-Al2O3颗粒的尺寸分布直接相关,因此通过调控γ-Al2O3颗粒的形貌和尺寸,可以合成出所需的梯度孔γ-Al2O3。研究表明,γ-Al2O3颗粒的形貌可由其前驱体的形貌拓扑转化而来。碳酸铝铵(AACH)作为一种γ-Al2O3的前驱体,它在煅烧过程中不产生对环境污染严重的气体,不发生热分解时的自溶解现象[4-5],具有独特优势。Ma等[6]证实了在不同温度下,纤维状AACH分解制得的γ-Al2O3形貌与AACH形貌基本一致。因此,可通过调控AACH的形貌和尺寸,间接控制γ-Al2O3的形貌和尺寸,最终得到梯度孔γ-Al2O3。
目前,国内外主要采用液相法合成AACH。液相法的反应条件要求比较严格,易有γ-AlOOH凝胶生成[7]。在本研究中,笔者采用低温固相反应[8-9],用硝酸铝和碳酸氢铵作原料,聚乙二醇作形貌诱导剂,在较温和的条件下合成出棒状前驱体AACH,再经高温煅烧,转化形成具有梯度分布的孔结构、高比表面积和大孔容的γ-Al2O3粉体。
1 实验部分
1.1 原料
Al(NO3)3·9H2O、聚乙二醇-400(PEG-400)、碳酸氢铵、乙醇, AR,国药集团化学试剂有限公司产品。
1.2 梯度孔γ-Al2O3的制备
将0.1 mol的Al(NO3)3·9H2O置于玛瑙研钵中充分研磨。分别将0、4、16、32和500 mmol的形貌诱导剂PEG-400滴加到0.4 mol的碳酸氢铵粉末中,充分研磨,然后将其与上述Al(NO3)3·9H2O混合,研磨。混合物很快变成泡沫状,持续8 min左右固化,继续研磨变为乳白色膏状物质。将膏状物置于晶化釜中, 80℃下陈化7 h,然后用大量去离子水洗涤、抽滤3次,用乙醇洗涤、抽滤1次,在120℃烘箱中干燥2 h,得到碳酸铝铵(AACH)晶体。采用不同量PEG-400所制备的AACH样品分别记作P-0、P-1、P-2、P-3和P-4。将这些样品分别置于坩埚中,缓慢升温在500℃下煅烧4 h,制得相应的梯度孔γ-Al2O3粉体样品,分别记为P-0-A、P-1-A、P-2-A、P-3-A和P-4-A。
1.3 产品的表征
采用荷兰帕纳科(Panalytical)公司X’Pert Pro MPD型X射线衍射仪测定试样的晶相结构(XRD),CuKα(λ= 0.15406 nm)射线,管电压45 kV,管电流40 mA;采用美国麦克公司Micromeritics ASAP 2010型物理吸附仪以N2吸附-脱附方法测定试样的比表面积和孔结构参数;采用美国Thermo Nicolet公司NEXUS型傅里叶变换红外光谱仪测定试样的FT-IR谱;采用日本日立公司S-4800型冷场发射扫描电子显微镜和日本电子JEM-2100UHR型透射电镜观察试样的颗粒形貌(SEM,TEM)。
2 结果与讨论
2.1 碳酸铝铵(AACH)热转化形成γ-Al2O3的过程
在n(NH4HCO3)/n(Al(NO3)3)=4、陈化时间7 h、陈化温度80℃和形貌诱导剂PEG-400用量为4 mmol的条件下,得到AACH样品P-1及其在300℃和500℃下煅烧得到样品的XRD谱如图1所示。由图1可知,P-1确定为AACH晶体(NH4[AlO(OH)HCO3])(JCPDS Card No. 00-042-0250),P-1在300℃下煅烧后出现了薄水铝石和γ-Al2O3的特征衍射峰,在500℃下煅烧后出现了γ-Al2O3的特征衍射峰。说明AACH晶体在高温煅烧下经历过薄水铝石中间态,继续升温煅烧得到纯的γ-Al2O3。
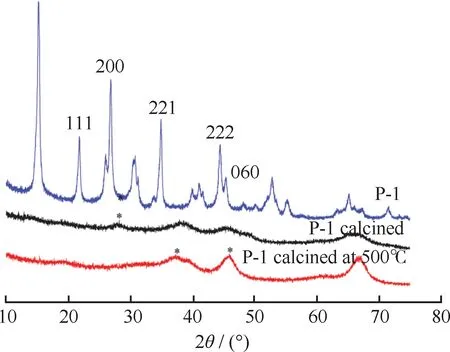
图1 P-1及其在不同温度下煅烧所得样品的XRD谱


图2 P-1及其在不同温度下煅烧所得样品的TEM照片
2.2 梯度孔γ-Al2O3织构性能的调控
图3为不同PEG-400用量所制备的AACH样品的XRD谱,图4为这些样品的SEM照片。由图3可知,不论是否加入PEG-400,在实验条件下均能得到AACH晶体,且随着PEG-400用量的增加,其特征衍射峰强度有所下降。说明随着PEG-400用量的增加,所得AACH晶体的结晶度和晶粒大小均有所下降。由图4可以看出,不加入PEG-400的P-0样品的晶体呈细小颗粒状;随着少量PEG-400的加入,AACH开始呈现棒状晶体, PEG-400的加入量为32 mmol的P-3样品的棒状晶体长约75 nm,直径约25 nm;加入大量PEG-400制备的P-4样品的晶体呈球形,其直径大约为50 nm。这说明PEG-400在AACH的合成过程中起到形貌诱导剂的作用,通过调变PEG-400的用量能调控AACH的形貌。由2.1节讨论可知,棒状AACH晶体在焙烧过程中转化形成棒状γ-Al2O3,其形貌基本保持不变。因此,通过调节形貌诱导剂PEG-400的用量可间接调控γ-Al2O3纳米粒子的形貌,而γ-Al2O3的织构性能与其纳米粒子的形貌和堆积方式密切相关,最终达到调控γ-Al2O3织构性能的目的。
各AACH样品焙烧得到γ-Al2O3样品的织构性能列于表1。由表1可见,由细小颗粒状P-0焙烧得到的P-0-A样品的比表面积和孔容很小,而随着少量PEG-400的加入,由棒状P-1~P-3焙烧得到的P-1-A~P-3-A的比表面积、孔容和平均孔径均得到显著提高。P-3-A的比表面积和孔容高达422.1 m2/g和1.90 mL/g。但球形颗粒的P-4焙烧得到的P-4-A的比表面积和孔容都有所下降。这表明通过调变形貌诱导剂PEG-400的用量调控γ-Al2O3前驱体AACH的形貌,最终可起到调控γ-Al2O3织构性能的作用。

图3 不同PEG用量所制备P-0~P-4样品的XRD谱

图4 不同PEG用量所制备P-0~P-4样品的SEM照片
表1 由各个AACH样品焙烧得到的γ-Al2O3样品的比表面积和孔结构参数
Table 1 Surface area and pore structural parameters ofγ-Al2O3samples prepared by calcination of AACH
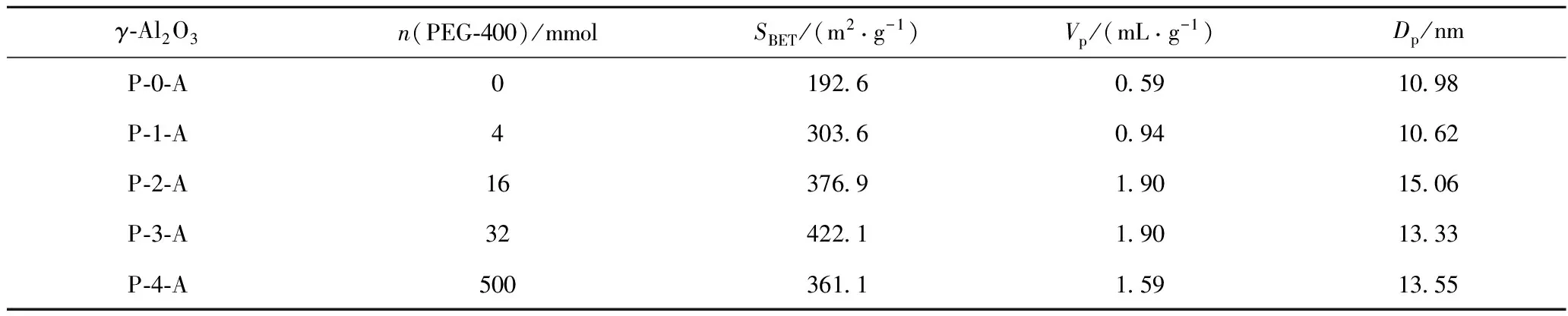
γ⁃Al2O3n(PEG⁃400)/mmolSBET/(m2·g-1)Vp/(mL·g-1)Dp/nmP⁃0⁃A0192 60 5910 98P⁃1⁃A4303 60 9410 62P⁃2⁃A16376 91 9015 06P⁃3⁃A32422 11 9013 33P⁃4⁃A500361 11 5913 55
研究表明, P-0-A和P-1-A不是梯阶孔γ-Al2O3,样品P-2-A、P-3-A和P-4-A均为梯阶孔γ-Al2O3。但P-4-A的梯阶孔是由球形γ-Al2O3纳米粒子堆积而成。球形颗粒在工业生产中易形成“墨水瓶”型孔,“墨水瓶”型孔结构联通性差,易造成大分子在其底部的吸附与结焦。因此,具有工业应用前景的阶梯孔γ-Al2O3样品为P-2-A和P-3-A。图5为样品P-2-A和P-3-A的孔径分布曲线和N2吸附-脱附等温线。由图5(a)可知, P-2-A和P-3-A均呈梯度孔分布,孔径主要集中在3~6 nm和10~35 nm之间。3~6 nm处的孔由AACH热分解产生的气体扩孔作用形成[9],而10~35 nm的孔主要由棒状γ-Al2O3纳米颗粒堆积形成。由图5(b)可知,样品P-2-A和P-3-A的N2吸附-脱附等温线均呈现IUPAC分类中的Ⅳ型吸附等温线特征。
2.3 梯度孔γ-Al2O3的形成机制
梯度孔γ-Al2O3的织构性能与其纳米粒子的形貌和堆积方式密切相关,通过调节γ-Al2O3纳米粒子的形貌来达到调控γ-Al2O3织构性能的目的,而γ-Al2O3纳米粒子又由其前驱体拓扑转化而来,因此,可通过调控γ-Al2O3前驱体AACH的形貌来间接调控γ-Al2O3的织构性能。棒状AACH形成机制如图6所示。图7为样品P-3晶体和相应P-3-A的FT-IR谱。带结晶水的铝盐在研磨过程中表面提供1个微型的水溶性体系,在此水溶性体系中碳酸氢铵与铝盐发生反应,生成了AACH纳米晶,纳米晶立即与亲水性醇类PEG-400通过氢键形成强吸附,由图7可以得到证明,其吸附作用类似于SIFF(The surfactant-induced fiber formation)机理[10-11]。氢键的存在降低了AACH纳米晶的成核活化能,在PEG-400的作用下连成几十个纳米的簇状结构;在高温陈化过程中,簇状结构可转化成纳米晶,然后按一定的方向生长,形成棒状或片状结构的碳酸铝铵次级晶体,此过程遵循Ostwald熟化机理[12]。
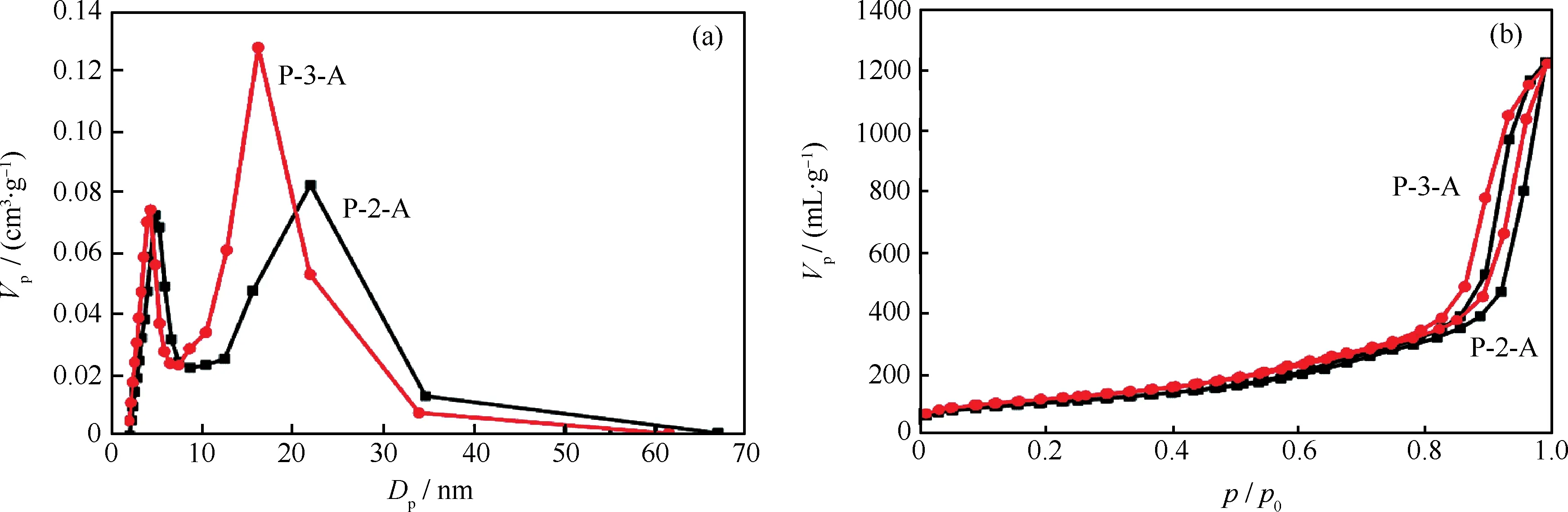
图5 γ-Al2O3样品P-2-A、P-3-A的孔径分布曲线和N2吸附-脱附等温线
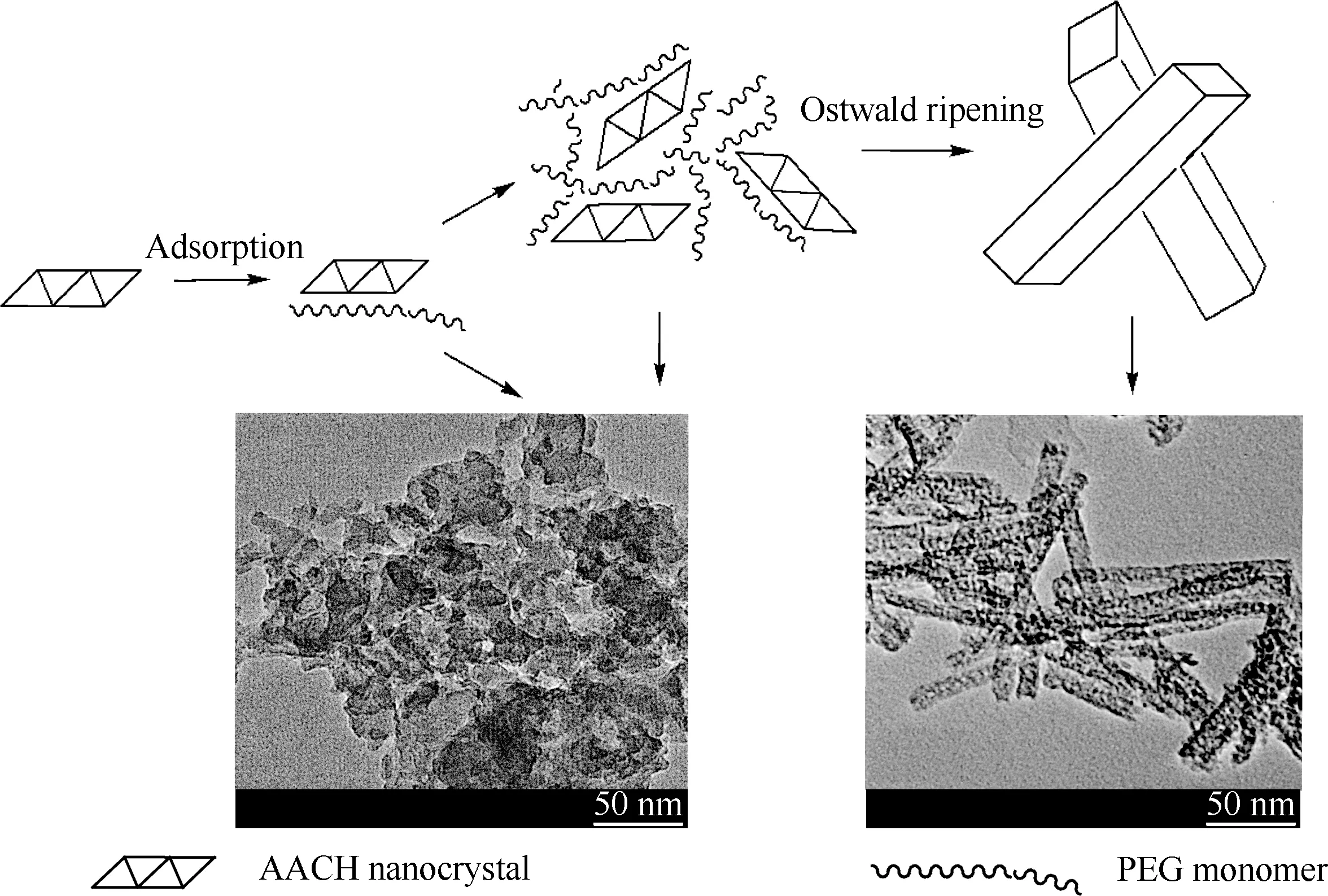
图6 PEG诱导形成AACH纳米棒的机制
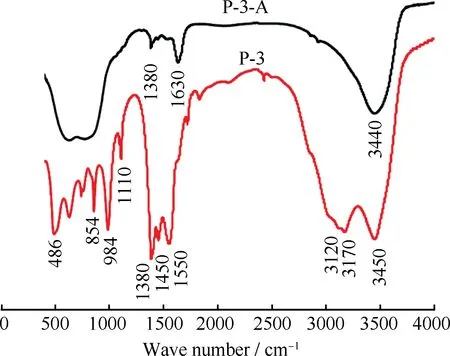
图7 P-3和P-3-A的FT-IR谱

棒状AACH在焙烧过程中产生气体(如CO2和NH3),气体的扩孔作用使得生成的γ-Al2O3具有3~6 nm的孔,同时也增加了γ-Al2O3的比表面积和孔容[8-9];并且在焙烧过程中棒状AACH形貌基本得以保持,得到了短棒状γ-Al2O3纳米颗粒,如图8所示,而棒状γ-Al2O3纳米颗粒堆积又形成10~35 nm左右的孔,得到比表面积和孔容高达422.1 m2/g和1.90 mL/g的梯度孔γ-Al2O3。

图8 P-3-A的SEM照片
3 结 论
(1) 棒状AACH在高温煅烧下经历过薄水铝石中间态,在500℃下得到纯γ-Al2O3;此过程中AACH的形貌发生拓扑转变,得到的γ-Al2O3纳米粒子仍呈棒状结构。
(2) 通过调节形貌诱导剂PEG-400的用量可调控AACH的形貌,从而间接调控γ-Al2O3的形貌,得到一定织构性能的γ-Al2O3。
(3) 棒状AACH晶体是由AACH纳米晶与PEG-400通过氢键吸附作用形成的纳米簇,煅烧过程中产生气体,煅烧后得到棒状γ-Al2O3纳米粒子。棒状AACH晶体焙烧产生气体的扩孔作用和棒状γ-Al2O3纳米颗粒的堆积作用形成了具有高比表面积和大孔容(422.1 m2/g和1.90 mL/g)的梯度孔γ-Al2O3。
[1] 董岩,蒋建清, 梁超,等. 小粒径氧化铝粉的制备及其在荧光粉合成中的应用[J]. 中国陶瓷,2005, 41(3):12-15.(DONG Yan, JIANG Jianqing, LIANG Chao, et al. Preparation of disperseα-Al2O3powder of small particle size and its application in aluminate phosphor[J]. China Ceramics, 2005, 41(3): 12-15.)
[2] 刘华,史中华, 陈耀强,等. 以氨水和碳酸铵为沉淀剂制备氧化铝的对比研究[J]. 无机化学学报,2004,20(6):688-692.(LIU Hua, SHI Zhonghua, CHEN Yaoqiang, et al. The comparison of aluminas prepared by ammonium carbonate and ammonium hydroxide as precipitation agents[J]. Chinese Journal of Inorganic Chemistry, 2004, 20(6): 688-692.)
[3] 饶拴民, 朱建军, 杜海荣. 大孔容活性氧化铝的用途和制备方法[J]. 轻金属,2002,(3):17-18.(RAO Shuanmin, ZHU Jianjun, DU Hairong. Application and preparation method of active alumina with a large porosity[J]. Light Metals, 2002, (3): 17-18.)
[4] 吴志鸿,周龙昌, 陈智鹏,等. 纤维状碱式碳酸铝铵的低热固相合成及其超分子自组装特征[J]. 广西大学学报(自然科学版),2008,33(2):141-143.(WU Zhihong, ZHOU Longchang, CHEN Zhipeng, et al. Synthesis of ammonium aluminium carbonate hydroxide with fibre shape via solid state reaction and its supramolecular self-assembly characters[J]. Journal of Guangxi University(Nat Sci Ed), 2008, 33(2): 141-143.)
[5] 肖劲,万烨, 邓华, 等. 碳酸铝铵热解法制备超细Al2O3[J]. 轻金属,2006,(11):21-24.(XIAO Jin, WAN Ye, DENG Hua, et al. Preparing ultrafine alumins powder by AACH thermal decomposition[J]. Light Metals, 2006, (11): 21-24.)
[6] MA Chicheng, ZHOU Xuexi, XU Xin, et al. Synthesis and thermal decomposition of ammonium aluminum carbonate hydroxide (AACH) [J]. Materials Chemistry and Physics, 2001, 72(3):374-379.
[7] 李继光,孙旭东, 张民, 等. 碳酸铝铵热分解制备α-Al2O3超细粉[J]. 无机材料学报,1998,13 (6):803-807.(LI Jiguang, SUN Xudong, ZHANG Min, et al. Synthesis of ultrafine α-alumina powder by pyrolysis of ammonium aluminium carbonate hydroxide[J]. Journal of Inorganic Materials, 1998, 13(6): 803-807.)
[8] 胡小夫,张敏, 李国良,等.γ-Al2O3载体的固相法合成及Ni-Mo-P/γ-Al2O3催化剂的加氢脱硫性能[J]. 石油学报(石油加工),2013,9(2):191-197.(HU Xiaofu, ZHANG Min, LI Guoliang, et al. Synthesis ofγ-Al2O3by solid-state reaction and the hydrodesulfurization evaluation of Ni-Mo-P/γ-Al2O3[J]. Acta Petrolei Sinica (Petroleum Processing Section), 2013, 9(2): 191-197.)
[9] HU Xiaofu, LIU Yunqi, TANG Zhe, et al. Fabrication of high-surface-areaγ-alumina by thermal decomposition of AACH precursor using low-temperature solid-state reaction [J]. Material Research Bulletin, 2012, 47(12): 4271-4277.
[10] ZHU H Y, RICHES J D, BARRRY J C.γ-Alumina nanofibers prepared from alumina hydrate with poly(ethylene oxide) surfactant[J]. Chem Mater, 2002, 14: 2086-2093.
[11] BAI Peng, SU Fabing, WU Pingping, et al. Copolymer-controlled homogeneous precipitation for the synthesis of porous microfibers of alumina[J]. Langmuir, 2007, 23(8): 4599-4605.
[12] KABALNOV A. Ostwald ripening and related phenomena[J]. Dispersion Science and Technology, 2001, 11(1): 1-12.
[13] 朱振峰,孙洪军, 刘辉,等. 表面活性剂辅助水热法制备碳酸铝铵纤维及其生长机理初探[J]. 人工晶体学报, 2010, 39(1): 110-119. (ZHU Zhenfeng, SUN Hongjun, LIU Hui, et al. Surface assisted hydrothermal synthesis of AACH microfiber and its growth mechanism[J]. Journal of Synthetic Crystals, 2010, 39(1): 110-119.
Synthesis of Hierarchical Porousγ-Al2O3by Solid-State Reaction and Its Formation Mechanism
HU Xiaofu1,2, LIU Yunqi2, LI Guoliang3,MA Yuelong1,LIU Chenguang2
(1.ChinaHuadianScienceandTechnologyInstitute,Beijing100077,China;2.StateKeyLaboratoryofHeavyOilProcessing,ChinaUniversityofPetroleum,Qingdao266555,China;3.LvyuandaCleanFuelLimitedCompanyofBeijingGas,Beijing100772,China)
Ammonium aluminum carbonate hydroxide (AACH) with nanorods morphology was synthesized by a low-temperature solid-state reaction with NH4HCO3and Al(NO3)3as reactants and PEG-400 as morphology inducer. Meanwhile, the hierarchical porousγ-Al2O3with open porous structure, high surface area and large pore volume was obtained by a topological transformation of the morphology and size of AACH after calcination. The synthesized AACH and hierarchical porousγ-Al2O3samples were then characterized by means of XRD, BET, SEM. The change of the phases and morphologies of AACH during thermal conversion and the influence of PEG-400 for the textural properties of hierarchical porousγ-Al2O3were investigated. The formation mechanism of hierarchical porousγ-Al2O3was also discussed. The results demonstrated that the morphology of AACH could be controlled by adjusting the dosage of PEG-400, thereby the morphology ofγ-Al2O3was indirectly regulated, and finally the hierarchical porousγ-Al2O3product with high surface area (422.1 m2/g) and large pore volume (1.90 mL/g) was obtained. The formation of hierarchical porousγ-Al2O3is possibly attributed to the pore enlargement of gas produced from the calcination of AACH, resulting in the hole with the size range of 3-6 nm, and the stacking ofγ-Al2O3nanoparticles, resulting in the hole with the size range of 10-35 nm.
hierarchical porous; alumina; low-temperature solid-state; synthesis
2014-02-19
国家重点基础研究发展计划“973”项目(2010CB226905)资助
胡小夫,女,博士,从事石油与天然气加工方面的研究;Tel:010-59216273;E-mail: xiaofu-hu@chdi.ac.cn
1001-8719(2015)03-0684-07
TE624.4
A
10.3969/j.issn.1001-8719.2015.03.011
