水飞蓟宾通过降低MEK/ERK途径依赖的MMP-9蛋白表达抑制人乳腺癌细胞生长和侵袭转移机制的实验研究
2015-05-24车佳
车佳
水飞蓟宾通过降低MEK/ERK途径依赖的MMP-9蛋白表达抑制人乳腺癌细胞生长和侵袭转移机制的实验研究
车佳
目的 探讨水飞蓟宾对人乳腺癌细胞生长和侵袭转移的影响及机制。方法 用不同浓度水飞蓟宾处理人乳腺癌细胞系MCF-7 24h,采用MTT(噻唑蓝)法和台盼蓝染色法检测水飞蓟宾对MCF-7细胞的抑制作用;采用transwell技术检测水飞蓟宾对MCF-7细胞侵袭转移的影响;Western blot检测水飞蓟宾对MCF-7细胞MEK及ERK(均为丝裂原激活的蛋白激酶)蛋白磷酸化水平及基质金属蛋白酶-9(MMP-9)表达水平的影响。结果 水飞蓟宾可显著抑制MCF-7细胞的增殖并造成肿瘤细胞死亡,与对照组比较,水飞蓟宾增殖抑制率[20μM(8.9±3.8)%、50μM(19.7±4.2)%、100μM(29.8±5.7)%比0]、台盼蓝染色率[50μM(16.1±4.8)%、100μM(25.3±5.1)%比(3.4±1.4)%],均升高(P<0.05,P<0.01);水飞蓟宾通过抑制MEK(水飞蓟宾20μM:0.26±0.03、50μM:0.15±0.03、100μM:0.11±0.02比对照组:0.35±0.04)和ERK(水飞蓟宾20μM:0.23±0.03、50μM:0.12±0.02、100μM:0.07±0.01比对照组:0.32±0.05)的磷酸化降低MMP-9(水飞蓟宾50μM:0.18±0.03、100μM:0.14±0.02比对照组:0.29±0.04)的表达并抑制MCF-7[水飞蓟宾20μM:(14.3±2.1)%、50μM:(35.6± 5.7)%、100μM(53.1±6.5)%比对照组:0]细胞侵袭转移的能力(P<0.05,P<0.01)。结论 水飞蓟宾抑制人乳腺癌细胞的生长和侵袭转移。
乳腺癌;水飞蓟宾;MEK/ERK;MMP-9;肿瘤侵袭
水飞蓟宾是水飞蓟素中最主要的生物活性成分,来源于水飞蓟属植物奶蓟种子的提取物,临床上主要用于保护肝细胞,对肝炎、胆囊疾病有良好的疗效,具有高效、低毒、低副作用的特性[1]。近年研究发现水飞蓟宾有抑制肿瘤细胞增殖,诱导肿瘤细胞凋亡的作用[2],研究人员还发现水飞蓟宾治疗能推迟Her2/neu(一种原癌基因)转基因小鼠自发性乳腺癌的发生并减小肿瘤的体积和质量[3]。乳腺癌的发生率和死亡率仅次于肺癌,而在女性群体中是发生率最高的恶性肿瘤,它的高转移性使之目前仍无法治愈[4]。基质金属蛋白酶-9(MMP-9)是一种明胶酶,能降解肿瘤附近组织基底膜的Ⅳ型胶原,从而促进肿瘤细胞向正常组织的侵袭和转移[5],乳腺癌患者血清MMP-9水平如果显著升高往往预示着肿瘤的转移和恶化[6]。本研究发现水飞蓟宾能抑制乳腺癌细胞的生长,更重要的是,水飞蓟宾还能通过抑制MMP-9的表达抑制乳腺肿瘤细胞的侵袭转移。
1 材料与方法
1.1 细胞培养 人乳腺癌细胞系MCF-7来自于ATCC(American type culture collection,美国模式培养物研究所)。细胞培养在RPMI-1640(roswell park memorial institute-1640)培养基中,含10%胎牛血清,加入100U/L青霉素和100mg/mL链霉素,培养环境为37℃恒温且通入5%的CO2。
1.2 实验试剂 RPIM-1640培养基购自Gibco公司;胎牛血清购自杭州四季青生物工程有限公司;水飞蓟宾、二甲亚砜、MTT、台盼蓝购自美国Sigma公司;β-actin、MMP-9、p-MEK(磷酸化MEK)、p-ERK(磷酸化ERK)抗体购自美国Cell signal公司;transwell小室购于美国康宁公司。
1.3 细胞增殖抑制试验 将MCF-7细胞悬液用培养基调成5×104个/mL浓度,取200μL接种于96孔板,设置3个复孔,治疗组分别加入10、20、50和100μM的水飞蓟宾培养24h,对照组不加水飞蓟宾培养24h,加5mg/mLMTT 20μL,继续培养4h。弃上清,往孔中加150μL二甲亚砜,在570nm波长下用酶标仪检测OD(吸光度)值,肿瘤细胞生长抑制率=(对照组OD值-治疗组OD值)/对照组OD值× 100%。
1.4 水飞蓟宾对MCF-7细胞杀伤活性试验 在MCF-7细胞培养体系中分别加入 10、20、50和100μM的水飞蓟宾培养24h,对照组不加水飞蓟宾培养24h,用台盼蓝染死细胞,低倍镜下计数受染细胞数占总细胞数的比值即为水飞蓟宾对MCF-7细胞的杀伤率。
1.5 Western blot试验 在MCF-7细胞培养体系中分别加入10、20、50和100μM的水飞蓟宾培养2h,对照组不加水飞蓟宾培养2h,之后将细胞裂解后做Western blot检测磷酸化MEK和磷酸化ERK的含量,MMP-9蛋白表达水平需在上述培养体系中用水飞蓟宾培养24h再用Western blot检测,各蛋白表达量由它们在胶片上显色后的灰度与相应β-actin的灰度比表示。
1.6 肿瘤细胞侵袭转移试验 将MCF-7细胞悬液用无血清培养基调成2×104个/mL浓度,取500μL接种于transwell小室(即上室)中置于普通24孔板上,设置3个复孔,在上室中分别加入10、20、50和100μM的水飞蓟宾培养24h,对照组不加水飞蓟宾培养24h。普通24孔板(即下室)中培养基为含10%胎牛血清的RPMI-1640。培养24h后取出transwell小室,用磷酸盐缓冲液(PH7.4)洗去小室内的细胞,将transwell膜用3%多聚甲醛固定15min后用0.1%结晶紫染色20min,低倍镜(100×)观察4个随机选择的区域,计算细胞总数,膜上细胞数越多表明肿瘤细胞的侵袭转移力越强。
1.7 统计学方法 所有实验重复3次,应用SPSS 15.0统计分析软件进行处理,计量资料以(±s)表示,P值计算采用非配对双边t检验以及单因素方差分析,P<0.05为差异有统计学意义。
2 结果
2.1 水飞蓟宾对MCF-7细胞的抑制作用 在水飞蓟宾作用下实验组相比于对照组均呈现剂量依赖性抑制效应(P<0.05),证实了水飞蓟宾有体外抑制乳腺肿瘤细胞增殖的生物活性。台盼蓝染色试验发现随着水飞蓟宾浓度的增加,MCF-7细胞染色率随之增加,表明水飞蓟宾有体外杀伤乳腺癌细胞的生物活性,见表1。
表1 水飞蓟宾对MCF-7细胞的抑制作用(±s)
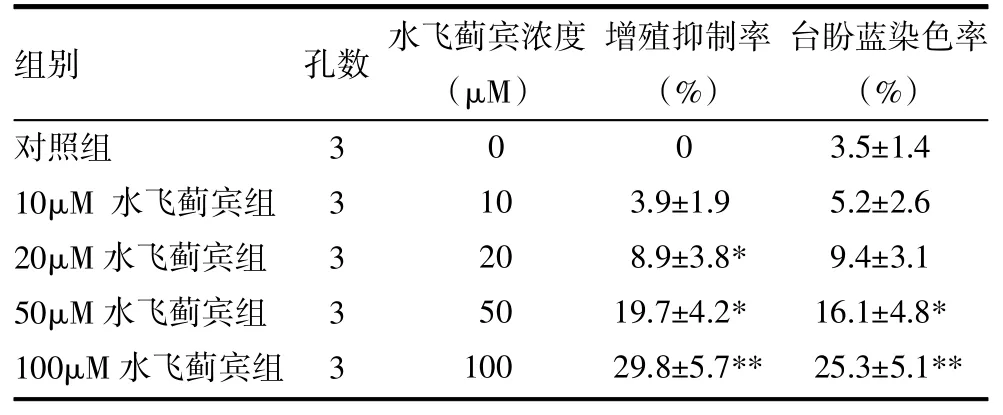
表1 水飞蓟宾对MCF-7细胞的抑制作用(±s)
注:与对照组比较,*P<0.05,**P<0.01
对照组10μM水飞蓟宾组20μM水飞蓟宾组50μM水飞蓟宾组100μM水飞蓟宾组33333 0 10 20 50 100 0 3.9±1.9 8.9±3.8* 19.7±4.2* 29.8±5.7** 3.5±1.4 5.2±2.6 9.4±3.1 16.1±4.8* 25.3±5.1**
2.2 水飞蓟宾抑制MCF-7细胞的侵袭转移 随着水飞蓟宾剂量的增加,transwell膜上的细胞数显著减少(P<0.05,P<0.01),且水飞蓟宾对MCF-7的侵袭力的抑制率显著高于同浓度下水飞蓟宾对MCF-7的增殖抑制率(增殖抑制率为表1数据)(P<0.05,P<0.01)。证实水飞蓟宾不仅能直接抑制乳腺肿瘤细胞的增殖,同时也能显著抑制乳腺肿瘤细胞的侵袭转移,见表2。
表2 水飞蓟宾对乳腺癌细胞侵袭力的影响(±s)

表2 水飞蓟宾对乳腺癌细胞侵袭力的影响(±s)
注:与对照组比较,*P<0.05,**P<0.01;与同浓度水飞蓟宾治疗后的增殖抑制率比较,△P<0.05,△△P<0.01
组别对照组10μM水飞蓟宾组20μM水飞蓟宾组50μM水飞蓟宾组100μM水飞蓟宾组孔数33333水飞蓟宾浓度(μM)0 10 20 50 100细胞个数(个)305.4±33.8 288.6±46.7 261.5±38.3* 196.9±31.3** 143.6±18.1**侵袭抑制率(%)0 5.6±0.9 14.3±2.1* 35.6±5.7**△53.1±6.5**△△增殖抑制率(%)0 3.9±1.9 8.9±3.8* 19.7±4.2* 29.8±5.7**
表3 水飞蓟宾对MCF-7细胞MEK及ERK蛋白磷酸化水平及MMP-9表达水平的影响(±s)

表3 水飞蓟宾对MCF-7细胞MEK及ERK蛋白磷酸化水平及MMP-9表达水平的影响(±s)
注:与对照组比较,*P<0.05,**P<0.01;MMP-9:基质金属蛋白酶-9;p-MEK:磷酸化MEK;p-ERK:磷酸化ERK
组别对照组10μM水飞蓟宾组20μM水飞蓟宾组50μM水飞蓟宾组100μM水飞蓟宾组孔数33333水飞蓟宾浓度(μM)0 10 20 50 100灰度比(MMP-9/β-actin)0.29±0.04 0.28±0.05 0.24±0.04 0.18±0.03* 0.14±0.02**灰度比(p-MEK/β-actin)0.35±0.04 0.30±0.04 0.26±0.03* 0.15±0.03* 0.11±0.02**灰度比(p-ERK/β-actin)0.32±0.05 0.29±0.05 0.23±0.03* 0.12±0.02** 0.07±0.01**
2.3 水飞蓟宾对MCF-7细胞MEK及ERK蛋白磷酸化水平及MMP-9表达水平的影响 水飞蓟宾能有效抑制MEK和ERK的磷酸化,从而使其下游的MMP-9蛋白表达受到抑制(P<0.05,P<0.01),减弱MCF-7细胞的侵袭力,见表3。
3 讨论
乳腺癌的高度转移性是乳腺癌难治及死亡率高的重要原因,肿瘤细胞在营养缺乏的环境下会向营养充足的组织侵袭迁移[7]。在这一过程中,基质金属蛋白酶(MMPs)起着至关重要的作用,MMPs已经被证实与肿瘤的分化、转移和预后有关,而MMP-9是MMPs中的重要成员,有文献报道,当MMP-9表达显著增加时肿瘤的侵袭力增强,反之当MMP-9表达受抑制时肿瘤细胞的侵袭力减弱[8-9]。MMP-9基因的启动子序列包含两个转录因子的结合位点,即AP-1(activator protein-1,激活子蛋白-1)和NF-κB[10](nuclear factor-κB,核因子-κB)。这两个转录因子与启动子的结合依赖于ERK蛋白激酶的激活,Raf/ MEK/ERK信号通路已经被证实是AP-1和NF-κB活化的重要途径[11-12]。本研究结果提示水飞蓟宾可以通过阻断这条信号通路抑制AP-1和NF-κB的活化从而抑制它们与MMP9基因启动子的结合,这可能是水飞蓟宾抑制乳腺癌细胞侵袭转移的重要机制之一。水飞蓟宾近些年来被发现具有良好的抗肿瘤活性,对于多种肿瘤均具有良好抑制作用[13-14],是一种非常高效且低毒低副作用的天然药物。本研究不但证实水飞蓟宾具有很好的抗乳腺癌细胞增殖的活性,而且还提示了它能有效减弱乳腺癌对周围组织的侵袭和转移,为水飞蓟宾的临床抗肿瘤应用提供了新的理论基础和前景。
[1]Wang Y,Zhang L,Wang Q,et al.Recent advances in the nanotechnology-based drug delivery of Silybin[J].JBiomed Nanotechnol,2014,10(4):543-558.
[2]Akhtar R,Ali M,Mahmood S,et al.Anti-proliferative action of silibinin on human colon adenomatous[J].cancer HT-29 cells[J].Nutr Hosp,2014,29(2):388-392.
[3] Provinciali M,Papalini F,Smorlesi A,et al.Effect of the silybinphosphatidylcholine complex(IdB 1016)on the development of mammary tumors in HER-2/neu transgenic mice[J].Cancer Res,2007,67(5):2022-2029.
[4]Jemal A,Siegel R,Xu J,et al.Cancer statistics[J].CA Cancer JClin,2009,59(4):225-249.
[5]Li H,Zhang K,Xiao T,et al.A systematic review ofmatrix metalloproteinase 9 as a biomarker of survival in patients with osteosarcoma[J].Tumour Biol,2014,35(6):5487-5491.
[6]Li HC,Cao DC,Shao ZM,et al.Prognostic value of matrix metalloproteinases(MMP-2 and MMP-9)in patients with lymph node-negative breast carcinoma[J].Breast Cancer Res Treat,2004,88(1):75-85.
[7]Oskarsson T.Extracellularmatrix components in breast cancer progression and metastasis[J].Breast,2013,22(Suppl 2):S66-72.
[8]Falcao AS,Kataoka MS,Pinheiro JJ,et al.A Novel Cell Line Derived from Pleomorphic Adenoma Expresses MMP2,MMP9,TIMP1,TIMP2,and Shows Numeric Chromosomal Anomalies[J].PLoSOne,2014,9(8):e105231.
[9]Jang SY,Kim A,Lee JY,et al.Metformin Inhibits Tumor Cell Migration via Down-regulation of MMP9 in Tamoxifen-resistant Breast Cancer Cells[J].Anticancer Res,2014,34(8):4127-4134.
[10]Sen T,Dutta A,Chatterjee A.Epigallocatechin-3-gallate(EGCG)downregulates gelatinase-B(MMP-9)by involvement of FAK/ERK/NFkappaB and AP-1 in the human breast cancer cell line MDA-MB-231[J].Anticancer Drugs,2010,21(6):632-644.
[11]Fuchs O.Targeting of NF-kappaB signaling pathway,other signaling pathways and epigenetics in therapy of multiple myeloma[J].Cardiovasc HematolDisord Drug Targets,2013,13(1):16-34.
[12]Hollenhorst PC.RAS/ERK pathway transcriptional regulation through ETS/AP-1 binding sites[J].Small GTPases,2012,3(3):154-158.
[13]Akhtar R,Ali M,Mahmood S,et al.Anti-proliferative action of silibinin on human colon adenomatous.cancer HT-29 cells[J].Nutr Hosp,2014,29(2):388-392.
[14]Kumar S,Raina K,AgarwalC,etal.Silibinin strongly inhibits the growth kinetics of colon cancer stem cell-enriched spheroids bymodulating interleukin 4/6-mediated survival signals[J].Oncotarget,2014,5(13):4972-4989.
(收稿:2014-08-10 修回:2014-10-31)
Silibinin Inhibits M etastasis and Invasion of Breast Cancer Cells Via Decreasing the Expression of MMP-9 Dependent on MEK/ERK Pathway
CHE Jia. Clinical Laboratory,Zhejiang Provincial Tongde Hopsital, Hangzhou(310012),China
Objective To investigate the effect of silibinin on proliferation and invasion of breast cancer cells and the underlying mechanism.M ethods Human breast cancer cell line MCF-7 were treated with various concentrations of silibinin for 24h,then MTT assay was used to detect cell proliferation.The effect of silibinin on invasion of MCF-7 cells was measured by transwell.The phosphorylation of MEK and ERK proteins and the expression of MM-9 protein were evaluated by western blot.Results The inhibitory rate of silibinin on MCF-7 cell proliferation was(8.9±3.8)%at 20μM,(19.7±4.2)%at 50μM,and(29.8±5.7)%at 100μM,with significant difference compared with control group(P<0.05).Typan blue staining rate of MCF-7 cells treated with silibinin at concentration of 50 and 100μM was(16.1±4.8)%and(25.3±5.1)%,respectively,both with significant difference compared with that of control group[(3.4±1.4)%,P<0.05].Silibinin at concentration of 20,50,and 100μM inhibited the phosphorylation of MEK(0.26±0.03,0.15±0.03,0.11±0.02 vs 0.35±0.04)and ERK(0.23±0.03,0.12±0.02,0.07±0.01 vs 0.32±0.05)proteins.Silibinin of 50 and 100μM decreased the expression of MMP-9 protein(0.18±0.03,0.14±0.02 vs 0.29±0.04).Silibinin inhibited metastasis and invasion of MCF-7 cells[20μM:(14.3±2.1%),50μM:(35.6±5.7)%, 100μM:(53.1±6.5)%vs 0].Conclusion Silibinin can inhibit the growth and invasion of breast cancer cells.
Breat cancer;Silibinin;MEK/ERK;MMP-9;Tumor invasion
浙江省立同德医院检验科(杭州 310012)
