H2O分子在锐钛矿型TiO2(101)表面的吸附特性与微观机理
2015-03-23张菊花
杨 英, 冯 庆, 张菊花
(重庆师范大学物理与电子工程学院,重庆 400047)
H2O分子在锐钛矿型TiO2(101)表面的吸附特性与微观机理
杨 英, 冯 庆, 张菊花
(重庆师范大学物理与电子工程学院,重庆 400047)
本文采用基于密度泛函理论(DFT)的平面波超软赝势方法,模拟计算H2O分子在锐钛矿型TiO2(101)无氧空位和有氧空位表面的吸附行为,对吸附能、吸附距离、吸附前后表面电子态密度以及光学性质分别进行分析,结果表明:H2O分子在无氧空位锐钛矿型TiO2(101)表面不容易被吸附,在含有氧空位缺陷的表面容易被吸附;稳定吸附后,H2O分子平面垂直于TiO2表面;负电中心(O端)距空位越近,吸附越稳定,且氧空位浓度越高,吸附效果越明显;通过电子态密度分析发现,H2O分子吸附于含氧空位的表面后,由于H2O分子中O原子的2p孤对电子掺入,新峰值在费米能级附近出现,提高了材料在可见光低能区域的跃迁几率,明显改善了对可见光的吸收系数和反射率,光学气敏传感特性显著.
锐钛矿; 光学气敏传感材料; 表面吸附; 密度泛函理论
1 引 言
近年来,光学气敏湿度传感器随着光纤技术和光集成技术的发展而被广泛应用,在气敏传感材料领域中,由于TiO2具有灵敏度高、响应时间快等优点而受到广泛关注.以前的气敏传感特性研究主要集中在材料吸附分子后电阻性质的改变来体现吸附特性,是一种电阻型气敏传感.而光学气敏传感的机理是由于材料吸附气体分子后引起光学性质改变来体现传感特性.光学气敏传感具有灵敏度高,响应时间短,分辨率高等优点逐渐受到研究者的关注.当前,在气敏传感器研究领域中,由于TiO2是具有良好物理化学性质的传感材料,对其表面结构与性质已有了较多的研究,但对其吸附气体分子后的光学气敏传感特性研究还不多,气体分子在表面的吸附是表面反应进行的前提.TiO2在自然界中稳定存在的主要有金红石型和锐钛矿型,锐钛矿型TiO2具有较高的活性[1],近年来在光催化氧化、太阳能电池、气敏传感器等方面受到越来越多的重视[1-7].K.-O.N[8]和F. Labat[9]等人发现锐钛矿型TiO2的主要(最稳定)晶面是(101)面(占94%),同时暴露的还有(001)表面(仅占6%),又由于锐钛矿TiO2(101)面具有较低表面能[10-19],因此当前锐钛矿TiO2的吸附研究主要集中在TiO2(101)面.水是研究材料气敏传感性质最理想的探针分子,简单的无机小分子在材料表面吸附、分解等反应过程中绝大多数都涉及到了与水的相互作用.Vittadini[20]等根据DFT的计算结果预测,水分子在锐钛矿型TiO2的(101)表面上不论是在低覆盖度下还是在单分子层吸附时都以分子吸附为主要存在形式;何云斌[21]等结合DFT计算和STM观测发现,由于电荷重组导致近表面的水分子在锐钛矿相TiO2(101)表面上影响更多的水分子吸附,而在不同晶面上由于短程的排斥力或吸引力的作用不同,将使水分子在此表面上形成局域有序的(2x2)结构.金属氧化物半导体材料暴露在空气中时表面大部分含有较多的氧空位,作者所在课题小组近年来分别对锐钛矿(101)面[17]和金红石(110)面的特性以及NO[22]、NO2[23]、NH3[24]、CO[25]等小分子气体在表面的吸附微观机理做了一些研究,但对H2O分子在TiO2(101)面吸附的微观研究还很少涉及,本文基于密度泛函理论(DFT)模拟计算锐钛矿型TiO2(101)面吸附H2O分子引起的表面光学性质变化,对H2O分子与其表面的吸附距离、吸附能、电子态密度、光学性质等予以分析,为该材料的光学气敏传感特性研究提供理论基础.
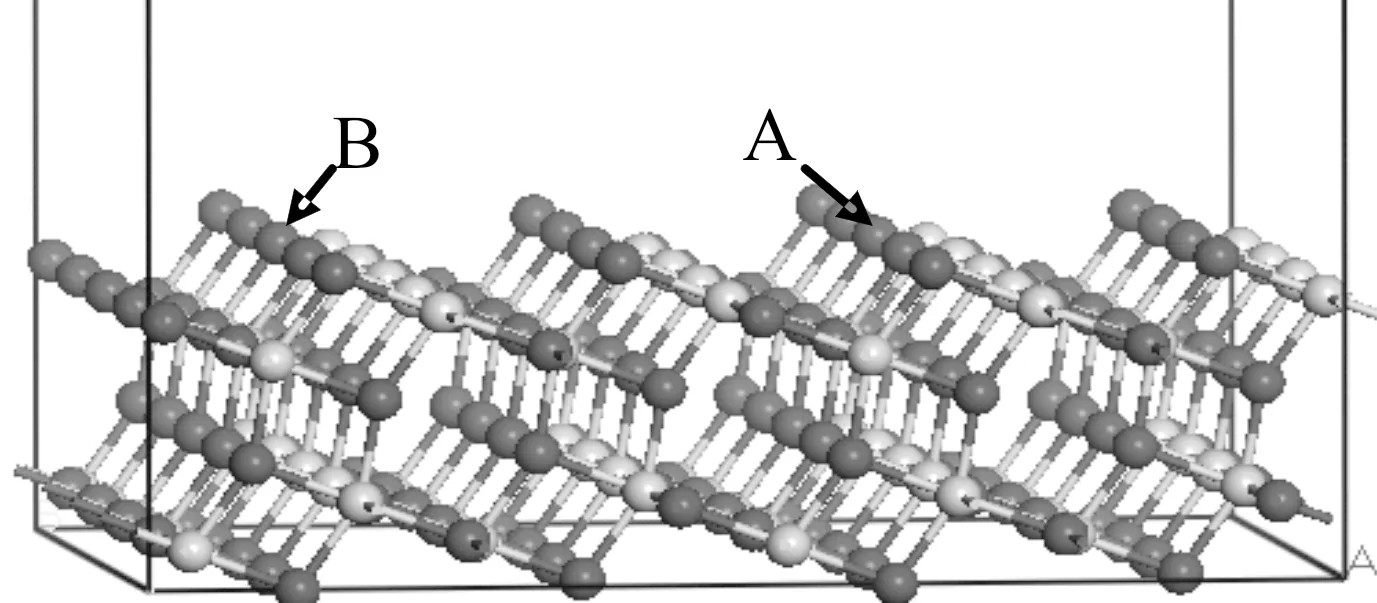
图1 锐钛矿相TiO2(101)无氧空位表面原子结构模型Fig. 1 Atomic structure model of the anatase TiO2(101) surface
2 模型构建与计算方法
本文计算采用基于密度泛函理论(DFT)中的平面波超软赝势方法,交换关联能采用广义梯度近似(GGA)中的PBE泛函处理,平面波截断能设置为320 eV,第一布里渊区的积分计算使用Monkhorst-Pack方案选取3×5×2进行分格.
作为四方晶体的锐钛矿型TiO2,4个TiO2分子组成一个原胞,每个八面体与周围8个八面体相连接(4个共边,4个共顶角).由于锐钛矿型TiO2暴露在外(最稳定)的主要的表面是(101)面[8,9],因此作者构造了(2×4×2)的锐钛矿型TiO2超晶胞,对该结构在垂直[101]方向进行剪切,采用的表面原子结构模型[18],如图1所示,最表层终止于两配位O原子,次层为五配位的Ti原子表面总能量最低,最稳定[19,21].距离表面12层以外的内部原子已可忽略对表面吸附的影响,因此建立12层厚度的晶胞,真空层厚度为12 Å,在该模型基础上,分别建立无氧空位表面、含有一个氧空位缺陷(空位浓度7.7%)和含有两个氧空位缺陷的锐钛矿型TiO2(101)表面模型(空位浓度为15.4%),空位的位置在图中A和B处,H2O分子距离表面初始距离均为1.700 Å,固定最下层原子,仅让表面上11层原子层对H2O分子吸附模型进行几何优化.
3 计算结果及讨论
3.1 吸附微观模型及吸附距离
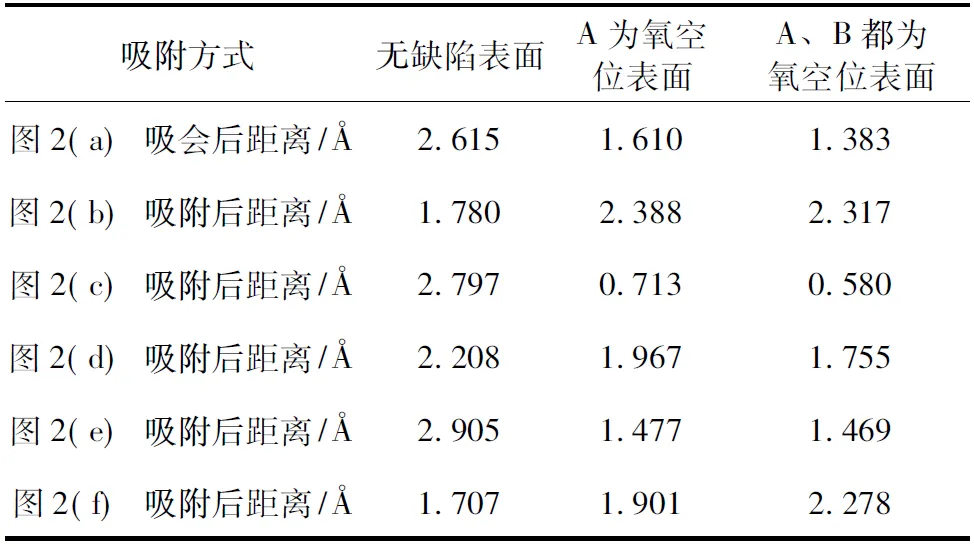
H2O分子以不同方式放置于锐钛矿型TiO2(101)表面二配位的氧原子正上方,如图2所示,A、B分别为表面氧原子或氧空位位置.各个模型氧原子与表面的初始距离均为1.700 Å,分别用d表-O和d表-H表示氧原子和氢原子离表面的距离.锐钛矿型TiO2(101)表面吸附H2O分子后距离如表1所示,可以得到:
1)放置在无氧空位表面的H2O分子,六种放置方式优化后都远离了表面,说明H2O不容易被无氧空位的TiO2(101)表面吸附.
2)H2O分子吸附于具有氧空位缺陷TiO2(101)表面时,H2O分子O端吸附后位置离表面距离减小,而H端吸附离表面距离增大,说明H2O分子吸附于氧空位表面以O端吸附为主.
3)氧空位浓度越大,H2O分子吸附于表面的距离越短,说明氧空位缺陷浓度越大,其吸附效果越明显.
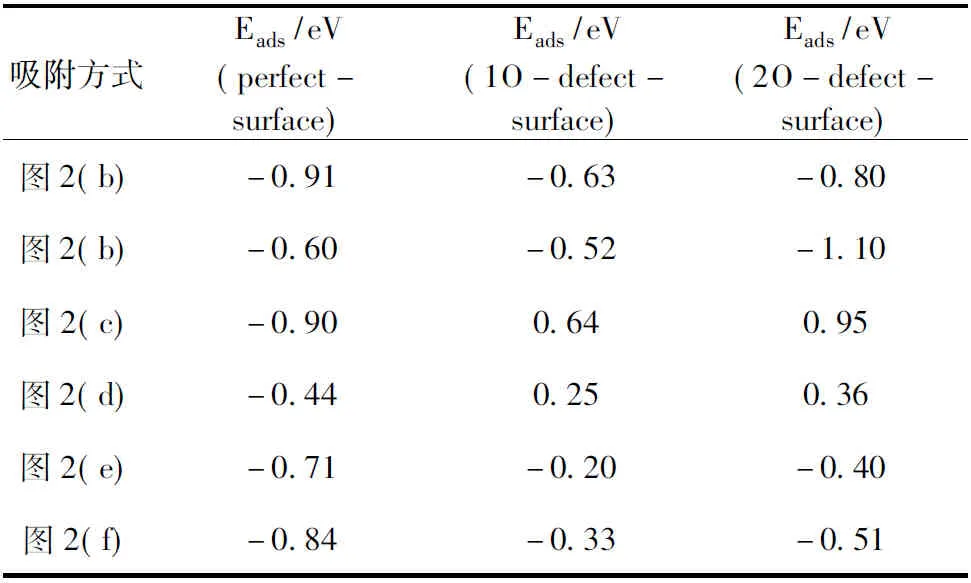
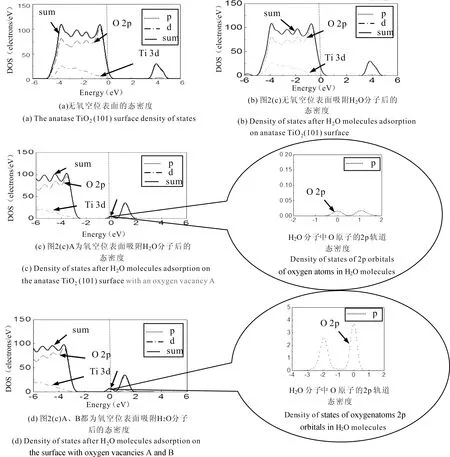
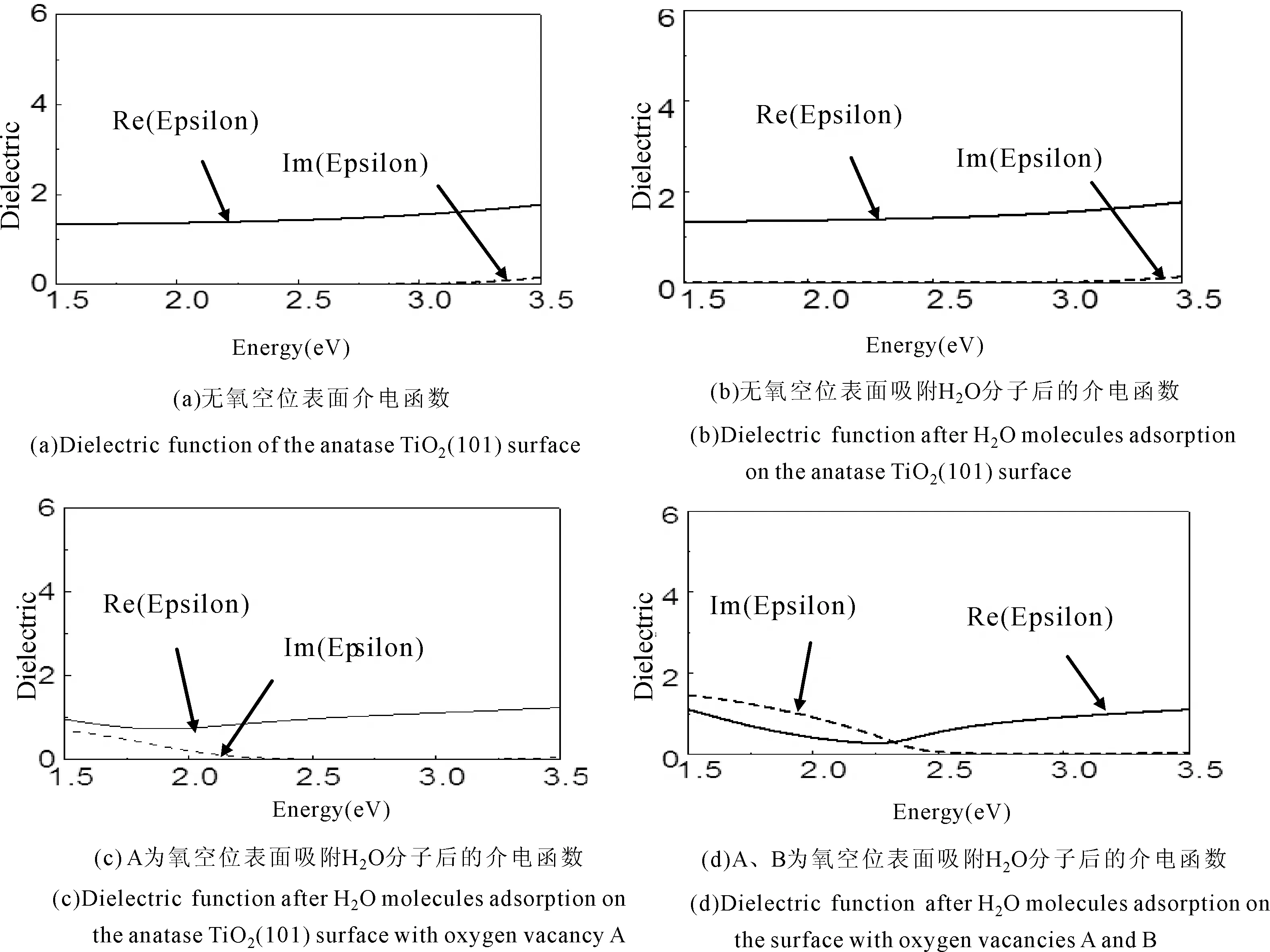
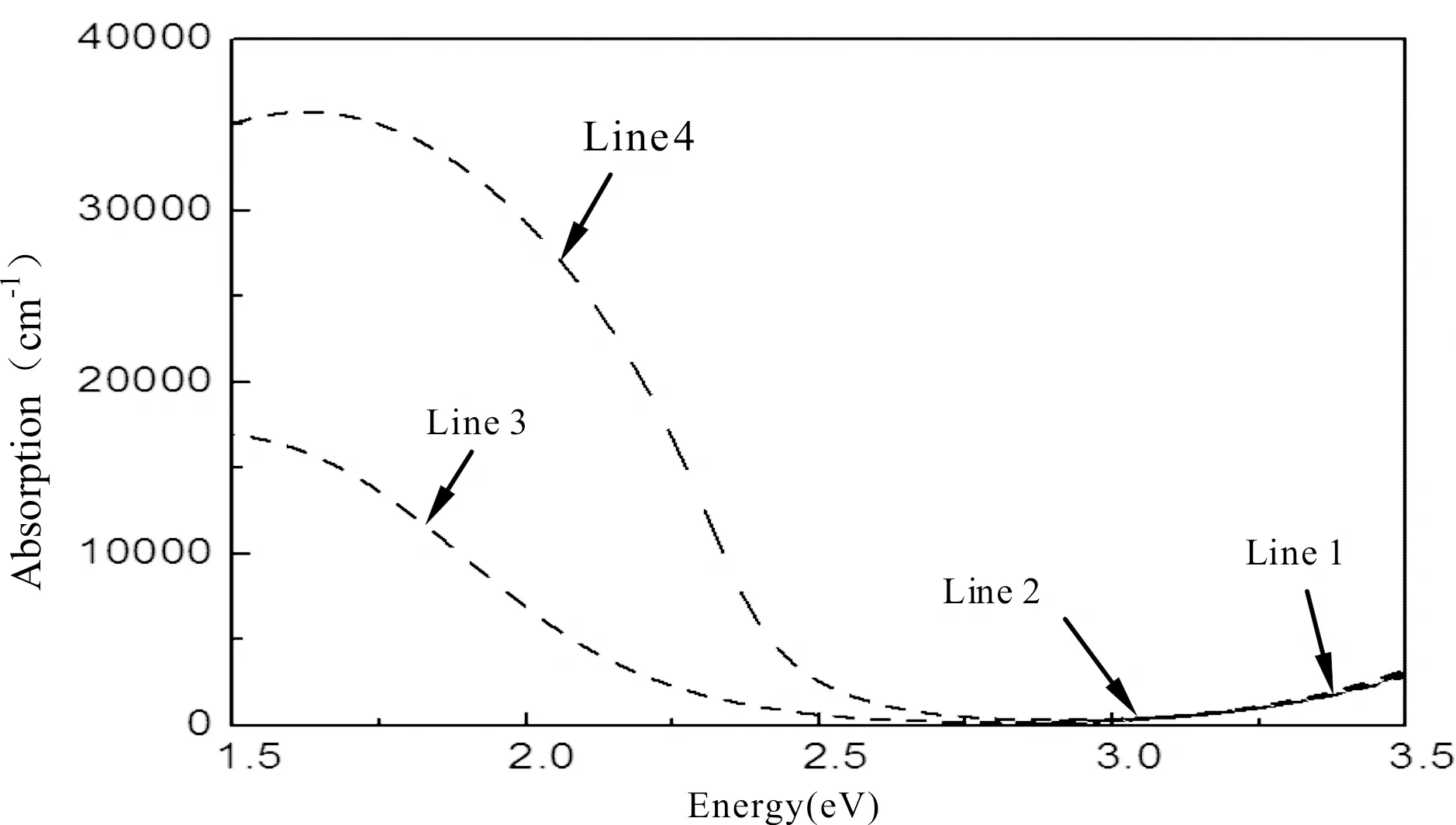
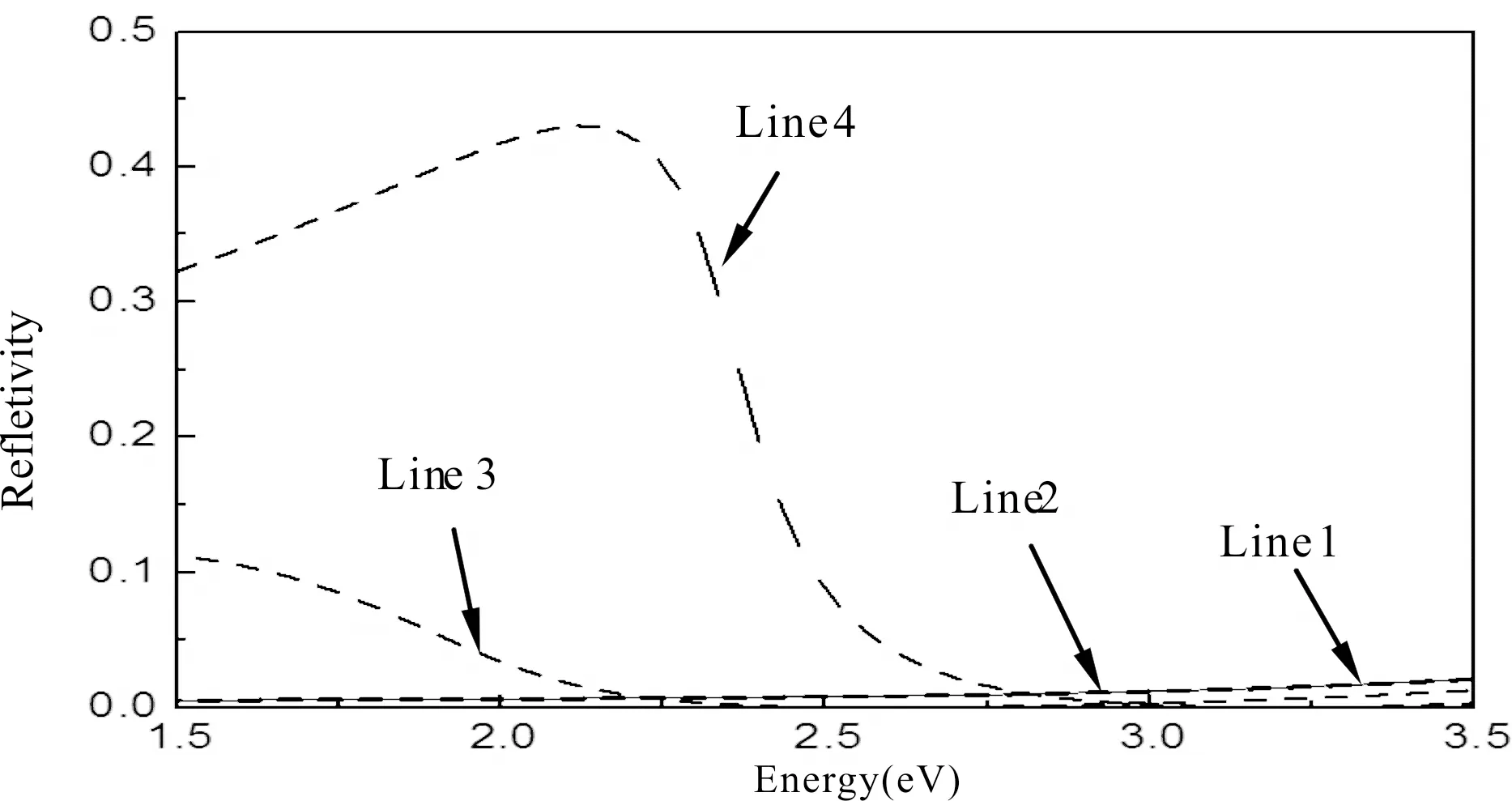
4)比较三种O端吸附方式,可以得到,以图2(c)模型,即H2O分子竖直放置(d表-O 3.2 吸附能 H2O分子吸附于TiO2(101)表面的吸附能(adsorption energy,ads)为吸附前后表面超晶胞总能量的差值,即公式[26]: Eads=E表TiO2+EH2O-ETiO2+H2O (1) 其中E表TiO2为TiO2(101)表面超晶胞的能量,EH2O为一个H2O分子的能量,ETiO2+H2O为H2O分子吸附在TiO2(101)表面几何优化后的总能量.表2列出了六种吸附模型的吸附能. 吸附能大于零,说明吸附过程放热,吸附后结构更加稳定.从表2中可以得出: 1)H2O分子稳定吸附于TiO2(101)表面后, 图2 H2O在锐钛矿型TiO2(101)表面的吸附模型Fig.2 The adsorption model of H2O molecules in anatase TiO2(101) surface 表1 H2O分子以不同方式放置吸附后与锐钛矿相 TiO2(101)表面距离 Table 1 Adsorption distances after H2O molecules adsorption on the anatase TiO2(101) surface when it is placed in different ways 表2 H2O分子吸附于TiO2表面的吸附能 Table 2 Energies of adsorption after H2O molecules adsorption on the anatase TiO2(101) surface 分子平面垂直于材料表面,(图2(c)和图2 (d))此时吸附能为正; 2)O端距离表面氧空位越近,吸附能越大,吸附越稳定 (E图2(c)>E图2(d)); 3)其他吸附方式的吸附能均为负值,表明这些吸附方式优化后分子结构皆不稳定,不是稳定的吸附方式; 4)氧空位浓度越大,吸附能越大,吸附越容易实现. 3.3 电子态密度分析 经过前面计算分析,得到图2(c)吸附模型为最稳定的吸附状态,所以分别计算了图2(c)模型H2O分子在无氧空位、有氧空位TiO2(101)表面吸附前后的态密度.禁带宽度定义为从体系价带最高点到导带最低点之间的距离,作者计算出纯TiO2的禁带宽度为2.346 eV,小于实验测量值3.200 eV.这是由于密度泛函理论本身的缺陷造成的,在分析电子结构时使用“剪刀算符”0.854 eV进行修正,结果如图3所示. 从图3(a)中可以发现:无氧空位表面导带主要由Ti-3d轨道构成,价带则主要由O-2p轨道构成,费米能级靠近价带顶.当H2O分子吸附于无氧空位表面后,导带底和价带顶几乎没有发生变化,分子中的电子对表面几乎没有造成的影响,如图3(b)所示.氧空位在TiO2中相当于一个正电荷中心,空位本身就是一种P型杂质,当出现氧空位缺陷后,整个导带向低能方向偏移,费米面上移,带隙宽度变窄,费米能级附近出现了新的峰值(如图3(c)(d)箭头所示),且空位浓度越大,峰值越高.在导带底产生了新的杂质能级,这非常有利于电子从价带跃迁到导带,这正是H2O分子中氧原子的掺入所引起的.H2O分子中O原子的2p孤对电子的掺入,与表面的导带电子充分交叠,使价带明显下移,并在禁带中间形成新的施主能级.氧空位浓度影响施主能级的态密度峰值的大小.新的峰值起到“垫脚石”的作用,有利用电子的二次激发跃迁,改善TiO2作为良好半导体材料的特性. 3.4 介电函数 半导体的光学性质描述中介电函数非常重要,通常用复介电函数ε(ω)=ε1(ω)+iε2(ω)或复折射率N(ω)=n(ω)+ik(ω)来描述材料对可见光的光学响应函数,其中ε1=n2-k2,ε2=2nk.在光学性质的研究中,可先根据费米黄金定律,从直接跃迁概率的定义推导出介电函数的虚部ε2[19],即 (1) 本文计算图2(c)模型H2O分子在TiO2(101)表面吸附前后的介电函数,如图4所示,可以得到:在可见光(1.6-3.1)eV范围内,完美表面虚部在3eV之后才大于零,而实部几乎在1.6eV左右维持;当H2O分子在完美表面吸附后,介电函数几乎没有变化;当分子在含有一个氧空位缺陷的表面吸附后,介电函数虚部值有所增大,对可见光低能区的响应在一定程度上有所提高,如图4(c)所示;当H2O分子在含有两个氧空位表面吸附时,虚部的值大幅度增加,如图4(d)所示,虚部在1.6eV附近达最大值约为1.7.因此,在可见光低能区范围内,按图2(c)模型,即H2O分子竖直放置(d表-O 图3 表面吸附H2O分子前后的态密度Fig.3 Demsity of states before and after H2O molecules adsorption on the anatase TiO2(101) surface 图4 吸附前后锐钛矿TiO2(101)表面的介电函数Fig.4 Dielectric function before and after adsorption on the anatase TiO2(101) surface 3.5 吸收谱和反射谱 为研究吸附H2O分子后表面的光学性质,本文计算了图2(c)模型的吸收光谱和反射光谱,分别如图5和图6所示. 低能电子吸收光子能量后跃迁至激发态,表现为吸收,通过计算材料的吸收光谱,可获得材料的有关物理性质.由图5吸收光谱可知:在(1.6~3.1) eV范围内,H2O分子吸附在完美表面后,对可见光的吸收几乎为零;当分子吸附于含一个氧空位的表面后,对可见光的吸收有所提高,吸收系数在1.6 eV处出现峰值约为15500 cm-1;当分子吸附在含有两个氧空位的表面后,在可见光低能区,吸收系数有显著提高,吸收系数在1.8 eV处出现峰值约为37000 cm-1. 光的反射过程可以解释为光吸收的后续过程,当材料受到光照射时,处于基态的电子吸收光子的能量跳跃到激发态,但是部分处于激发态的电子并不稳定,它必将往回跃迁,从激发态回到基态,在这个过程中,激发态与基态之间的能量差可能会以光子的形式释放出来,表现为材料对照射光的反射.越多的电子吸收光子而跃迁,就会有越多的电子释放能量回到低能级,表现为反射率就越高.图6为H2O分子吸附于TiO2(101)面前后的反射光谱,从图中可以看出:在可见光(1.6~3.1) eV范围内,无氧空位表面吸附H2O分子前后反射效果都不好,对可见光的反射率几乎为零;当分子在一个氧空位缺陷表面吸附后,其反射效果有所提高,反射率在1.6eV时最大值为0.11;当分子被含有两个氧空位的表面吸附后,在可见光低能区,反射率明显改善,在2.2 eV时达到峰值约为0.44. 图5 吸附前后表面的吸收谱线1:完美表面,线2:分子吸附在完美表面,线3:分子吸附在含1个氧空位的表面,线4:分子吸附在含2个氧空位表面Fig. 5 Absorption spectra before and after adsorption Line 1: perfect surface, Line 2: molecule adsorption on surface, Line 3: molecule adsorption on surface with an oxygen vacancy, Line 4: molecule adsorption on the surface with two oxygen vacancies 图6 吸附前后表面的反射谱线1:完美表面,线2:分子吸附在完美表面,线3:分子吸附在含1个氧空位的表面,线4:分子吸附在含2个氧空位表面Fig. 6 Reflectance spectra before and after adsorption Line 1: perfect surface, Line 2: molecule adsorption on surface, Line 3: molecule adsorption on surface with an oxygen vacancy, Line 4: molecule adsorption on the surface with two oxygen vacancies 综上所述,从吸收谱和反射谱中可以得到:在可见光低能区,图2(c)模型放置,即H2O分子竖直放置(d表-O 采用基于密度泛函理论(DFT)的平面波超赝势方法,对H2O分子在锐钛矿型TiO2(101)表面吸附行为的微观特性进行研究,分别计算了吸附前后表面的吸附能、几何结构、电子态密度、光学性质,通过对比吸附前后变化情况,得出以下结论: 1)H2O分子在含有氧空位的锐钛矿型TiO2(101)表面的吸附状态为分子平面垂直于材料表面,且O端距离氧空位越近时,吸附越稳定. 2)氧空位浓度越大,越有利于分子在表面的吸附. 3)仅有分子平面垂直于材料表面的吸附,且负电中心距氧空位较近时,吸附能才为正值,所以吸附的本质是氧空位对分子负电中心的吸引. 4)稳定吸附后,在导带底位置产生了新的杂质能级,这是由于H2O分子中O原子的2p孤对电子掺入的影响,也是光学性质改善的原因. 5)H2O分子在不同浓度的氧空位表面吸附时发现,氧空位浓度越大,吸附后在可见光低能区范围内的反射率和吸收系数变化越明显. [1] Tang Y C, Li W, Hu C,etal. Studies on morphological structure and photoactivity of TiO2heterogeneous photocatalysts [J].ProgressinChemistry, 2003, 9: 379. [2] Zhao W, Ma W H, Chen C C,etal. Efficient degradation of toxic organic pollutants with Ni2O3/TiO2-xB under visible irradiation [J].J.Am.Chem.Soc., 2004, 126(15): 4782. [3] Panchangam S C, Lin A Y, Shaik K L,etal. Decomposition of perfluorocarboxylic acids (PFCAs) by heterogeneous photocatalysis in acidic aqueous medium [J].Chemosphere, 2009, 7: 242. [4] Henrich V E, Cox P A.Thesurfacescienceofmetaloxides[M]. Cambridge: Cambridge University Press, 1996: 16. [5] Amy L Linsebigler, Lu G Q, Yates J T. Photocatalysis on TiO2surfaces: principles, mechanisms, and selected results [J].Chem.Rev., 1995, 95 (3): 735. [6] Fujishima A, Rao T N, Ryk D A. Titanium dioxide photocatalysis [J].J.Photochem.Photobiol. CPhotochem.Rev., 2000, 1(1): 1. [7] Bickley I B, Gonzalez-Carreno T, Lees J S,etal. A structural investigation of titanium dioxide photocatalysts [J].J.SolidStateChem., 1991, 92: 178. [8] Kwok On Ng, David Vanderbilt. Structure and apparent topography of TiO2(110) surfaces [J].Phys.Rev. B, 1997, 56: 10544. [9] Labat F, Baranek P, Adamo C. Structural and electronic properties of selected rutile and anatase TiO2surfaces: an ab-initio investigation [J].JournalofChemicalTheoryandComputation, 2008, 4: 341. [10] Vittadini A, Selloni A, Rotzinger F P,etal. Structure and energetics of water adsorbed at TiO2anatase (101) and (001) surfaces [J].Phys.Rev.Lett., 1998, 81: 2954. [11] Gong X Q, Selloni A, Batzill M,etal. Steps on anatase TiO2(101) [J].Nat.Mater., 2006, 5(8): 665. [12] Herman G S, Dohnalek Z, Ruzycki N,etal. Experimental investigation of the interaction of water and methanol with anatase-TiO2(101) [J].J.Phys.Chem. B, 2003, 107: 2788. [13] He Y B, Dulub O, Cheng H Z,etal. Evidence for the predominance of subsurface defects on reduced anatase TiO2(101) [J].Phys.Rev.Lett., 2009, 102(10): 106105. [14] Sorescu D C, Al-Saidi W A, Jordan K D. CO2adsorption on TiO2(101) anatase: A dispersion-corrected density functional theory study [J].JournalofChemicalPhysics, 2011, 135(12): 124701. [15] Indrakanti V P, Kubicki J D, Schobert H H. Quantum chemical modeling of ground states of CO2chemisorbed on anatase (001), (101), and (010) TiO2surfaces [J].Energy&Fuels, 2008, 22(4): 2611. [16] Li Z B, Wang X, Chi B. First principles investigation of the conversion of N2O and CO to N2and CO2on a modified N + Fe/TiO2(101) surface [J].RSCAdv., 2014, (4): 17896. [17] Yang Y, Feng Q, Wang W H,etal. First-principle study on the electronic and optical properties of the anatase TiO2(101) surface [J].JournalofSemiconductors, 2013, (7): 0730041. [18] Ma X G, Tang C Q, Huang J Q,etal. First-principle calculation on the geometry and relaxation structure of anatase TiO2(101) surface [J].ActaPhys.Sin., 2006, 55(8): 4208 (in Chinese) [马新国, 唐超群, 黄金球, 等. 锐钛矿型TiO2(101)面原子几何及弛豫结构的第一性原理计算[J]. 物理学报, 2006, 55(8): 4208] [19] Lu B.FirstprinciplesstudyofanataseTiO2(101)surface[D]. Msater Degree Thesis of Qingdao University of Science &Technology, 2012: 28 (in Chinese) [鲁冰.锐钛矿型TiO2(101)面第一性原理研究 [D]. 青岛科技大学硕士学位论文, 2012: 28] [20] CrossRef Vittadini A, Selloni A, Rotzinger F P,etal. Structure and energetics of water adsorbed at TiO2anatase (101) and (001) surfaces [J].Phys.Rev.Lett., 1998, 81: 2954. [21] He Y B, Tilocca A, Dulub O,etal. Local ordering and electronic signatures of submonolayer water on anatase TiO2(101) [J].Nat.Mater., 2009, 8(7): 585. [22] Feng Q, Yue Y X, Wang W H,etal. First-principles study on anatase TiO2(101) surface adsorption of NO [J].Chin.Phys. B, 2014, 23(4): 0431011. [23] Yang Y, Feng Q. Study micro-character theory on anatase TiO2(101) surface adsorption of NO2[J].JournalofChongqingNormalUniversity(NaturalScience), 2014, 31(5): 108. [24] Zhu H Q, Feng Q. A study on microscopic mechanism and optical gas sensing materail characteristics of rutile titanium dioxide(110) surface adsorption NH3molecules [J].ActaOpticaSinica, 2014, 34(10): 10160021. [25] Zhu H Q, Feng Q. Microscopic characteristics mechanism of optical gas sensing material rutile titanium dioxide (110) surface adsorption of CO molecules [J].ActaPhys.Sin., 2014, 63(13): 1331011. [26] Han Y, Liu C J, Ge Q F. Interaction of Pt clusters with the anatase TiO2(101) surface: a first principles study [J].J.Phys.Chem. B, 2006, 110(14): 7463. Adsorption characteristic and microcosmic mechanism of anatase TiO2(101) surface adsorption of H2O molecules YANG Ying, FENG Qing, ZHANG Ju-Hua (College of Physics and Electronic Engineering, Chongqing Normal University, Chongqing 400047, China) In this paper, the adsorption energy, adsorption distance, density of states and optical properties were studied from the plane wave ultra-soft pseudo-potential technology based on the density function theory (DFT). The results through simulation calculation of H2O adsorbed on the anatase TiO2(101) surface show that the surface only containing oxygen vacancy can stably adsorbs H2O molecules. After stable adsorption, the H2O molecule plane is perpendicular to TiO2(101) surface. The closer the negative charge center (O-terminal) to the surface, the more easily the adsorption; and the higher of oxygen vacancy concentration, the more obvious adsorption effect. Compared with the density of states, a new peak appears nearby the fermi level because of 2p lone-pair electrons of H2O molecules doping in surface. The transition probability, optical gas sensitive features, absorption coefficient and reflectivity can be improved in the low-energy scope of visible light. Anatase; Optical gas sensing material; Surface absorption; Density functional theory 2014-12-03 国家自然科学基金(61274128, 61106129);重庆市自然科学基金(CSTC2013JCYJA0731, CSTC2014JCYJA50015);重庆市教委科学技术研究项目(KJ120614, KJ1400524) 杨英,女,讲师,研究方向为原子分子物理的理论研究.E-mail: ying_yang@126.com 103969/j.issn.1000-0364.2015.08.029 O469 A 1000-0364(2015)08-0695-08

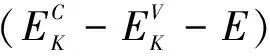
4 结 论
