温阳通痹丸质量标准研究
2015-02-01谢强王志梅邬伟魁
谢强 王志梅 邬伟魁
(梅州市食品药品监督检验所,广东 梅州 514071)
温阳通痹丸质量标准研究
谢强 王志梅 邬伟魁
(梅州市食品药品监督检验所,广东 梅州 514071)
目的:建立温阳通痹丸的质量标准。方法:采用薄层色谱法(TLC)鉴别温阳通痹丸中的赤芍和麻黄,采用高效液相色谱法(HPLC)测定赤芍中芍药苷的含量。色谱条件:色谱柱为岛津SHIADZU VP-ODS(250 mm ×4.6 mm,5μm),流动相为乙腈-水(18∶82),流速1.0 m L/m in,柱温30℃,检测波长为230 nm。结果:TLC的斑点清晰,阴性对照无干扰;芍药苷在10.22~ 204.40μg/m L(r=0.999 9)范围内线性关系良好,平均回收率为98.45%,RSD为0.7%(n=6)。结论:所建标准可用于温阳通痹丸的质量控制。
温阳通痹丸;芍药苷;盐酸麻黄碱;薄层色谱法;高效液相色谱法
温阳通痹丸为梅州市人民医院的制剂,临床疗效良好,需求较大。该制剂主要由赤芍、麻黄、黄芪、红参、乳香等药味组成;具有益气养阴,活血祛瘀,温阳通痹的作用。用于糖尿病四肢麻木、凉、痛、烂及全身疼痛等症。赤芍为方中君药,可清热凉血,散瘀止痛,用于热入营血,温毒发斑,吐血衄血,目赤肿痛,肝郁胁痛,经闭痛经,癥瘕腹痛,跌扑损伤,痈肿疮疡[1]。药理研究表明,赤芍具有抗炎、抗凝血、免疫调节等作用[2]。麻黄性温,可温经通阳,为方中臣药。赤芍和麻黄的主要化学成分分别为芍药苷和盐酸麻黄碱。原标准已不能有效控制制剂质量,本文参考现行药典收载方法及文献报道[3-5],研究建立了赤芍、麻黄的薄层色谱法(TCL)鉴别和高效液相色谱法(HPLC)测定芍药苷含量的方法。该方法简便、快速、准确、重复性好,可更好地控制温阳通痹丸的质量。
1 仪器与试药
高效液相色谱仪:Agilent 1100;色谱柱:SHIADZU VP-ODS(250 mm ×4.6 mm,5μm),SN:8022538;电子分析天平:AB204-N,NO:1202410309;超声仪:KQ250DE;硅胶G(青岛海洋化工集团公司,批号:0120213,自制薄层板规格为10 ×20 cm,厚0.5 mm);乙腈为色谱纯;水为超纯水(自制);其他试剂均为分析纯。芍药苷对照品(批号:110736-201136),盐酸麻黄碱对照品(批号:171241-200506)均由中国药品生物制品检定所提供;温阳通痹丸(梅州市人民医院提供,批号:20130502,20130715,20131007)。
2 方法与结果
2.1 TLC鉴别
2.1.1 赤芍取本品粉末5 g,加乙醇20 m L,超声处理30分钟,滤过,滤液蒸干,残渣加水15 m L使溶解,滤过,滤液用乙醚振摇提取2次,每次15 m L,弃乙醚液,水溶液用水饱和的正丁醇振摇提取3次,每次15 m L,合并正丁醇提取液,蒸干,残渣加乙醇1 m L使溶解,作为供试品溶液。另取芍药苷对照品,加乙醇制成每1 m L含1 mg的溶液,作为对照品溶液。另按处方配比及制法制备缺赤芍的阴性样品,同上述供试品溶液制备法制备阴性对照溶液。照TLC(附录ⅥB)试验,吸取上述3种溶液各5μL,分别点于同一硅胶G薄层板上,以二氯甲烷-乙酸乙酯-甲醇-甲酸(40∶5∶10∶0.2)为展开剂,展开,取出晾干,喷以5%香草醛硫酸溶液,加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的荧光斑点,阴性无干扰。见图1。
2.1.2 麻黄取本品粉末5 g,加乙醚20 m L与浓氨试液1 m L,密塞,放置2小时,时时振摇,滤过。药渣用乙醚15 m L分3次洗涤,滤过,合并滤液,加盐酸乙醇溶液(1→20)1 m L,摇匀,蒸干,残渣加甲醇2 m L使溶解,滤过,滤液作为供试品溶液。另取盐酸麻黄碱对照品,加甲醇制成每1 m L含1 mg的溶液,作为对照品溶液。另按处方配比及制法制备缺麻黄的阴性样品,同上述供试品溶液制备法制备阴性对照溶液。照TLC(附录ⅥB)试验,吸取上述3种溶液各5μL,分别点于同一硅胶G薄层板上,以二氯甲烷-甲醇-浓氨试液(40∶7∶1)为展开剂,展开,取出晾干,喷以茚三酮试液,在105℃加热至斑点显色清晰。供试品色谱中,在与对照品色谱相应的位置上,显相同颜色的斑点,阴性无干扰。见图2。
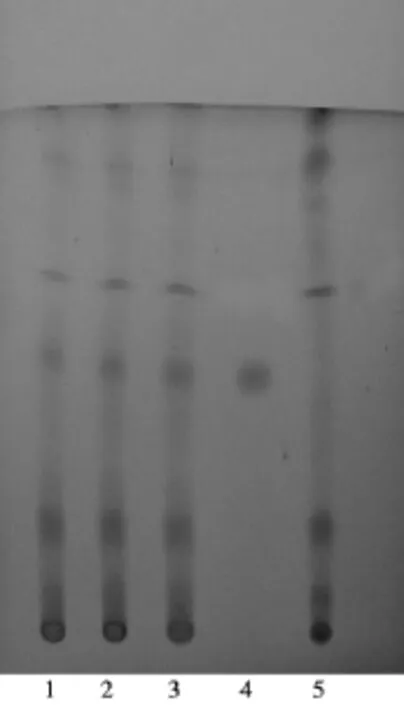
图1 赤芍TLC图
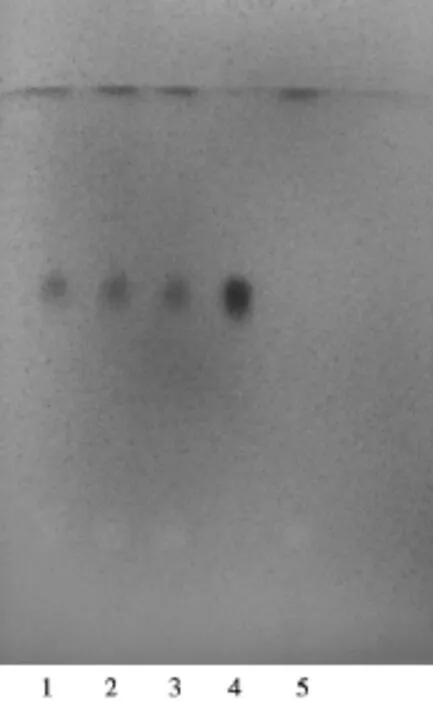
图2 麻黄TLC图
2.2 含量测定
2.2.1 色谱条件色谱柱:岛津 SHIADZU VP-ODS(250 mm ×4.6 mm,5μm);流动相:乙腈-水(18∶82);流速:1.0 m L/m in;柱温:30℃;检测波长为230 nm;进样量为10μL。
2.2.2 溶液的制备①对照品溶液:取芍药苷对照品适量,加甲醇制成每1 m L含40μg的溶液。②供试品溶液:取本品粉末约 1 g,精密称定,置具塞锥形瓶中,精密加入甲醇50 m L,密塞,称定质量,超声处理(功率250 W,频率40 kHz)30 m in,取出,放冷,称定质量,用甲醇补足减失质量,摇匀,滤过,取续滤液,即得。③阴性对照溶液:按处方比例及工艺,制成不含赤芍的阴性样品,并按上述供试品溶液的制备方法制备阴性对照溶液。
2.2.3 专属性考察吸取对照品溶液、供试品溶液、阴性对照溶液各10μL,分别按上述色谱条件进行分析,记录色谱图。结果阴性对照色谱在与对照品色谱相应位置上无干扰峰出现,说明处方中其他成分对测定结果无影响。芍药苷的保留时间约为6 m in,分离度大于1.5,理论板数按芍药苷峰计算不低于5 000。见图3。
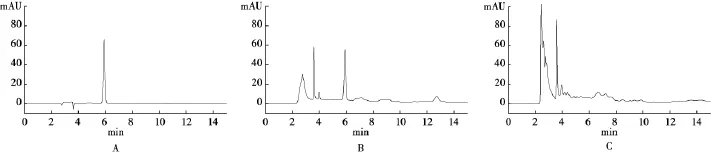
图3 芍药苷HPLC图
2.2.4 标准曲线的制定分别精密吸取芍药苷对照溶液 0.5,1.0,2.0,4.0,8.0,10.0 m L置 10 m L量瓶中,加甲醇稀释至刻度,摇匀,分别取 10μL注入液相色谱仪中,测定芍药苷的含量,以进样浓度(X)为横坐标,以峰面积(Y)为纵坐标,得回归方程为
Y=13.757 3X-0.593 7。
r=0.999 9,结果表明,芍药苷在 10.22~204.40μg/m L范围内与峰面积线性关系良好。
2.2.5 精密度试验精密吸取对照品溶液,连续进样6次,测得芍药苷峰面积的RSD为0.71%,表明仪器精密度良好。
2.2.6 重复性试验取同一批样品(批号:20130502)6份,依法制备供试品溶液并测定含量,结果样品中含芍药苷平均值为 1.66 mg/g,RSD为 1.09%(n=6)。
2.2.7 稳定性试验取同一份供试品溶液(批号:20130502),分别于0,1,2,4,8,12,24 h进样10μL,测定其峰面积,结果芍药苷在0~ 24 h测定的峰面积的RSD为 0.35%,表明供试品溶液在24小时内稳定。
2.2.8 加样回收率试验取已知含量的同一批样品(批号:20130502)适量,精密加入一定量的芍药苷对照品,按供试品溶液的制备方法制备加样供试品溶液,测定,计算加样回收率。结果见表1。
2.2.9 样品含量测定分别取3批样品按2.2.2项下方法制得供试品溶液,进行测定,计算含量。结果 3批样品中芍药苷含量分别为 1.66,1.65,1.61 mg/g。
根据以上3批样品的含量测定,确定本品的含量限度为:本品每1 g含赤芍以芍药苷(C23H28O11)计,不得少于1.3 mg。
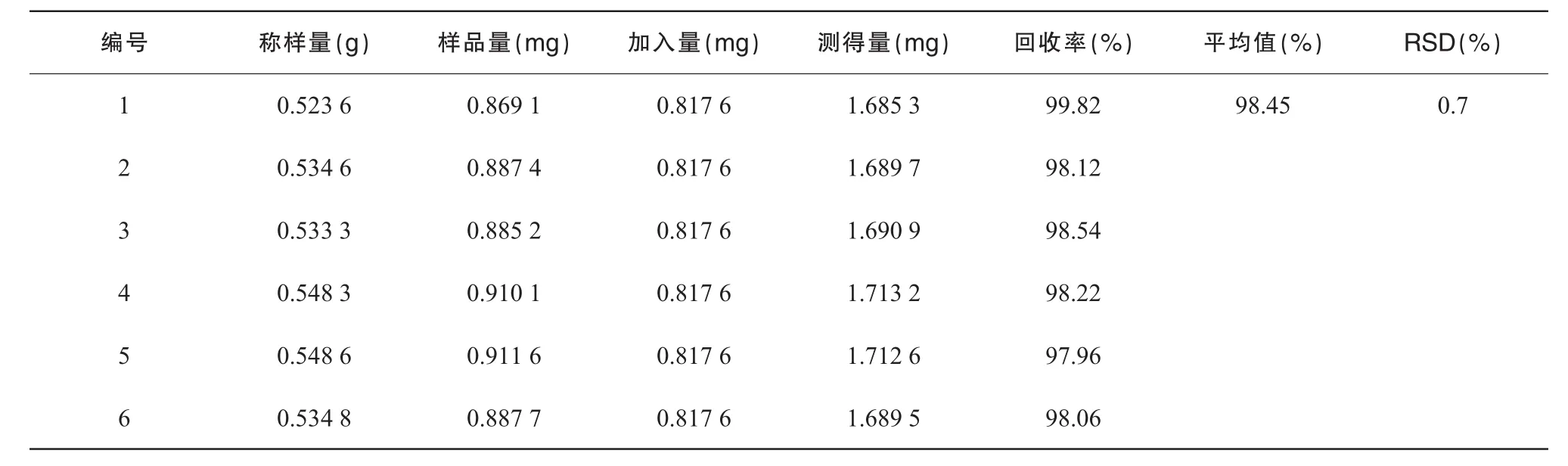
表1 加样回收试验
3 讨论
原标准为广东省食品药品监督管理局医疗机构制剂注册标准——粤ZB20110015(Z)。原标准仅对麻黄(盐酸麻黄碱)进行了TLC鉴别,无含量测定方法。原标准中供试品的提取溶剂为三氯甲烷,本研究更换了试剂,优化了供试品的制备方法;原展开系统为三氯甲烷-甲醇-浓氨试液(20∶5∶0.5),使用了毒性较大的三氯甲烷,本研究通过实验更换成毒性较小的试剂并调整了展开剂的比例,调整后的展开系统为二氯甲烷-甲醇-浓氨试液(40∶7∶1),实验所得色谱斑点清晰,供试品色谱在与对照药材色谱相应的位置上斑点对应良好,且阴性对照无干扰。
芍药苷含量测定流动相选择时,曾参照现行药典,流动相为乙腈-0.05 mol/L磷酸二氢钾溶液(12∶88),但保留时间较长,最后选用乙腈-水(18∶82)[6],缩短了保留时间。
值得注意的是,目前对赤芍的质量控制主要是根据芍药苷的含量高低来进行评价,近年来,有研究者[7]采用HPLC建立了评价赤芍质量的特征指纹图谱分析方法,指纹图谱在制剂[8]质量评价中的应用也日渐增多。此外,一测多评[9-10]也是近年来兴起的符合中药特点的中药产品质量控制[11]模式。很多医疗机构中药制剂的临床需求量都较大,但其质量控制总体水平尚落后于市售中成药。在一些医院制剂大品种的质量标准提高时,建议有条件的医院引进先进的中药质量控制技术,严格控制产品的质量,确保制剂的临床安全性和有效性。
[1] 国家药典委员会.中华人民共和国药典(一部)[S].北京:中国医药科技出版社,2010:147.
[2] 杨琪伟,杨莉,熊爱珍,等.赤芍和白芍抗炎作用的UPLC-MS代谢组学初步研究[J].中国中药杂志,2011,36(6):694-697.
[3] 李海燕,宋汉敏,李振国.培元通脑胶囊质量标准研究[J].中国实验方剂学杂志,2013,19(2):129-132.
[4] 张建军,李伟,王丽丽,等.赤芍和白芍品种、功效及临床应用述评[J].中国中药杂志,2013,38(20):3595-3601.
[5] 余敬波,章军,王文全,等.赤芍野生品与栽培品4种化学成分含量的比较[J].中国实验方剂学杂志,2011,17(18):107-111.
[6] 谢晓梅,余长柱,徐衡,等.赤芍饮片质量标准研究——芍药苷的含量测定[J].中国中药杂志,2004,29(8):759-762.
[7] 王瑞,黄山君,杨琪伟,等.赤芍与白芍HPLC特征指纹谱的建立及其在质量控制中的应用[J].中国中药杂志,2011,36(6):729-733.
[8] 王云龙,李延雪,邵礼梅,等.元胡止痛片HPLC指纹图谱研究[J].中草药,2011,42(3):495-497.
[9] 王智民,高慧敏,付雪涛,等.“一测多评”法中药质量评价模式方法学研究[J].中国中药杂志,2006,31(23):1925-1928.
[10] 高慧敏,宋宗华,王智民,等.适合中药特点的质量评价模式——QAMS研究概述[J].中国中药杂志,2012,37(4):405-416.
[11] 王智民,钱忠直,王永炎.中药产品质量过程控制[J].中国中药杂志,2011,36(6):656-656.
Studies on Quality Standard of W enyang Tongbi Pills
Xie Qiang,Wang Zhimei,Wu Weikui(Meizhou Institute for Food and Drug Control,Guangdong Meizhou 514071,China)
Objective:To establish the quality standard of wenyang tongbi pills.M ethods:TLC was used to determine Paeonide radix rubra and Ephedrae herba in wenyang tongbi pills,and HPLC was used to determ ine the content of paeoniflorin.A chromatographic column of SHIADZU VP-ODS(250 mm ×4.6 mm,5μm)was used w ith a mobile phase of acetonitrile-water (18∶82)at a flow rate of 1.0 m L/m in,the detection wavelength was at 230 nm and the room temperature was at 30℃.Results:The spots of TLC were fairly clear and the negative control w ithout interference.A good linear relationship of paeoniflorin was from 10.22 to 204.40μg/m L(r= 0.999 9).The average recovery was 98.45%,RSD was 0.7%(n=6).Conclusion:The established standard is applicable for the quality control of wenyang tongbi pills.
Wenyang Tongbi Pills;Paeoniflorin;Ephedrin Hydrochloride;TLC;HPLC
10.3969/j.issn.1672-5433.2015.05.007
2015-01-23)
谢强,男,副主任药师。主要从事药品质量研究工作。E-mail:xqmzmzb@21cn.net
王志梅,女,主管中药师。主要从事药品检验及质量标准研究工作。通讯作者E-mail:wangzhimei@gdda.gov.cn
