GC法测定盐酸乙胺丁醇原料中残留溶剂的含量
2014-07-07张立光
张立光,李 扬
(1.苏州卫生职业技术学院,江苏 苏州 215009;2.江苏省昆山市虹桥医院,江苏 昆山 215300)
GC法测定盐酸乙胺丁醇原料中残留溶剂的含量
张立光1,李 扬2
(1.苏州卫生职业技术学院,江苏 苏州 215009;2.江苏省昆山市虹桥医院,江苏 昆山 215300)
目的 建立测定盐酸乙胺丁醇原料中残留溶剂含量的方法。方法 气相色谱法与顶空进样法。色谱柱为 DB-624毛细管柱,柱温为50℃,进样口温度为150℃;检测器为FID,温度为200℃;载气为氮气,流速为32 KP;进样量100 μL。结果 结果表现出了良好的线性关系,甲醇、异丙醇、1,2-二氯乙烷、环己烷检测浓度线性范围分别为2.5~20 mg·L-1(r=0.998 5)、250~1 000 mg·L-1(r=0.998 1)、0.25~2 mg·L-1(r=0.995 3)、2.5~20 mg·L-1(r=0.996 2),平均回收率分别为101.54%、103.66%、103.07%、99.17%,RSD分别为2.1%、1.8%、4.4%、3.8%,最低检测限分别为0.5、25、0.05、0.5 mg· L-1。结论 建立的方法简便、灵敏、准确,适用于盐酸乙胺丁醇原料的残留溶剂含量的测定。
气相色谱法;盐酸乙胺丁醇;残留溶剂;顶空进样
The method is simple,sensitive and accurate,which is suitable for content determination of residual solvents in ethambutol hydrochloride.Key words:GC;ethambutol hydrochloride;residual solvents;headspace sample injection
结核病是一种古老的慢性传染病,它在全世界广泛流行,夺去了数亿人的生命。自 20世纪50年代以来,由于不断发现有效的抗结核药物,使结核病流行得到了一定的控制。盐酸乙胺丁醇是 R G Wikinson于 1962年在研究1,2-亚乙胺衍生物时发现的抗结核药物,现已成为一线四大抗结核药之一[1-3]。该药可渗入分枝杆菌体内干扰 RNA的合成,从而抑制细菌的繁殖,只对生长繁殖期的分枝杆菌有效,对结核杆菌有较强的抑制作用,但对其他细菌作用不明显,而且与其它抗结核药无交叉耐药性,长期服用可缓慢产生耐药性,广泛应用于治疗各型肺结核及肺外结核,其用量占市场份额的13%以上。该药单独使用时细菌可迅速产生耐药性,因此必须与其他抗结核药联合应用,用于曾接受抗结核药的患者时,应至少与一种以上药物合用,临床可用于对链霉素或异烟肼产生耐药的患者,其与利福平或异烟肼联用可增强疗效并延缓耐药性的产生。该药的合成过程中一般都使用甲醇、异丙醇、1,2-二氯乙烷与环己烷。药物中的残留溶剂系指在原料药或辅料的生产中,以及在制剂制备过程中使用或产生而又未能完全去除的有机溶剂。药品残留溶剂分析是当今药物分析的热点之一,已经成为药品质量控制的重要组成部分,是药品检验实验室的常规检测项目。根据国际化学品安全性纲要以及美国环境保护机构、世界卫生组织等公布的研究结果,很多有机溶剂对环境、人体都有一定的危害,因此,为保障药物的质量和用药安全,以及保护环境,需要对残留溶剂进行研究和控制。中国药典2010年版附录[4]中《残留溶剂测定法》和美国药典[5]中均规定了溶剂的类别和限度,各国药典收载的残留溶剂种类和限度是一致的,目前均遵守人用药物注册技术要求国际协调会议(ICH)指导原则。ICH根据危害程度对残留溶剂进行了系统分类,依据毒性的不同,将 69种残留溶剂分成了四类。第一类溶剂为人体致癌物、疑为人体致癌物或环境危害物,第二类溶剂为有非遗传致癌毒性或其他不可逆毒性、或其他严重的可逆毒性,第三类溶剂为对人体低毒,第四类溶剂为尚无足够毒理学资料的溶剂。查阅文献大都是盐酸乙胺丁醇含量测定的方法[6-11],国内未见有对盐酸乙胺丁醇残留溶剂的报道,世界各国药典均首选气相色谱法测定有机残留溶剂,但是具体在测定方法、色谱条件、供试品和对照品的制备、系统适用性方面有差别,参考ICH和《中国药典》的相关规定以及所查的相关文献[12-18],笔者建立了气相色谱法(GC)测定盐酸乙胺丁醇原料中的四种有机溶剂的残留量。
1 仪器与试药
GC-14C气相色谱仪(岛津公司)、氢火焰离子化检测器(FID)(岛津公司)、ClarityShimadzu色谱工作站(岛津公司)、DK-3001A顶空进样器(北京中兴分析仪器有限公司);BP121S分析天平(德国赛多利斯公司);KQ-100DB超声波清洗器(昆山市超声仪器有限公司)。
盐酸乙胺丁醇原料(印度卡迪拉制药有限公司,批号:201205056、201205057、201205058);1,2-二氯乙烷(天津市化学试剂厂 色谱纯);异丙醇(天津百世化工有限公司 色谱纯);甲醇(天津市四友精细化学品有限公司 色谱纯);环己烷(天津市博迪化工有限公司 色谱纯);超纯水。
2 方法与结果
2.1 溶液制备
2.1.1 对照品溶液 精密称定甲醇 0.1 g异丙醇10 g、1,2-二氯乙烷0.01 g、环己烷0.1 g,用水溶解并定容至 100 mL,分别取溶液 1 mL定容至 100 mL,超声5 min,冷却至室温。量取上述溶液5 mL,置顶空瓶中,密封,摇匀,作为对照品溶液。
2.1.2 供试品溶液 取供试品1.0 g,精密称定,置顶空瓶中,精密加入水5 mL,密封,摇匀,作为供试品溶液。
2.2 残留溶剂测定方法学的验证
2.2.1 色谱条件与系统适用性 色谱柱为 DB-624毛细管柱,柱温为50℃,进样口温度:150℃;检测器为 FID,温度为 200℃;载气为氮气,流速为 32 KP;进样方式为顶空进样,取2.1.1项下溶液70℃平衡30 min,进样100 μL。保留时间为1.16 min的色谱峰为甲醇峰,保留时间为1.72 min的色谱峰为异丙醇峰,保留时间为3.44 min的色谱峰为1,2-二氯乙烷峰,保留时间为3.56 min的色谱峰为环己烷峰。由色谱图看出,甲醇、异丙醇、1,2-二氯乙烷,环己烷得到良好的分离,分离度均大于1.5,理论塔板数大于5 000。
2.2.2 专属性 取空白溶剂水5 mL,量取2.1.1,2.1.2项下溶液于70℃加热30 min,分别进样100 μL。由色谱图(图1)可以看出,溶剂水不干扰测定,方法专属性良好。
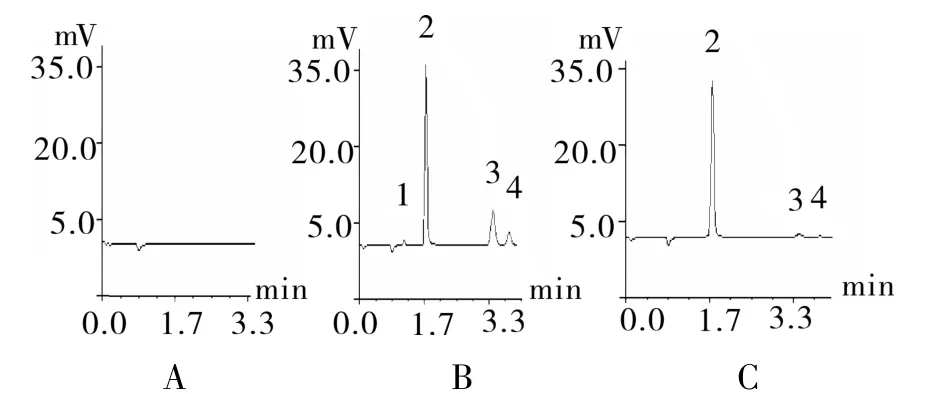
图1 气相色谱图
2.2.3 标准曲线及线性范围 精密称定甲醇 0.1 g、异丙醇10 g、1,2-二氯乙烷0.01 g、环己烷 0.1 g,用水溶解并定容至1 000 mL,超声5 min,冷却至室温,做为贮备液。分别量取上述溶液 2.5、5.0、10.0、15.0、20.0 mL,置于100 mL容量瓶中,用水定容至刻度,取5 mL置顶空瓶中,70℃加热30 min,进样100 μL。记录峰面积。以峰面积 A对浓度 C (mg·L-1)作图并进行线性回归。线性回归方程、线性范围及相关系数见表1。结果表明在各加入量范围内线性关系良好。

表1 各溶剂的回归方程、线性范围及相关系数(n=5)
2.2.4 日内精密度试验 取 2.1.1项下对照品溶液,70℃加热30 min,测定6次,记录峰面积,计算峰面积的RSD。甲醇、异丙醇、1,2-二氯乙烷、环己烷的6次测定的峰面积的RSD分别为2.1%、1.8%、4.4%、3.8%。
2.2.5 日间精密度试验 连续 6 d配制对照品溶液,70℃加热 30 min,测定,记录峰面积,计算峰面积的 RSD。甲醇、异丙醇、1,2-二氯乙烷、环己烷的6 d连续测定的峰面积的 RSD分别为 3.1%、4.8%、4.9%、4.8%。
2.2.6 溶液稳定性试验 取 2.1.1项下对照品溶液5份各5 mL,分别于 0、1、2、4、8 h 70℃加热 30 min,测定,记录峰面积,计算峰面积的 RSD。结果表明样品溶液在8 h内稳定。
2.2.7 检测限试验 取对照品溶液,逐级稀释得到系列浓度的溶液,按上述色谱条件和方法进样分析。当信噪比为 3∶1,确定为检测限。甲醇、异丙醇、1,2-二氯乙烷、环己烷的检测限分别为 0.5、25、0.05、0.5 mg·L-1。
2.2.8 定量限试验 取对照品溶液,逐级稀释得到系列浓度的溶液,按上述色谱条件和方法进样分析。当信噪比为10∶1,确定为定量限。甲醇、异丙醇、1,2-二氯乙烷、环己烷的检测限分别为2.0,100,0.2,2.0 mg·L-1。
2.2.9 加样回收率试验 取供试品(批号:201205056)1.0 g,分别加入相当于对照品溶液浓度80%,100%,120%的对照品溶液 b(每个质量浓度3份)5 mL,依法测定,每个浓度测定3次,根据峰面积计算回收率,结果见表2。
2.3 残留溶剂的含量测定结果 根据中国药典的规定并参考 ICH的规定,确定盐酸乙胺丁醇原料中甲醇的限度为0.005%,为第二类溶剂,异丙醇的限度为0.5%,为第三类溶剂,1,2-二氯甲烷的限度为0.000 5%,为第一类溶剂,环己烷的限度为0.05%,为第二类溶剂。按照上述经验证的方法考察了3批盐酸乙胺丁醇原料的残留溶剂,结果见表3。
3 讨论
GC法具有检测灵敏度高,选择性好的特点,采用此法需要的样品用量较少,基本可以满足所有残留溶剂测定的要求。GC法包括溶液直接进样和顶空进样两种进样方法。顶空色谱进样器可与国内外各种气相色谱仪相连接,它是将液体或固体样品中的挥发性组分直接导入气相色谱仪进行分离和检测的理想进样装置,使用顶空技术,可以免除冗长烦琐的样品前处理过程,避免有机溶剂带入的杂质对分析造成干扰,减少对色谱柱及进样口的污染。
顶空进样技术对溶液中的残留溶剂有富集作用,提高了对痕量有机溶剂的检测能力。美国药典对残留溶剂检测分为第一、二类残留溶剂和第三类残留溶剂 2种方法,其中第一、二类残留溶剂采用顶空进样技术,可以分为水溶性和水不溶性物质两种检测方法。

表3 盐酸乙胺丁醇原料中的残留溶剂含量测定结果(n=3)
GC法常用检测器有热导检测器、氢焰离子化检测器、电子捕获检测器和火焰光度检测器。火焰光度检测器主要检测含磷或含硫化合物,电子捕获检测器主要是目前分析痕量电负性有机化合物最有效的检测器。热导检测器具有结构简单,测定范围广,热稳定性好,线性范围宽,样品不易被破坏等优点,是一种通用型检测器,但灵敏度较低是其缺点。在用热导检测器时,选氢气为载气,可获得较高的检测灵敏度,但是不安全,氦气较理想,但是价格较贵。氢焰离子化检测器具有灵敏度高、响应快,线性范围宽等优点,是目前最常用的检测器之一,一般用于测定含碳有机物。因此,在本实验中采用氢焰离子化检测器。
顶空时间要确保供试品溶液的气—液达到平衡,顶空时间不宜过长,一般为 30~45 min。如果时间过长,可能引起顶空瓶的气密性变差,导致定量的准确性降低,如果时间不够,那么就不能保证气—液两相达到平衡。对照品溶液与供试品溶液必须使用相同的顶空条件。笔者前期试验中取对照溶液3份,分别在60、70、80℃下加热平衡30 min后进样测定。结果表明,平衡温度在 70℃重复性较好。另取混合对照溶液 3份,分别在 70℃加热20、30、40 min后进样测定,结果在平衡30 min时测得4种溶剂的峰面积重复性较好。故选择加热温度70℃,平衡时间30 min。
气相色谱柱的分离效果主要取决于其固定相,柱长度,柱内径,液膜厚度这几个因素,柱径直接影响柱子的效率、保留特性和样品容量。小口径柱比大口径柱有更高柱效,但柱容量更小。液膜厚度影响柱子的保留特性和柱容量。厚度增加,保留也增加。不同的固定相对不同的分析物的影响不同,根据相似相溶原理,性质越相近,固定相对其的流动阻力越大,其保留时间越长.笔者前期试验中曾选用不同极性的毛细管色谱柱,如聚乙二醇 20000、HP-FFAP(键合和改性的交联聚乙二醇)和 DB-624色谱柱,经多次试验,发现前二者的分离效果都不如 DB-624色谱柱,最后选择了 DB-624色谱柱。本试验测定结果表明,盐酸乙胺丁醇原料中 4种有机溶剂的量均符合相关规定,各峰间达到良好的分离。本方法操作简单、准确、可靠、灵敏度高,能达到残留溶剂的检测要求,可用于盐酸乙胺丁醇原料中残留溶剂的检测。
因为某一具体品种各生产企业引入的溶剂亦有不同而难以统一规定,残留溶剂检查统一在凡例中进行要求,即凡在原料和制剂生产中引入有机溶剂而需要去除者,均应符合《中国药典》2010年版附录(ⅧP)项下有关的各项规定。而美国药典有机残留溶剂的检查项下,使用一、二、三类有机溶剂的混合对照品,可以科学的测出样品中的未知有机溶剂,这就提示我们如果在药品的残留溶剂的研究检测中无法确定整个生产中都使用了哪些溶剂,我们可以参考美国药典,对残留溶剂进行预测,在方法开发时我们也可以借鉴。
[1] Jonsson S,Davidse A,Wilkins J,et al.Population Pharmacokinetics of Ethambutol in South African Tuberculosis Patients[J].Antimicrob[J].Agents Chemother,2011,55(9):4230-4237.
[2] Lacoma A,Garcla-Sierra N,Prat C,et,al.GenoType MTBDRsl for Molecular Detection of Second-Line-Drug and Ethambutol Resistance in Mycobacterium tuberculosis Strains and Clinical Samples [J].Journal of Clinical Microbiology,2012,50(1):30-36.
[3] Lakshmanan D,Werngren J,Jose L,et al.Ethyl p-methoxycinnamate isolated from a traditional anti-tuberculosis medicinal herb inhibits drug resistant strains of Mycobacterium tuberculosis in vitro[J].Fitoterapia,2011,82(5):757-761.
[4] 国家药典委员会.中国药典:二部[S].北京:中国医药科技出版社,2010:1317.
[5] The United States Pharmacopeial Convention,Inc.The United States Pharmacopeia[S].36th edi.Rochville MD:the United States Pharmacopeial Convention,Inc.,2012:467.
[6] 都小红.吡嗪酰胺和乙胺丁醇在结核性脑膜炎治疗中的效果对比分析[J].工业医刊,2013(4):300-301.
[7] 汤兴球,王伍承.HPLC-ELSD法同时测定烟肼丁醇片中盐酸乙胺丁醇和异烟肼的含量[J].安徽医药,2012(5):616-617.
[8] 吴春生.高效液相色谱-蒸发光散射检测器法同时测定烟肼丁醇片中盐酸乙胺丁醇和异烟肼含量[J].中国药业,2013,19:38-40.
[9] 董进臣,陈瑞敏.HPLC-RID法测定盐酸乙胺丁醇胶囊的含量[J].煤炭与化工,2013,06:142-143,150.
[10]王 冬,张 瑜.HPLC测定盐酸乙胺丁醇有关物质[J].药物分析杂志,2012,2:282-284.
[11]颜 鸣,隋 因,郭 涛,赵庆春.高效液相荧光法测定乙胺吡嗪利福异烟片中盐酸乙胺丁醇的含量[J].中国药师,2010,1:83-85.
[12]吴春丽,张俊霞,史云涛,等.顶空毛细管气相色谱法测定来曲唑原料药中有机溶剂残留量[J].中国药房,2010,21(17):1601.
[13]赵佳丽,章展煌,徐宏祥.顶空毛细管气相色谱内标法测定倍他米松磷酸钠中的 3种残留溶剂[J].中国药房,2010,21 (21):1999.
[14]叶海青,傅应华.毛细管气相色谱法测定丙酸倍氯米松中3种有机溶剂残留量[J].中国药房,2010,21(13):1235.
[15]宋 莉,黄 艳,刘雪峰.气相色谱法同时测定黑豆馏油软膏中桉油精和冰片的含量[J].安徽医药,2013,17(6):958-959.
[16]韩 薇,赵云丽,燕强勇,等.顶空气相色谱法测定埃索美拉唑钠中溶剂残留量[J].沈阳药科大学学报,2012,29(4):276-279.
[17]宋更申,姜建国,付 焱,等.顶空毛细管气相色谱法测定盐酸莫雷西嗪中残留溶剂的含量[J].沈阳药科大学学报,2011,28 (1):51-54.
[18]Wu G,Bao XX,Zhao SH,et al.Analysis of multi-pesticide residues in the foods of animal origin by GC-MS coupled with accelerated solvent extraction and gel permeation chromatography cleanup [J].Food Chemistry,2011,126(2):646-654.
Determination of residual solvents in material drug of ethambutol hydrochloride by gas chromatography
ZHANG Li-guang1,LI Yang2
(1.Suzhou Health College,Suzhou,Jiangsu 215009,China;2.Hongqiao Hospital,Kunshan,Jiangsu 215300,China)
Objective To establish a GC method for the determination of residual solvents in material drug of ethambutol hydrochloride.Methods GC and headspace sample injection method were adopted.The determination was performed with a DB-624 capillary column (column temperature was 50℃)using nitrogen gas as carrier gas at the flow rate of 32 KP and FID as detector.The injector temperature and detector temperature were controlled at 150℃ and 200℃,respectively.The sample volume was 100 μL.Results The results showed excellent linearity.The linear ranges of residual solvents of methanol,isopropanol,1,2-dichoroethane and cyclohexane were 2.5~20 mg·L-1(r=0.998 5),250~1 000 mg·L-1(r=0.998 1),0.25~2 mg·L-1(r=0.995 3),2.5~20 mg·L-1(r=0.996 2),respectively.And their recoveries were 101.54%,103.66%,103.07%and 99.17%,respectively.RSDs were 2.1%,1.8%,4.4%and 3.8%,respectively.The minimum detection limits were 0.5,25,0.05 and 0.5 mg·L-1,respectively.Conclusions
10.3969/j.issn.1009-6469.2014.05.013
2013-10-28,
2014-01-06)
