三取代钨硅酸二聚体有机-无机杂化化合物的合成与结构
2014-06-27刘洪波张春晶陈亚光
刘洪波,张春晶,陈亚光
(1.东北师范大学化学学院,多酸科学教育部重点实验室,吉林长春130024;2.长春医学高等专科学校药学系,吉林长春130031;
3.黑龙江中医药大学,黑龙江哈尔滨150040)
三取代钨硅酸二聚体有机-无机杂化化合物的合成与结构
刘洪波1,2,张春晶1,3,陈亚光1
(1.东北师范大学化学学院,多酸科学教育部重点实验室,吉林长春130024;2.长春医学高等专科学校药学系,吉林长春130031;
3.黑龙江中医药大学,黑龙江哈尔滨150040)
合成了2种三取代Keggin结构钨硅酸盐的无机-有机杂化化合物[Na3CuL6(H2O)6][(H3SiW9Fe3(OH)3O34)2(μ-OH)3]·21H2O(1)和(Him)6[Na2(H2O)2{SiW9Al3(OH)3(H2O)2O33(μ3-O2/2)}2]·14H2O(2)(L=6-氨基己酸,im=咪唑).采用X射线单晶衍射法测定了其结构.在化合物1中,2个三取代杂多阴离子SiW9Fe3(OH2)3O10-37缩去3个水分子、共用3个氧原子(Fe—O—Fe)形成二聚杂多阴离子.通过配离子、二聚阴离子和结晶水分子之间的氢键将其连接成晶体.在化合物2中,2个三取代杂多阴离子SiW9Al3(OH2)3O10-37共用AlO6八面体的一个边形成二聚杂多阴离子.钠离子接受2个二聚体的配位形成一维链结构.
无机-有机杂化化合物;二聚三取代钨硅酸盐;取代Keggin阴离子;晶体结构
多金属氧酸盐是一类以Mo,W和V为主要组成元素、具有多种结构类型的高相对分子质量化合物[1].由于这类化合物中的Mo,W和V元素通常处在最高氧化数区,且组成和酸度可调,多金属氧酸盐在催化、药物、材料等方面具有广阔的应用前景[2].向多金属氧酸盐体系中引入有机基团可以使其性质得到改善,即同时表现无机和有机化合物的性质.由于多金属氧酸盐的有机衍生物对有机物质的亲和力增加,因此它在有机溶剂中的溶解性增加.这些性质的改变有利于多金属氧酸盐在催化、医药领域的应用.Dolbecq等人概述了近10年来在这方面的研究进展[3].
自Keggin在1933年用X射线衍射法确定了H3PW12O40·5H2O的结构以来[4],对含有以其名字命名的结构(Keggin结构,XM12On-40,X=P,As,Si,Ge等,M=Mo,W)的杂多化合物的研究在全世界引起广泛关注[5].在溶液中,随溶液的pH值升高,Keggin结构阴离子XM12On-40进行逐级降解反应,生成单空缺杂多阴离子XM11On-39、双空缺杂多阴离子XM10On-37和三空缺杂多阴离子XM9On-34.在溶液的pH值升高到9以上时,降解为简单含氧酸根离子XOn-4和MOn-4[1].空缺杂多阴离子具有较高的负电荷,因此它们具有较高的反应活性.当体系中存在半径适宜的金属离子时,在一定条件下可以生成各类衍生物.以三空缺杂多阴离子为例,3个金属离子进入空缺阴离子的空缺位置,形成3个金属原子取代的Keggin型杂多化合物.已见报道的化合物有XW9M′3On-40,X=Si,P,Ge;M′=Ti,V,Mo或XW9M′3(H2O)3On-37,M′=Al,Ga,In,Fe,Co,Ni,Mn,Cu,Cr[6].在一定条件下2个三取代阴离子通过共用氧原子形成二聚体此类化合物报道得很少[7].空缺杂多阴离子从两侧对3个金属离子进行配位形成三金属夹心型衍生物.例如Si2W18Zr3[8]和(LnO)3(PW9O34)n2-(Ln为镧系元素)[9].3个金属离子位于一个平面,是整个阴离子的对称面.2个三缺位阴离子从两侧向处在一个平面上的4个金属离子配位则形成M4(H2O)2(XW9O34)2[10](Weakley型夹心化合物).在这类化合物中,金属离子保留2个配位水分子,这2个水分子可以被其他分子取代.当取代的分子是有机化合物时,则生成有机-无机杂化化合物.
由于取代型和夹心型杂多化合物中含有多个过渡金属离子,在磁性研究方面它们是很好的模型化合物[11],也表现明显的催化活性[12].因此,对这类化合物的研究即具有一定理论意义,也可以为催化材料的研究和应用提供物质源.本文合成了2种新的含取代杂多阴离子的化合物1和化合物2.
1 实验部分
1.1 试剂和仪器
试剂:化学试剂均为分析纯,使用前没有进一步纯化;实验中所用的水为蒸馏水;按文献方法[6d,6f]合成α-Na7[SiW9Fe3(H2O)3O37]·xH2O和α-Na7[SiW9Al3(H2O)3O37]·xH2O.
仪器:C,H和N的元素分析采用Perkin-Elmer 2400CHN元素分析仪进行;红外光谱在Alpha Centauri FT/IR红外光谱仪测定,测定范围400~4 000cm-1,KBr压片;单晶X射线衍射实验使用日本理学R-RAXIS型面探(IP)单晶衍射仪.
1.2 化合物的合成
(1)化合物1的合成
将α-Na7[SiW9Fe3(H2O)3O37]·xH2O,Cu(Ac)2·6H2O和6-氨基己酸(C6H13NO2,L)以物质的量的比为1∶2∶5的比例溶于水.用HCl调节所得溶液的pH至3.2,然后将溶液加热至80℃,搅拌30min.冷却后过滤除去少量不溶物.所得溶液在室温蒸发,15d后析出绿色块状晶体.产率为36%(按W计算).元素分析(单位为质量分数/%,括号内为理论值):C 6.86(3.95),H 1.06(1.17),N 1.48(1.36).
(2)化合物2的合成
将α-Na7[SiW9Al3(H2O)3O37]·xH2O,Cu(Ac)2·6H2O和咪唑(C3H4N2,im)以物质的量的比为1∶2∶5的比例溶于水.用HCl调节所得溶液的pH至3.2,然后将溶液加热至80℃搅拌30min.冷却至室温,滤去少量不溶物.将所得溶液在室温静止蒸发,10d后析出无色块状晶体.产率为31%(按W计算).元素分析(单位为质量分数/%,括号内为理论值):C 3.86(3.95),H 0.56(0.44),N 3.18(3.07).
1.3 晶体结构的测定
选取大小适宜的单晶,在293K下利用石墨-单色Mo-Kα射线(λ=0.071 073nm)、用Oscillation scans技术在一定的θ范围内收集衍射数据,并应用经验吸收法进行校正.化合物1和2的晶体结构均采用SHELXTL-97程序以直接法解析[13],用全矩阵最小二乘法修正.对所有非氢原子进行了各向异性修正.采用理论加氢的方式得到与碳结合的氢原子的位置.化合物1和2的晶体学数据及精修结果列于表1.
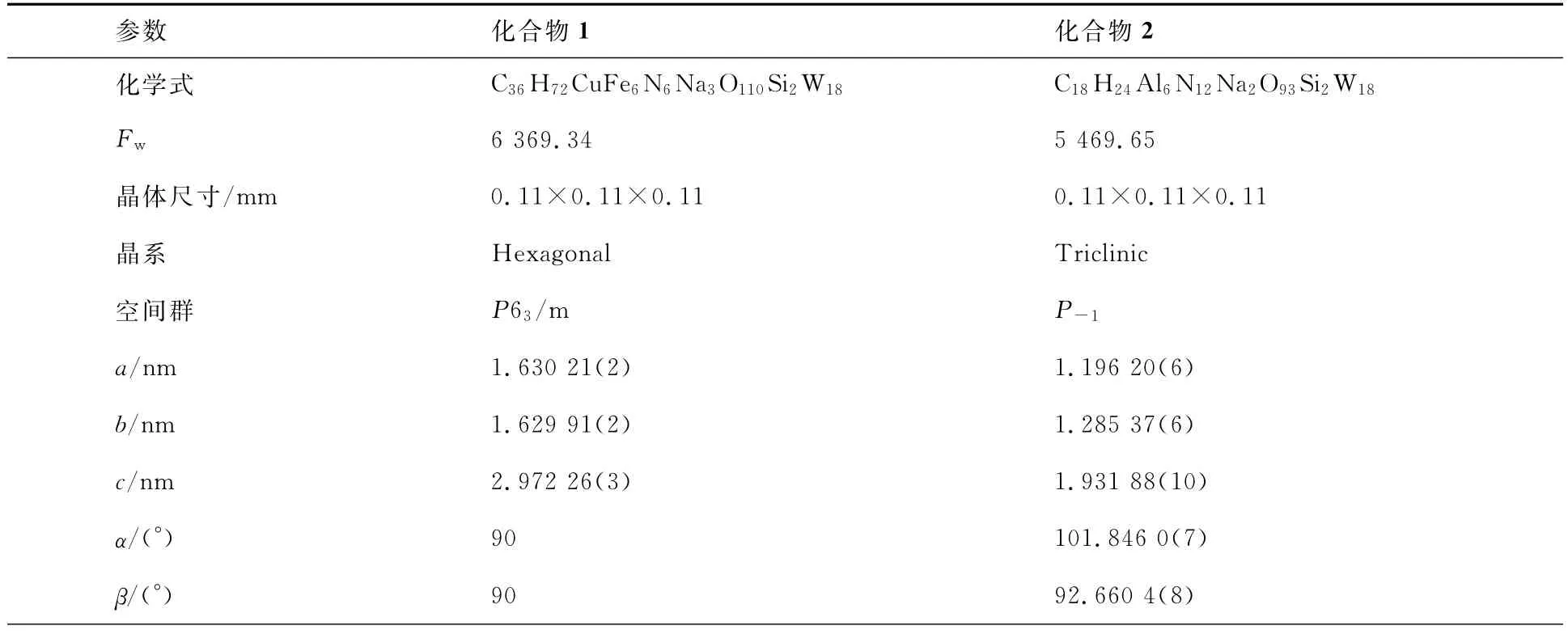
表1 化合物1和2的晶体学数据和精修数据
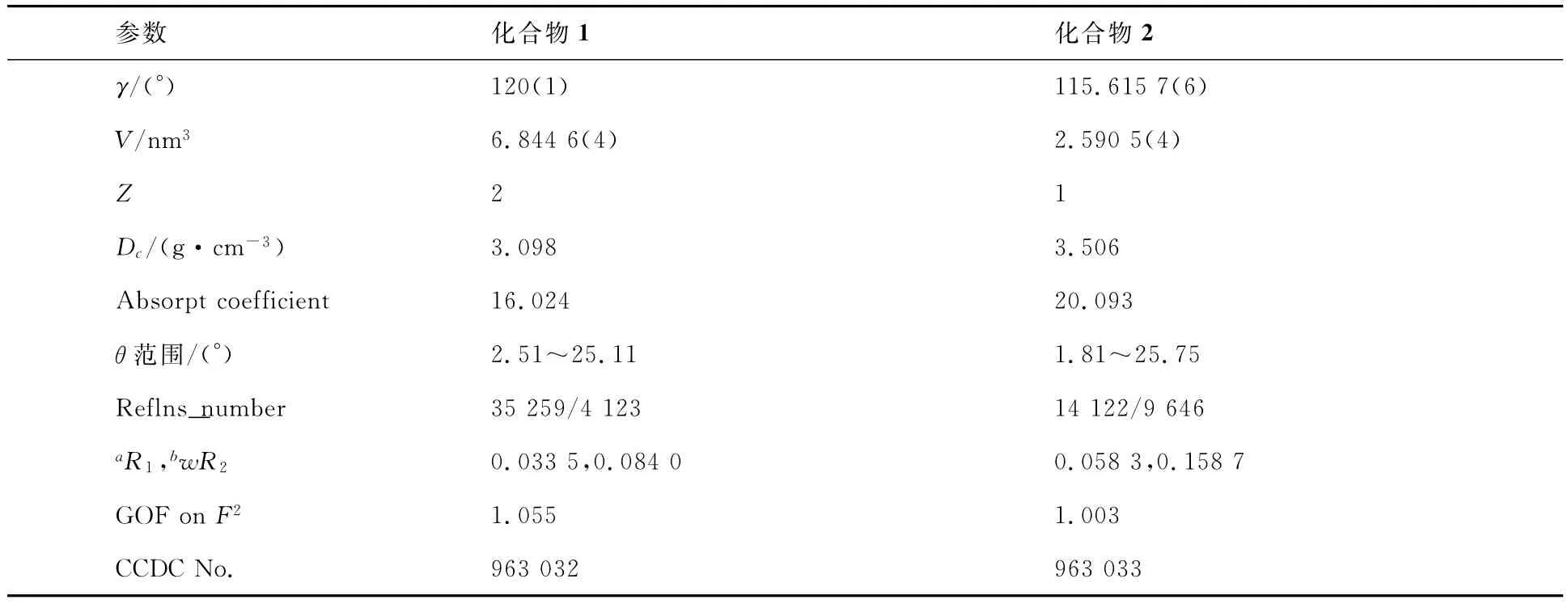
续表1
2 结果和讨论
2.1 化合物的晶体结构
2.1.1 化合物1的晶体结构
X射线单晶衍射分析结果表明,化合物1由一个[(H3SiW9Fe3(OH)3O34)2(μ-OH)3]5-二聚体(见图1a)和一个[Na3CuL6(H2O)6]5+配离子(见图1b)及结晶水构成.在[SiW9Fe3(OH)3O34]单元中,W原子分为4组,1组为3个WO6八面体共边相连并共用1个氧原子形成的W3O13次单元;另外的三组可以看成是从W3O13次单元移除1个W原子和3个氧原子而形成的W2O10次单元.在这些次单元之间,WO6八面体共角相连,构成1个A-型三空缺阴离子SiW9O34.3个Fe(OH)3O3八面体与W2O10次单元的WO6八面体共边相连,3个Fe(OH)3O3八面体彼此共角相连填充在空缺位置,即取代了原来以共角相连的3个WO6八面体,得到[SiFe3W9(OH)3O34]单元.2个[SiFe3W9(OH)3O34]单元通过3个Fe—μ-OH—Fe键连接形成[(SiW9Fe3(OH)3O34)2(μ-OH)3]二聚体.[(SiW9Fe3(OH)3O34)2(μ-OH)3]二聚体属于D3h点群对称性.
价键和计算[14]表明Fe1的氧化态是3.03,这与文献[6f]相吻合.价键计算也表明[SiFe3W9(OH)3O34]单元内以及单元之间的连接2个FeⅢ原子的氧原子的价键和为1.09(见表2),这说明这6个氧原子是质子化的.
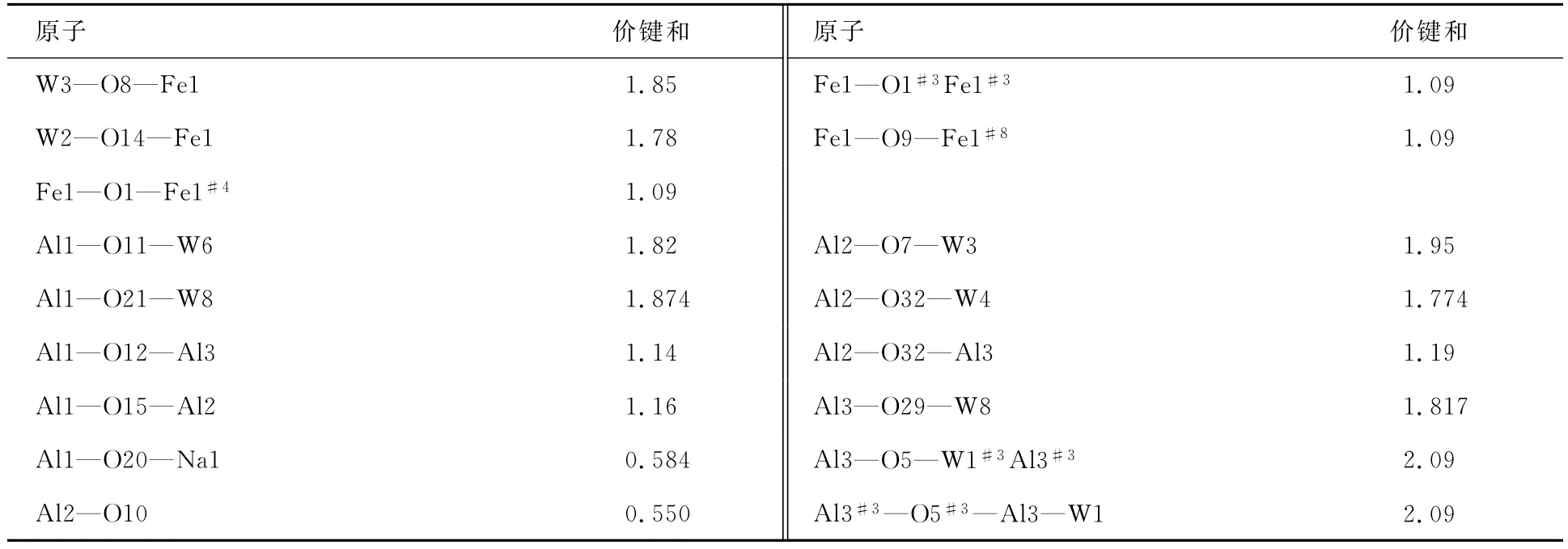
表2 化合物1和2中Fe原子和Al原子周围桥氧原子和端氧原子的价健和
在化合物1中,有一个晶体学独立的Cu2+和3个Na+.Cu2+位于3个Na+构成的平面三角形的中心,L配体采用螯合-桥连配位模式用羧基将Cu2+和2个Na+链接起来形成“双喇叭”型[CuL6Na3(H2O)6]5+配离子,Cu2+和Na+均位于由O原子构成的八面体中心.
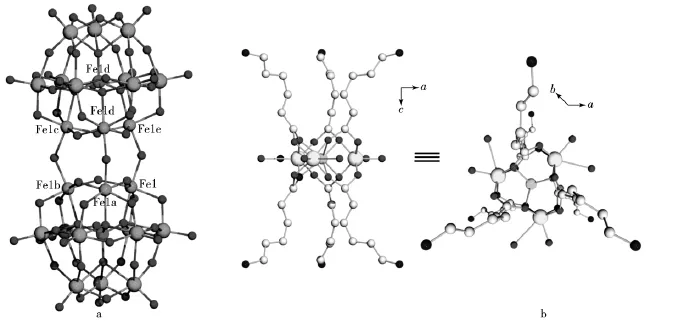
图1 化合物1中[(SiW9Fe3(OH)3O37)2(μ-OH)3]5-(a)和[Na3CuL6(H2O)6]5+(b)的球棍图
[Na3CuL6(H2O)6]5+配离子与[(H3SiW9Fe3(OH)3O34)2(μ-OH)3]5-二聚体的长轴与晶轴c平行.晶轴c方向上相邻的配离子交错排列.从晶轴c方向看到的配离子和二聚体的堆积见图2.化合物1中存在大量的水分子及质子化的氨基,氢键在氨基和二聚体之间(NH…O(POM)dN—O=0.289 5~0.308 9nm)、晶格水和二聚体之间(HOH…O(POM)dO—Oof 0.307 5nm)以及晶格水分子之间(HOH…O(H2O)dO—Oof 0.299 7nm)生成.
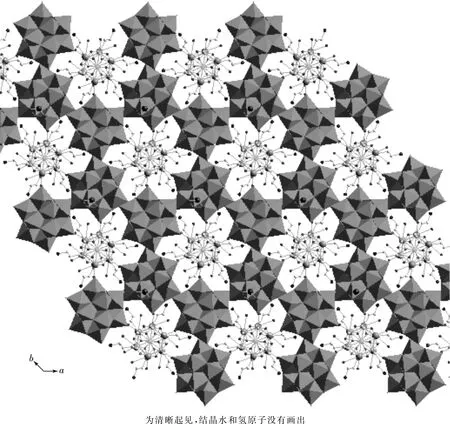
图2 化合物1的堆积图
2.1.2 化合物2的晶体结构
X射线单晶衍射分析结果表明,化合物2是由一个[SiW9Al3(H2O)2(OH)3O34(μ3-O2/2)]8-2双聚体、2个钠原子、6个咪唑分子和结晶水分子构成.
[SiW9Al3(HO)3(H2O)2O33(μ3-O2/2)双聚体是由2个[SiW9Al3(HO)3(H2O)2O33(μ3-O2/2)]4-单元通过共用AlO6八面体的一个边[O5—O5a]形成的.O5a是由O5通过倒反中心(1,0.5,0.5)对称操作产生的.[α-SiW9Al3(HO)3(H2O)2O33(μ3-O2/2)]4-单元是由一个中心四面体SiO4,一个W3O13次单元,2个W2Al(H2O)(HO)O11次单元,一个W2Al(HO)O12次单元通过共边和共角组成的.
在化合物2中,存在一个晶体学上独立的Na离子(Na1).这个Na+被来自2个[SiW9Al3(HO)3(H2O)2O33(μ3-O2/2)双聚体的2个氧原子和1个水分子及另一个水分子配位,呈现扭曲的四面体配位几何构型.Na—O的键长范围为0.262 9~0.285 7nm.每个[SiW9Al3(HO)3(H2O)2O33(μ3-O2/2)双聚体从两侧连接4个Na1,同时每个Na1原子连接2个[SiW9Al3(HO)3(H2O)2O33(μ3-O2/2)]82-双聚体,形成沿a轴方向伸展的一维链状结构(见图3).
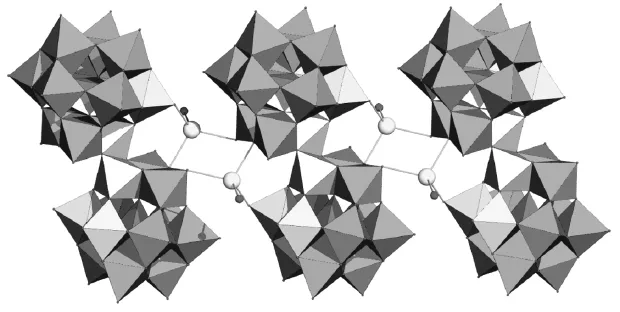
图3 化合物2中的一维链结构
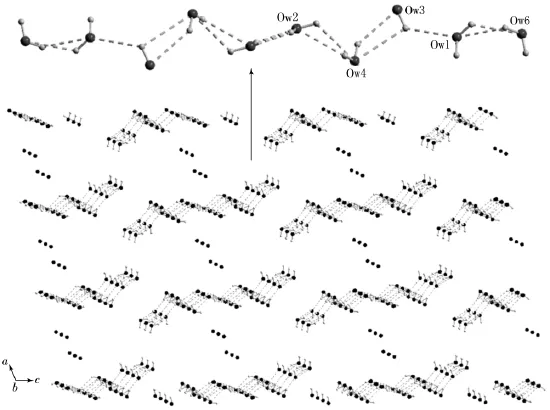
图4 化合物2中的十水分子链和在晶体中的堆积
在图2中,结晶水分子彼此之间通过氢键形成水链Ow6—Ow1—Ow3—Ow4—Ow2—Ow2′—Ow4′—Ow3′—Ow1′—Ow6′,O…O距离在0.268 7~0.282 8nm范围内(见图4).除Ow2外,每个水分子与双聚体通过氢键相连:Ow5—Hw5B…O10键长为0.276 0nm;Ow5—Hw5C…O1w键长为0.291 0nm;O1w—H1wA…O28[x+1,y,z]键长为0.295 0nm;O15—H15B…O4w键长为0.300 5nm;O19—H19B…O6w键长为0.297 7nm;O20—H20B…O36[x+1,y,z]键长为0.270 2nm).质子化的咪唑分子阳离子也通过氢键与2个链上的二聚体相连:O20—H20A…N6[-x+2,-y+1,-z+1]键长为0.307 3nm;N1—H1A…O34[-x+1,-y+1,-z]键长为0.294 3nm;N2—H2B…O7w键长为0.289 1nm;N3—H3D…O30键长为0.291 0nm;N4—H4B…O38键长为0.277 9nm;N5—H5B…O32[-x+1,-y,-z+1]键长为0.270 8nm;N6—H6B…O11[-x+2,-y+1,-z+1]键长为0.281 6nm.阴离子链及咪唑的堆积见图5.
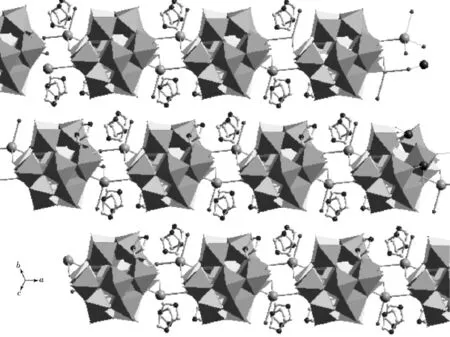
图5 化合物2中阴离子链及咪唑的堆积图
2.2 红外光谱
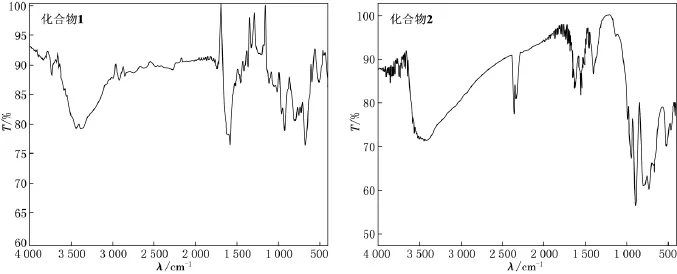
图6 化合物1和2的红外光谱
化合物1和2的红外光谱见图6.红外光谱的振动吸收峰由三部分组成.在500~1 000cm-1范围内的吸收峰由多金属氧酸盐阴离子产生.分别指认为W—Ot,W—Ob/c—W,Si—O键的振动吸收[6e,6f].在1 200~1 700cm-1范围的吸收峰有有机组分产生,包括C—N,C—O,═C O键的振动吸收.在2 800~3 000cm-1出现吸收峰表明CH2基团的存在.位于3 400cm-1附近的宽峰是水分子以及氢键的OH振动吸收.
3 结论
用常温水溶液合成法制得化合物1和2.在相同的实验条件下(反应温度、时间、pH),2个三取代Keggin阴离子形成2种不同结构的二聚阴离子,其主要原因是2个取代金属离子的性质不同.半径小的Al3+(51pm)形成共用边的二聚体(dAl—Al=0.289 6nm),而半径稍大的Fe3+(64pm)形成共用角的二聚体(dFe—Fe=0.360 5nm).
[1] POPE M T,Heteropoly and isopoly oxometalates[M].Berlin:Springer-Verlag,1983:1-10.
[2] (a)RHULE J T,HILL C L,JUDD D A.Polyoxometalates in medicine[J].Chem Rev 1998,98:327-357;(b)PROUST A,THOUVENOT R,GOUZERH P.Functionalization of polyoxometalates:towards advanced applications in catalysis and materials science[J].Chem Commun,2008:1837-1852.
[3] DOLBECQ A,DUAS E,MAYER,C R.Hybrid organic-inorganic polyoxometalate compounds:from structural diversity to application[J].Chem Rev,2010,110:6009-6048.
[4] KEGGIN J F.Structure of the molecule of 12-Phosphotungstic Acid[J].Nature 1933,131:908-909.
[5] LONG D-L,TSUNASHIMA R,ND LEROY CRONIN L.Polyoxometalates:building blocks for functional nanoscale systems[J].Angew Chem Int Ed,2010,49:1736-1758.
[6] (a)TEZÉA,HERVÉG.Relationship between structures and properties of undecatungstosilicate isomers and of some derived compounds[J].J Inorg Nucl Chem,1977,39:2151-2158;(b)FINKE R G,RAPKO B,SAXTON R J,et al.Trisubstituted heteropolytungstates as soluble metal oxide analogs.Ⅲ.synthesis,characterization,phosphorus-31,silicon-29,vanadium-51,and 1-and 2-D tungsten-183NMR,deprotonation,and proton mobility studies of organic solvent solute forms ofJ Am Chem Soc,1986,108:2947-2960;(c)ZONNEVIJLLE F,TOURNE C M, TOURNE G F.Preparation and characterization of heteropolytungstates containing group 3Aelements[J].Inorg Chem,1982,21:2742-2750;(d)QU L,ZHANG B,PENG J and LIU J.α-andβ-Tri-ferricononatungstosilicate isomers[J].Trans Met Chem,1988,13;183-186;(e)CHEN Y-G,QU L,PENG J,YU M.Synthesis and structure of potassiumα-andβtrivanadoenneatungstogermanates[J].Chem Res Chin Univ,1993,9:6-11;(f)CHEN Y-G,QU L,PENG J.Synthesis and properties of trialuminoenneatungstosilicate isomers[J].Acta Chimica Sinica,1991,49:889-893.
[7] (a)FINKE R G,DROEGE M W.Trisubstituted heteropolytungstates as soluble metal oxide analogs.1.The preparation,characterization,and reactions of organic solvent soluble forms of the silicon-niobium heteropolytungstates Si2W18Nb6,SiW9Nb3and the SiW9Nb3?supported organometallic complexC5Me5Rh.cntdot.SiW9Nb3O405-J.J Am Chem Soc,1984,106:7274-7481;(b)CHEN Y-G,QU L,PENG J,YU M.Structure of trisubstitutedtungstosilicate anion[A-β-SiW9Al3(H2O)2O36(μ3-O2/2[J].Chinese J Struct Chem,1993,12:338-343;(c)YAMSE T,OZEKI T,SAKAMOTO H.Structure of Hexatitanooctadecatungstodigermanate[J].Bull Chem Soc Jpn,1993,66:103-108;(d)WASSERMANN K,PALM R,LUNK H-J.Condensation of Keggin Anions Containing Chromium(Ⅲ)and Aluminum(Ⅲ),Respectively.1.synthesis and X-ray structural determination of[{A-.alpha.-SiO4W9O30(OH)3Cr3}2(OH)3]11-[J].Inorg Chem,1995,34:5029-5035;(e)ANDERSON T M,NEIWERT W A,HARDCASTLE K I,HILL C L.Multi-iron silicotungstates:synthesis,characterization and stability of polyoxometalate dimmers[J].Inorg Chem,2004,43:7353-7358;(f)BI L H,KORTZ U,NELLUATLA S.Structure,electrochemistry,and magnetism of the iron(Ⅲ)-substituted Keggin dimer,[Fe6(OH)3(A-GeW9O34(OH)3)2]11-[J].Inorg Chem,2005,44:896-903.
[8] (a)KNOTH W H,DOMAILLE P J,HARLOW R L.Heteropolyanions of the types M3(W9PO34)122-and MM′M″(W9PO34)122-:novel coordination of nitrate and nitrite[J].Inorg Chem,1986,25:1577-1582;(b)FINKE R G,RAPKO B,WEAKLEY T J R.Polyoxoanions derived from tungstosilicate,A-beta-SiW9:synthesis and crystallographic and tungsten-183NMR characterization of Si2W18Zr3O71,including its organic solvent soluble Bu4N+salt[J].Inorg Chem,1989,28:1573-1579;(c)LIN Y,WEAKLEY T J R,RAPKO B,et al.Polyoxoanions derived from tungstosilicate(A-beta-SiW9):synthesis,single-crystal structural determination,and solution structural characterization by tungsten-183NMR and IR of titanotungstosilicate(A-beta-Si2W18Ti6)[J].Inorg Chem,1993,32:5095-5101.
[9] (a)KNOTH W H,DOMAILLE P J,FARLEE R D.Anions of the type(RMOH2)3W18P2and[H2OCo]3W18P2O1628-.a reinvestigation of“B,.beta.-W9P”[J].Organometallics,1985,4:62-67;(b)CRACIUN C,DAVID L.Spectroscopic andmagnetic investigation of one sandwich-type uranium(Ⅳ)polyoxometalate with Ge(Ⅳ)as heteroatom[J].J Alloys Comp,2001,323-324:743-747.
[10] (a)WEAKLEY T J R,EVANS H T JR,SHOWELL J S,et al.18-Tungstotetracobalto(Ⅱ)diphosphate and related anions:a novel structural class of heteropolyanions[J].J Chem Soc Chem Commun,1973:139-140;(b)FINKE R G,DROEGE M,HUTCHINSON J R,et al.Trivacant heteropolytungstate derivatives:the rational synthesis,characterization,and tungsten-183 NMR spectra of P2W18M4(H2O)2O10-68(M=cobalt,copper,zinc)[J].J Am Chem Soc,1981,103:1587-1589;(c)KORTZ U,NELLUTLA,S,STOWE,A C.Sandwich-type germanotungstates:structure and magnetic properties of the dimeric polyoxoanions[M4(H2O)2(GeW9O34)2]12-(M2+=Mn,Cu,Zn,Cd)[J].Inorg Chem,2004,43(7):2308-2317;(d)ZHANG Z M,WANG E B,LI Y G.Synthesis,characterization,and crystal structures of two 6-cobalt-containing dimeric polyoxoanions:[Co2(H2O)10Co4(H2O)2(B-a-XW9O34)2]8-(X=Ge and Si)[J].J Mol Struct,2008,872:176-181.
[11] (a)CASAII-PASTOR N,BAS-SERRA J,CORONADO E,et al.First ferromagnetic interaction in a heteropoly complex:Experiment and theory for intramolecular anisotropic exchange involving the Four Co(Ⅱ)Atoms[J].J Am Chem Soc,1992,114,10380-10383;(b)KORTZ U,NELLUTLA S STOWE A C,et al.Structure and magnetism of the tetra-copper(Ⅱ)-substituted heteropolyanion[Cu4K2(H2O)8(α-AsW9O33)2]8-[J].Inorg Chem,2004,43:144-151;(c)CLEMENTE-JUAN J M,CORONADO E.Magnetic clusters from polyoxometalate complexes[J].Coord Chem Rev,1999,193-195:361-394.
[12] MBOMEKALLE I M,KEITA B,NIERLICH M,et al.Structure,magnetism,and electrochemistry of the multinickel polyoxoanions[Ni6As3W24O94(H2O)2]17-,[Ni3Na(H2O)2(AsW9O34)2]11-,and[Ni4Mn2P3W24O94(H2O)2]17-[J].Inorg Chem,2003,42:5143-5148.
[13] SHELDRICK G M,SHELXS97.Program for crystal structure solution[CP].Göttingen:University of Göttingen,1997.
[14] BROWN I D.The chemical bond in inorganic chemistry:the bond valence model[M].London:Oxford University Press,2002:292.
Synthesis and structure of two organic-inorganic hybrids of tri-substituted tungstosilicate dimmer
LIU Hong-bo1,2,ZHANG Chun-jing1,3,CHEN Ya-guang1
(1.Key Laboratory of Polyoxometalates Science of Ministry of Education,Faculty of Chemistry,Northeast Normal University,Changchun 130024,China;2.Department of Pharmaceutics,Changchun Medical College,Changchun 130031,China;3.Heilongjiang University of Chinese Medicine,Harbin 150040,China)
Two inorganic-organic hybrids containing dimeric tri-substituted Keggin anion,[Na3CuL6(H2O)6][(H3SiW9Fe3(OH)3O34)2(μ-OH)3]·21H2O(1)and(Him)6[Na2(H2O)2{SiW9Al3(OH)3(H2O)2O33(μ3-O2/2)}2]·14H2O(2)were prepared in conventional method and their structures were determined by single-crystal X-ray diffraction technique.In 1 two tri-substituted Keggin anions SiW9Fe3underwent a condensation process forming the dimeric anion having three Fe—O—Fe bridging bonds and hydrogen bonds fuse the anions and complex cations into three dimensional architecture.In 2 two tri-substituted Keggin anions SiW9Al3share an edge of octahedra forming the dimeric anion.The property of substituted metal ions leads to different dimeric forms.
inorganic-organic hybrid;dimeric tri-substituted tungstosilicate;Keggin anion;crystal structure
O 61 [学科代码] 150·10
A
(责任编辑:石绍庆)
1000-1832(2014)02-0078-08
10.11672/dbsdzk2014-02-016
2013-10-22
吉林省自然科学基金资助项目(201115002).
刘洪波(1967—),女,硕士,副教授;通讯作者:陈亚光(1955—),女,教授,主要从事多酸化学研究.
