烟酰胺磷酸核糖基转移酶在乳腺癌中的表达及临床意义
2014-04-08毕铁强梁文学李淑琴高希涛王培顺
毕铁强,周 军,梁文学,刘 毅,李淑琴,高希涛,沈 俊,王培顺
全球每年约120万妇女患乳腺癌,50万左右死于乳腺癌。北美、西欧乳腺癌发病率占女性肿瘤首位,我国乳腺癌发病率逐年上升,沿海大城市的发病率较内陆地区为高,已成为城市女性的“第一杀手”。大部分乳腺癌患者在就诊时已非早期,手术后辅以化放疗,治疗效果欠佳。肿瘤的侵袭、转移是影响乳腺癌患者术后生存的主要因素。因此,寻找对乳腺癌浸润、转移有价值的检测指标,将有助于乳腺癌患者的预后评估,从而及时采取进一步治疗措施,提高患者的无病生存率和总生存率。
烟酰胺磷酸核糖基转移酶(Nampt)是细胞内烟酰胺腺嘌呤二核苷酸(NAD)生物合成的限速酶,具有多种生物效应。在烟酸胺合成NAD的过程中,Nampt催化5-磷酸核糖基-1-焦磷酸盐(PRPP)转移磷酸核糖基团给烟酸胺形成烟酰胺单核苷酸 (NMN)和焦磷酸盐(PPi)。然后NMN再通过烟酰胺单核苷酸腺苷酰转移酶(Nmnat)催化生成NAD[1](图1)。

图1 烟酰胺(nicotinamide)生物合成烟酰胺腺嘌呤二核苷酸(NAD)
Nampt是一种具有多种功能的蛋白质,目前对其多种生物学功能,特别是在肿瘤发生发展、抗凋亡机制等方面的研究尚处于起步阶段[2]。2007年,Yang等[3]在《Cell》上发表的一篇着重于研究营养影响线粒体NAD水平与细胞生存关系的论文中,用甲磺酸甲脂(一种DNA烷化剂)和依托泊甙(拓扑异构酶Ⅱ抑制剂)分别处理Nampt高表达的和Nampt敲除的纤维肉瘤细胞以及胚肾细胞,发现Nampt高表达的细胞凋亡减少,提示Nampt高表达能抵抗DNA损伤所引起的细胞死亡。Folgueira 等[4]在阿霉素治疗乳腺癌的耐药基因筛选中,发现3个基因与阿霉素耐药有关,其中一个就是Nampt。
我们的前期研究发现Nampt在胃癌等多种恶性肿瘤中高表达,与恶性肿瘤生物学行为密切相关,且可能与肿瘤细胞对某些药物的化疗耐药有关[5-6]。本研究中,通过探讨乳腺癌组织中Nampt的表达与临床病理特征及患者预后的关系,以期为乳腺癌患者临床治疗、预后评估提供新的理论依据。
1 材料与方法
1.1 病理组织来源 采集2006年1月至2008年12月间83例我院手术治疗且随访资料完整的乳腺癌患者癌组织标本及对应的癌旁正常乳腺组织标本。患者均为女性,年龄29~66岁,平均年龄47岁。所有患者术前未经放疗或化疗。乳腺癌TNM分期采用AJCC标准(2009年版)。
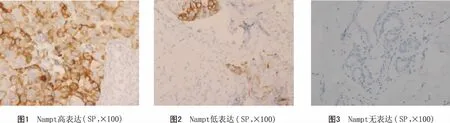
1.2 免疫组化方法 标本经35%甲醛水溶液固定,石蜡包埋,切成3 μm厚组织切片,附于玻片上,采用免疫组化SP法染色。应用图像信号采集与分析仪对所有切片进行图像采集。免疫组织化学染色后的切片按阳性率进行判断:Nampt阳性染色定位于细胞质,以见棕黄色或者棕褐色颗粒为阳性细胞。每张切片按阳性细胞占总细胞数的百分比定量评为1~4分:≤25%为1分;26%~50%为2分;51%~75%为3分;≥76%为4分。1~2分归为低表达,3~4分归为高表达。由两名病理科医师独立判定每一个样本,少数不统一的结果进行重新评估,取协商后一致的意见。
1.3 统计学方法 采用SPSS 17.0软件进行统计学分析,Nampt在组织中表达的差异及与临床病理学特性的关系采用χ2检验,Nampt表达与预后的关系采用Kaplan-Meier法绘制生存曲线,曲线之间的差异采用Log-rank检验评价。以P<0.05为差异有统计学意义。
2 结果
2.1 Nampt在乳腺癌组织及正常乳腺组织中的表达(图1) 48.19%(40/83)的乳腺癌组织标本中Nampt高表达,51.81%(43/83)的乳腺癌组织标本中Nampt低表达。正常乳腺组织中Nampt均几无表达。
2.2 Nampt表达与乳腺癌临床病理间的关系及与ER、PR、Her-2表达的相关性 由表1可见,Nampt的表达与患者年龄、肿瘤部位及组织分化程度无关,与肿瘤大小、淋巴结转移及TNM分期有关(P<0.05)。Nampt表达与ER、PR的表达呈负相关,而与Her-2的表达之间没有显著相关性。
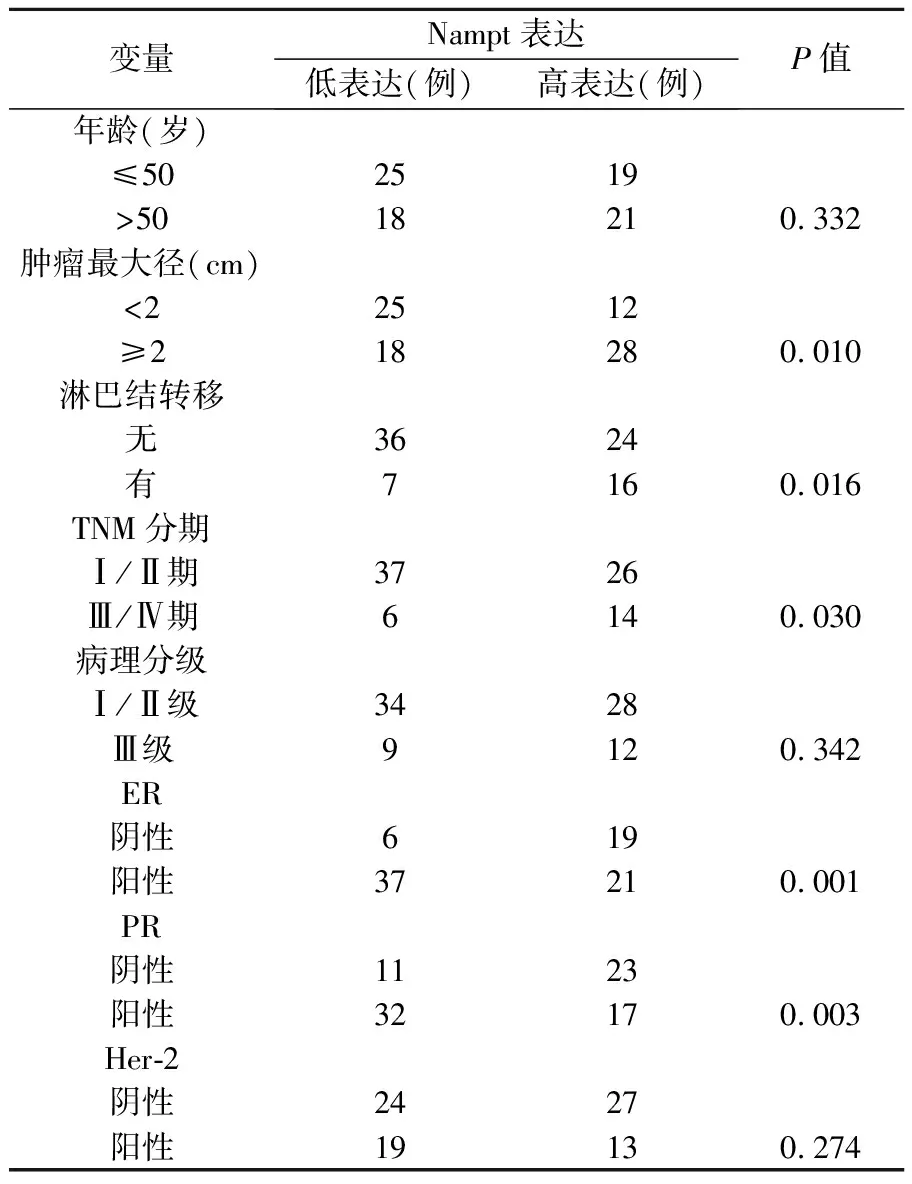
表1 Nampt表达与乳腺癌临床病理间的关系及与ER、PR、Her-2表达的相关性
2.3 Nampt的表达与乳腺癌患者预后的关系 将Nampt高表达和低表达患者的同期生存率相比较后发现,Nampt高表达患者的5年无病生存率和总生存率低于低表达者,差异均有统计学意义(P<0.05)(图2、图3)。
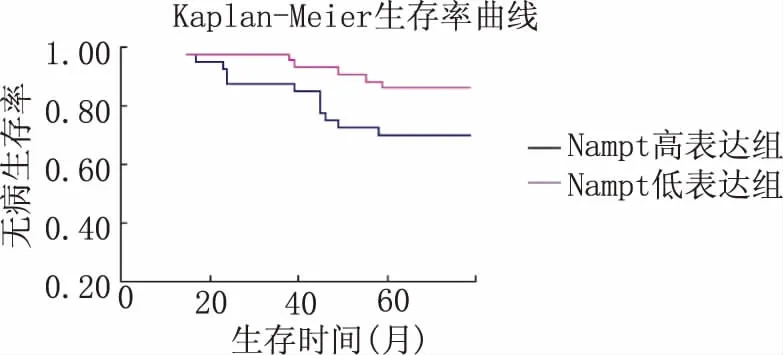
图2 Nampt表达与乳腺癌患者5年无病生存率关系曲线

图3 Nampt表达与乳腺癌患者5年总生存率关系曲线
3 讨论
Nampt与肿瘤之间的关系正逐渐引起研究者们的兴趣。研究证实Nampt在多种恶性肿瘤中高表达。多项研究检测Nampt在相关肿瘤性疾病中血清水平和(或)组织水平的表达均得到了阳性结果,认为其可作为相关肿瘤的分子标记物[2]。Nakajima等[7-8]对胃癌及结肠癌患者血清中的多种因子进行检测和分析后认为,Nampt可作为诊断进展期胃癌和结肠癌的一种新的生物标记物。Wang等[9]发现Nampt在前列腺癌中高表达,其抑制剂能有效抑制前列腺癌细胞生长和侵袭。Bajrami等[10]在近期通过裸鼠实验发现,Nampt抑制剂联合PARP抑制剂对三阴性乳腺癌有明显的治疗作用。
一种经化学方法新筛选出的小分子化合物FK866(APO866),能通过抑制Nampt引起NAD耗竭导致肿瘤细胞凋亡。FK866能抑制烟酰胺合成NAD以阻断肿瘤细胞赖以生存的途径,而对正常细胞影响很小,因此其有望成为一种新的抗癌药物[11]。
我们的研究发现,Nampt在乳腺癌中高表达,其表达程度与肿瘤大小、淋巴结转移及TNM分期有关。随着乳腺癌恶性程度及分期的增高,Nampt的表达也随之增加,这表明Nampt可能参与了乳腺癌的发展和转移过程,是乳腺癌进展过程中的重要蛋白,可用来辅助判定乳腺癌的分期或恶性程度。本研究还表明,与乳腺癌组织中Nampt低表达的患者相比较,Nampt高表达的患者术后无病生存率及总生存率低,提示Nampt可用来预测乳腺癌患者的预后和指导临床治疗,特别是在结合TNM分期及受体表达时,可能对预后的判断更为准确。
综上所述,Nampt在乳腺癌组织中呈高表达状态,参与乳腺癌的发展和转移过程,不仅可用于评估乳腺癌患者的预后,而且可作为乳腺癌潜在的治疗靶点,为开发新的治疗药物提供思路。
参考文献:
[1] Shackelford RE,Mayhall K,Maxwell NM,et al.Nicotinamide Phosphoribosyltransferase in Malignancy:A Review[J].Genes Cancer,2013, 4(11-12):447-456.
[2] Bi TQ, Che XM.Nampt/PBEF/visfatin and cancer[J].Cancer Biol Ther,2010, 10(2):119-125.
[3] Yang H,Yang T,Baur JA,et al.Nutrient-sensitive mitochondrial NAD+ levels dictate cell survival[J].Cell,2007,130(6):1095-1107.
[4] Folgueira MA,Carraro DM,Brentani H,et al.Gene expression profile associated with response to doxorubicin-based therapy in breast cancer[J].Clin Cancer Res, 2005, 11(20):7434-7443.
[5] Bi TQ, Che XM, Liao XH,et al.Over-expression of Nampt in gastric cancer and chemopotentiating effects of the Nampt inhibitor FK866 in combination with fluorouracil[J].Oncol Rep,2011,26(5):1251-1257.
[6] 龙厚隆,车向明,毕铁强,等.烟酰胺磷酸核糖转移酶、血管内皮生长因子A在胃癌组织中的表达及临床意义[J].中华外科杂志,2012,50(9):839-842.
[7] Nakajima TE, Yamada Y, Hamano T, et al.Adipocytokine levels in gastric cancer patients: resistin and visfatin as biomarkers of gastric cancer [J].J Gastroenterol, 2009, 44(7):685-690.
[8] Nakajima TE, Yamada Y, Hamano T, et al.Adipocytokines as new promising markers of colorectal tumors:adiponectin for colorectal adenoma and resistin and visfatin for colorectal cancer[J].Cancer Sci,2010, 101(5):1286-1291.
[9] Wang B,Hasan MK,Alvarado E,et al.NAMPT overexpression in prostate cancer and its contribution to tumor cell survival and stress response[J].Oncogene,2011,30(8):907-921.
[10] Bajrami I,Kigozi A,Van Weverwijk A,et al.Synthetic lethality of PARP and NAMPT inhibition in triple-negative breast cancer cells[J].EMBO Mol Med,2012,4(10):1087-1096.
[11] Zerp SF,Vens C,Floot B,et al.NAD+ depletion by APO866 in combination with radiation in a prostate cancer model,results from an in vitro and in vivo study[J].Radiother Oncol,2014,110(2):348-354.
