异丙醇-盐-水体系萃取分离苏丹红I-IV
2013-10-25郭名霞何池洋
郭名霞,何池洋
异丙醇-盐-水体系萃取分离苏丹红I-IV
郭名霞,何池洋*
(武汉纺织大学 化学与化工学院,湖北 武汉 430073)
基于异丙醇-盐-水双水相体系建立一种萃取分离苏丹红I-IV的新方法,考察了盐的种类及用量、苏丹红浓度对该体系萃取行为的影响。研究结果表明在异丙醇-K2CO3-水体系中苏丹红萃取率达92%-102%,线性检测范围为0.1-20 μg·mL-1,检出限均为10 ng·mL-1(S/N=3)。该方法操作简便、无污染,与液相色谱法联用有望能用于复杂样品中苏丹红I-IV的检测。
异丙醇; 双水相; 苏丹红I-IV; 萃取; 高效液相色谱
苏丹红是一类红色偶氮类染料(其化学式和结构式如图1所示),主要用于工业和科学研究中的染色[1]。已有研究表明,苏丹红具有一定的致癌性[1]。中国及许多欧盟国家和地区都禁止将其用于食品生产。然而,仍有不少食品厂家非法将其作为食用色素,以改善食品色泽,降低成本。为此不少国家已制定出相关检测标准。由于一般样品中苏丹红浓度低,直接分析较困难,通常在检测前需富集浓缩。目前苏丹红的预富集浓缩方法大多采用传统的液液萃取和固相萃取[1-4]。由于此两种方法均使用有毒的有机熔剂,污染环境,且危害检测人员的身体健康,同时操作步骤也繁琐,因而急需研究出绿色、无污染、操作简便的富集分离方法。
双水相体系是一种新型无污染且操作简便的萃取体系[5]。双水相体系一般是含一种聚合物和无机盐的水溶液,或两种不同水溶性聚合物的水溶液,在一定条件下溶液会分成界面清晰的两层水相[5]。由于表面性质、电荷作用和各种作用力(如疏水作用,离子键,氢键)等因素的影响,被分离的物质在双水相体系两相间的分配系数不同,导致其在上下相的浓度不同,从而达到分离的目的。双水相萃取体系已广泛应用于生物化学、细胞生物学、食品化工和药物分离等领域[5-8],具有广阔的应用前景。双水相体系有望能用于苏丹红的萃取分离中,然而目前国内外尚未见报道。本文基于异丙醇—盐—水双水相体系,通过考查盐的种类、盐的用量和苏丹红浓度对其萃取率影响,建立了一种萃取分离苏丹红I-IV的新方法。
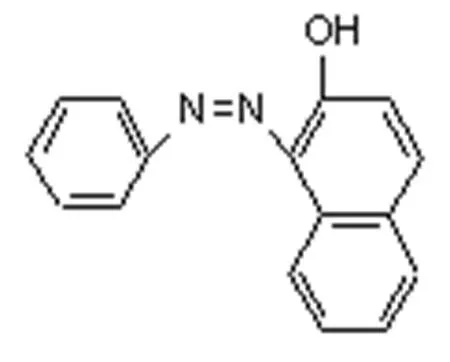
苏丹红I
苏丹红II
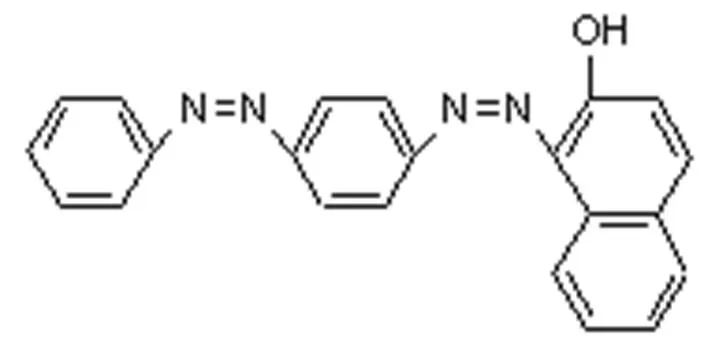
苏丹红III
苏丹红IV
图1 苏丹红I-IV的化学结构式
1 实验部分
1.1 仪器与试剂
高效液相色谱仪:SPD-10Avp SHIMADZU VWD紫外检测器,LC-10ATvp SHIMIDZU 单元泵,江申色谱工作站。色谱柱:Shim Pack UP-ODS(150×4.6 mm)。
苏丹红I-IV(>99%)、甲醇(>99.8%,色谱纯 )、乙腈(>99.8%,色谱纯)、异丙醇(>99.5%,分析纯)、甲酸(>88.0%,分析纯)、碳酸钾(>99.0%,分析纯)、磷酸氢二钾(>99.0%,分析纯)和氢氧化钾(>82%,分析纯)均购自国药集团化学试剂有限公司。所用水均为二次蒸馏水。
1.2 苏丹红I-IV样品溶液的配制
准确称取0.1 g苏丹红I-IV,用乙腈溶解定容至100 mL,即为各种苏丹红的贮备液,浓度均为1 mg·mL-1。以乙腈为溶剂将贮备液稀释至100 μg·mL-1,即为苏丹红样品工作液。
1.3 双水相体系的制备
于一个带刻度的10 mL具塞离心管中,依次加入适量盐、苏丹红溶液、5.0 mL 水和0.5 mL异丙醇,旋涡混合1-2 min后,离心10 min (1800 rpm),得到界面清晰的两相,读取上相体积u。
直接吸取上相进液相色谱仪测定其中苏丹红的浓度,计算萃取率,描述苏丹红在双水相中的分配行为。萃取率的计算公式为:%=(u·/m)×100%,式中指加入的苏丹红质量,指上相中苏丹红的质量浓度。
1.4 色谱分析条件
流动相:含0.1%甲酸的甲醇溶液,或0.1%乙酸水溶液+乙腈(30:70, v/v);流速:1.0 mL·min-1;柱温:室温;检测波长:480 nm;进样体积:20 μL(通过定量管进样)。
2 结果与讨论
2.1 流动相的选择
实验中考察了两种流动相对苏丹红I-IV的分离效果及保留时间的影响。所采用的流动相组成及流速分别是:A. 含0.1%甲酸的甲醇溶液,流速1.0 mL·min-1;B. 0.1%乙酸水溶液+乙腈 (30:70,v/v),流速1.0 mL·min-1。所用的苏丹红浓度均为5 μg·mL-1。所得的色谱图见图2和图3。
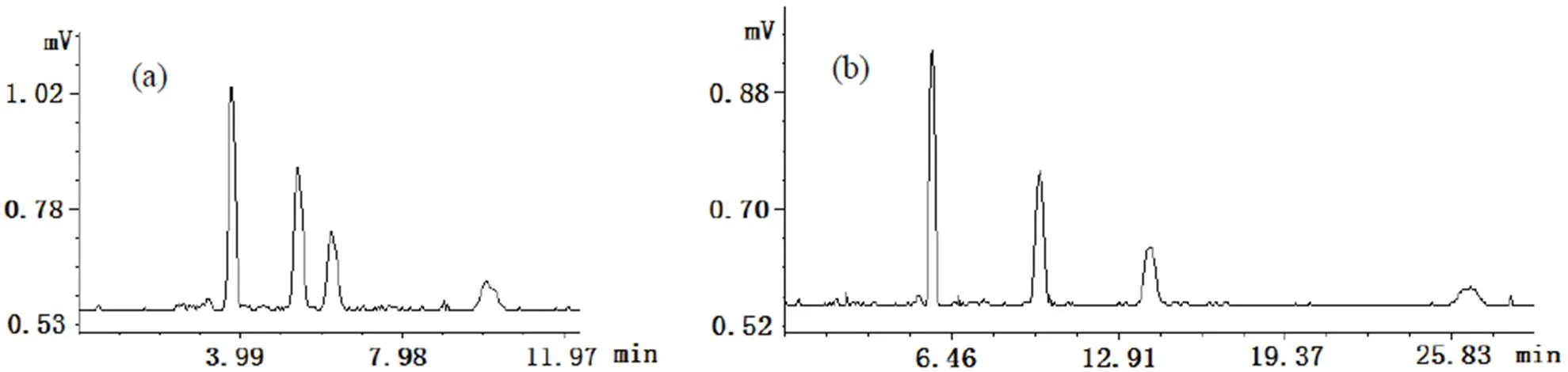
图2 苏丹红I-IV混合液的HPLC色谱图: (a) 流动相A; (b) 流动相B.
可见,当使用流动相A时,苏丹红I-IV均能较好分离,且保留时间均在10 min以内,利于快速分析,因而在考察苏丹红染料在双水相体系中的分配行为时可采用此流动相。本文在相关实验中采用流动相A。
当使用流动相B时,苏丹红I-IV分离得更开,利于复杂体系中苏丹红系列染料的分离,且保留时间均小于30 min,因而该流动相适用于复杂样品中苏丹红I-IV的分离分析。
2.2 标准曲线的绘制
分别吸取浓度为100 μg·mL-1的苏丹红工作液5 μL、25 μL、50 μL、0.1 mL、0.25 mL、0.35 mL、0.5 mL、0.75 mL和1 mL于10支离心管中,用乙腈稀释至5 mL,得到浓度分别为0.1μg·mL-1、0.5μg·mL-1、1 μg·mL-1、2 μg·mL-1、5 μg·mL-1、7 μg·mL-1、10 μg·mL-1、15 μg·mL-1和20 μg·mL-1的苏丹红标准溶液。定量进样20 μL苏丹红标准溶液,进入液相色谱分析,所用流动相为含0.1%甲酸的甲醇溶液。以各色谱峰面积和相应苏丹红的浓度绘制苏丹红系列染料的标准曲线,线性回归方程及相应相关系数如表1所示。可见,苏丹红I-IV浓度在0.1-20 μg·mL-1范围内,各组分的色谱峰面积与其浓度均具有很好的线性关系,表明该方法具有较宽线性范围。

表1 苏丹红染料的标准曲线及相应相关系数
2.3 盐对双水相体系分相行为的影响
为了选择较合适的盐及其用量,实验中考察了盐的种类及其用量对双水相体系分配行为的影响。所考察的盐为K2HPO4、K2CO3和KOH。图3是双水相的上相体积u随盐的种类及用量而变化的情况。如图3所示,当加入2.5-4.5 g K2HPO4时,上相体积呈下降趋势;而加入2.5-4.5 g K2CO3或2.5-4.5 g KOH时,上相体积变化不大。其中在K2CO3体系中,上相的体积最小,即该体系的富集倍数最大,富集倍数为5.0-5.5。
2.4 盐对苏丹红萃取率的影响
研究了盐的种类及用量对其萃取率的影响。当0.5mL异丙醇用于萃取含7.5 μg苏丹红I-IV的水溶液时,K2HPO4、K2CO3和KOH三种盐对苏丹红萃取率的影响各不相同。结果如图4、图5、图6所示。当2.5g-4.5g K2HPO4和2.5-5.0 g KOH用作分相盐时,苏丹红染料的萃取率不稳定,因均不是理想的分相盐。只有使用2.0g-4.5g K2CO3时,苏丹红I-IV的萃取率均比较稳定,且最高萃取率可分别达到99%、109%、99%和101%,因而较适合作为分相盐用于定量萃取苏丹红。综合考虑到该体系中富集倍数最佳,因此本实验采用4.5 g K2CO3作为分相盐。
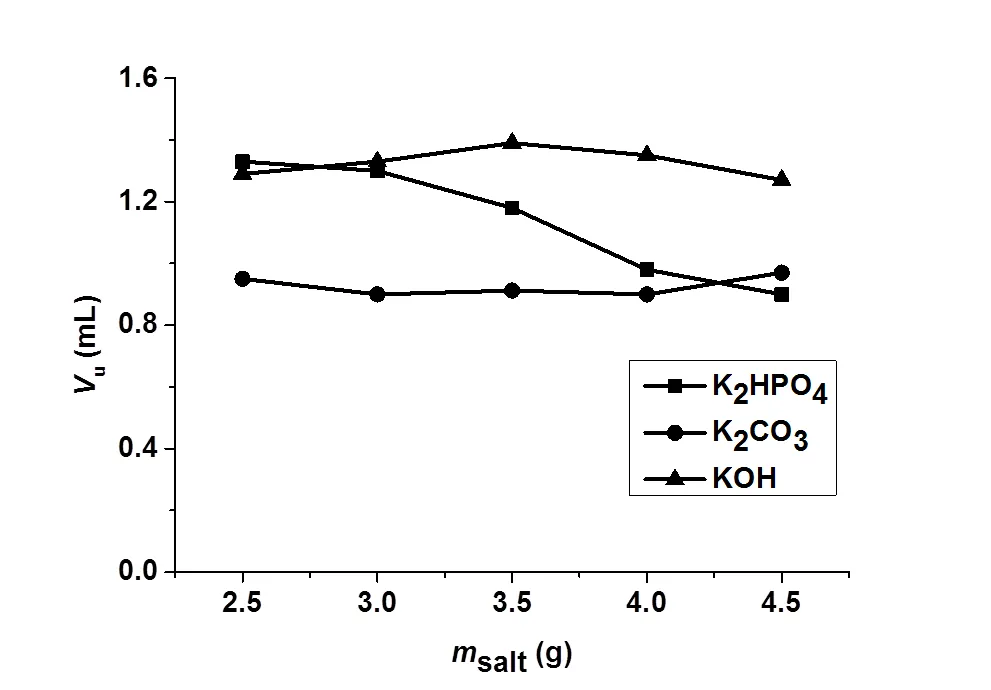
图3 盐的种类及用量对上相体积的影响
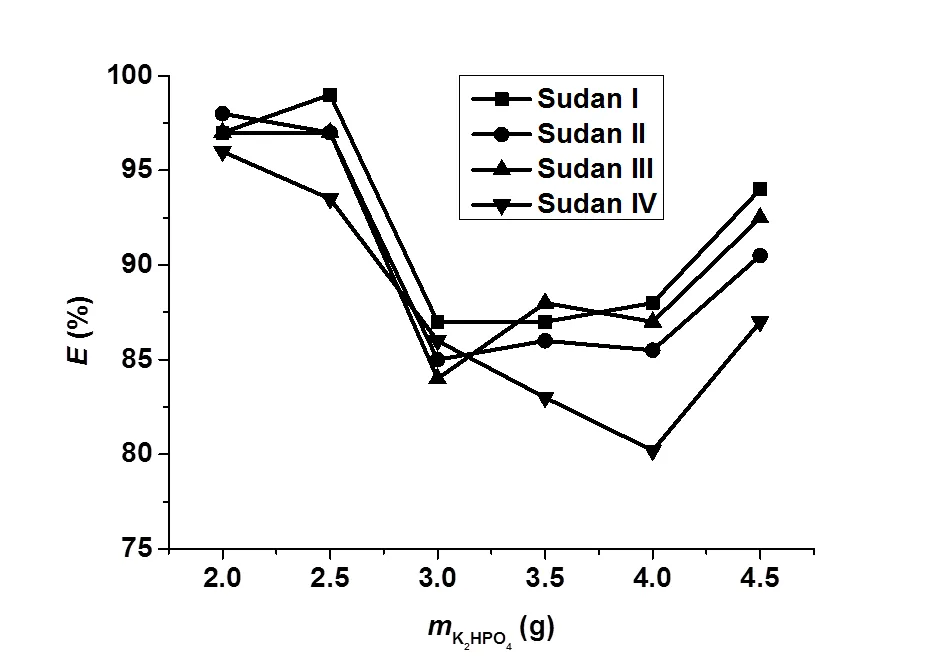
图4 磷酸氢二钾用量对苏丹红萃取率的影响
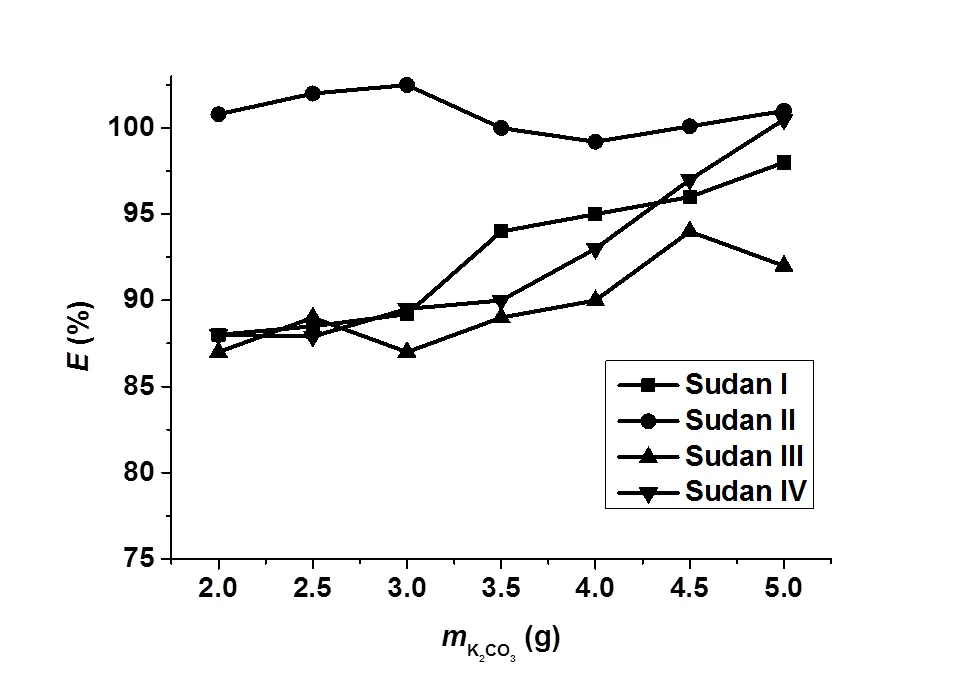
图5 碳酸钾用量对苏丹红萃取率的影响
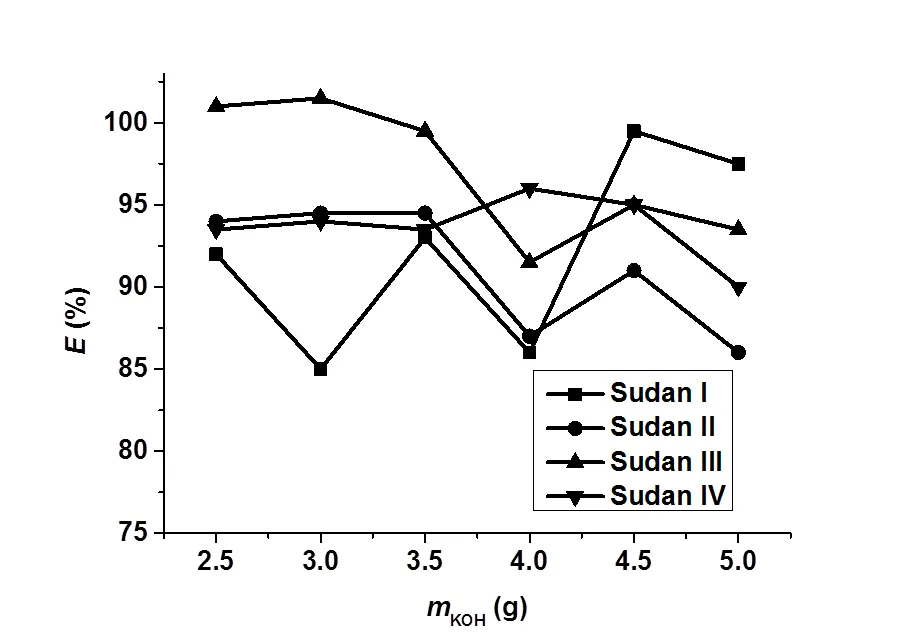
图6 氢氧化钾用量对苏丹红萃取率的影响
2.5 分析物浓度对萃取率的影响
考察了苏丹红浓度对其萃取率的影响。以4.5 g K2CO3为分相盐,0.5 mL异丙醇为萃取剂,分别研究了1 μg·mL-1、5 μg·mL-1和10 μg·mL-1三种不同浓度的苏丹红I--IV溶液在异丙醇—K2CO3—水体系中的分配行为。实验结果如图7所示。可见苏丹红浓度对其萃取率的影响不大。另外,经异丙醇—K2CO3—水体系富集后,测得苏丹红I-IV的检出限均为10 ng·mL-1(S/N=3)。
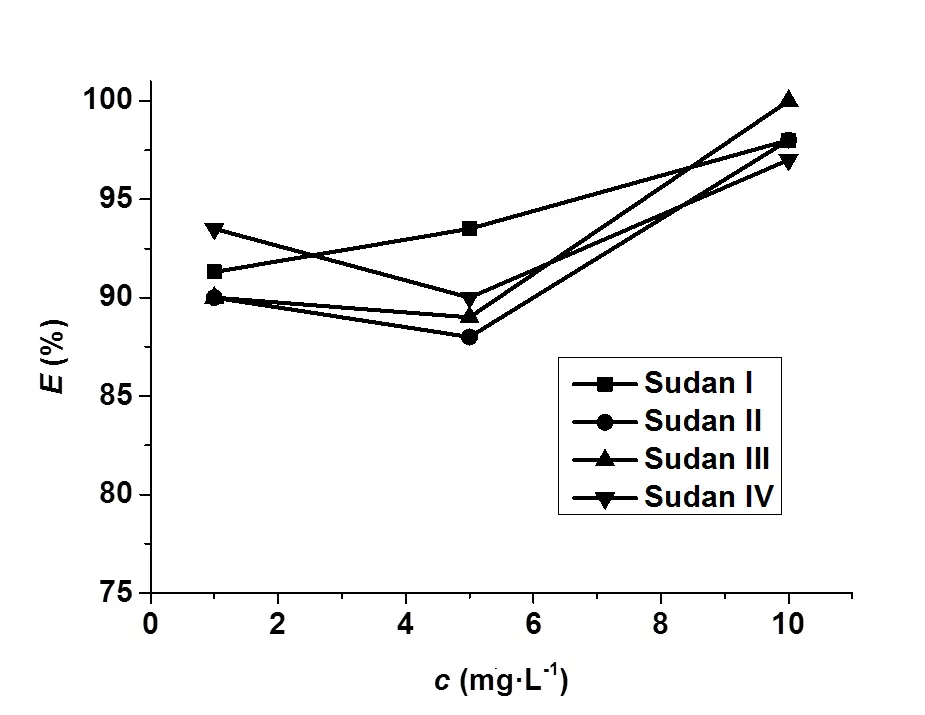
图7 苏丹红浓度对其萃取率的影响
3 结论
基于异丙醇—K2CO3—水双水相体系,建立了一种萃取分离苏丹红的新方法。与传统的液液萃取或固相萃取相比,该方法操作简单,萃取上相可直接进入液相色谱仪分析;萃取效率高,经一次萃取便可达到理想的萃取率;不使用有毒的有机溶剂,且只需要极少量的萃取剂,因而对环境无污染。这种新型萃取方法与高效液相色谱法联用,有望能用于复杂样品(如食品)中微量苏丹红的富集、分离和测定。
[1] Rebane R, Leito I, Yurchenko S, et al. A review of analytical techniques for determination of Sudan I–IV dyes in food matrixes [J]. Journal of Chromatography A, 2010, 1217: 2747-2757.
[2] Yan HY, Gao MM, Qiao JD. New Ionic Liquid Modified Polymeric Microspheres for Solid-Phase Extraction of Four Sudan Dyes in Foodstuff Samples [J]. Journal of Agricultural and Food Chemistry, 2012, 60: 6907-6912.
[3] Fukuji TS, Castro-Puyana M, Tavares MFM, et al. Fast Determination of Sudan Dyes in Chilli Tomato Sauces Using Partial Filling Micellar Electrokinetic Chromatography [J]. Journal of Agricultural and Food Chemistry, 2011, 59: 11903-11909.
[4] Qiao FX, Geng YR, He CQ, et al. Molecularly imprinted microspheres as SPE sorbent for selective extraction of four Sudan dyes in catsup products [J]. Journal of Chromatography B, 2011, 879: 2891-2896.
[5] He CY, Li SH, Liu HW, et al. Extraction of testosterone and epitestosterone in human urine using aqueous two-phase systems of ionic liquid and salt [J]. Journal of Chromatography A, 2005, 1082: 143-149.
[6] Freire MG, Cláudio AFM., Araújo JMM, et al. Aqueous biphasic systems: a boost brought about by using ionic liquids [J]. Chemical Society Reviews, 2012, 41: 4966-4995.
[7] Oppermann S, Stein F, Kragl U. Ionic liquids for two-phase systems and their application for purification, extraction and biocatalysis [J]. Applied Microbiology and Biotechnology, 2011, 89: 493-499.
[8] Ruiz-Ruiz F., Benavides J., Aguilar O, et al. Aqueous two-phase affinity partitioning systems: Current applications and trends [J]. Journal of Chromatography A, 2012, 1244: 1-13.
Extraction of Sudan I-IV Using 2-Propanol–Salt–H2O System
GUO Ming-xia, HE Chi-yang
(College of Chemistry and Chemical Engineering, Wuhan Textile University, Wuhan Hubei 430073, China)
Based on the 2-propanol–salt–H2O system, a new extraction method was developed for the separation of Sudan I-IV from water sample. The effect of salt type, salt amount and dye concentration on extraction behavior of the aqueous two-phase system were investigated. Results showed that in 2-propanol–K2CO3–H2O system the extraction efficiencies of dyes were 92-102%, the linear detection range were 0.1-20 μg·mL-1, and the detection limitation was 10 ng·mL-1(S/N=3). Compared with traditional methods, the new extraction method is simpler and more environmentally friendly. When coupled with HPLC method, the proposed extraction method could be potentially used for the determination of Sudan I-IV in food samples.
2-Propanol; Aqueous Two-Phase System; Sudan I-IV; Extraction; High-Performance Liquid Chromatography
O652.62
A
2095-414X(2013)03-0072-04
国家自然科学基金项目(20775003).
何池洋(1968-),男,博士,教授,研究方向:色谱及分离分析.
