钩吻素子亲水凝胶骨架缓释片的处方优化及其体外释放度研究
2013-09-27范振东石冬梅苏燕评廖凯君俞昌喜
范振东,石冬梅,苏燕评,廖凯君,张 丽,俞昌喜
钩吻(GelsemiumelegansBenth.)为马钱科植物胡蔓藤的全草,盛产于我国的闽、浙、桂等地,民间一直应用钩吻原植物治疗各类疼痛[1-2]。钩吻的主要有效成分为吲哚类生物碱,其总碱曾以注射剂、口服剂和外用膏药几种不同的剂型用于疼痛、肿瘤等疾病的治疗[3-5],但其毒性大,治疗指数低。钩吻素子(Koumine)是钩吻总碱中含量最高的一种单体[6],本课题组先期系列研究表明钩吻素子具有高效低毒的治疗慢性疼痛、抗焦虑和抗类风湿性关节炎作用[7-11],提示钩吻素子具有创制新型药物的重大潜能。由于慢性疼痛和抗风湿性关节炎的治疗疗程长,为此拟将钩吻素子设计成长效缓释剂型,以减少给药次数,增加患者的顺应性。缓释制剂中骨架缓释片因其生产设备和制备工艺简单、缓释效果好而受到广泛应用,因此,本研究拟优化筛选钩吻素子亲水凝胶骨架缓释片的处方并对其释放度进行考察,为研制质量可靠,药物释放稳定、缓慢、完全的钩吻素子缓释片提供实验基础。
1 材料与方法
1.1 仪器与试剂 高效液相色谱仪(Angilent 1100)、紫外检测器(G1314B)及色谱工作站(Angilent 1100)(美国 Angilent公司);磁力搅拌器(ZNCL-S,巩义市予华仪器有限责任公司);精密酸度计(pHS-407,上海大普仪器有限公司);手摇便携式压片机(TDP-1.5T,上海超亿制药机械设备有限公司);智能药物溶出仪(RCZ-8A,天津大学精密仪器厂)。甲醇(色谱纯,中国国药集团化学试剂有限公司);预胶化淀粉(药用辅料,上海卡乐康包衣技术有限公司);羟丙甲基纤维素和微粉硅胶(大连业建贸有限公司);乳糖和硬脂酸镁(山东聊城阿华制药有限公司);其他试剂均为中国国药集团化学试剂有限公司市售分析纯;钩吻素子对照品为本课题组前期提取分离精制而成,经高效液相色谱(HPLC)鉴定,纯度为99.1%。
1.2 方法
1.2.1 钩吻素子含量HPLC测定
1.2.1.1 色谱条件及系统适用性试验 色谱柱:依利特 Hypersil ODS2高效液相色谱柱(5μm,4.6mm×250mm),流动相:甲醇-0.2%正丁胺水溶液(58∶42),流动相流速:1.0mL/min,柱温:25℃,紫外检测波长:256nm。
1.2.1.2 方法学考察 分别制备空白磷酸盐缓冲溶液(PBS)和含钩吻素子的PBS溶液,以上述HPLC法进样分析,结果显示空白PBS溶液对钩吻素子的测定没有干扰,该方法专属性良好;分别配制2.024,16.182和32.364μg/mL的钩吻素子的PBS溶液,以上述HPLC法进样分析,重复性试验显示高、中、低3个浓度的峰面积RSD均<3%,分别为2.38%,0.65%和0.53%,该法重复性良好(n=5);精密度试验显示,日内RSD均<3%,分别为2.13%,2.63% 和1.60%,回 收 率 分 别 为103.75%,96.53%和104.62%;日间RSD均<5%,分别为3.43%,1.44%和0.46%,该法精密度良好,回收率符合测定要求(n=5)。
1.2.1.3 标准曲线制备与线性关系考察 以PBS溶液(pH 6.8)配制浓度分别为2.024,5.06,10.12,20.24,50.6和84.3μg/mL的钩吻素子对照品溶液,按上述HPLC色谱条件进样分析,以钩吻素子浓度Y(μg/mL)对峰面积X进行线性回归,得到标准曲线为Y=14.831X-8.025 6,钩吻素子PBS溶液在2.02~84.3μg/mL浓度范围内线性关系良好,r=0.999 4。
1.2.2 钩吻素子亲水凝胶骨架缓释片的处方筛选
采用L9(34)进行正交设计,以 HPMC黏度、HPMC用量和乳糖用量为3因素,选取3水平进行试验,正交试验方案见表1。制备不同处方的钩吻素子缓释片剂,分别测定它们在1,2,4,6,8,10和12h的累积释药百分率。参考中国药典2010版二部附录缓控释制剂指导原则的规定[12],结合文献[13],拟采用P值为指标评价处方的释药性能:以2h释放度25%为标准,计算∣R2-25%∣;同理,选取6h释放度65%为标准,12h释放度90%为标准,各点的权重为1,总得分的评价公式为:
P=∣R2-25%∣×1×100+∣R6-65%∣×1×100+∣R12-90%∣×1×100
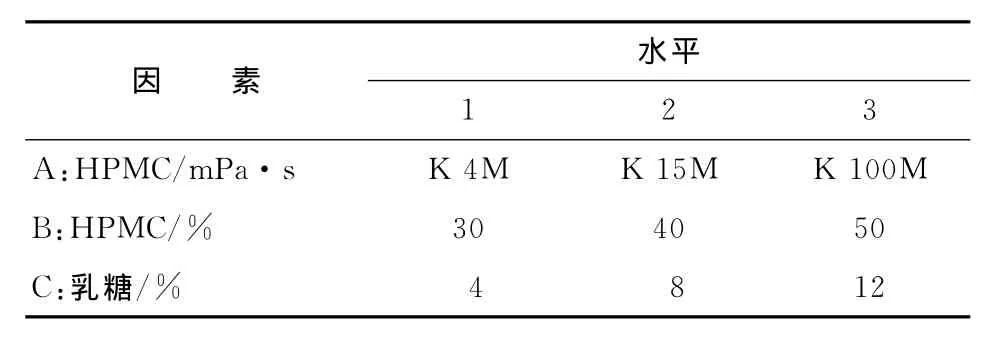
表1 优化因素水平表Tab 1 Factors and levels of orthogonal design
1.2.3 钩吻素子亲水凝胶骨架缓释片的制备工艺
按处方2配比,称取钩吻素子对照品、乳糖、预胶化淀粉、微粉硅胶,均过100目筛,充分混匀后,加入适量硬脂酸镁作润滑剂,混合均匀后,干法直接压片,得外观光洁白色片剂,每片含钩吻素子10mg。
1.2.4 钩吻素子亲水凝胶骨架缓释片释放度测定
取按处方2制备的钩吻素子缓释片3片,参照文献[12],按照释放度测定法,采用溶出度测定装置,以pH 6.8的PBS溶液500mL为释放介质,转速100r/min,温度(37±0.5)℃,于第1,2,4,6,8,10和12h分别取溶液3mL(并即时补充等量溶剂),0.45μm微孔滤膜滤过,HPLC法测定,依据钩吻素子浓度与峰面积标准曲线计算本品在选定时间点的累积释放度。
2 结 果
2.1 优化的钩吻素子缓释片处方 采用L9(34)进行正交设计,以HPMC黏度、HPMC用量和乳糖用量为3因素,选取3水平进行试验,正交试验结果见表2。极差R反映各因素对钩吻素子亲水凝胶骨架缓释片评价指标P的影响程度,R值越小表示该因素对P影响越小,反之则影响越大。正交试验结果显示,3因素对钩吻素子亲水凝胶骨架缓释片的P值影响的主次顺序为A>B>C,HPMC黏度对P值影响最大,HPMC用量次之,乳糖用量影响最小,各因素最佳组合为A1B2C2,因此选择处方2作为最佳试验处方,制备钩吻素子亲水凝胶骨架缓释片。

表2 钩吻素子亲水凝胶骨架缓释片处方筛选正交试验结果Tab 2 The result of orthogonal design experiment on Koumine hydrophilic matrix sustained-release tablets
2.2 钩吻素子亲水凝胶骨架缓释片释放度 优选的钩吻素子亲水凝胶骨架缓释片释放度结果见图1。结果表明,钩吻素子在2h内累积释放度为35%~40%,6h内累积释放度为60%~65%,12h内累积释放度>90%。
2.3 钩吻素子亲水凝胶骨架缓释片的释药机制
将上述缓释片体外释放度数据按零级模型、一级模型、Higuchi模型、Ritger-Peppas模型和 Weibull模型进行拟合,结果见表3。由表3可得,钩吻素子亲水凝胶骨架缓释片的体外释放与一级模型、Higuchi模型、Ritger-Peppas方程模型和 Weibull方程模型均具有良好的拟合度。其中Ritger-Peppas模型是将药物释放的扩散项与溶蚀项相加,提出的一个简单的半经验指数方程[14],一般情况下,药物从骨架片中的释放机制可以通过Peppas经验公式描述。
W=Ktn
对数转化:lnW=nlnt+C
W为药物在t时间的累积释放百分数,K为释放速率常数,t为释放时间点,释放指数n是表征释放机制的指数,对于圆柱体制剂(片剂等)而言,n=0.5454,符合0.45<n<0.89,扩散机制为非Fick扩散,该制剂释药过程中扩散和骨架溶蚀均起作用。
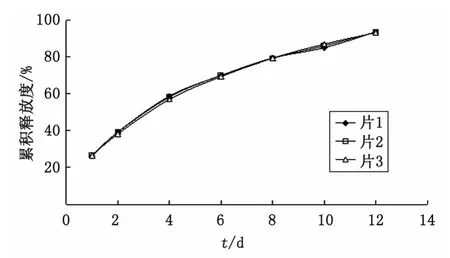
图1 钩吻素子亲水凝胶骨架缓释片体外累积释放度Fig 1 Release profiles of the optimized Koumine hydrophilic matrix sustained-releases tablets
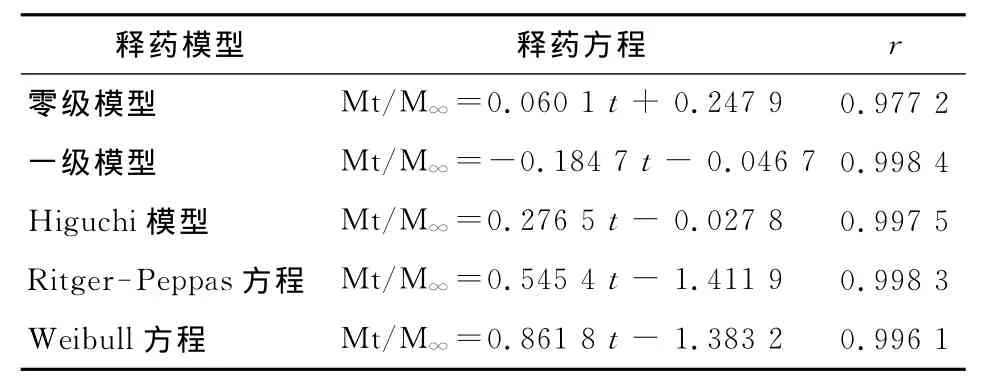
表3 钩吻素子亲水凝胶骨架缓释片的不同释药模型拟合Tab 3 Analysis of release models of Koumine hydrophilic matrix sustained-release tablets using different equations
3 讨 论
骨架型缓释制剂中骨架材料的选择至关重要。文献表明,以HPMC为骨架材料制备缓释片剂的工艺重现性好,发生崩解和突释可能性小,可压性良好[15]。因此选择HPMC作为骨架材料,采用正交试验设计,最终确定钩吻素子亲水凝胶骨架缓释片处方为:钩吻素子10mg,HPMC K4M112mg,乳糖22.4mg,预胶化淀粉132.8mg,微粉硅胶1.4mg,硬脂酸镁1.4mg;该缓释片2h内累积释放度为35%~40%,6h内累积释放度为60%~65%,12h内累积释放度>90%,药物在12h内稳定、缓慢、完全释放。
钩吻素子亲水凝胶骨架缓释片遇水时,首先在片剂表面润湿,形成水凝胶层,使表面钩吻素子溶出;凝胶层继续水化,骨架膨胀,凝胶层增厚,延缓了钩吻素子的释放,这时钩吻素子可通过凝胶层扩散释出;随着时间的延长,片剂外层骨架逐渐水化并溶蚀,内部再形成凝胶,再溶解,直至水分向片芯渗透至骨架完全释放。此外,本研究对处方优化后的钩吻素子亲水凝胶骨架缓释片的释放度按不同释药方程进行拟合,结果显示其释药机制符合Peppas方程。释放参数n是Peppas方程中表征释放机制的特征参数,与制剂的骨架形状有关,对于片剂而言,Peppas方程认为当n<0.45时,药物的释放机制即为Fick’s扩散;当0.45<n<0.89,药物释放机制为非Fick’s扩散,即药物扩散和骨架溶蚀协同作用;当n>0.89时,药物的释放机制为骨架溶蚀机制[14,16]。经处方优化后的钩吻素子亲水凝胶骨架缓释片的n值在0.45~0.89之间,显示其释药机制为扩散和骨架溶蚀的协同作用。
:
[1] 陈翼胜.中国有毒植物[M].北京:科学出版社,1990:371-376.
[2] 国家中医药管理局《中华本草》编委会.中华本草(第16卷)[M].上海:上海科学技术出版社,1999:213.
[3] 陆健敏,齐子荣,刘国廉,等.钩吻碱注射液对肿瘤细胞增殖能力的影响[J].癌症,1990,9(6):472-474.
[4] 张晴龙.一种抗癌镇痛的中药钩吻总生物碱和含它的药物组合物及其制备方法:中国,03159674.6[P].2003-09-26.
[5] 张 雷,谭 敏,李 晶,等.钩吻凝胶剂的制备与质量控制[J].中国医院药学杂志,2009,29(7):581-582.
[6] Su Y P,Shen J,Xu Y,etal.Preparative separation of alkaloids fromGelsemiumelegansBenth.using pH-zone-refining counter-current chromatography[J].JChromatogrA,2011,1218(23):3695-3698.
[7] Xu Y,Qiu H Q,Liu H,etal.Effects of koumine,an alkaloid ofGelsemiumelegansBenth.,on inflammatory and neuropathic pain models and possible mechanism with allopregnanolone[J].PharmacologyBiochemistryandBehavior,2012,101:504-514.
[8] 俞昌喜,许 盈,刘 浩.作为唯一活性成分的钩吻素子在制备治疗慢性疼痛药物中的应用:中国,200810071467.X[P].2011-08-31.
[9] Liu M,Huang H H,Yang J,etal.The active alkaloids ofGelsemiumelegansBenth.are potent anxiolytics[J].Psychopharmacology(Berl),2013,225(4):839-851.
[10] 俞昌喜,刘 铭,许 盈,等.钩吻素甲、钩吻素子、1-甲氧基钩吻碱在制备治疗焦虑症药物中的应用:中国,201110130826.6[P].2013-02-26.
[11] 俞昌喜,许 盈,杨 渐,等.钩吻素子在制备治疗类风湿性关节炎药物中的应用:中国,201110174657.6[P].2012-08-29.
[12] 国家药典委员会.中华人民共和国药典(2010年版第二部)[M].北京:中国医药科技出版社,2010:附录XD,XC,XE,XIXD.
[13] Cheng X,Sun M,Gao Y,etal.Design and evaluation of osmotic pump-based controlled release system of Ambroxol Hydrochloride[J].PharmDevTechnol,2011,16(4):392-399.
[14] Rigter P L,Peppas N A.A simple equation for description of solute release I.Fickian and non-Fickian release from nonswellable devices in the form of slabs,spheres,cylinders or discs[J].JControlledRelease,1987,5(1):23-36.
[15] 王 平,肖昌录,袁训贤.布洛芬缓释片的制备及其体外释放度考察[J].中国药房,2011,22(9):829-831.
[16] Jamzad S,Tutunji L,Fassihi R.Analysis of macromolecular changes and drug release from hydrophilic matrix systems[J].IntJPharm,2005,292(1-2):75-85.
