酮洛芬薄膜包衣脉冲控释片的制备
2016-05-25李彩艳李新亮
李彩艳,李新亮
(1山西职工医学院药学系,晋中 030619; 2离石区人民医院骨科; *通讯作者,E-mail:abc-lcy@163.com)
酮洛芬薄膜包衣脉冲控释片的制备
李彩艳1*,李新亮2
(1山西职工医学院药学系,晋中030619;2离石区人民医院骨科;*通讯作者,E-mail:abc-lcy@163.com)
摘要:目的研制夜间服药、凌晨释放的酮洛芬脉冲控释片。 方法采用湿法制粒压片法制备片芯,滚转包衣锅法包控释衣膜。通过对片芯、衣膜处方中崩解剂、填充剂、致孔剂、增塑剂、包衣增重进行单因素考察,并采用星点设计效应面法对处方进行优化。 结果单因素考查表明崩解剂、致孔剂、包衣增重对释药时滞有明显影响,采用星点设计效应面法得到的最优处方为:片芯处方KPF 50 mg(25%),MCC 40 mg(20%),乳糖70 mg(35%),L-HPC 40 mg(20%);包衣液处方为Eudragit L100 与EC比例是65 ∶35,PEG6000 15%,包衣增重9.0%。其体外释放时滞为3.75 h,释药时间为0.5 h。 结论酮洛芬薄膜包衣片能实现脉冲释药,达到定时速释的要求。
关键词:酮洛芬;脉冲控释片;释药;星点设计效应面法
脉冲释放制剂是根据人体时辰药理学特点,实现定时给药,即在用药后,制剂不是立即释药,而是在人体最需要的时候释放药物[1,2]。关节炎病常在凌晨加重,出现“晨僵”等症状,而此时服药极不方便。因此,我们制备酮洛芬(ketoprofen,KPF)脉冲控释片,以期制剂在临睡前被服用,一定时滞后,迅速释药发挥药效。从而避免了凌晨起床服药的麻烦和持续血药浓度带来的副作用,更有效地预防和治疗关节炎的发作。
本研究采用薄膜包衣技术,在具有一定膨胀力的片芯上进行乙基纤维素包衣。主要考察了片芯中不同崩解剂种类和用量、不同填充剂种类和用量对膨胀力大小的影响,及衣膜中各因素(如增塑剂、致孔剂)等对药物释放的影响,并在此基础上采用星点设计效应面法优化处方,确定脉冲控释片的最佳处方。
1仪器与试药
1.1仪器
UV-9100型紫外-可见分光光度计(北京瑞利分析仪器公司);ZRD6-B型药物溶出仪(上海黄海制药机械厂);ZDY型重型单冲压片机(上海制药机修三厂);BY300A型小型包衣机(上海黄海药检仪器厂)。
1.2试药
酮洛芬原料药(浙江九洲药业股份有限公司,批号:10010101);微晶纤维素(MCC,德国JRS公司);乳糖(营口奥达制药有限公司);低取代羟丙基纤维素(L-HPC,信越化学工业株式会社);羧甲基淀粉钠(CMS-Na,德国JRS公司);交联聚维酮(PVPP,德国JRS公司);交联羧甲基纤维素钠(CCNa,德国JRS公司);柠檬酸三乙酯(TEC,德国Röhm公司);邻苯二甲酸二乙酯(DEP,德国Röhm公司);硬脂酸镁(营口奥达制药有限公司);优特奇L100(Eudragit L 100,德国德固赛投资有限公司);乙基纤维素(EC,天津市博迪化工有限公司);聚乙二醇4000(PEG 4000)和聚乙二醇6000(PEG 6000)均由天津天成制药有限公司提供,其他试剂均为分析纯。
2方法与结果
2.1释放度测定方法
2.1.1检测波长的选择精密称取干燥至恒重的KPF及辅料适量,分别用0.1 mol/L盐酸溶液、pH 6.8磷酸盐缓冲液溶解,稀释,配置成适宜浓度的溶液,按紫外分光光度法(《中国药典》2010版二部附录XC)在200-400 nm波长范围内进行扫描,结果表明KPF在0.1 mol/L盐酸溶液、pH 6.8磷酸盐缓冲液中在258 nm处有最大吸收,且辅料无吸收干扰。故选择258 nm波长为检测波长。
2.1.2标准曲线的绘制精密称取KPF 35 mg置500 ml容量瓶中,分别用0.1 mol/L盐酸溶液和pH6.8磷酸盐缓冲液溶解并稀释至刻度,摇匀,作储备液备用。精密吸取储备液2,4,6,8,10,12,14,16,18 ml,分别置于100 ml容量瓶中,分别用0.1 mol/L盐酸溶液和pH 6.8磷酸盐缓冲液稀释至刻度,摇匀,作为标准供试液[3]。分别以0.1 mol/L盐酸溶液和pH 6.8磷酸盐缓冲液为空白对照,于258 nm波长处测吸收度,以吸收度A对浓度C作线性回归,得KPF在pH 1.0和pH 6.8两种介质中的标准曲线方程分别为:A=0.062 3C+0.010 4(R=0.999 8),A=0.060 5C+0.007 4(R=0.999 9),线性范围均为1.4-11.2 μg/ml。
2.1.3释放度测定方法参照《中国药典》2010版二部酮洛芬肠溶胶囊释放度测定标准,桨法,转速100 r/min,温度37 ℃,先以0.1 mol/L HCl溶液750 ml为释放介质,经2 h后,向溶出杯中加入37 ℃的0.2 mol/L磷酸钠250 ml,混匀,继续搅拌,直至药物完全释放。在预定的时间间隔内取样5 ml,同时补充相同体积介质,样品溶液经0.8 μm微孔滤膜滤过,弃去初滤液,取续滤液3 ml,在258 nm下测定吸收度A,计算累积释放量。
2.2脉冲控释片的制备
2.2.1片芯制备将KPF和辅料分别过80目筛,称量KPF 50 mg,一定量的微晶纤维素(MCC)、乳糖(填充剂)、崩解剂,等量递加混合均匀,加适量黏合剂(95%乙醇)制成软材,过20目筛制粒,于55 ℃干燥,过18目筛整粒,加入润滑剂硬脂酸镁混匀,计算片重,用直径8 cm冲模压片。
2.2.2控释膜的包衣控释膜的基本处方组成为:Eudragit L100(致孔剂),EC(水不溶膜材),PEG6000(增塑剂),无水乙醇(溶剂)。
包衣液的配制:将Eudragit L100边搅拌边加入到一定体积的无水乙醇中,待溶解后,加入一定量的EC和增塑剂,继续搅拌3-4 h,待溶液澄清得包衣液。
包衣过程:实验中包衣工艺参数为:包衣锅直径20 cm;包衣锅转速为40 r/min;进风温度为40-45 ℃;片床温度为(30±1)℃;进风流量为7 m3/min;包衣液喷射速度为1 ml/min;喷气雾化压力为0.15 MPa;直至片芯外包衣膜增重达到预定要求为止。取出包衣片,置于40 ℃恒温烘箱中4 h,除去残余的有机溶剂。制得的包衣片外形完整,表面光滑。
2.3脉冲控释片处方单因素考察
2.3.1崩解剂种类对释药行为的影响固定片芯以下组分和用量(KPF 50 mg,MCC 70 mg,乳糖40 mg)不变,改变崩解剂种类(分别用30 mg的L-HPC、CMS-Na、PVPP和CCNa作为崩解剂)制备四种KPF片芯,用同种包衣液在相同的包衣工艺条件下包相同厚度衣层(约增重9.0%),制得4种脉冲片,测定体外释放度,结果见图1。
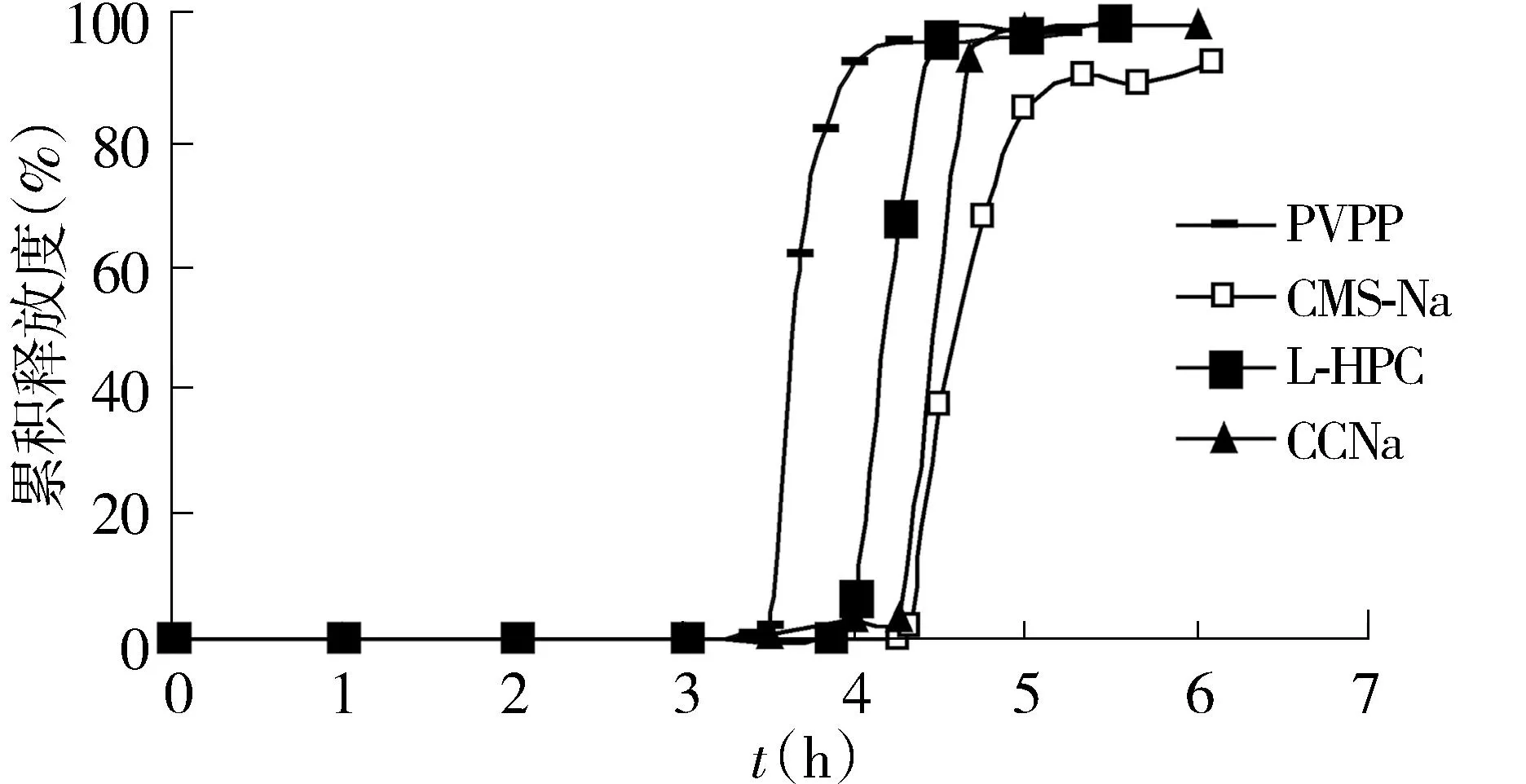
图1 不同崩解剂种类对药物释放的影响Figure 1 The effects of different disintegrants of the core tablets on the release profiles
由图1可知,用4种崩解剂制备的片芯,其崩解性能依次为PVPP>L-HPC>CCNa>CMS-Na。但PVPP成本较贵。以CMS-Na为崩解剂的脉冲片释药速率较以L-HPC为崩解剂的慢,时滞较长。L-HPC和MCC混合压片时可压性和成型性良好,故采用L-HPC为崩解剂制备脉冲控释片。
2.3.2崩解剂用量对释药行为的影响固定片芯中其他组分不变,以L-HPC为崩解剂,改变其用量(0,20,30,40,60 mg)制备5种不同的KPF片芯,包衣后考察体外释放度,结果见图2。

图2 不同崩解剂用量对药物释放的影响Figure 2 The effects of the amount of disintegrants of the core tablets on the release profiles
为了保证释药过程前期无明显的药物释放,由预实验可知:制剂的包衣增重必须大于5%才能实现。因此,崩解剂必须具有足够的量才能产生薄膜破裂所需的膨胀力,但崩解剂的大量加入会导致膜过早破裂,因而在制剂中必须控制其用量。由试验结果可知,当崩解剂的量大于30 mg时,即可实现4 h后包衣膜的破裂。
2.3.3填充剂的用量对释药行为的影响固定片芯以下组分和用量(KPF50mg,L-HPC 30 mg)不变,制备微晶纤维素与乳糖比例分别为110 ∶0,40 ∶70,20 ∶90,0 ∶110的片芯,包相同厚度衣层(增重8.9%),测定释放度。
结果表明,当乳糖量较少时,释放时滞较大;当达到40 ∶70时,随乳糖含量的增加,时滞基本不变,但释放速度减慢(见图3),因此MCC ∶乳糖的比值应不大于40 ∶70。但由于乳糖随水分子的渗入会逐渐溶解,减小片芯的体积,不利于片芯的膨胀,所以乳糖的加入量应控制在一定的范围内。由图3可知,当选取MCC与乳糖比例为40 ∶70即可满足脉冲控释片释放的要求。2.3.4致孔剂的用量对释药行为的影响制备片芯,改变包衣液中Eudragit L100与EC的比例(分别为55 ∶45,65 ∶35,75 ∶25,PEG6000为15%),包衣,制备包衣脉冲片,包衣增重9.1%,测定体外释放度,结果见图4。

图3 不同填充剂用量对药物释放的影响Figure 3 The effects of the amount of filler on the release profiles

图4 致孔剂用量对药物释放的影响Figure 4 The effects of the amount of pore-former on the release profiles
由图4可知,致孔剂Eudragit L100的用量对时滞时间影响较大。当Eudragit L100与EC比例为65 ∶35,时滞为4 h;增大Eudragit L100用量(75 ∶25),衣膜渗透性加强,时滞提前至2.5 h;降低Eudragit L100用量(55 ∶45),衣膜渗透性差,时滞时间显著延长为5.5 h。
2.3.5增塑剂种类对释药行为的影响制备片芯,改变包衣液中增塑剂种类分别为PEG4000、PEG6000、TEC及DEP(包衣液中Eudragit L100与EC的比例为65 ∶35,增塑剂用量为15%),包衣,制备包衣脉冲片,包衣层增重9.0%,测定体外释放度,结果见图5。
结果表明,增塑剂种类对时滞影响较大。以PEG6000为增塑剂,时滞4 h后,可以实现瞬间爆破。而含TEC、DEP的脉冲片,时滞分别为7.8 h和8.2 h。而在等量的前提下,PEG4000的时滞较靠前,因此本实验选用PEG6000为增塑剂。
2.3.6增塑剂的用量对释药行为的影响制备片芯,改变包衣液中增塑剂PEG6000的用量(分别为0%,10%,15%,20%,30%,包衣液中Eudragit L100与EC的比例为65 ∶35),包衣,制备包衣脉冲片,包衣层增重9.0%,测定体外释放度,结果见图6。
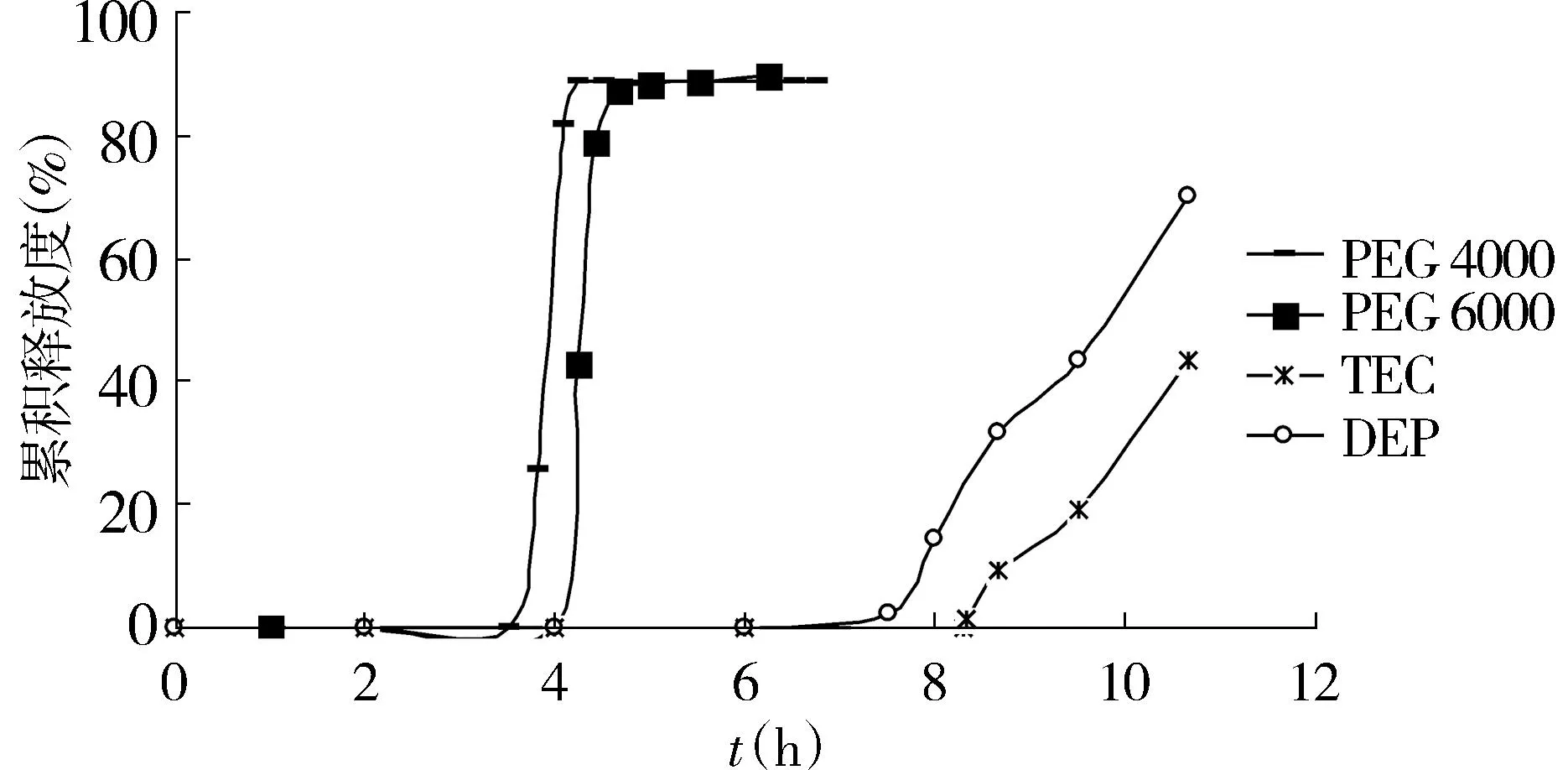
图5 增塑剂种类对药物释放的影响Figure 5 The effects of different plasticizers on the release profiles

图6 增塑剂用量对药物释放的影响Figure 6 The effects of the amount of plasticizer on the release profiles
由图6可知,增塑剂用量对时滞和脉冲释药时间均有较大影响。当增塑剂用量为0%时,时滞时间为6 h。增塑剂用量越大,时滞时间越短。这是因为增塑剂用量较大时包衣膜表面张力较小,黏附性差;而增塑剂用量过低则使包衣液表面张力较大,不易形成雾滴从喷枪中喷出。当用量大于15%之后,时滞基本变化不大。
2.3.7包衣增重对释药行为的影响制备片芯,按2.2.2项下的包衣液及包衣工艺条件,制备不同包衣厚度的脉冲片(包衣增重分别为5.3%,6.8%,9.0%,10%,12.1%),测定体外释放度,结果见图7。
由图7可知,包衣膜厚度对释药影响较大。包衣增重过小,衣膜薄,衣膜破裂所需的膨胀力亦小,导致制剂时滞较短;随包衣厚度增加,脉冲片时滞延长。随着包衣膜加厚,抗张能力加强,同时水分渗入片芯的速度和程度减慢。
2.4星点设计效应面法优化处方
2.4.1试验设计在单因素考察的基础上,我们选择对释药行为影响比较显著的3个因素作为考察因素,即L-HPC用量比例(X1),Eudragit L100用量比例(X2),包衣膜增重比例(X3)。选择时滞时间(Y1)和释药时间(Y2)为考察指标。按照星点设计原理设计了3因素5水平的实验方案,各因素水平代码值和实际操作物理量值见表1,具体试验设计和试验结果见表2。

图7 包衣增重对药物释放的影响Figure 7 The effects of coating level on the release profiles
表1各因素水平代码值和实际操作值(%)
Table 1Factors and levels of the central composite design experiments(%)

变量level-1.682-1011.682X159.315.521.726X25559.16570.975X35.56.9911.112.5
2.4.2星点设计效应面法优化结果采用Design Expert 8.0软件对各水平进行多元非线性回归[4],得到二项式拟合方程分别为:


采用Origin8.0软件绘制二次多项式模型中X1、X2、X3中任意两因素对各评价指标的效应面图(见图8-13)。
综合效果图8-13,以因变量时滞Tlag=3.75-4.25h,T=0.33-0.75h为目标值,将6个效果图自变量的最优区域取交集,即得最优处方区域为:L-HPC用量比例X1为13%-22%,Eudragit L100用量比例X2为55%-68%,包衣膜增重比例X3为7%-9%。
表2试验设计安排及测定结果
Table 2Results of the central composite design experiments

No.X1(%)X2(%)X3(%)Y1(h)Y2(h)115.5065.009.004.0830.500215.5065.005.502.3330.250315.5065.009.004.0000.50049.2670.9511.084.1670.667526.0065.009.004.0830.250621.7470.956.922.6670.125721.7470.9511.083.6670.33389.2659.056.923.5000.667915.5065.009.004.0000.5001021.7459.056.924.2500.333119.2670.956.922.8330.4161215.5065.0012.505.7500.8331315.5055.009.004.4170.667149.2659.0511.085.0830.7501515.5075.009.002.5000.250165.0065.009.004.2770.8331715.5065.009.004.0830.5001815.5065.009.004.0830.5001921.7459.0511.085.5000.3332015.5065.009.004.0000.500

图8 X3=9%时Y1对X1、X2的效应面Figure 8 The response surface of Y1 with X1, X2 under the condition of X3=9%
2.4.3优化处方的验证为验证所建立模型的预测能力,按照星点设计效应面优化法制备一批在星点设计中没有考察的处方[5]。选取目标值Tlag=4.0 h,T=0.5 h,固定Eudragit L100用量比例X2=65%包衣膜增重比例X3=9%,可得L-HPC用量比例X1=20%。按上述处方平行制备三批酮洛芬薄膜包衣脉冲控释片,进行溶出度测定并绘制溶出曲线,所得平均溶出曲线见图14,并考察其实测值,结果见表3。

图9 X2=65%时Y1对X1、X3的效应面Figure 9 The response surface of Y1 with X1, X3 under the condition of X2=65%

图10 X1=15.5%时Y1对X2、X3的效应面Figure 10 The response surface of Y1 with X2, X3 under the condition of X1=15.5%

图11 X3=9%时Y2对X1、X2的效应面Figure 11 The response surface of Y2with X1, X2 under the condition of X3=9%

图12 X2=65% 时Y2对X1、X3的效应面Figure 12 The response surface of Y2 with X1,X3 under the condition of X2=65%

图13 X1=15.5%时Y2对X2、X3的效应面Figure 13 The response surface of Y2 with X2, X3 under the condition of X1=15.5%
由结果可见,优化范围内优化处方的实测值均在目标区域内。
因此,确定酮洛芬脉冲控释片的优化处方是:片芯处方为KPF 50 mg(25%),MCC 40 mg(20%),乳糖70 mg(35%),L-HPC 40 mg(20%);包衣液处方为Eudragit L100与EC比例是65 ∶35,PEG6000 15%,包衣增重9.0%。

图14 星点设计验证试验Figure 14 The verification result of the central composite design
表3星点设计验证试验目标值结果
Table 3Comparison of target value and true value

参数 目标区域实测值Tlag(h)3.75-4.253.75T(h)0.33-0.750.50
3讨论
本研究制备的酮洛芬薄膜包衣脉冲控释片原理为膜时控-崩解原理,使用的崩解剂是具有良好溶胀作用的H-LPC,且与MCC混用,可压性良好。以CMS-Na为崩解剂的脉冲片释药速率较以L-HPC为崩解剂的慢,脉冲时间长,原因可能是由于CMS-Na吸水后,虽然胀破衣膜能力强,但其以水凝胶形式的状态存在,减缓了释药速率[6]。
包衣膜中的Eudragit L100是pH敏感性材料,其在酸中不溶,当介质pH>6时开始溶解,在包衣膜中起致孔剂作用[7]。在pH>6的介质中,Eudragit L100首先溶解产生小孔,水分通过小孔渗透进入片芯,片芯吸水膨胀,衣膜瞬间爆破,实现脉冲释放。Eudragit L100含量越大,孔隙越多,在相同时间内水分渗入量大,因此脉冲释放时间短。
以PEG6000为增塑剂的衣膜在体内水化后,机械强度及抗张强度显著降低,易于破裂[8]。而含TEC、DEP脉冲片的时滞较长,原因是TEC、DEP为脂溶性增塑剂,不溶于释放介质,导致水分渗透入片芯的速度较慢,时滞较长,同时以TEC、DEP为增塑剂的衣膜,其抗张强度较强,具有优良的机械性能,水化后不易破裂。
星点设计效应面法是近年来国内外应用较多的一种实验设计方法,与正交设计、均匀设计相比,可基于线性和非线性模型进行数据分析[9],建立因素与响应值之间的函数关系式,效应曲线图更直观地反映了效应值随各因素的变化趋势。星点实验的设计范围比较精确,由效应面图所得到的最优值区域也比较大,即在较大的范围内设计处方都能够达到目标值要求[5]。本研究在充分预实验和单因素考察实验的基础上,利用星点设计效应面法优化处方设计,达到预期释放目标。说明该方法有效、可行,可用于酮洛芬薄膜包衣脉冲控释片的处方制备。
参考文献:
[1]何绍雄.时间药理学与时间治疗学[M].天津:天津科学技术出版社,1993:46-201.
[2]Lemmer B.Circadian rhythms and drug delivery[J].J Controlled Release,1991,16(122):63-74.
[3]郭映君,邱诗,孙辉辉,等.酮洛芬缓释微丸的制备及体外药物释放考查[J].中国药剂学杂志,2009,7(4):218-226.
[4]罗旦朝,魏杨一方,江洁,等.氯沙坦钾氢氯噻嗪渗透泵片的制备及星点设计优化处方[J].中国新药杂志,2014,23(22):2671-2677.
[5]刘强,徐赫鸣,李钊,等.星点设计-效应面法优化盐酸地尔硫片择时释放渗透泵控释片[J].中国新药杂志,2013,22(9):1094-1099.
[6]范田园,魏树礼,严文伟,等.盐酸地尔硫片爆破型延迟-脉冲缓释片研究[J].药学学报,2002,37(3):221-225.
[7]顾纪锋,张娜,席延卫,等.富马酸美托洛尔爆破型脉冲片体外实验研究[J].中国药学杂志,2006,41(20):1560-1564.
[8]张立超,胡晋红,李珍,等.丙烯酸树脂包衣控释膜中增塑剂的优选[J].药学学报,2001,36(12):937-942.
[9]李娇,王扣存,棕莉.扎来普隆脉冲释放微丸的制备及体外释放[J].中国现代应用药学,2012,29(10):924-930.
Preparation of film-coated tablets for pulsed-controlled release of ketoprofen
LI Caiyan1*,LI Xinliang2
(1DepartmentofPharmacy,ShanxiMedicalCollegeforContinuingEducation,Jinzhong030619,China;2DepartmentofOrthopedics,RenminHospitalofLishiDistrict;*Correspondingauthor,E-mail:abc-lcy@163.com)
Abstract:ObjectiveTo develop a pulsed-controlled release system of ketoprofen for bedtime dosing and released drug in the early morning.MethodsThe tablet core was prepared by the wet-granulation and spray coated with controlled-release film. Based on the single factor study on disintegrant, filler, pore-former, plastifier and the weight gain of controlled membrane in the tablet core and film, the central composite design and response surface method was chosen to optimize the formula.ResultsThe single factor study showed that the disintegrant, pore-former and the weight gain of controlled membrane had significant effect on the lag time of drug release. The optimum formula was that tablet core was composed of KPF 50 mg(25%),MCC 40 mg(20%),lactose 70 mg(35%) and L-HPC 40 mg(20%), and that film was composed of Eudragit L100 ∶EC of 65 ∶35,PEG 6000(15%), the weight gain of controlled membrane(9.0%). This preparation had a lag time of about 3.75 h, and the release time was about 0.5 h.ConclusionThe film-coated tablets for pulsed-controlled release of ketoprofen are timing and quickly released tablets.
Key words:ketoprofen;pulsed-controlled release tablets;release drug;central composite design and response surface method
[收稿日期:2015-11-20]
作者简介:李彩艳,女,1986-01生,硕士,助教,E-mail:abc-lcy@163.com.
中图分类号:TQ460.6
文献标志码:A
文章编号:1007-6611(2016)02-0132-07
DOI:10.13753/j.issn.1007-6611.2016.02.007
