石灰石煅烧/碳酸化过程中微观结构的演变特性
2013-09-21危日光陈江涛陈鸿伟
危日光, 陈江涛, 陈鸿伟, 陈 龙
(华北电力大学 能源动力与机械工程学院,保定071003)
石灰石分解的早期研究主要针对脱除化石燃料燃烧过程中产生的SO[1-2]x.近年来,温室气体CO2的收集和回收成了广大科研工作者关注的焦点.利用来源广泛、价格低廉的石灰石等钙基吸收剂循环煅烧/碳酸化反应(cyclic calcination/carbonation reaction,CCCR)法分离燃煤电厂烟气中的CO2日益受到各国学者的普遍关注[3-6].
对于钙基吸收剂CCCR法,大量的研究主要集中在:(1)钙基吸收剂CCCR宏观动力学特性;(2)钙基吸收剂循环碳酸化转化率的变化规律及钙基吸收剂的改性;(3)基于钙基吸收剂CCCR法的双循环流化床反应器的设计与实现[7].目前,有关钙基吸收剂CCCR过程中产物微观结构特性的研究相对较少.在钙基吸收剂CCCR过程中,煅烧产物的孔隙结构直接决定了碳酸化转化率的变化规律,同时也间接影响到宏观动力学特性,而且钙基吸收剂的改性归根为微观结构的改良,因此深入研究微观结构特性对更好地理解钙基吸收剂CCCR宏观特性具有重要意义.
一些学者已经对CaO的微观结构特性进行了研究.Gullett等[8]通过对比水合CaO和普通CaO微观结构特性的异同,对水合CaO高效脱硫的根本原因进行了分析.王宏等[9]研究了O2/CO2方式下钙基吸收剂脱硫过程中微观结构的变化特性.近年来,李英杰等[10]对不同循环次数的煅烧产物CaO的微观结构变化特性进行了深入研究.王春波等[11]对钙基吸收剂产物CaO的孔径分布进行了模拟.笔者在上述科研工作者长期对石灰石脱硫、脱碳研究的基础上,选择一次煅烧/碳酸化反应法对过程产物进行了微观结构分析,得到基本的微观结构演变规律.
1 试验样品和试验方法
选取保定的天然石灰石,经破碎和筛分,取粒度在48~62μm的石灰石颗粒作为试验样品,其化学成分见表1.

表1 石灰石样品的化学成分Tab.1 Chemical composition of the limestone sample %
采用热重分析仪对石灰石进行煅烧/碳酸化试验,实时得到试样的热重曲线,并通过后续的数据处理软件得到转化率x-t曲线.热重分析仪的称重范围为±200g,测温范围为0~1 000℃,灵敏度为0.1mg,重复性试验误差为±1%,试验装置示意图见图1.
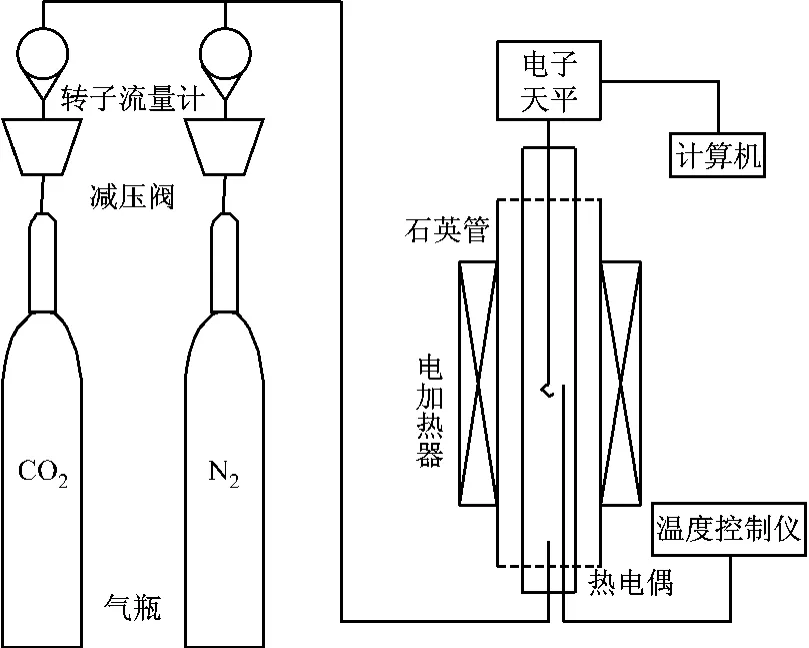
图1 试验装置示意图Fig.1 Schematic diagram of the experimental apparatus
试验条件如下:煅烧温度为900℃,煅烧气氛为N2,流量为1 000mL/min;碳酸化温度为700℃,碳酸化气氛为150mL/min的CO2和850mL/min的N2混合而成.试验过程如下:称取样品并将其放入坩埚内,在设定的煅烧条件下对石灰石进行煅烧试验.煅烧试验完成后,将试验条件调节到设定的碳酸化条件,对煅烧产物进行碳酸化试验.不同煅烧/碳酸化时间样品的表面空隙结构采用美国Micromeritics公司生产的TristarⅡ3020全自动比表面积和孔隙度分析仪进行分析,将该仪器放入液氮饱和温度(77K)下进行静态等温吸附测量,根据吸附/脱附曲线采用BET法计算样品的比表面积,并采用BJH法得到样品的比孔容、孔容分布及表面积分布.
2 试验结果与讨论
2.1 石灰石煅烧/碳酸化特性
图2给出了石灰石煅烧/碳酸化反应的转化率曲线.由图2可知:石灰石煅烧分解反应迅速,煅烧转化率呈线性提高,煅烧过程基本由化学反应阶段控制,到6.5min时已完全分解;碳酸化反应首先是反应速率较快的化学反应控制阶段,然后随着反应转化率的提高,速率明显降低,最后变化逐渐趋于平缓,并进入产物层扩散阶段.由于产物层扩散阻力的存在,导致碳酸化转化率不能达到100%,本试验中碳酸化12min时的转化率只有73%左右.

图2 石灰石煅烧/碳酸化转化率Fig.2 Calcination and carbonation conversion rate of limestone
2.2 氮吸附/脱附等温线
图3给出了石灰石不同煅烧/碳酸化反应阶段的氮吸附/脱附等温线.由图3可知:原始石灰石在低压、中压阶段的吸附量很小,说明原始石灰石中微孔和中孔数量极少,在高压阶段,吸附曲线较陡,说明原始石灰石存在一些大孔,这些大孔可能是由颗粒之间的堆积、颗粒表面的凹坑以及缺陷等组成的,但由于最大吸附量仅为1.3cm3/g,说明大孔的数量不多.依据1940年Brunauer等提出的吸附等温线分类方法,其他7种工况的氮吸附/脱附等温线为Ⅳ型.Ⅳ型等温线的特点是固体表面与第1层(单分子层)吸附分子的吸附作用能E1大于第n层(n>1)和第(n+1)层的吸附作用能En,则固体表面具有中孔与大孔.脱附等温线与吸附等温线不重合,脱附等温线在吸附等温线的上方,产生吸附滞后环[11].显然,图3中8种工况的样品皆出现了吸附滞后现象,但只有图3(b)~图3(f)中出现了闭合的吸附滞后环.根据国际纯粹与应用化学联合会(IUPAC)的分类方法,此吸附滞后环的类型为H1型.H1型滞后环所反映的典型孔结构是两端开口的圆筒形孔,由于此形状的孔在吸附时弯月形液面的形成过程和脱附时弯月形液面的消失过程不同,导致吸附滞后环出现[12].另外,图3(a)、图3(g)和图3(h)中的吸附/脱附等温线并未闭合,可能是样品中微孔数量较少的缘故.通过对比吸附滞后环的大小可知,随着煅烧过程的进行,吸附滞后环有减小的趋势.但是,随着碳酸化的进行,吸附滞后环却会增大.滞后环的大小反映一定的孔结构.滞后环减小说明中孔孔径分布变窄,即随着煅烧过程的进行,中孔孔径分布变窄,微孔和大孔增加.反之,滞后环的增大说明碳酸化过程中微孔和大孔孔径分布变窄,中孔孔径分布相对变宽.
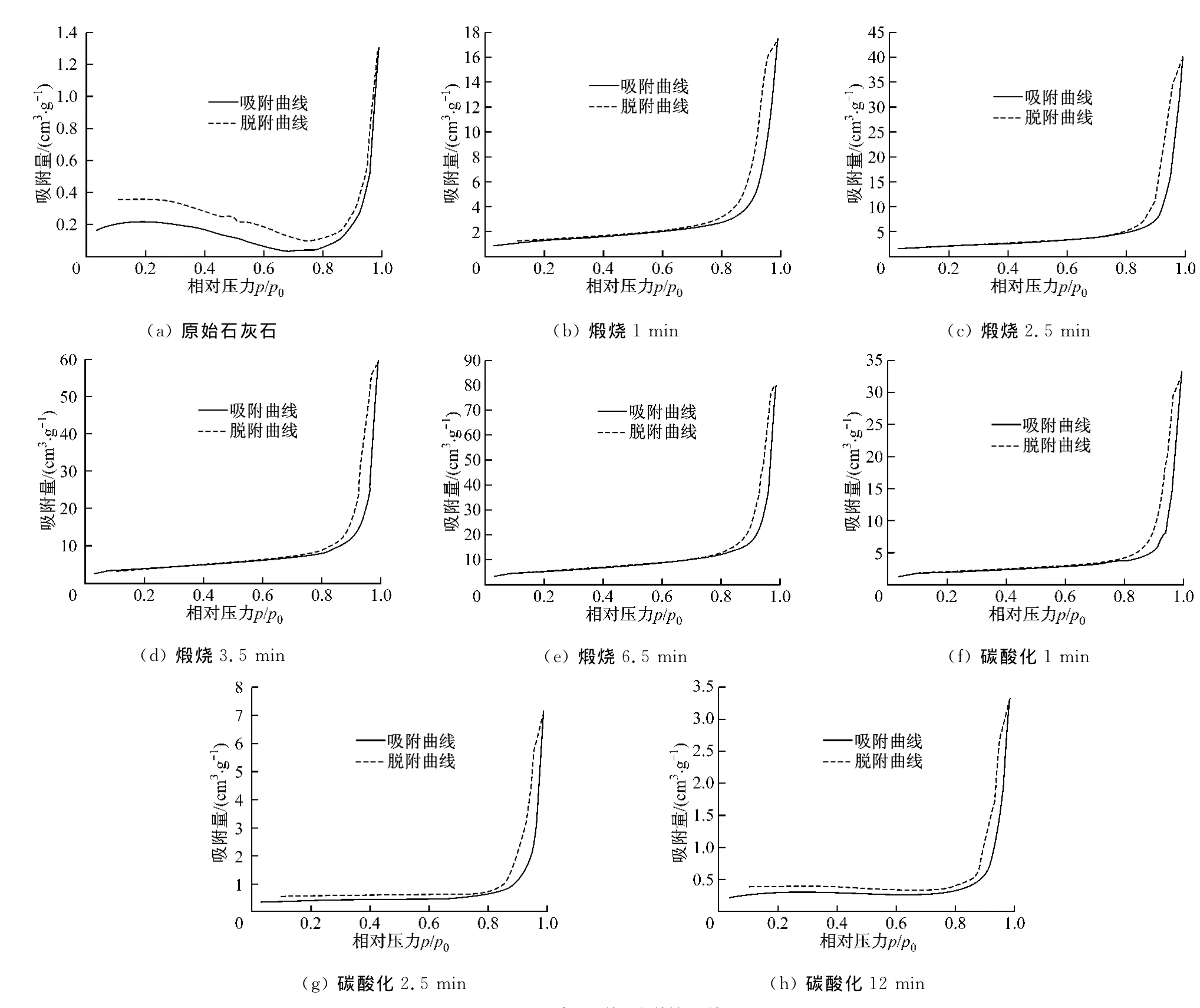
图3 氮吸附/脱附等温线Fig.3 Nitrogen adsorption-desorption isotherms
2.3 石灰石煅烧/碳酸化反应过程中产物的比表面积和比孔容

图4 石灰石不同反应过程中产物的比表面积和比孔容Fig.4 Variation of specific surface area and pore volume during calcination and carbonation process
比表面积和比孔容是表征材料微观结构的典型参数.石灰石在煅烧/碳酸化反应过程中因中间产物的成分不同,则其表面特性也不相同.图4给出了石灰石煅烧和碳酸化过程中产物的比表面积和比孔容.由图4可知:原始石灰石的比表面积和比孔容均较小,煅烧反应促使煅烧产物的比表面积和比孔容随着煅烧时间的增加呈线性增加,但碳酸化反应的进行却导致碳酸化产物的比表面积和比孔容呈指数规律迅速衰减,由煅烧而获得的较大比表面积和比孔容在碳酸化快速反应阶段基本耗尽.具体变化为:石灰石煅烧1min后产物的比表面积和比孔容与原始石灰石相比,分别增长7.6倍和13.7倍,而煅烧2.5min后产物的比表面积和比孔容与原始石灰石相比,分别增长13.2倍和31.6倍.经比较可知,煅烧过程中比孔容的增长速度比比表面积的增长速度快.石灰石煅烧6.5min后完全分解且未产生烧结,此时比表面积和比孔容均达到最大,分别为原始石灰石的30.5倍和62.7倍.当碳酸化1min后,碳酸化产物的比表面积和比孔容迅速衰减为最大值的33%和41%;当碳酸化2.5min后,石灰石产物的比表面积和比孔容基本耗尽,分别衰减至最大值的7%和9%.当对石灰石继续进行碳酸化时,碳酸化进程逐渐过渡到扩散控制阶段,碳酸化转化率从2.5 min到12min只提高了0.1左右,比表面积和比孔容衰减至最大值的5%和4%,但仍为原始石灰石的1.5倍和2.6倍.因此,随着碳酸化时间的延续,碳酸化转化率会继续缓慢提高,以逐渐耗尽剩余的比表面积和比孔容.
2.4 石灰石煅烧/碳酸化反应过程中产物的孔分布
在石灰石煅烧/碳酸化反应过程中,产物的孔分布包括孔面积分布和孔容积分布,它们显示了不同大小孔隙所占的孔面积和孔容积.孔分布的变化可以客观地反映出石灰石煅烧/碳酸化过程中孔结构的变化.根据IUPAC对孔径尺寸的分类,孔径小于2nm的为微孔,介于2~50nm的为中孔,大于50 nm的为大孔[13].微孔为石灰石煅烧/碳酸化反应提供巨大的内表面,中孔是进入微孔的主通道,大孔则是输送参加反应组分的粗通道.
图5给出了石灰石煅烧/碳酸化过程中不同尺寸的孔对孔面积和孔容积的贡献.从图5可知:随着石灰石煅烧/碳酸化反应的进行,煅烧/碳酸化产物的孔分布呈有规则的变化.从图5(a)可知:原始石灰石基本上为无孔形态,因此其比表面积和比孔容均很小.经煅烧1min后,双峰凸显,微孔、中孔和大孔出现,但3种孔的总体数量较少,因此此时煅烧产物的比表面积和比孔容仍然较小.在煅烧2.5min后,第1峰变化不大,但第2峰的峰值迅速增大,说明中孔快速形成,促使比表面积和比孔容进一步增大,中孔在煅烧过程中快速形成是比孔容相对比表面积增大更快的主要原因.当煅烧至6.5min时,石灰石完全分解,CaO的孔隙基本形成,主要由中孔和大孔构成,但仍存在一定量的微孔,孔容分布呈双峰结构,第1峰分布在1.7~10nm,第2峰分布在10~80nm,峰值均达到最大,同时比表面积和比孔容也达到最大值.经碳酸化1min后,孔容的双峰峰值锐减,剩余孔隙与煅烧1min后的产物类似,孔的数量较少.经碳酸化2.5min和12min后,碳酸化产物的孔容分布基本相同,微孔基本消失,只剩下极少量的中孔和大孔.
图5(b)和图5(c)反映了不同类型的孔对孔容积和孔面积的贡献程度.随着石灰石煅烧反应的进行,微孔对孔容积的增加几乎没有贡献,而对孔面积的增加有一定的贡献;中孔和大孔对孔容积和孔面积的贡献均较大.碳酸化反应为煅烧反应的逆反应,煅烧反应获得的孔容积和孔面积在碳酸化反应过程中加以消耗.从图5(b)和图5(c)可知:随着碳酸化反应的进行,微孔、中孔和大孔所贡献的孔容积和孔面积被同时消耗.当反应趋于稳定时,孔容积和孔面积几乎被消耗殆尽.图5(d)为孔径变化时的累积孔面积.从图5(d)可知:煅烧反应的进行使孔面积不断增大,而碳酸化反应的进行则使孔面积不断减小,在微孔处出现的曲线陡峭进一步说明了微孔对孔面积的增加有较大的影响.
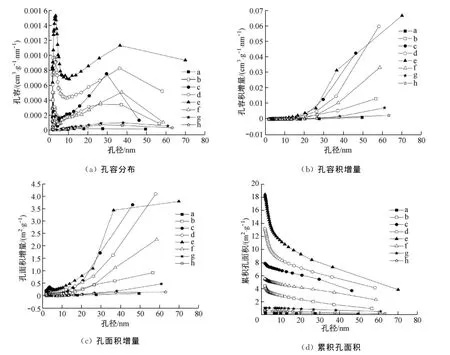
图5 石灰石煅烧/碳酸化过程中不同尺寸的孔对孔面积和孔容积的贡献Fig.5 Contributions of differently sized pores to the surface area and pore volume during calcination and carbonation process
2.5 微观结构参数与煅烧/碳酸化转化率的关系
在石灰石煅烧/碳酸化反应过程中微观结构演变规律的基础上,笔者进一步研究了微观结构参数与煅烧/碳酸化转化率的关系.图6给出了比表面积和比孔容与转化率的关系.由图6可知:随着比表面积和比孔容的增大,石灰石煅烧转化率呈线性增大趋势,但是CaO的碳酸化转化率则呈指数衰减.试验数据与拟合曲线的最小相关系数为0.98,说明微观结构参数与转化率之间存在较好的函数关系.从微观结构参数与转化率之间的函数关系可以看出:石灰石煅烧/碳酸化反应的实质是微观结构参数的变化,而转化率只是宏观的表现.综上分析得出:从宏观层面上看,石灰石在煅烧过程中的转化率随着时间的延长呈线性提高;从微观层面上看,各种类型的孔相继出现,数量不断增加,表明孔结构参数的比表面积和比孔容也随着时间的延长呈线性增大,因此转化率与比表面积、比孔容也保持了较好的线性关系.但是,碳酸化反应只在初期的化学反应阶段反应较快,而在后续的产物层扩散阶段反应较缓慢,因此煅烧生成的大量孔隙在化学反应阶段被快速填充,最终导致比表面积和比孔容呈指数规律快速衰减.总之,煅烧反应促使比表面积和比孔容不断增大,碳酸化反应则不断地消耗由煅烧过程获得的比表面积和比孔容,煅烧/碳酸化反应过程实质上就是微观孔隙循环生成与消耗的过程.

图6 比表面积和比孔容与转化率的关系Fig.6 Relationship between specific surface area,pore volume and the conversion rate
3 结 论
(1)石灰石不同煅烧/碳酸化阶段产物的氮吸附/脱附等温线为Ⅳ型.随着煅烧反应的进行,煅烧产物先出现了H1型吸附滞后环,之后碳酸化反应导致吸附/脱附等温线在低压段分离,虽然滞后现象依然存在,但吸附滞后环消失.在煅烧/碳酸化进程中,吸附滞后环呈现出先减后增的趋势,间接反映了孔径分布的变化规律.
(2)石灰石在煅烧前比表面积和比孔容均较小,煅烧反应促使煅烧产物的比表面积和比孔容随着煅烧时间的增加呈线性增加,而碳酸化反应则导致碳酸化产物的比表面积和比孔容均呈指数规律迅速衰减,由煅烧获得的较大比表面积和比孔容在碳酸化快速反应阶段基本耗尽.
(3)石灰石完全分解产物的孔容积分布曲线呈双峰结构,第1峰分布在1.7~10nm,第2峰分布在10~80nm.在煅烧初期,双峰凸显;随着煅烧反应继续,双峰峰值不断增大,在完全煅烧且未产生烧结时,峰值达到最大.碳酸化反应导致双峰峰值锐减,在2.5min后双峰基本消失.微孔、中孔和大孔对孔容积和孔面积增加的贡献不同.微孔只对孔面积的增加有一定贡献,而中孔和大孔对孔容积和孔面积的增加均有较大贡献.(4)微观结构参数与转化率之间存在较好的函数关系.随着比表面积和比孔容的增大,石灰石煅烧转化率呈线性增大趋势,而CaO的碳酸化转化率则呈指数衰减.从它们的函数关系可以得出,石灰石煅烧/碳酸化反应的实质是微观结构参数的变化,而转化率只是宏观的表现.
[1]汤龙华,赵长遂,侯栋歧.石灰石颗粒在高温气流中热解脱硫过程的研究[J].动力工程,1997,17(6):62-68.TANG Longhua,ZHAO Changsui,HOU Dongqi.Research on calcination and desulfurization with limestone injection into the furnace[J].Journal of Power Engineering,1997,17(6):62-68.
[2]董建勋,李振中,冯兆兴,等.石灰石炉内高温煅烧脱硫及产物活性的试验[J].动力工程,2004,24(5):711-715.DONG Jianxun,LI Zhenzhong,FENG Zhaoxing,et al.Experimental research on desulfurization of limestones and activity of calcination products in furnace[J].Journal of Power Engineering,2004,24(5):711-715.
[3]陈传敏,赵长遂,梁财,等.O2/CO2气氛下石灰石脱硫特性的研究[J].动力工程,2005,25(6):883-887.CHEN Chuanmin,ZHAO Changsui,LIANG Cai,et al.Study on desulfurization characteristics of limestone in a O2/CO2atmosphere[J].Journal of Power Engineering,2005,25(6):883-887.
[4]ABANADES J C,ANTHONY E J,WAN G J,et al.Fluidized bed combustion systems integrating CO2capture with CaO [J].Environ Sci Technol,2005,39(8):2861-2866.
[5]SALVADOR C,LU D,ANTHONY E J,et al.Enhancement of CaO for CO2capture in an FBC environment[J].Chem Eng J,2003,96(3):187-195.
[6]STANMORE B R,GILOT P.Review calcinations and carbonation of limestone during thermal cycling for CO2sequestration [J].Fuel Process Technol,2005,86(16):1707-1743.
[7]蔡宁生,房凡,李振山.钙基吸收剂循环煅烧/碳酸化法捕集CO2的研究进展[J].中国电机工程学报,2010,30(26):35-44.CAI Ningsheng,FANG Fan,LI Zhenshan.Research and development on cyclic calcinations/carbonation reaction with Ca-based sorbents to CO2capture from flue gases[J].Proceedings of the CSEE,2010,30(26):35-44.
[8]GULLETT B K,BRUCE K R.Pore distribution changes of calcium-based sorbents reacting with sulfur dioxide[J].AIChE J,1987,33(10):1719-1726.
[9]王宏,张礼知,陆晓华,等.O2/CO2方式下钙基吸收剂在脱硫过程中微观结构变化的研究[J].工程热物理学报,2001,22(1):127-130.WANG Hong,ZHANG Lizhi,LU Xiaohua,et al.Microstructure changes of calcium-based sorbent during desulfurization in O2/CO2mixture[J].Journal of Engineering Thermophysics,2001,22(1):127-130.
[10]李英杰,赵长遂,陈惠超.循环煅烧/碳酸化反应中CaO微观结构变迁特性[J].东南大学学报:自然科学版,2009,39(2):262-269.LI Yingjie,ZHAO Changsui,CHEN Huichao.Variation behavior of CaO microstructure during cyclic calcination/carbonation[J].Journal of Southeast University:Science and Technology,2009,39(2):262-269.
[11]王春波,李永华,危日光,等.钙基吸收剂煅烧过程中产物CaO孔径分布的模拟[J].动力工程,2007,27(4):625-629.WANG Chunbo,LI Yonghua,WEI Riguang,et al.Simulation of pore size distribution of process produced CaO during calcination of calcium-based sorbents[J].Journal of Power Engineering,2007,27(4):625-629.
[12]近藤精一,石川达雄,安部郁夫.吸附科学[M].北京:化学工业出版社,2005.
[13]徐如人,庞文琴.分子筛与多孔材料化学[M].北京:科学出版社,2004:145-148.
