HPLC法测定右旋糖酐40原料中5-羟甲基糠醛的含量
2013-09-10刘海静王嫦鹤丁丽霞杜冠华陕西省食品药品检验所西安7006陕西中医学院中国药学会中国医学科学院北京协和医学院药物研究所
刘海静,雷 琨,王嫦鹤,王 发,丁丽霞,杜冠华(陕西省食品药品检验所,西安 7006; 陕西中医学院; 中国药学会; 中国医学科学院北京协和医学院药物研究所)
右旋糖酐是蔗糖经肠膜状明串珠菌L.M-1226号菌发酵后生成的高分子葡萄糖聚合物,能沉积在红细胞膜上,使红细胞聚集,因此在临床上常使用右旋糖酐40作血浆扩容剂[1]。发酵法生产工艺中使用的培养基以高浓度蔗糖为主,肠膜状明串珠菌培养16~20h,多糖产量即可达到最高值。右旋糖酐的理论产率约为蔗糖的47%,但实际上仅为20%~30%。由于大分子右旋糖酐作为血浆代用品安全性较差,因此须用稀酸水解,以获得较低分子量的药用右旋糖酐;但是水解的同时,也会使部分右旋糖酐分解成低聚糖,经异麦芽三糖、异麦芽二糖,最终生成葡萄糖[2]。5-羟甲基糠醛 (5-HMF)是己糖 (葡萄糖、果糖等单糖)与氨基酸发生美拉德 (Maillard)反应的降解产物[3],即己糖 (葡萄糖、果糖等单糖)与氨基酸在高温、酸性条件或微生物的作用下脱水生成的醛类化合物。5-HMF过量存在会对人身体有损害[4],因此,《中国药典》2010年版二部在含有葡萄糖的注射剂项下均增加了5-HMF的限度检查,以确保葡萄糖注射液用药的安全性。本实验室的前期研究结果表明,右旋糖酐40氯化钠注射液中含有少量的5-HMF,含量约为0.25mg·L-1。本研究参考有关文献[5-7],建立了用HPLC法测定右旋糖酐40原料中5-HMF含量的方法,对收集到的国内5个生产厂家提供的9批右旋糖酐40原料中5-HMF的含量进行考察,为该药品质量标准的修订和提高奠定基础。
1 仪器与试药
1.1 仪器
Waters Alliance 2695高效液相色谱仪,Waters 2487紫外检测器;Waters 2996二极管阵列检测器;塞多利斯ME-235S型电子分析天平。
1.2 试药
5-HMF对照品 (中国药品生物制品检定所,化学纯,批号:111626-200905)。右旋糖酐40原料 (国内5个厂家共9批原料);甲醇 (美国Tedia公司,色谱纯);磷酸 (国药集团化学试剂有限公司,分析纯);水为北京同泰联科TTL-10B超纯水(18.2Ω),其余试剂均为分析纯。
2 方法与结果
2.1 色谱条件
色谱柱:Kromasil C18柱 (4.6mm×250mm,5μm);流动相:1.0g·L-1磷酸溶液-甲醇 (90∶10);检测波长:284nm;流速:1.0mL·min-1;柱温: (35±5)℃;进样量:20μL。理论板数:4630;分离度:2.1。
2.2 对照品储备液的制备
精密称取5-羟甲基糠醛 (5-HMF)对照品10.00mg,用水稀释并定容于100mL量瓶中,摇匀,作为对照品储备液。
2.3 供试品溶液的制备
取5个厂家共9批右旋糖酐40原料,每批约6g,分别置9个100mL量瓶中,加适量流动相超声 (功率:45W,频率:59kHz)20min使溶解,定容,用0.45μm微孔滤膜滤过,取续滤液,作为供试品溶液。
2.4 系统适用性试验
取空白溶液 (流动相)、对照品溶液、供试品溶液各20μL,注入液相色谱仪,经 Waters 2487紫外检测器记录色谱图,见图1。结果显示,空白溶液对5-HMF测定无干扰,各色谱峰分离良好。

图1 HPLC色谱图
2.5 线性关系考察
分别精密量取对照品储备液适量,用流动相稀释制成质量浓度分别为 0.1、0.5、1、2、5、10μg·mL-1的对照品溶液。分别精密量取上述溶液各20μL,注入液相色谱仪,采用 Waters 2487紫外检测器,按 “2.1”项下色谱条件分别测定,以峰面积Y对质量浓度X作线性回归,得线性方程:Y=6.7412×104X-1.1307×103r=1.000
结果表明,5-羟甲基糠醛在0.100~10.00μg·mL-1浓度范围内与峰面积呈良好的线性关系。
2.6 紫外色谱鉴定图
分别精密量取浓度为2μg·mL-1的对照品溶液和批号为20091214的供试品溶液各20μL,注入液相色谱仪,采用Waters 2996二极管阵列检测器进行分析,分别提取对照品色谱图中主峰位置的紫外全扫描图谱和样品中相应位置色谱峰的紫外全扫描图谱,见图2。由图2可见,样品中杂质和对照品5-羟甲基糠醛紫外全扫描光谱图一致。
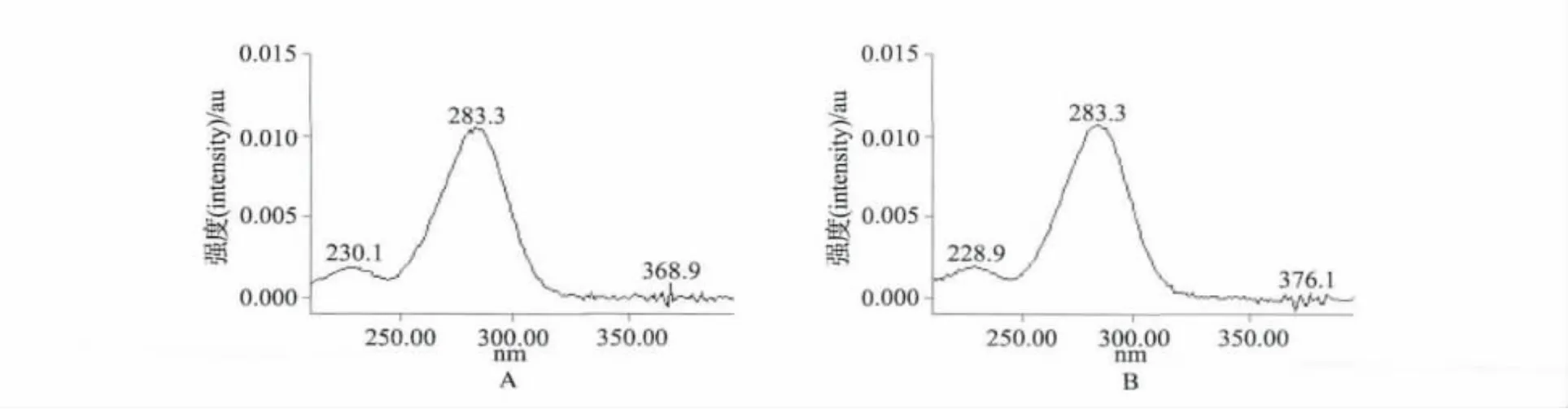
图2 5-羟甲基糠醛紫外全扫描图
2.7 精密度试验
取线性关系考察项下质量浓度为2μg·mL-1的对照品溶液,连续进样6次,测定峰面积,计算5-羟甲基糠醛峰面积平均值为15146,RSD为0.6%。
2.8 重复性试验
取同一厂家原料样品 (批号:100520)6份,按 “2.3”项下方法制备供试品溶液,按上述色谱条件进行测定,计算5-羟甲基糠醛含量平均值为2.37μg·mL-1,RSD为0.3%。
2.9 稳定性试验
取同一供试品溶液,分别于配制后0、1、4、8和12h,在上述色谱条件下进样测定,计算5-羟甲基糠醛峰面积平均值为13648,RSD为0.4%。表明供试品溶液在12h内基本稳定。
2.10 加样回收率试验
取已知5-羟甲基糠醛含量的原料样品 (批号:100520)12g,置于1个200mL量瓶中,加适量流动相超声 (功率:45W,频率:59kHz)20min使溶解,定容,用0.45μm微孔滤膜滤过,依次用10mL胖肚移液管精密移取9份续滤液置于20mL容量瓶中,每3份为1组,每组分别精密加入10mL含量为10、20、30μg的对照品溶液,按上述色谱条件测定,计算回收率,结果见表1。表明该方法回收率良好。
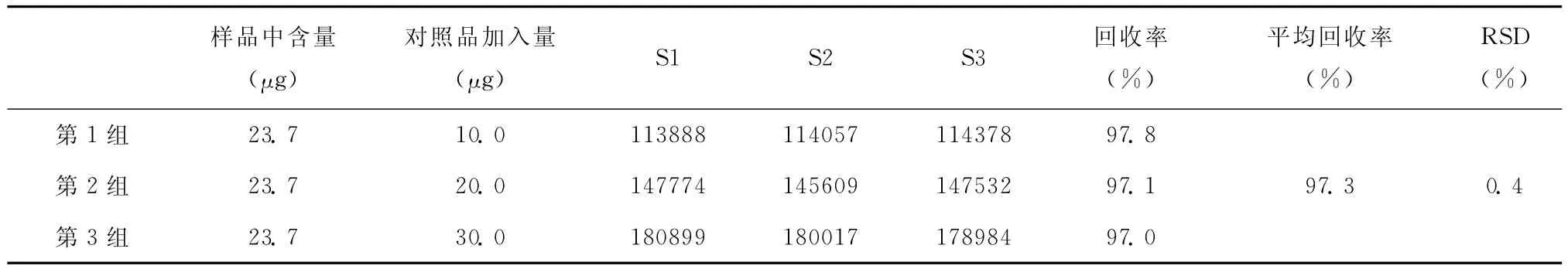
表1 回收率试验结果
2.11 样品含量测定
分别精密量取供试品溶液和质量浓度为2μg·mL-15-羟甲基糠醛对照品溶液各20μL,注入液相色谱仪,按上述色谱条件分别测定,按外标法以峰面积计算5-羟甲基糠醛含量。测定5个厂家共9批原料样品,样品中所含5-HMF结果见表2。

表2 右旋糖酐40原料中5-羟甲基糠醛测定结果
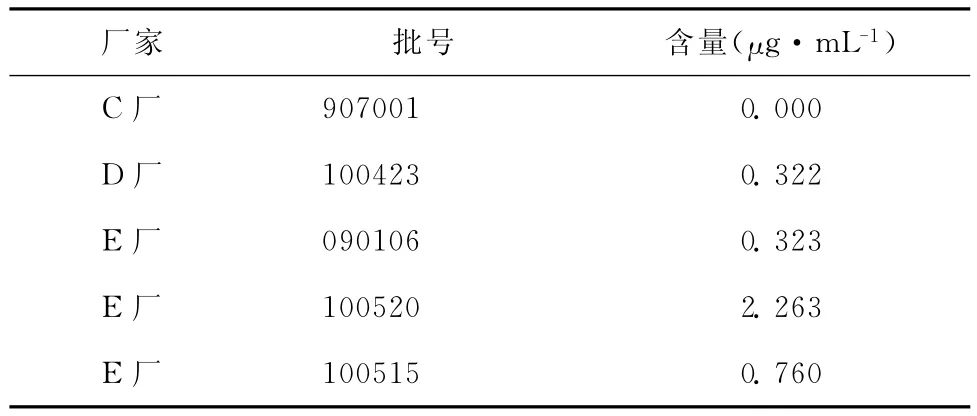
(续表2)
3 讨论
5-HMF限度检查是葡萄糖制剂中重要的质量控制指标,但检查右旋糖酐40原料中5-HMF的含量目前尚未见报道。笔者采用HPLC法进行检测,结果9批右旋糖酐40原料均检测出了5-HMF。分析其产生的原因:右旋糖酐40是葡萄糖的聚合物,其原料在发酵过程中的高温或酸性条件下,可能会产生少量的5-HMF,并且随原料被引入到右旋糖酐40的制剂中。由于其潜在的危害性,因此有必要对右旋糖酐40原料中5-羟甲基糠醛进行控制。
[1]黄勋,陈槐卿,王玲,等.右旋糖酐40,70对红细胞与内皮细胞粘附的影响 [J].生物医学工程学杂志,1998,15(3):240-242.
[2]李艳,陈学武,牟德华.右旋糖酐的生产及应用 [J].山西食品工业,1998,3:36-37.
[3]杨朝霞,李梅,董建军,等.高效液相色谱同时测定啤酒中的5-羟甲基糠醛和糠醛 [J].酿酒科技,2006,9:88-89.
[4]刘潇潇,杨立伟,于江泳,等.HPLC法测定参芪扶正注射液中5-羟甲基糠醛的含量及其来源的初步探讨 [J].药物分析杂志,2012,32 (4):639-640.
[5]钟克俭,陈景联.5-羟甲基糠醛对测定甲硝唑葡萄糖注射液中甲硝唑含量的影响 [J].中国药事,1997,11 (1):53-54.
[6]王发,王嫦鹤,张秉华,等.HPLC法检查右旋糖酐40氯化钠注射液中5-羟甲基糠醛的限量 [J].西北药学杂志,2011,12,26 (6):410-411.
[7]陈雪帆,陶巧凤,李会林.HPLC法测定甲硝唑葡萄糖注射液中5-羟甲基糠醛的含量 [J].中国卫生检验杂志,2010,1,20 (1):72-73.
