回肠间置术对糖尿病大鼠糖脂代谢的影响
2013-07-27张林君蔡景理陈登刚姜明哲滕明星胡春雷刘长宝
张林君,蔡景理,陈登刚,姜明哲,滕明星,胡春雷,刘长宝
(温州医学院附属第二医院,浙江 温州 325027,1.肛肠外科;2.普外科)
回肠间置术(IT)或称回肠转位术是一种新型手术方式,它通过将一定长度的末端回肠前移至上段空肠,使食物提前刺激末端回肠细胞分泌肠促胰岛素激素来达到缓解2型糖尿病的效果。它最初是为研究外科手术治疗2型糖尿病的相关机制而设计的一种对照术式。2型糖尿病患者在糖代谢紊乱的同时,往往还存在脂代谢的紊乱。本研究选择自发性非肥胖型糖尿病大鼠(GK大鼠)作为实验动物,通过建立大鼠IT模型,观察其对GK大鼠糖类和脂类代谢的影响。
1 材料和方法
1.1 实验材料 12周龄雄性GK大鼠30只由上海斯莱克动物中心提供。主要仪器:稳豪倍益血糖仪及试纸(强生,中国);7071A型全自动生化分析仪(日立,日本)。
1.2 动物分组 动物饲养于温州医学院实验动物中心SPF级屏障系统。适应环境1周后,随机分成IT组10只、假手术饮食控制组(C组)10只及假手术空白对照组(B组)10只。所有大鼠进食高脂饲料(购于上海史莱克公司)及饮用高压灭菌水,保持12 h昼夜交替光照。IT组进行IT,C组及B组行假手术。IT组和B组大鼠自由进食,C组大鼠限制进食(进食量与IT组对应时间总量相同),所有大鼠自由饮水。
1.3 手术方法 IT组GK大鼠施行IT,术前常规禁食24 h,10%的水合氯醛(0.3 mL/kg)麻醉,在距离回盲部10 cm处离断肠管,沿断端向肠管近端量取10 cm回肠,离断肠管,将带血管蒂的10 cm“间置段”肠管以湿纱布包裹后送入腹腔,以免缺血坏死。近端回肠和远端回肠作端端吻合。在距十二指肠屈氏韧带10 cm处离断空肠,将“间置段”回肠的近端和空肠近端、远端和空肠远端分别做端端吻合,甲硝唑3 mL冲洗腹腔,关腹。术毕皮下注射0.9%氯化钠溶液5 mL。整个手术过程约80 min。C组和B组均行假手术,术前准备及麻醉方式均与IT组相同,在与IT组大鼠相应的肠段位置切开肠管,并做原位吻合。手术时程及其他相关处理均与IT组相同。
1.4 观察指标 术后每日8时称重各组GK大鼠进食量及体质量。术前及术后每周用强生稳豪倍益血糖仪测量禁食12 h血糖。各组分别于术前及术后第4、第8周行口服糖耐量试验(OGTT),采用50%葡萄糖溶液2 g/kg灌胃。术前及术后第8周,7170A型全自动生化分析仪检测血总胆固醇、甘油三脂、高密度脂蛋白。
1.5 标本收集 8周后常规处死GK大鼠,各组大鼠行心脏采血,静置1 h,以4000 r/min离心15 min,用移液枪移取血清,置于Eppendorf管及-20 ℃冰箱保存待用。
1.6 统计学处理方法 使用SPSS17.0统计软件进行分析。实验数据为计量资料,采用±s表示。检验各组变量正态分布情况,术前各组大鼠观测指标有无差异应用方差分析(ANOVA),不同组别观测指标有无差异采用独立LSD-t检验;同一组别手术前后指标比较采用配对t检验。P<0.05为差异有统计学意义。
2 结果
2.1 存活率 IT组大鼠死亡3只,存活率为70%,其中2只根据术后尸检发现死于吻合口瘘引起的腹膜炎,另1只在术后第12天因极度消瘦而死亡;C组有1只大鼠于术后10日死于术后粘连性肠梗阻,存活率为90%;B组大鼠全部成活,存活率为100%。
2.2 IT对大鼠进食量及体质量的影响 三组术前GK大鼠平均周进食量及体质量差异无统计学意义。术后实验动物进食量情况:IT组GK大鼠在术后第1周进食量较术前锐减,而后逐渐增加,至第4周基本恢复至术前水平(约140 g/周),与B组比较,IT组GK大鼠除术后第1、第2、第3周进食量明显减少(P<0.05)外,余各周差异均无统计学意义(见表1)。C组进食量限制与IT组GK大鼠的进食量相同。术后实验动物的体质量情况:术后3组GK大鼠体质量均显著下降,IT组大鼠术后第4周升至术前水平,较其他两组滞后。IT组和C组比较,除术后第3~第5周以外,其他各时间点体质量差异均无统计学意义(见表2)。
表1 IT组和B组大鼠手术前、后周平均进食量比较(g,±s)

表1 IT组和B组大鼠手术前、后周平均进食量比较(g,±s)
与B组比:aP<0.05
组别 n 术前 第1周 第2周 第3周 第4周 第5周 第6周 第7周 第8周IT组 7145.50±7.0949.20±6.49a78.36±7.38a104.90±6.52a138.47±6.29153.44± 7.88156.53±7.73162.91±7.67160.87±7.49 B组 10148.00±8.8458.00±8.76100.30±8.97120.50±8.10142.30±8.42155.60±7.39158.20±7.26158.70±7.66161.30±7.32
表2 三组GK大鼠手术前后体质量比较(g,±s)

表2 三组GK大鼠手术前后体质量比较(g,±s)
与C组比:aP<0.05;与B组比:bP<0.05
组别 n 术前 第1周 第2周 第3周 第4周 第5周 第6周 第7周 第8周IT组 7335.81±10.78304.33±11.29306.91±9.70b325.83±10.59ab340.14±11.00ab355.16± 11.20ab369.87±11.59375.96±11.50380.91±10.96 C组 9 332.26±9.90305.54±10.82310.58±8.84337.47±9.63352.34±10.69365.37±11.03372.82±11.09374.81±10.34383.21±10.12 B组 10 334.15±9.90309.70±10.37320.45±8.75347.65±10.11355.75±11.03367.90±10.88371.55±10.83377.50±10.57382.35±10.85
2.3 IT对血糖的影响 IT组术后空腹血糖与术前比较明显下降(P<0.05)。IT组与C组及B组比较明显下降,各时间点空腹血糖差异均具有统计学意义(P<0.05);C组与B组比较,除了术后第2周,空腹血糖显著低于B组,其余各时间点差异均无统计学意义(P>0.05)。见表3。
表3 各组GK大鼠手术前后血糖变化情况(±s,mmol/L)

表3 各组GK大鼠手术前后血糖变化情况(±s,mmol/L)
与C组比:aP<0.05;与B组比:bP<0.05;与术前比:cP<0.05
组别IT组C组B组术前17.77±2.94 17.43±2.41 16.94±3.14第1周8.20±2.41abc 10.97±1.86c 10.80±2.65c第2周8.40±2.18abc 11.31±1.87bc 14.69±2.32第4周10.30±1.56abc 16.16±2.13 16.90±2.11第8周10.13±1.27abc 17.26±2.15 17.30±2.18
2.4 OGTT 术前、术后第4、第8周分别为三组GK大鼠进行OGTT。组间比较:IT组术后4周、8周曲线下面积与C组、B组相比差异有统计学意义。各组大鼠术后OGTT曲线,见图1-3。
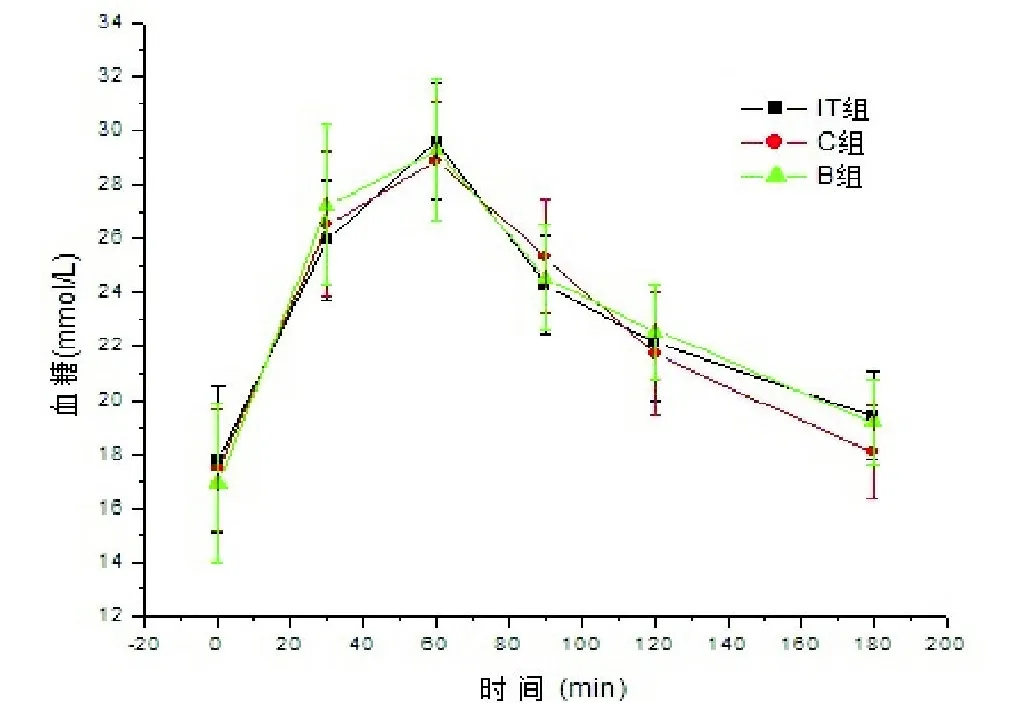
图1 术前3组GK大鼠OGTT曲线
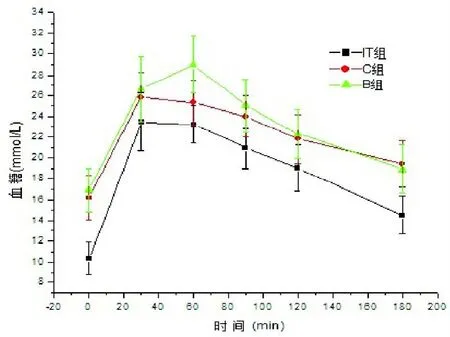
图2 术后4周GK大鼠OGTT曲线
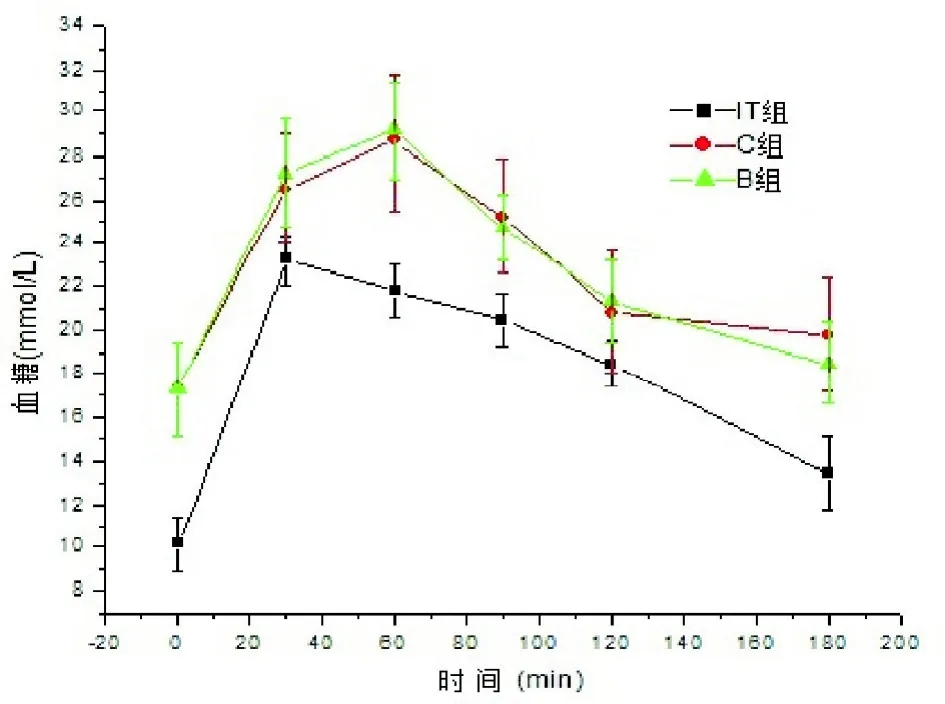
图3 术后8周GK大鼠OGTT曲线
2.5 各组脂质代谢变化 IT组术后总胆固醇和甘油三酯较术前显著下降(P<0.05),同时高密度脂蛋白明显升高,和C组和B组比较差异有统计学意义(P<0.05)。C组和B组术后总胆固醇、甘油三酯较术前有不同程度升高,但差异无统计学意义。C组和B组比较,差异无统计学意义。见表4。
3 讨论
以Roux-en-Y胃旁路术为代表的外科手术在治疗肥胖症的同时,对2型糖尿病有显著的治疗作用。然而手术治疗2型糖尿病的确切机制目前尚不明确,仍是国内外研究的热点问题。IT作为研究胃旁路术后2型糖尿病改善的机制而设计的一种对照术式,由Koopmans等[1]最先报道。它是基于“后肠假说”设计的,该理论认为:胃肠道重建术后未完全消化的食物提早进入回肠,刺激远端回肠L细胞胰高血糖素样肽-1(GLP-1)、肽YY(PYY)等肠道激素的分泌有助于降低血糖、改善β细胞功能。与胃旁路术不同,IT既不减少胃容量也没有旷置十二指肠和部分空肠,仅仅通过将一定长度的末端回肠前移至上段空肠,使食物提前刺激末端回肠细胞。因此,研究IT对2型糖尿病的治疗作用和机制可以更好地明确“肠-胰岛素轴”在2型糖尿病发病机制和治疗中的作用。
糖尿病患病率逐年升高,我国目前有糖尿病患者约9420万人,其中又以2型糖尿病为主。2型糖尿病是以胰岛素抵抗和胰岛功能进行性减退为特征的一种代谢性疾病,并伴有因胰岛素分泌或作用缺陷引起的糖、脂肪和蛋白质代谢异常。40% 2型糖尿病患者合并有脂代谢紊乱,血脂异常又对大小血管并发症的发生发展起了很重要的作用,脂毒性和糖毒性又相互影响、相互促进,由此引发一系列并发症。
我们的实验结果显示:与B组和C组相比,IT组GK大鼠术后1周空腹血糖由术前(17.77±2.94)mmol/L降至(8.20±2.41)mmol/L,差异具有统计学意义(P<0.05),随着观察周期的延长,IT组GK大鼠术后空腹血糖一直保持在较低水平,始终显著低于术前。IT组与C组及B组比较,术后各时间点空腹血糖明显下降,差异均具有统计学意义(P<0.05)。IT组GK大鼠术后第4、第8周0GTT曲线下面积也由术前的70.66±4.30下降至57.84±3.81和55.62±3.25,与术前及其他两组比较差异均具有统计学意义(P<0.05)。这说明IT可改善GK大鼠血糖代谢,IT对GK大鼠2型糖尿病的改善是持久的。IT不减少胃容量也没有旷置十二指肠和部分空肠,因此,它对GK大鼠的进食量和体质量影响是一过性的。术后IT组与C组进食量相等,但空腹血糖及口服糖耐量试验均提示IT组优于C组,表明改善糖代谢的作用并不是单纯进食量的减少(一过性进食量减少)所致。我们的实验结果也显示:IT后总胆固醇和甘油三酯明显下降,而高密度脂蛋白明显升高。提示IT在改善GK大鼠2型糖尿病的同时,同样显著改善GK大鼠伴随的脂质代谢紊乱。而与术前相比,C组和B组脂质代谢指标均有不同程度升高,可能跟术后继续长期进食高脂饲料有关。
表4 手术前后各组血脂水平变化情况(±s)
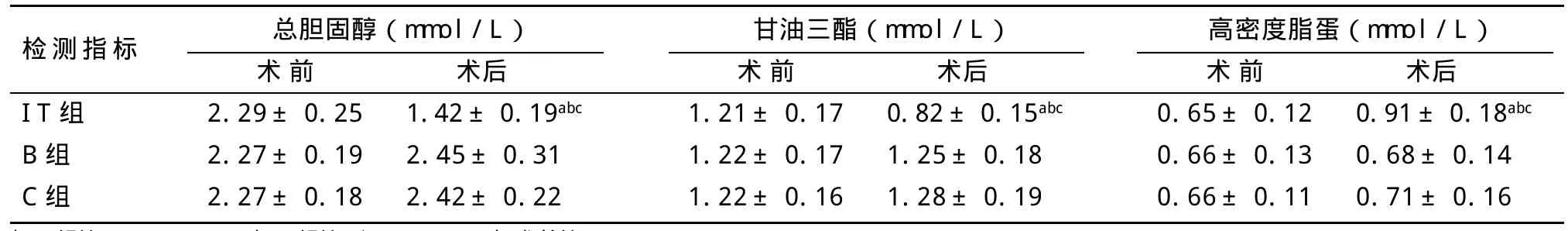
表4 手术前后各组血脂水平变化情况(±s)
与C组比:aP<0.05;与B组比:bP<0.05;与术前比:cP<0.05
检测指标IT组B组C组总胆固醇(mmol/L) 甘油三酯(mmol/L)术前2.29±0.25 2.27±0.19 2.27±0.18术后1.42±0.19abc 2.45±0.31 2.42±0.22高密度脂蛋(mmol/L)术前1.21±0.17 1.22±0.17 1.22±0.16术后0.82±0.15abc 1.25±0.18 1.28±0.19术前0.65±0.12 0.66±0.13 0.66±0.11术后0.91±0.18abc 0.68±0.14 0.71±0.16
IT术后糖类和脂质代谢得到明显改善,然而其对糖尿病GK大鼠治疗作用的确切机制尚不明确。我们的研究显示:IT治疗2型糖尿病与体质量下降和进食量关系不密切,这和之前的学者的研究[2]是一致的。IT改善2型糖尿病的机制可能与肠-胰岛素轴有关[3]。其中最主要的激素是GLP-1和抑胃肽(GIP)。GLP-1主要在回肠和结肠的朗格汉斯细胞(L细胞)内合成,目前GLP-1被认为是最重要的肠促胰岛素,发挥着70%~80%的肠促胰岛素活性[4]。GLP-1具有促进胰岛素的合成和分泌的功能,并且可以通过促进胰岛细胞的再生和抑制凋亡来调控胰岛功能。术后GLP-1分泌增加是IT改善糖脂代谢的主要原因之一。IT术后GLP-1明显升高[5-6],使胰岛功能得到改善,同时机体对胰岛素的敏感性增加,进一步逆转体内的糖代谢紊乱。另有研究发现,GLP-1具有通过刺激脂肪的氧化来减轻脂毒性的功能[7]。
Gagner[8]通过实验证明,IT联合袖状胃切除对肥胖型糖尿病大鼠Zucker大鼠具有与胃旁路术相当的减重和改善糖代谢的效果。在IT基础上联合袖状胃切除,可以达到袖状胃切除术降低瘦素以及IT增加PYY、GLP-1的共同作用来改善糖尿病[9]。我们的实验结果表明,IT不仅能改善GK大鼠血糖代谢而且脂类代谢也有所好转。但IT研究时间尚短,其改善2型糖尿病的相关机制有待于进一步的研究。
[1] Koopmans HS, Sclafani A. Control of body weight by lower gut signals[J]. Int J Obes, 1981, 5(5):491-495.
[2] Wang TT, Hu SY, Gao HD, et al. Ileal transposition controls diabetes as well as modified duodenal jejunal bypass with better lipid lowering in a nonobese rat model of type II diabetes by increasing GLP-1[J]. Ann Surg, 2008, 247(6):968-975.
[3] Mason EE. The mechanism of surgical treatment of type 2 diabetes[J]. Obes Surg, 2005, 15(4):459-461.
[4] 杨红旺, 刘洋, 袁勃, 等. GLP-1的生理作用与临床[J]. 中国糖尿病杂志, 2009, 17(1):78- 80.
[5] Strader AD, Clausen TR, Goodin SZ, et al. Ileal interposition improves glucose tolerance in low dose streptozotocintreated diabetic and euglycemic rats[J]. Obes Surg, 2009, 19(1):96-104.
[6] Patriti A, Aisa MC, Annetti C, et al. How the hindgut can cure type 2 diabetes. Ileal transposition improves glucose metabolism and beta-cell function in Goto-kakizaki rats through an enhanced Proglucagon gene expression and L-cell number[J]. Surgery, 2007, 142(1):74-85.
[7] Sancho V, Trigo MV, Martin-Duce A, et al. Effect of GLP-1 on D-glucose transport, lipolysis and lipogenesis in adipocytes of obese subjects[J]. Int J Mol Med, 2006, 17(6):1133-1137.
[8] Gagner M. Laparoscopic sleeve gastrectomy with ileal interposition (SGIT):a modified duodenal switch for resolution of type 2 diabetes mellitus in lesser obese patients (BMI<35)[J]. World J Surg, 2011, 35(1):109-110.
[9] Boza C, Munoz R, Yung E, et al. Sleeve gastrectomy with ileal transposition (SGIT) induces a significant weight loss and diabetes improvement without exclusion of the proximal intestine[J]. J Gastrointest Surg, 2011, 15(6):928-934.
